ГОСТ 34448-2018
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЯСО И МЯСНЫЕ ПРОДУКТЫ
Методы определения L-(+)-глутаминовой кислоты
Meat and meat products. Methods for the determination of L-(+)-glutamic acid
МКС 67.120.10
Дата введения 2019-09-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2015 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным научным учреждением "Федеральный научный центр пищевых систем имени В.М.Горбатова РАН" (ФГБНУ "ФНЦ пищевых систем им.В.М.Горбатова" РАН)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 27 июля 2018 г. N 110-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по МК (ИСО 3166) 004-97 | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
Узбекистан | UZ | Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 24 августа 2018 г. N 527-ст межгосударственный стандарт ГОСТ 34448-2018 введен в действие в качестве национального стандарта Российской Федерации с 1 сентября 2019 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
1 Область применения
Настоящий стандарт распространяется на продукты убоя и мясную продукцию, а также на мясо птицы, субпродукты и продукты его переработки, комплексные пищевые добавки и ингредиенты, используемые в мясной промышленности, и устанавливает спектрофотометрический и хроматографический методы определения свободной, не связанной в белке L-(+)-глутаминовой кислоты.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
________________
В Российской Федерации действует ГОСТ Р 12.1.019-2009 "Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты".
ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2493-75 Реактивы. Калий фосфорнокислый двузамещенный 3-водный. Технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ ISO 3696-2013 Вода для лабораторного анализа. Технические требования и методы контроля
________________
В Российской Федерации действует ГОСТ Р 52501-2005 (ИСО 3696:1987) "Вода для лабораторного анализа. Технические условия".
ГОСТ 4025-95 Мясорубки бытовые. Технические условия
ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
ГОСТ 4199-76 Реактивы. Натрий тетраборнокислый 10-водный. Технические условия
ГОСТ ИСО 5725-2-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
________________
В Российской Федерации действует ГОСТ Р ИСО 5725-2-2002 "Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений".
ГОСТ ИСО 5725-6-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
________________
В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002 "Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике".
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 7269-2015 Мясо. Методы отбора образцов и органолептические методы определения свежести
ГОСТ 9792-73 Колбасные изделия и продукты из свинины, баранины, говядины и мяса других видов убойных животных и птиц. Правила приемки и методы отбора проб
ГОСТ 9793-2016 Мясо и мясные продукты. Методы определения влаги
ГОСТ 20469-95 Электромясорубки бытовые. Технические условия
ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26272-98 Часы электронно-механические кварцевые наручные и карманные. Общие технические условия
ГОСТ 26678-85 Холодильники и морозильники бытовые электрические компрессионные параметрического ряда. Общие технические условия
ГОСТ 29224-91 (ИСО 386-77) Посуда лабораторная стеклянная. Термометры жидкостные стеклянные лабораторные. Принципы устройства, конструирования и применения
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31467-2012 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
ГОСТ 33319-2015 Мясо и мясные продукты. Метод определения массовой доли влаги
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Требования безопасности
3.1 При подготовке и проведении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007.
3.2 Помещение, в котором проводятся измерения, должно быть оснащено приточно-вытяжной вентиляцией. При проведении работ необходимо соблюдать правила личной гигиены и противопожарной безопасности в соответствии с требованиями ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
3.3 При работе с электроприборами соблюдают требования безопасности по ГОСТ 12.1.019.
4 Отбор и подготовка проб
4.1 Отбор проб проводят по ГОСТ 7269, ГОСТ 9792, ГОСТ 31467, а также в соответствии с нормативными или техническими документами, действующими на территории государства, принявшего настоящий стандарт, на конкретные виды продуктов.
4.2 Пробы измельчают на гомогенизаторе или дважды пропуская через мясорубку, а затем тщательно перемешивают. При этом температура пробы должна быть не более 25°С.
Подготовленную пробу хранят не более 24 ч в герметически закрытом контейнере таким образом, чтобы предотвратить порчу и изменение состава.
При необходимости допускается хранить подготовленную пробу в замороженном состоянии при температуре не выше минус 18°С не более 7 сут.
Комплексные пищевые добавки отбирают равными порциями из верхнего, нижнего и среднего слоев упаковки и гомогенизируют.
5 Спектрофотометрический метод
5.1 Сущность метода
L-(+)-глутаминовую кислоту экстрагируют из пробы, подготовленной по 4.2, ледяным раствором хлорной кислоты. Смесь центрифугируют, фильтруют и доводят кислотность фильтрата до требуемого значения. Проводят ферментативное преобразование L-(+)-глутамата в -кетоглутамат в ходе реакции с никотинамидадениндинуклеотидом (НАД) в присутствии глутаматдегидрогеназы (ГДГ):
![]() . (1)
. (1)
Затем окисляют эквивалентное количество восстановленной формы НАДН хлоридом иодонитротетразолия (ИНТ) в присутствии липоамиддегидрогеназы (ЛАДГ):
![]() . (2)
. (2)
Измеряют оптическую плотность образовавшегося формазана на спектрофотометре при длине волны 492 нм и окончательно рассчитывают массовую долю L-(+)-глутаминовой кислоты. Диапазон измерений массовой доли L-(+)-глутаминовой кислоты составляет от 0,01 до 0,14%.
5.2 Средства измерений, вспомогательное оборудование, материалы и реактивы
Мясорубка механическая по ГОСТ 4025 или электромясорубка бытовая по ГОСТ 20469, с решеткой, диаметр отверстий которой не более 4 мм.
Гомогенизатор.
Ледяная баня.
Контейнеры для хранения проб.
Лабораторная центрифуга с центрифужными пробирками вместимостью 50 или 100 см, которая обеспечивает центрифугирование при 2000 g.
рН-метр с диапазоном измерений от 0 до 14 ед. рН с пределом допускаемой абсолютной погрешности не более ±0,02 ед. рН.
Термометр жидкостный стеклянный лабораторный по ГОСТ 29224, с диапазоном измерения температуры от 0 до 100°С и ценой деления 1°С.
Бумажный фильтр диаметром 15 см.
Колбы мерные 2-50-2, 2-100-2, 2-250-2, 2-500-2 по ГОСТ 1770.
Колбы конические Кн-1-10-14/23 ТС, Кн-1-50-14/23, Кн-1-250-24/29 ТС по ГОСТ 25336.
Воронки В-56-80 ХС, В-75-80 ХС по ГОСТ 25336.
Стакан В-1-100 ТХС по ГОСТ 25336.
Пипетки градуированные 1-1-1-1, 1-2-1-1, 1-1-1-5, 1-2-1-5, 1-1-1-10, 1-2-1-10, 1-1-1-25, 1-2-1-25 по ГОСТ 29227 или дозаторы автоматические с переменным объемом дозирования и относительной погрешностью дозирования ±1%.
Фотометрические кварцевые кюветы со слоем поглощения 10 мм.
Спектрофотометр, обеспечивающий измерение при длине волны 492 нм.
Пластиковые шпатели или стеклянные палочки.
Весы неавтоматического действия по ГОСТ OIML R 76-1 специального или высокого класса точности или лабораторные весы по нормативным документам, действующим на территории государства, принявшего стандарт, с пределами допускаемой абсолютной погрешности не более ±1,00 мг.
Холодильник бытовой электрический по ГОСТ 26678.
Вода дистиллированная по ГОСТ 6709 или вода для лабораторного анализа по ГОСТ ISO 3696 первой степени очистки.
Примечание - Дистиллированная вода не должна содержать следы ионов металлов, которые могут снижать активность ферментов. Деминерализованная вода не должна содержать микроорганизмы, которые могут вызывать специфическую ферментативную фоновую активность и отрицательно сказываться на результатах анализа.
Бидистиллированная вода с электропроводимостью менее 10 мкСм.
Лед.
Хлорная кислота с содержанием основного вещества не менее 70,0%.
Калия гидроокись по ГОСТ 24363, х.ч.
Гидрохлорид триэтаноламин, х.ч.
Октилфенолдекаэтиленгликолевый эфир.
Калий фосфорнокислый двузамещенный по ГОСТ 2493, ч.д.а.
Калий фосфорнокислый однозамещенный ГОСТ 4198, х.ч.
Никотинамидадениндинуклеотид (НАД).
Иодонитротетразолия [2-(4-иодофенил)-3-(4-нитрофенил)-5-фенилтетразолия] хлорид, х.ч.
Глутаматдегидрогеназа (ГДГ) с удельной активностью не менее 900 Е/см.
Лиофильно высушенная диафораза (липоамиддегидрогеназа, ЛАДГ).
L-(+)-глутаминовая кислота с содержанием основного вещества не менее 99,0%.
Допускается применение других средств измерений с метрологическими характеристиками и вспомогательного оборудования с техническими характеристиками, а также материалов и реактивов по качеству не ниже указанных в настоящем стандарте.
5.3 Подготовка к измерению
5.3.1 Вода, используемая для приготовления растворов ферментов, должна быть деминерализованной или бидистиллированной, полученной в стеклянном дистилляторе.
Вода, используемая для приготовления растворов химических реактивов и подготовки проб, должна быть дистиллированной или деминерализованной.
5.3.2 Приготовление раствора хлорной кислоты молярной концентрации с (![]() )=1 моль/дм
)=1 моль/дм
8,6 см хлорной кислоты (массовая доля - 70%, плотность - 1,67 г/см
) помещают в мерную колбу вместимостью 100 см
, доводят объем раствора до метки водой и перемешивают.
Примечание - При использовании хлорной кислоты с меньшей массовой долей проводят пересчет объема кислоты, используемой для осаждения белков.
5.3.3 Приготовление раствора гидроксида калия молярной концентрации с (![]() )=2 моль/дм
)=2 моль/дм
Растворяют 56,1 г гидроксида калия в 400 см дистиллированной воды в мерной колбе вместимостью 500 см
, затем раствор охлаждают до комнатной температуры, доводят объем раствора до метки дистиллированной водой и перемешивают.
5.3.4 Приготовление буферного раствора (рН=8,6 ед. рН)
5.3.4.1 Растворяют 1,86 г гидрохлорида триэтаноламина в воде, доводят рН до 8,6 ед. рН раствором гидроксида калия, используя для измерений рН-метр. Затем добавляют 0,68 г октилфенолдекаэтиленгликолевого эфира (например, Тритон Х-100), доводят объем раствора до 100 см водой и перемешивают полученный раствор (далее - раствор 1).
5.3.4.2 Растворяют 0,86 г двузамещенного фосфорнокислого калия (![]() ) и 0,007 г однозамещенного фосфорнокислого калия (
) и 0,007 г однозамещенного фосфорнокислого калия (![]() ) в воде, доводят объем раствора до 100 см
) в воде, доводят объем раствора до 100 см и перемешивают полученный раствор (далее - раствор 2).
5.3.4.3 Смешивают 20 см раствора 1 и 5 см
раствора 2.
Раствор хранят при температуре (4±2)°С не более 2 мес.
5.3.5 Приготовление раствора никотинамидадениндинуклеотида (НАД)
5 мг НАД растворяют в 5,0 см воды в небольшой колбе со шлифом, колбу закрывают пробкой.
Раствор хранят в темноте при температуре (4±2)°С не более 2 мес.
5.3.6 Приготовление раствора иодонитротетразолия [2-(4-иодофенил)-3-(4-нитрофенил)-5-фенилтетразолия] хлорида (ИНТ-хлорида)
Растворяют 30 мг ИНТ-хлорида в 50 см воды, колбу закрывают пробкой.
Раствор хранят в темноте при температуре (4±2)°С не более 2 мес.
5.3.7 Приготовление раствора диафоразы (липоамиддегидрогеназы) (ЛАДГ)
Растворяют 3 мг лиофильно высушенной диафоразы в 1 см воды.
Раствор хранят в темноте при температуре (4±2)°С не более 1 мес.
5.3.8 Приготовление раствора глутаматдегидрогеназы (ГДГ)
Используют раствор глутаматдегидрогеназы концентрации 10 мг/см, свободный от сульфата аммония, этилендиаминтетрауксусной кислоты и глутаминазы, поставляемый в готовом виде (например, в расфасовке по 1,0 см
).
Раствор хранят при температуре (4±2)°С не более 12 мес.
5.3.9 Приготовление стандартного раствора L-(+)-глутаминовой кислоты
Растворяют 50 мг L-(+)-глутаминовой кислоты в 25 см воды в мерной колбе вместимостью 50 см
. Устанавливают рН=7,0 ед. рН раствором гидроксида калия, после чего доводят объем до метки водой и перемешивают.
Раствор хранят при температуре (4±2)°С не более 2 мес.
Непосредственно перед использованием раствор разводят водой в соотношении 1:49 (по объему).
5.3.10 Приготовление экстракта пробы
5.3.10.1 Взвешивают приблизительно 50 г подготовленной пробы (10 г - для пищевых добавок) с точностью до 0,01 г и переносят в гомогенизатор. В гомогенизатор к пробе добавляют 100 см охлажденного льдом раствора хлорной кислоты, приготовленного по 5.3.2, и смесь гомогенизируют.
5.3.10.2 50 см гомогенизата переносят в центрифужную пробирку и центрифугируют в течение 10 мин при 2000 g. Затем, осторожно отодвинув слой жира, отфильтровывают супернатант через гофрированный бумажный фильтр в коническую колбу вместимостью 250 см
. Первые 10 см
фильтрата отбрасывают.
50 см профильтрованного раствора, который должен быть только слегка опалесцирующим, переносят в стакан вместимостью 100 см
и с помощью рН-метра доводят рН до 10 ед. рН раствором гидроксида калия, приготовленного по 5.3.3. Содержимое стакана количественно переносят в мерную колбу вместимостью 100 см
, доводят водой до метки и перемешивают. Раствор охлаждают в ледяной бане в течение 10 мин и фильтруют через гофрированный бумажный фильтр, отбросив первые 10 см
фильтрата.
5.3.10.3 25 см фильтрата переносят в мерную колбу вместимостью 250 см
и доводят объем фильтрата до метки водой.
Примечание - Объем фильтрата выбирают так, чтобы концентрация L-(+)-глутаминовой кислоты была приблизительно 0,030 г/дм.
5.3.11 Определение массовой доли влаги в пробе проводят по ГОСТ 33319.
5.4 Проведение измерений
5.4.1 Выполняют два параллельных определения.
5.4.2 Температуру буферного раствора по 5.3.4 и экстракта пробы по 5.3.10 доводят до (22±2)°С. Для проведения ферментативной реакции берут две фотометрические кюветы, в каждую из которых пипеточным дозатором добавляют:
- 2,50 см буферного раствора;
- 0,20 см раствора НАД;
- 0,20 см раствора ИНТ;
- 0,05 см раствора диафоразы.
Затем в одну из кювет вносят 0,50 см экстракта по 5.3.10.3, получая исследуемый раствор, а во вторую - 0,50 см
воды, получая контрольный раствор.
Растворы в кюветах перемешивают пластиковыми шпателями или стеклянными палочками и измеряют оптическую плотность относительно воды при длине волны 492 нм: - оптическая плотность исследуемого раствора,
- оптическая плотность контрольного раствора.
Температура растворов - от 20 до 25°С.
5.4.3 В каждую кювету вносят по 0,05 см раствора ГДГ и тщательно смешивают с содержимым, используя шпатель или стеклянную палочку.
Растворы выдерживают 15 мин. Затем измеряют оптические плотности при длине волны 492 нм, повторяя измерения через каждые 2 мин до достижения постоянных значений.
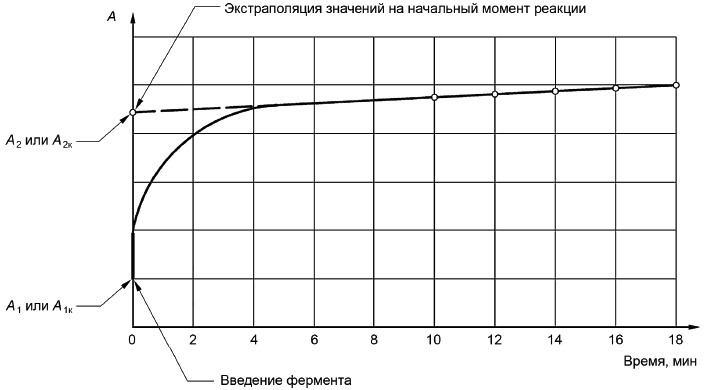
Строят графики зависимости оптических плотностей растворов от времени и экстраполируют их на момент внесения фермента ГДГ. Пример построения графика зависимости оптической плотности раствора от времени приведен в приложении А.
Получают экстраполированные значения оптических плотностей исследуемого () и контрольного (
) растворов.
5.4.4 Определяют молярный коэффициент оптической плотности формазана, повторяя операции по 5.4.1 и 5.4.2*, но заменяя 0,5 см экстракта в первой фотометрической кювете на 0,5 см
стандартного раствора L-(+)-глутаминовой кислоты.
________________
* Письмом Росстандарта от 25.02.2021 г. N 605-ОГ/03 разъясняется, что "В п.5.4.4 ГОСТ 34448-2018 допущена опечатка". Следует читать: по 5.4.1, 5.4.2 и 5.4.3. - .
Получают следующие значения оптических плотностей:
- -стандартного раствора L-(+)-глутаминовой кислоты;
- - контрольного раствора;
- - стандартного раствора L-(+)-глутаминовой кислоты;
- - контрольного раствора.
5.5 Обработка результатов
5.5.1 Массовую долю L-(+)-глутаминовой кислоты в пробе , %, вычисляют по формуле
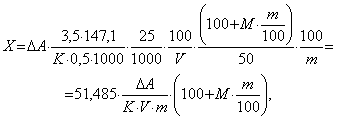 (3)
(3)
где ![]() ;
;
- молярная масса L-(+)-глутаминовой кислоты, г/моль;
- массовая доля влаги в пробе, %, которую определяют по ГОСТ 33319 или ГОСТ 9793;
- масса пробы, г;
- объем фильтрата, взятый на определение, см
;
- молярный коэффициент оптической плотности формазана при длине волны 492 нм, дм
/ммоль·см, рассчитанный по формуле
![]() , (4)*
, (4)*
здесь ![]() .
.
________________
* Письмом Росстандарта от 21.01.2021 г. N 156-ОГ/03 разъясняется, что "В п.п.5.5.1, а именно в формуле (4) ГОСТ 34448-2018 допущена опечатка". Следует читать: ![]() . - .
. - .
За окончательный результат принимают среднеарифметическое значение двух параллельных определений, округленное до второго десятичного знака.
6 Хроматографический метод
6.1 Сущность метода
Метод основан на экстракции свободной L-(+)-глутаминовой кислоты из пробы и последующем разделении методом высокоэффективной жидкостной хроматографии (ВЭЖХ) с предколоночной дериватизацией.
Количественное определение осуществляют по площади пика L-(+)-глутаминовой кислоты относительно градуировочной зависимости, полученной при использовании градуировочных растворов аминокислоты в аналогичных условиях.
Диапазон измерений массовой доли L-(+)-глутаминовой кислоты составляет от 0,14 до 95,0%.
6.2 Средства измерений, вспомогательное оборудование, материалы и реактивы
Высокоэффективный жидкостный хроматограф, оснащенный:
- устройством для автоматического введения анализируемой пробы;
- внутренним термостатированным реактором для проведения дериватизирующей реакции аминокислот;
- внутренним двухканальным проточным спектрофотометрическим детектором, обеспечивающим измерение при длине волны 338 нм;
- внутренним автоматическим устройством для введения растворенного образца с делением потоков и ловушкой пузырьков;
- набивной хроматографической колонкой С18 РА, 3,5 мкм, 4,6 мм150 мм;
- записывающим устройством с компьютерным управлением и автоматической программой обработки хроматографических данных в соответствии с комплектацией жидкостного хроматографа.
Мясорубка механическая по ГОСТ 4025 или электромясорубка бытовая по ГОСТ 20469 с решеткой, диаметр отверстий которой не более 4 мм.
Весы неавтоматического действия по ГОСТ OIML R 76-1 специального или высокого класса точности или лабораторные весы по нормативным документам государства, принявшего стандарт, с пределами допускаемой абсолютной погрешности не более ±1,00 мг.
Лабораторная водяная баня с подогревом для поддержания температуры от 20 до 60°С.
Холодильник бытовой электрический по ГОСТ 26678.
Часы электронно-механические по ГОСТ 26272.
рН-метр с диапазоном измерений от 0 до 14 ед. рН с пределом допускаемой абсолютной погрешности не более ±0,02 ед. рН.
Термометр жидкостный стеклянный по ГОСТ 29224, с диапазоном измерения температуры от 0 до 100°С и ценой деления 1°С.
Контейнеры для хранения проб вместимостью 250-500 см.
Автоматические дозаторы с переменным объемом дозирования и относительной погрешностью дозирования не более ±1%.
Колба мерная 2-1000-2 по ГОСТ 1770.
Колба коническая Кн-1-100-24/29 ТС по ГОСТ 25336.
Лабораторная центрифуга с центрифужными пробирками вместимостью 50 или 100 см, которая обеспечивает центрифугирование при 2000 g.
Цилиндры 1-25, 1-500 по ГОСТ 1770.
Стакан В-1-600 ТХС по ГОСТ 25336.
Воронки В-56-80 ХС, В-75-80 ХС по ГОСТ 25336.
Центрифужные пробирки с крышкой типа "Эппендорф" вместимостью 50 или 100 см.
Мембранный фильтр из политетрафторэтилена с диаметром пор 0,45 мкм.
Флаконы - хроматографические виалы из стекла вместимостью 2 см.
Вода дистиллированная по ГОСТ 6709 или вода для лабораторного анализа по ГОСТ ISO 3696 первой степени очистки.
Дистиллированная вода для ВЭЖХ или бидистиллированная вода с электропроводимостью менее 10 мкСм.
Вода для ВЭЖХ.
Азид натрия, х.ч.
Кислота соляная по ГОСТ 3118, х.ч.
о-Фталевый альдегид, х.ч.
Ацетонитрил для ВЭЖХ, содержание основного вещества не менее 99,9%.
Трихлоруксусная кислота, х.ч.
Натрия гидрофосфат двузамещенный, содержание основного вещества не менее 99,0%.
Натрий тетраборнокислый по ГОСТ 4199, х.ч.
Метанол для ВЭЖХ с содержанием основного вещества не менее 99,9%.
Стандартный образец L-(+)-глутаминовой кислоты с содержанием основного вещества не менее 99,0% или стандартный раствор L-(+)-глутаминовой кислоты в смеси аминокислот молярной концентрации 2,5 мкмоль/см.
Допускается применение других средств измерений с метрологическими характеристиками, вспомогательного оборудования с техническими характеристиками не хуже, а также реактивов по качеству не ниже указанных в настоящем стандарте.
6.3 Подготовка к измерению
6.3.1 Приготовление растворов
6.3.1.1 Приготовление воды для хроматографического анализа
Используют дистиллированную воду для ВЭЖХ или применяют бидистиллированную воду с электропроводимостью менее 10 мкСм, которую подвергают дополнительной фильтрации через мембранный фильтр с диаметром пор 0,45 мкм.
Воду хранят в герметично укупоренном сосуде при комнатной температуре не более 24 ч.
6.3.1.2 Приготовление раствора соляной кислоты (рН=2,2 ед. рН)
В стакан вместимостью 600 см вносят 500 см
дистиллированной воды, осторожно под тягой добавляют по каплям концентрированную соляную кислоту (50-150 мм
) до установления рН раствора равным 2,2 ед. рН.
Раствор хранят в герметично укупоренном сосуде при комнатной температуре не более 6 мес.
6.3.1.3 Приготовление 20%-ного раствора трихлоруксусной кислоты
В коническую колбу вместимостью 100 см вносят 20,0 г трихлоруксусной кислоты и 80 см
дистиллированной воды, перемешивают.
Раствор хранят в герметично укупоренном сосуде при комнатной температуре не более 6 мес.
6.3.1.4 Приготовление промывочного элюента А
Смешивают в автоматическом режиме или вручную в отдельной емкости ацетонитрил, метанол и воду для ВЭЖХ в соотношении 45:45:10.
6.3.1.5 Приготовление элюента Б
В стакане в 600 см дистиллированной воды для ВЭЖХ растворяют 1,42 г двузамещенного гидрофосфата натрия (
![]() ) и 2,02 г тетрабората натрия (
) и 2,02 г тетрабората натрия (![]() ), устанавливают рН раствора концентрированной соляной кислотой до значения 8,2 ед. рН и добавляют 100 мг азида натрия (в качестве консерванта). Раствор переносят в мерную колбу вместимостью 1000 см
), устанавливают рН раствора концентрированной соляной кислотой до значения 8,2 ед. рН и добавляют 100 мг азида натрия (в качестве консерванта). Раствор переносят в мерную колбу вместимостью 1000 см, доводят объем раствора до метки водой, перемешивают и фильтруют через мембранный фильтр с диаметром пор 0,45 мкм.
Раствор хранят в герметично укупоренном сосуде при комнатной температуре не более 1 мес.
6.3.1.6 Приготовление градуировочного раствора L-(+)-глутаминовой кислоты
В мерную колбу вместимостью 1000 см вносят 0,37 г L-(+)-глутаминовой кислоты, добавляют 600 см
раствора соляной кислоты (рН=2,2 ед. рН), перемешивают и доводят объем до метки этим же раствором. Полученный раствор фильтруют через мембранный фильтр с диаметром пор 0,45 мкм. Перед применением раствор дегазируют на водяной лабораторной бане с подогревом при температуре от 60 до 80°С в течение 10 мин.
Раствор хранят в герметично укупоренном сосуде в холодильнике при температуре (4±2)°С не более 2 мес.
Допускается применять стандартный раствор L-(+)-глутаминовой кислоты в смеси аминокислот молярной концентрации 2,5 мкмоль/см.
Примечание - Для хроматографической идентификации целесообразно использовать стандартные растворы различной концентрации. Величина концентрации для оптимального сигнала регистрации на экране устанавливается экспериментально для конкретного типа хроматографа. Хорошая идентификация пиков на фотометрическом детекторе анализатора наблюдается при получении выходного сигнала более 50 мВ с интенсивностью до 1000 мВ.
6.3.2 Приготовление раствора пробы
5 г подготовленной пробы (1 г - для пищевых добавок) вносят в центрифужные пробирки, добавляют 100 см раствора соляной кислоты (рН=2,2 ед. рН) и 4 см
20%-ного раствора трихлоруксусной кислоты. Смесь тщательно перемешивают и выдерживают в течение 2 ч при комнатной температуре. Затем экстракт центрифугируют в течение 5 мин при 2000 g и фильтруют через мембранный фильтр с диаметром пор 0,45 мкм. После этого фильтрат переносят в виалу и проводят дериватизацию по 6.3.3.
6.3.3 Дериватизация ортофталевым альдегидом
6.3.3.1 В ручном режиме дериватизацию проводят последовательным смешиванием в виале 50 мм ортофталевого альдегида и 10 мм
раствора пробы, приготовленного по 6.3.1. Объем введенной пробы в хроматограф должен составлять 10 мм
.
6.3.3.2 В автоматическом режиме при помощи устройства введения проб в хроматограф вводят: 10 мм ортофталевого альдегида и 2 мм
раствора пробы. Объем введенной пробы должен составлять 12 мм
.
6.3.3.3 Для градуировки системы проводят дериватизацию градуировочного раствора L-(+)-глутаминовой кислоты, используя вместо раствора пробы градуировочный раствор, приготовленный по 6.3.1.6.
6.4 Проведение измерений
6.4.1 Хроматографические условия измерений
Проводят два параллельных определения в условиях повторяемости по ГОСТ ИСО 5725-2.
В соответствии с инструкцией по эксплуатации хроматографа проводят его включение и задают программируемый метод анализа.
6.4.2 Условия измерений с фотометрическим детектором
Для хроматографа с фотометрическим детектором и набивной колонкой выставляют следующие параметры: канал детектора с длиной волны 338 нм, температура колонки в термостате - 40°С, рабочее давление - 1,6 МПа, поток элюента - 1 см/мин, время анализа - 25 мин. Подача элюента осуществляется по капиллярным шлангам высокого давления с внутренним диаметром 0,2 мм, вводят 10-15 мм
раствора пробы.
В хроматографе реализуется следующая программа подачи элюентов, которую уточняют под конкретный тип прибора. Используют элюент А и элюент Б с программируемым градиентом (см. таблицу 1). Скорость потока 1,5 см/мин.
Таблица 1
Время, мин | Элюент А, % | Элюент Б, % |
0 | 2 | 98 |
0,5 | 2 | 98 |
5,0 | 57 | 43 |
5,1 | 100 | 0 |
7,0 | 100 | 0 |
7,6 | 2 | 98 |
10 | 2 | 98 |
10-25 | 100 | 0 |
После окончания измерений колонку промывают элюентом А в течение 15-20 мин со скоростью потока 0,5 см/мин.
6.4.3 Градуировка системы
Градуировочные растворы, приготовленные по 6.3.1.6 и 6.3.3.3, подвергают анализу в условиях по 6.4.2. Для каждого градуировочного раствора проводят по три параллельных измерения. Полученные хроматограммы обрабатывают с использованием компьютерной системы обработки данных. Определяют абсолютное время удерживания пика глутаминовой кислоты (см. приложение Б) с отклонением ±0,2 мин. С использованием средств программного обеспечения строят градуировочную зависимость площади пика определяемого вещества от концентрации аминокислоты в пробе.
Коэффициент линейной корреляции полученной градуировочной зависимости должен быть не менее 0,99. При невыполнении этого условия выясняют причины, приводящие к неудовлетворительным результатам, и устраняют их. В случае необходимости готовят новые градуировочные растворы.
Проведение градуировки обязательно при замене хроматографической колонки, а также при систематическом получении неудовлетворительных результатов контроля, выполняемого в соответствии с разделом 8.
6.4.4 Контроль аналитической системы
Контроль выполняют с использованием приготовленных по 6.3.1.6 и 6.3.3.3 градуировочных растворов. Полученный результат определения не должен отличаться от действительного значения концентрации определяемых веществ в градуировочном растворе более чем на 3%, относительное стандартное отклонение времени удерживания аналитов не более чем на 5%. В случае невыполнения указанного критерия стабильности градуировочной характеристики проводят новую градуировку.
Контроль аналитической системы осуществляется при условиях, указанных в 6.4.1-6.4.2, перед началом проведения измерений, а также при смене хроматографической колонки, чистке блоков аналитического прибора и т.д.
6.4.5 Выполнение измерений
В хроматографические виалы вместимостью 2 см вносят 0,5 см
пробы, подготовленной по 6.3.2 и 6.3.3.1 или 6.3.3.2, и дважды проводят определение при условиях, указанных в 6.4.1-6.4.2.
Виалы с определяемой пробой устанавливают в штатив автоматического термостатированного инжектора. Ввод пробы осуществляется в соответствии с программой. Анализ происходит автоматически.
Определение L-(+)-глутаминовой кислоты (в анализе выявляется наличие примесей других аминокислот) осуществляют по абсолютному времени удерживания и относительной интенсивности пика.
На рисунке Б.1 (см. приложение Б) приведена хроматограмма с концентрацией аминокислоты, равной 2 мкмоль/см.
По значению площади хроматографического пика с использованием установленной градуировочной характеристики и программы обработки данных находят массовую концентрацию L-(+)-глутаминовой кислоты в анализируемом растворе.
Вычисление массовой доли аминокислоты в анализируемой пробе проводят для каждого из двух параллельных определений.
6.5 Обработка результатов
6.5.1 В соответствии с данными, полученными при анализе градуировочных растворов, проводят количественную обработку хроматограмм с использованием программного обеспечения. Расчеты содержания L-(+)-глутаминовой кислоты выполняются системой обработки данных в автоматическом режиме.
6.5.2 Массовую долю L-(+)-глутаминовой кислоты , %, вычисляют по формуле
![]() , (5)
, (5)
где - массовая концентрация L-(+)-глутаминовой кислоты в градуировочном растворе, мкг/см
;
- площадь пика L-(+)-глутаминовой кислоты в анализируемой пробе, усл. ед.;
- объем раствора для растворения аналита после подготовки пробы, см
;
- площадь пика L-(+)-глутаминовой кислоты в градуировочном растворе, усл. ед.;
- масса пробы, г.
- коэффициент пересчета в проценты.
За окончательный результат принимают среднеарифметическое значение двух параллельных определений, округленное до второго десятичного знака.
7 Метрологические характеристики
7.1 Метрологические характеристики метода при доверительной вероятности P=0,95 приведены в таблице 2.
Таблица 2
Наименование показателя | Метод | Диапазон измерений массовой доли глутаминовой кислоты, % | Границы относительной погрешности, | Предел повторяе- | Предел воспроизво- |
Массовая доля L-(+)-глутаминовой кислоты | Спектрофотометрический | От 0,01 до 0,14 включ. | 20 | 0,25 | 0,35 |
Хроматографический | От 0,14 до 10 включ. | 15 | 0,20 | 0,30 | |
От 10 до 50 включ. | 10 | 0,15 | 0,20 | ||
От 50 до 95 включ. | 5 | 0,10 | 0,15 | ||
Примечания 1 2 | |||||
7.2 Расхождение между результатами двух параллельных определений, выполненных одним оператором при анализе одной и той же пробы с использованием одних и тех же средств измерений и реактивов, не должно превышать предела повторяемости (сходимости) , значения которого приведены в таблице 2.
Результат анализа при доверительной вероятности P=0,95 представляют в виде
![]() , (6)
, (6)
где и
- результаты параллельных измерений, %;
- предел повторяемости, %.
7.3 Расхождение между результатами двух определений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости , значения которого приведены в таблице 2.
Результат анализа при доверительной вероятности P=0,95 представляют в виде
![]() , (7)
, (7)
где и
- результаты двух определений, выполненных в разных лабораториях, %;
- предел воспроизводимости, %.
7.4 Границы относительной погрешности , находящиеся с доверительной вероятностью P=0,95, при соблюдении условий настоящего стандарта не должны превышать значений, приведенных в таблице 2.
8 Контроль точности результатов измерений
8.1 Процедуру контроля стабильности результатов определений (повторяемости, промежуточной прецизионности и погрешности) проводят в соответствии с порядком, установленным в лаборатории, по ГОСТ ИСО 5725-6.
8.2 Проверку приемлемости результатов определений, полученных в условиях повторяемости (сходимости), осуществляют в соответствии с требованиями ГОСТ ИСО 5725-2. Расхождение между результатами определений не должно превышать предела повторяемости . Значения
приведены в таблице 2.
8.3 Проверку приемлемости результатов определений, полученных в условиях воспроизводимости, проводят с учетом требований ГОСТ ИСО 5725-2. Расхождение между результатами определений, полученными двумя лабораториями, не должно превышать предела воспроизводимости . Значения
приведены в таблице 2.
Приложение А
(справочное)
А.1 Пример построения графика зависимости оптической плотности раствора от времени приведен на рисунке А.1.
|
Рисунок А.1
Приложение Б
(справочное)
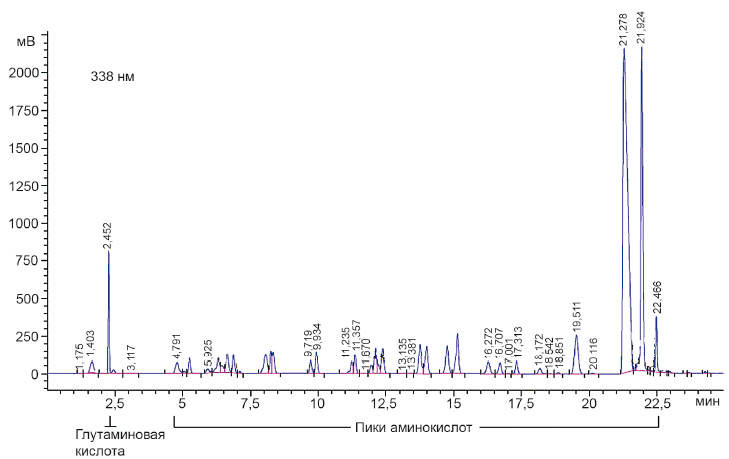
Б.1 Хроматограмма аминокислоте концентрацией 2 мкмоль/см приведена на рисунке Б.1.
|
Рисунок Б.1 - Хроматограмма аминокислот с концентрацией 2 мкмоль/см, 2,45 мин - пик L-(+)-глутаминовой кислоты, колонка С18 РА, 3,5 мкм, 4,6 мм
150 мм
УДК 547.466:006.354 | МКС 67.120.10 |
Ключевые слова: мясо, мясо птицы, мясная продукция, L-(+)-глутаминовая кислота, спектрофотометрический метод, хроматографический метод | |
Электронный текст документа
и сверен по:
, 2018