ГОСТ 34132-2017
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЯСО И МЯСНЫЕ ПРОДУКТЫ
Метод определения аминокислотного состава животного белка
Meat and meat products. Determination of amino acids composition of animal protein
МКС 67.120.10
Дата введения 2019-01-01
Предисловие
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2015 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным научным учреждением "Всероссийский научно-исследовательский институт мясной промышленности имени В.М.Горбатова" (ФГБНУ "ВНИИМП им.В.М.Горбатова")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 30 августа 2017 г. N 102-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
Узбекистан | UZ | Узстандарт |
Украина | UA | Минэкономразвития Украины |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 14 сентября 2017 г. N 1093-ст межгосударственный стандарт ГОСТ 34132-2017 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2019 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
1 Область применения
Настоящий стандарт устанавливает хроматографический метод определения аминокислотного состава белков мяса, включая мясо птицы, субпродуктов, мясных и мясосодержащих продуктов, а также изготовленных из мяса птицы продуктов.
Диапазон измерений массовой доли аминокислот составляет от 50 до 1000 мг/кг с минимальным уровнем их содержания в растворе 0,5 мкмоль/см.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
________________ В Российской Федерации действует ГОСТ Р 12.1.019-2009 "Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты".
ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 177-88 Водорода перекись. Технические условия
ГОСТ 199-78 Реактивы. Натрий уксуснокислый 3-водный. Технические условия
ГОСТ 1077-79 Горелки однопламенные универсальные для ацетилено-кислородной сварки, пайки и подогрева. Типы, основные параметры и размеры и общие технические требования
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2062-77 Реактивы. Кислота бромистоводородная. Технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ ISO 3696-2013 Вода для лабораторного анализа. Технические требования и методы контроля
________________ В Российской Федерации действует ГОСТ Р 52501-2005 (ИСО 3696:1987) "Вода для лабораторного анализа. Технические условия".
ГОСТ 4025-95 Мясорубки бытовые. Технические условия
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ ИСО 5725-2-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
________________ В Российской Федерации действует ГОСТ Р ИСО 5725-2-2002 "Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений".
ГОСТ ИСО 5725-6-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
________________ В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002 "Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике".
ГОСТ 5848-73 Реактивы. Кислота муравьиная. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
ГОСТ 7269-2015 Мясо. Методы отбора образцов и органолептические методы определения свежести
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 9656-75 Реактивы. Кислота борная. Технические условия
ГОСТ 9792-73 Колбасные изделия и продукты из свинины, баранины, говядины и мяса других видов убойных животных и птиц. Правила приемки и методы отбора проб
ГОСТ 10157-2016 Аргон газообразный и жидкий. Технические условия
ГОСТ 10652-73 Реактивы. Соль динатриевая этилендиамин-N,N,N',N'-тетра-уксусной кислоты 2-водная (трилон Б). Технические условия
ГОСТ 20015-88 Хлороформ. Технические условия
ГОСТ 20469-95 Электромясорубки бытовые. Технические условия
ГОСТ 22280-76 Реактивы. Натрий лимоннокислый 5,5-водный. Технические условия
ГОСТ 23042-2015 Мясо и мясные продукты. Методы определения жира
ГОСТ 25011-81 Мясо и мясные продукты. Методы определения белка
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26272-98 Часы электронно-механические кварцевые наручные и карманные. Общие технические требования
ГОСТ 26678-85 Холодильники и морозильники бытовые электрические компрессионные параметрического ряда. Общие технические условия
ГОСТ 28165-89 Приборы и аппараты лабораторные из стекла. Аквадистилляторы. Испарители. Установки ректификационные. Общие технические требования
ГОСТ 29224-91 (ИСО 386-77) Посуда лабораторная стеклянная. Термометры жидкостные стеклянные лабораторные. Принципы устройства, конструирования и применения
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31467-2012 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 аминокислота: Природное соединение, входящее в состав белков и относящееся к классу органических кислот.
Примечание - Перечень и систематическое международное наименование аминокислот приведены в приложении А.
3.2 аналит: Вещество, определяемое при анализе.
4 Требования безопасности
4.1 При подготовке и проведении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007.
4.2 Помещение, в котором проводят измерения, должно быть оснащено приточно-вытяжной вентиляцией. Работу необходимо проводить, соблюдая правила личной гигиены и противопожарной безопасности в соответствии с требованиями ГОСТ 12.1.004, и иметь средства пожаротушения по ГОСТ 12.4.009.
4.3 При работе с электроприборами необходимо соблюдать требования безопасности по ГОСТ 12.1.019.
5 Сущность метода
Метод основан на кислотном гидролизе белка до его полного распада на составляющие аминокислоты с последующим хроматографическим определением смеси на автоматическом жидкостном аминокислотном анализаторе для выявления состава и определения массовой доли индивидуальных аминокислот.
Количественное определение осуществляют по площади пика идентифицированных соединений относительно градуировочной зависимости, полученной при хроматографировании градуировочных растворов аминокислот в аналогичных условиях.
6 Средства измерений, вспомогательное оборудование, материалы и реактивы
Анализатор аминокислотный жидкостной, укомплектованный:
- внешним устройством для автоматического введения анализируемой пробы;
- внутренним термостатированным реактором для проведения цветной реакции аминокислот с нингидрином;
- внутренним двухканальным проточным спектрофотометрическим детектором на длину волны 440 и 570 нм;
- внутренним автоматическим устройством для введения растворенного образца с делением потоков и ловушкой пузырьков;
- набивной хроматографической колонкой с карбоксильным катионитом;
________________ В настоящем стандарте используется колонка ВТХ-С (-COONa) производства Biotronic (Германия). Данная информация является рекомендуемой, приведена для удобства пользователей настоящего стандарта и не исключает возможность использования другой аппаратуры с аналогичными свойствами.
- записывающим устройством с компьютерным управлением и автоматической программой обработки хроматографических данных в соответствии с комплектацией жидкостного хроматографа.
Мясорубка механическая по ГОСТ 4025 или электрическая по ГОСТ 20469.
Весы неавтоматического действия по ГОСТ OIML R 76-1 специального или высокого класса точности или весы лабораторные по нормативным документам, действующим на территории государства, принявшего стандарт, с пределами допускаемой абсолютной погрешности не более ±0,001 г.
Баня водяная, обеспечивающая поддержание температуры от 20°С до 100°С, с точностью ±0,5°С.
Холодильник бытовой электрический по ГОСТ 26678.
Часы электронно-механические по ГОСТ 26272.
pH-метр с диапазоном измерений от 0 до 14 ед. pH с пределом допускаемой абсолютной погрешности не более ±0,001 ед. pH.
Термометр по ГОСТ 29224, с диапазоном измерения температуры от 0°С до 150°С и ценой деления 1°С.
Горелка газовая универсальная по ГОСТ 1077.
Испаритель ротационный по ГОСТ 28165.
Банки стеклянные вместимостью 250-500 см.
Пипетки градуированные 1-1-1-1 или 1-2-1-1, 1-1-1-2 или 1-2-1-2, 1-1-1-5 или 1-2-1-5, 1-1-1-10 или 1-2-1-10 по ГОСТ 29227 или дозаторы автоматические с переменным объемом дозирования и относительной погрешностью дозирования не более ±1%.
Колба круглодонная К-1-250-29/32 ТС по ГОСТ 25336.
Колба мерная 2-100-2, 2-1000-2 по ГОСТ 1770.
Колба коническая Кн-1-250-24/29 ТС по ГОСТ 25336.
Цилиндры 1-25, 1-100, 1-500 по ГОСТ 1770.
Стакан В-1-600 ТХС по ГОСТ 25336.
Воронка В-56(75)-80 ХС по ГОСТ 25336.
Ампула стеклянная вместимостью 20 см или пробирка с тефлоновой завинчивающейся крышкой по [1].
Термостат, обеспечивающий поддержание температуры от 20°С до 150°С, с точностью ±0,5°С.
Пробирки пластиковые с крышкой типа "Эппендорф" вместимостью 1 см или 2 см
.
Ступка фарфоровая по ГОСТ 9147.
Фильтр мембранный из политетрафторэтилена с диаметром пор 0,45 мкм.
Флаконы - виалы хроматографические из темного стекла вместимостью 1-2 см.
Аргон газообразный по ГОСТ 10157.
Гелий газообразный (сжатый) высокой чистоты.
Вода дистиллированная по ГОСТ 6709 или вода для лабораторного анализа по ГОСТ ISO 3696 первой степени очистки.
Вода бидистиллированная с электропроводимостю менее 10 мкСм или вода дистиллированная квалификации HPLC.
Кислота соляная по ГОСТ 3118, х.ч.
Натрия ацетат по ГОСТ 199, х.ч.
Кислота муравьиная по ГОСТ 5848, х.ч.
Кислота уксусная по ГОСТ 61, х.ч. ледяная.
Кислота индолпропионовая с массовой долей основного вещества не менее 98%, х.ч.
Кислота тиогликолевая с массовой долей основного вещества не менее 98%, х.ч.
Кислота каприловая с массовой долей основного вещества не менее 98%, х.ч.
Соль динатриевая этилендиаминтетрауксусной кислоты (Трилон Б) по ГОСТ 10652, х.ч.
Натрия гидроокись по ГОСТ 4328, х.ч.
Кислота борная по ГОСТ 9656, х.ч.
Метанол-яд по ГОСТ 6995, х.ч.
Натрий лимоннокислый по ГОСТ 22280, х.ч.
Тиодигликоль (2,2'-тиодиэтанол) с массовой долей основного вещества не менее 98%, х.ч.
Нингидрин с массовой долей основного вещества не менее 98%, х.ч.
Гидридантин гидрат с массовой долей основного вещества не менее 98%, х.ч.
Метилцеллозольв с массовой долей основного вещества не менее 98%, х.ч.
Водорода перекись по ГОСТ 177, медицинская с массовой долей перекиси водорода 30%.
Кислота бромистоводородная по ГОСТ 2062, с массовой долей бромистоводородной кислоты 47%, ч.д.а.
Хлороформ по ГОСТ 20015.
Кислота индолпропионовая с массовой долей основного вещества не менее 98%, х.ч.
Кислота тиогликолевая с массовой долей основного вещества не менее 98%, х.ч.
Стандартные образцы аминокислот: глицина, аланина, валина, лейцина, изолейцина, пролина, фенилаланина, тирозина, метионина, цистеина, аспарагиновой кислоты, глутаминовой кислоты, лизина, аргинина, гистидина, серина, треонина, с содержанием основного вещества не менее 98,0%, х.ч. или стандартный раствор смеси указанных аминокислот молярной концентрации 2,5 мкмоль/см
.
_______________ В настоящем стандарте используется градуировочный раствор смеси аминокислот производства Supelco (США). Данная информация является рекомендуемой, приведена для удобства пользователей настоящего стандарта и не исключает возможности использования другой смеси с аналогичными свойствами.
Допускается применение других средств измерений с метрологическими характеристиками, вспомогательного оборудования с техническими характеристиками не ниже, а также реактивов по качеству не ниже указанных в настоящем стандарте.
7 Отбор и подготовка проб
7.1 Отбор проб проводят по ГОСТ 7269, ГОСТ 9792, ГОСТ 31467.
7.2 Пробу измельчают, дважды пропуская через мясорубку с диаметром отверстий решетки 2-4 мм, и тщательно перемешивают.
7.3 Подготовленную пробу помещают в стеклянную банку вместимостью 250-500 см, закрывают крышкой и хранят при температуре (4±2)°С до окончания испытаний.
Допускается хранить подготовленную пробу в замороженном состоянии при температуре не выше минус 18°С не более 7 сут.
8 Подготовка к измерению
8.1 Приготовление растворов
8.1.1 Приготовление раствора соляной кислоты молярной концентрации c(HCI)=6 моль/дм
В стакан вместимостью 600 см под тягой вносят 100 см
дистиллированной воды и осторожно по каплям прибавляют равный объем (100 см
) концентрированной соляной кислоты.
Раствор хранят в герметично укупоренном сосуде при комнатной температуре в течение 2 мес.
8.1.2 Приготовление воды для хроматографического анализа
Используют дистиллированную воду квалификации HPLC или применяют бидистиллированную воду с электропроводимостью менее 10 мкСм, которую подвергают дополнительной фильтрации через мембранный фильтр с диаметром пор 0,45 мкм. Воду хранят в герметично укупоренном сосуде при комнатной температуре не более 24 ч.
8.1.3 Приготовление буферного раствора А, pH=3,3 ед. pH
8,2 г ацетата натрия вносят в мерную колбу вместимостью 1000 см и растворяют в небольшом количестве дистиллированной воды HPLC (около 600 см
). Добавляют под тягой 3,0 см
муравьиной кислоты, 15,0 см
уксусной кислоты, 100,0 мм
каприловой кислоты и устанавливают pH раствора равным 3,3 ед. pH путем добавления по каплям необходимого дополнительного количества ледяной уксусной кислоты, добавляют 75,0 см
метанола и доводят объем раствора водой до метки. Полученный раствор фильтруют через мембранный фильтр 0,45 мкм. Перед применением буферный раствор деаэрируют с использованием насоса ротационного испарителя путем вакуумирования при 2,0-3,5 кПа в течение 10-15 мин. Допускается использование готового буферного раствора А, поставляемого в комплекте с аминокислотным анализатором.
Раствор хранят в укупоренном сосуде при комнатной температуре не более 6 мес.
8.1.4 Приготовление буферного раствора Б, pH=3,6 ед. pH
8,2 г ацетата натрия вносят в мерную колбу вместимостью 1000 см и растворяют в небольшом количестве дистиллированной воды HPLC (около 600 см
). Добавляют под тягой 3,0 см
муравьиной кислоты, 20,0 см
уксусной кислоты, 100,0 мм
каприловой кислоты и устанавливают pH раствора равным 3,6 ед. pH путем добавления по каплям необходимого дополнительного количества ледяной уксусной кислоты и доводят объем раствора водой до метки. Полученный раствор фильтруют через мембранный фильтр. Перед применением буферный раствор деаэрируют путем вакуумирования при 2,0-3,5 кПа в течение 10-15 мин. Допускается использование готового буферного раствора Б, поставляемого в комплекте с аминокислотным анализатором.
Раствор хранят в герметично укупоренном сосуде при комнатной температуре не более 6 мес.
8.1.5 Приготовление буферного раствора В, pH=4,5 ед. pH
8,2 г ацетата натрия вносят в мерную колбу вместимостью 1000 см и растворяют в небольшом количестве дистиллированной воды HPLC (около 600 см
). Добавляют под тягой 2,0 см
муравьиной кислоты, 1,5 см
уксусной кислоты, 100,0 мм
каприловой кислоты и устанавливают pH раствора равным 4,5 ед. pH путем добавления по каплям необходимого дополнительного количества ледяной уксусной кислоты и доводят объем раствора водой до метки. Полученный раствор фильтруют через мембранный фильтр. Перед применением буферный раствор деаэрируют путем вакуумирования при 2,0-3,5 кПа в течение 10-15 мин. Допускается использование готового буферного раствора В, поставляемого в комплекте с аминокислотным анализатором.
Раствор хранят в герметично укупоренном сосуде при комнатной температуре не более 6 мес.
8.1.6 Приготовление буферного раствора Г, pH=11,0 ед. pH
8,2 г ацетата натрия, 0,5 г динатриевой соли этилендиаминтетраацетата, 6,0 г гидроксида натрия и 2,0 г борной кислоты вносят в мерную колбу вместимостью 1000 см, осторожно растворяют под тягой в небольшом количестве дистиллированной воды HPLC (около 600 см
). Добавляют 1,2 см
муравьиной кислоты, 5,0 см
уксусной кислоты, 100,0 мм
каприловой кислоты, устанавливают pH раствора равным 11,0 ед. pH путем добавления по каплям необходимого дополнительного количества ледяной уксусной кислоты и доводят объем раствора водой до метки. Полученный раствор фильтруют через мембранный фильтр. Перед применением буферный раствор деаэрируют путем вакуумирования при 2,0-3,5 кПа в течение 10-15 мин. Допускается использование готового буферного раствора Г, поставляемого в комплекте с аминокислотным анализатором.
Раствор хранят в герметично укупоренном сосуде при комнатной температуре не более 6 мес.
8.1.7 Приготовление буферного раствора Д, pH=11,0 ед. pH
12,0 г гидроксида натрия вносят в мерную колбу вместимостью 1000 см, осторожно под тягой растворяют в небольшом количестве дистиллированной воды HPLC (около 600 см
). Добавляют 100,0 мм
каприловой кислоты, устанавливают pH раствора равным 11,0 путем добавления по каплям необходимого дополнительного количества каприловой кислоты и доводят объем раствора водой до метки. Полученный раствор фильтруют через мембранный фильтр. Перед применением буферный раствор деаэрируют путем вакуумирования при 2,0-3,5 кПа в течение 10-15 мин. Допускается использование готового буферного раствора Д, поставляемого в комплекте с аминокислотным анализатором.
Раствор хранят в герметично укупоренном сосуде при комнатной температуре не более 6 мес.
8.1.8 Приготовление раствора Е для автоматического аминокислотного анализатора
200,0 см метанола вносят в мерную колбу вместимостью 1000 см
и доводят объем раствора до метки дистиллированной водой HPLC. Полученный раствор фильтруют через мембранный фильтр 0,45 мкм. Перед применением буферный раствор деаэрируют путем вакуумирования при 2,0-3,5 кПа в течение 10-15 мин. Допускается использование готового раствора Е, поставляемого в комплекте с аминокислотным анализатором.
Раствор хранят в герметично укупоренном сосуде при комнатной температуре не более одного года.
8.1.9 Приготовление буферного раствора для растворения проб, pH=2,2 ед. pH
9,8 г цитрата натрия вносят в мерную колбу вместимостью 1000 см, растворяют в небольшом количестве дистиллированной воды HPLC (около 600 см
), осторожно под тягой добавляют 8,3 см
концентрированной соляной кислоты, 1,0 см
тиодигликоля, 50,0 мм
каприловой кислоты, устанавливают pH раствора равным 2,2 ед. pH путем добавления по каплям необходимого дополнительного количества соляной кислоты и доводят объем раствора водой до метки. Полученный раствор фильтруют через мембранный фильтр. Допускается использование готового буферного раствора для растворения проб pH=2,2 ед. pH, поставляемого в комплекте с аминокислотным анализатором.
Раствор хранят в герметично укупоренном сосуде при комнатной температуре не более 6 мес.
8.1.10 Приготовление ацетатного буферного раствора, pH=4,8 ед. pH
2 г гидроксида натрия вносят в мерную колбу вместимостью 1000 см, осторожно под тягой растворяют в небольшом количестве дистиллированной воды HPLC (около 600 см
), добавляют 14,0 см
ледяной уксусной кислоты, устанавливают pH раствора равным 4,8 ед. pH путем добавления по каплям необходимого дополнительного количества уксусной кислоты и доводят объем раствора водой до метки. Полученный раствор фильтруют через мембранный фильтр. Раствор хранят в герметично укупоренном сосуде в холодильнике при температуре 4°С не более 6 мес.
8.1.11 Приготовление нингидринового раствора Ж для фотометрической идентификации аминокислот в автоматическом аминокислотном анализаторе
15,0 г нингидрина, 0,55 г гидридантин гидрата, 10 см метилцеллозольва вносят в мерную колбу вместимостью 1000 см
, добавляют 100 см
метанола, перемешивают в колбе до полного растворения и доводят объем раствора до метки ацетатным буферным раствором с pH=4,8 ед. pH. Полученный раствор фильтруют через мембранный фильтр. Перед применением буферный раствор деаэрируют путем вакуумирования при 2-3,5 кПа в течение 10-15 мин. Допускается использование готового нингидринового раствора Ж, поставляемого в комплекте с аминокислотным анализатором.
Раствор хранят в герметично укупоренном сосуде в холодильнике при температуре 4°С не более 2 мес.
8.1.12 Приготовление надмуравьиной кислоты для окисления серосодержащих аминокислот
В мерной колбе вместимостью 100 см смешивают 10 см
30%-ного пероксида водорода с 90 см
муравьиной кислоты. Смесь охлаждают до температуры 4°С и выдерживают в холодильнике в течение 45 мин (для проведения реакции).
Раствор готовят непосредственно перед проведением анализа.
8.1.13 Приготовление градуировочного раствора смеси аминокислот
Применяют готовый раствор, содержащий 2,5 мкмоль каждой аминокислоты в 1 см раствора, или готовят градуировочный раствор аминокислот. Для этого в мерной колбе вместимостью 1000 см
в небольшом количестве (около 600 см
) буферного раствора pH=2,2 ед. pH растворяют 0,19 г глицина, 0,22 г аланина, 0,29 г валина, 0,33 г лейцина, 0,33 г изолейцина, 0,29 г пролина, 0,41 г фенилаланина, 0,45 г тирозина, 0,37 г метионина, 0,31 г цистеина, 0,33 г аспарагиновой кислоты, 0,37 г глутаминовой кислоты, 0,37 г лизина, 0,44 г аргинина, 0,39 г гистидина, 0,26 г серина и 0,3 г треонина и доводят объем раствора до метки этим же буферным раствором. Полученный раствор фильтруют через мембранный фильтр. Перед применением раствор деаэрируют путем вакуумирования при 2,0-3,5 кПа в течение 10-15 мин.
Раствор хранят в герметично укупоренном сосуде в холодильнике при температуре 4°С не более 2 мес.
Примечание - При использовании смеси аминокислот целесообразно для последующей хроматографической идентификации использовать стандартные растворы различной концентрации. Величина оптимальной концентрации для достаточного сигнала регистрации на экране устанавливается экспериментально для конкретного типа хроматографа. Хорошая идентификация пиков на фотометрическом детекторе аминокислотного анализатора наблюдается при получении выходного сигнала более 50 мВ с общей интенсивностью сигнала до 1000 мВ.
8.2 Гидролиз белков и приготовление раствора пробы
8.2.1 Для снижения влияния на результат анализа липидных примесей пробу продукта подвергают обезжириванию хлороформом в аппарате Сокслета по ГОСТ 23042. Обезжиренную пробу измельчают, растирая в ступке до получения однородного порошка.
8.2.2 Обезжиренную пробу массой 0,05 г, взвешенную с погрешностью не более ±0,001 г, помещают в ампулу вместимостью 20 см, заливают 5 см
раствора соляной кислоты молярной концентрации 6 моль/дм
, троекратно вакуумируют содержимое ампулы под вакуумом на ротационном испарителе до начала закипания раствора и заполняют верхнюю внутреннюю часть ампулы аргоном таким образом, чтобы максимально заместить воздушный слой над раствором на аргон. Наличие остатков кислорода способствует разрушению при гидролизе серосодержащих и некоторых других аминокислот, для стабилизации которых дополнительно вносят в пробу гидролизата несколько кристалликов индолпропионовой или тиогликолевой кислоты
.
________________ Указанные вещества вносят при необходимости проведения точного количественного содержания метионина и цистеина.
Ампулу герметично запаивают на горелке. Допускается проводить гидролиз в герметично укупориваемой пробирке с тефлоновой завинчивающейся крышкой, удерживающей давление паров соляной кислоты, и боковым отводом в соответствии с [1].
Ампулу или укупоренную пробирку помещают в термостат и выдерживают смесь в течение 24 ч при температуре 110°С.
8.2.3 Для удаления избытка соляной кислоты гидролизат количественно переносят в круглодонную колбу вместимостью 250 см, упаривают досуха на ротационном испарителе, добавляют 20 см
дистиллированной воды и упаривают под вакуумом при 2,0-3,5 кПа досуха для удаления избытка соляной кислоты при температуре 60°С. Операцию повторяют трижды.
Освобожденный от соляной кислоты гидролизат растворяют в 5 см буферного раствора pH=2,2 ед. pH.
0,5 см раствора пробы переносят в виалу для помещения в штатив автоматического устройства введения анализируемой пробы.
8.2.4 Для точного определения цистеина и метионина применяют предварительное окисление. Для этого обе аминокислоты необходимо превратить в устойчивую окисленную форму до гидролиза. В ходе окисления из цистеина образуется цистеиновая кислота, а из метионина и метионин сульфоксида образуется метионин сульфон.
Примечание - Важно, что в ходе окисления полностью разлагается тирозин и частично гистидин.
Для проведения процесса окисления в колбу с притертой пробкой вместимостью 250 см вносят 35 мг белоксодержащей пробы, добавляют 100 см
надмуравьиной кислоты, закрывают пробкой, перемешивают до растворения пробы и выдерживают в холодильнике в течение 15 ч при температуре 4°С. Избыток надмуравьиной кислоты разрушают осторожным, по капле, добавлением 12 см
бромистоводородной кислоты. Раствор переносят в колбу ротационного испарителя вместимостью 250 см
, упаривают досуха под вакуумом при 2-3 кПа при температуре бани 50°С, добавляют 20 см
воды и дважды повторяют упаривание досуха.
К сухому остатку добавляют 3 см буферного раствора pH=2,2 ед. pH и анализируют цистеин и метионин на аминокислотном анализаторе.
9 Проведение измерений
9.1 Хроматографические условия измерений
В соответствии с инструкцией по эксплуатации аминокислотного анализатора проводят его включение, устанавливая в случае необходимости давление инертного газа на входном манометре хроматографа 5 МПа. В соответствии с характеристиками хроматографа задают программируемый метод анализа.
9.2 Условия измерений с фотометрическим детектором
Для хроматографа с фотометрическим детектором и набивной колонкой с катионитом выставляют параметры: канал 1 с длиной волны 440 нм, канал 2 с
570 нм, температура колонки в термостате 47°С; температура нингидринового реактора 125°С; рабочее давление 1,6 МПа, поток гелия - 1 см
/мин; поток элюента 0,2 см
/мин, время анализа 90 мин. Подача элюента осуществляется по капиллярным шлангам высокого давления с внутренним диаметром 0,2 мм, ввод 20 мм
пробы.
В автоматическом аминокислотном анализаторе реализуется следующая программа подачи элюентов, которая уточняется под конкретный тип анализатора (таблица 1).
________________
В настоящем стандарте используется автоматический аминокислотный анализатор LC3000 Biotronic. Данная информация является рекомендуемой, приведена для удобства пользователей настоящего стандарта и не исключает возможности использования других средств измерений с аналогичными свойствами.
Таблица 1
Этап, N | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
Время, мин | 5,6 | 11,0 | 3,0 | 2,0 | 9,0 | 6,5 | 11,0 | 9,0 | 15,0 | 0,1 | 8,0 | 4,0 | 6,5 | 0,5 |
Ввод пробы | - | x | - | - | - | - | - | - | - | - | - | - | - | - |
Раствор З | x | x | x | x | x | x | x | x | x | - | - | - | - | - |
Буфер А | x | x | - | - | - | - | - | - | - | - | - | x | x | x |
Буфер Б | - | - | x | x | - | - | - | - | - | - | - | - | ||
Буфер В | - | - | - | - | x | x | - | - | - | - | - | - | - | - |
Буфер Г | - | - | - | - | - | - | x | x | x | - | - | - | - | - |
Буфер Е | - | - | - | - | - | - | - | - | - | x | x | - | - | - |
Температура колонки, °С | 47 | 47 | 48 | 48 | 49 | 50 | 52 | 56 | 60 | 60 | 70 | 70 | 55 | 47 |
Поток, см | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,3 | 0,2 | 0,2 |
Через каждые 50-100 анализов и по мере необходимости, когда рабочее давление возрастает, через анализатор пропускают последовательно в течение 10 мин буферные растворы А и Д, дистиллированную воду, раствор Е, дистиллированную воду.
Для промывки шприца в автосамплере и очистки колонки применяют последовательное введение буферных растворов А, Д и раствора Е.
До определения анализируемых проб проводят калибровку. Для этого в хроматограф в автоматическом режиме в соответствии с заданной программой вводят 1 мм стандартного раствора аминокислот с концентрацией 2,5 мкмоль/см
в буферном растворе pH=2,2 ед. pH.
В таблицу автоматического обсчета результатов анализа вносят установленные времена выхода пиков для каждой аминокислоты с отклонением ±0,2 мин. Калибровку проверяют и сверяют с ранее полученными калибровками ежедневно, а также после выполнения подряд более десяти анализов.
Для уточнения времени выхода пика для отдельной аминокислоты используют метод введения добавки. Для этого в раствор пробы вносят известную концентрацию конкретной аминокислоты, превышающую в 3-5 раз уровень ее содержания в пробе, и проводят хроматографирование, устанавливая время выхода нового более интенсивного пика, соответствующее времени выхода введенной аминокислоты.
Для анализа проб с низким, менее 10 мг/кг, содержанием аминокислот проводят хроматографирование с использованием концентрирования раствора в 2-10 раз.
Допускается использование других хроматографических условий, обеспечивающих разделение компонентов пробы.
9.3 Градуировка системы
Приготовленный по 8.1.13 градуировочный раствор подвергают анализу в условиях, выбранных в соответствии с 9.1, 9.2. Для каждого уровня анализируют по три параллельные пробы. Полученные хроматограммы обрабатывают с использованием компьютерной системы обработки данных. Определяют абсолютное время удерживания целевых веществ. С использованием средств программного обеспечения строят градуировочную зависимость площади пика определяемых веществ от концентрации аналита в пробе.
Коэффициент линейной корреляции полученной градуировочной зависимости должен быть не менее 0,99. При невыполнении этого условия выясняют причины, приводящие к неудовлетворительным результатам, и устраняют их. В случае необходимости готовят новые градуировочные растворы.
Проведение градуировки обязательно при замене хроматографической колонки, а также при систематическом получении неудовлетворительных результатов контроля, выполняемого в соответствии с разделом 12.
9.4 Контроль аналитической системы
Контроль выполняют с использованием приготовленных по 8.1.13 градуировочных растворов аминокислот концентрацией 2,5 мкмоль/см.
Полученный результат определения не должен отличаться от действительного значения концентрации определяемых веществ в градуировочном растворе более чем на 3%, относительное стандартное отклонение времени удерживания аналитов не более чем на 5%. В случае невыполнения указанного критерия стабильности градуировочной характеристики проводят новую градуировку.
Контроль аналитической системы осуществляется при условиях, указанных в 9.1, 9.2 перед началом проведения измерений, а также при смене хроматографической колонки, чистке блоков аналитического прибора и т.д.
9.5 Выполнение измерений
В виалы анализатора вместимостью 1-2 см вносят 0,5 см
подготовленной по 8.2 пробы и дважды определяют в анализаторе массовые доли аминокислот при условиях, указанных в 9.1, 9.2.
Виалы с определяемой пробой устанавливают в поворачивающийся штатив автоматического термостатированного инжектора. Ввод пробы осуществляется в соответствии с программой в хроматографическую колонку с ионообменником с карбоксильными ионогенными группами в Nа-форме. Разделение аминокислот происходит автоматически. После разделительной колонки раствор поступает в реактор для проведения цветной реакции с нингидриновым раствором, что позволяет получить фоточувствительный комплекс аминокислот, окрашенный в синий цвет. Его анализируют автоматически в УФ детекторе при 570 нм, пролин и оксипролин - при 440 нм.
Определение индивидуальных аминокислот осуществляют по абсолютным временам удерживания и относительной интенсивности пиков.
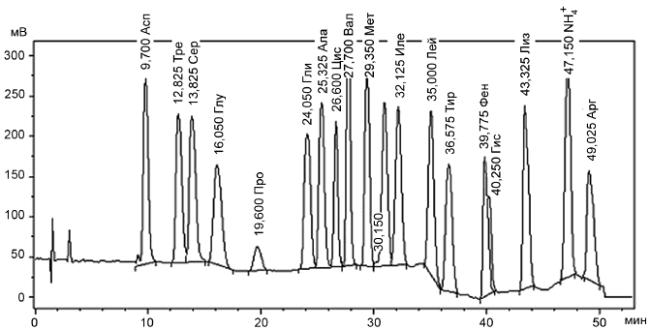
На рисунке Б.1 (приложение Б) приведена хроматограмма аминокислот с концентрацией 2 мкмоль/см.
По значению площади хроматографического пика с использованием установленной градуировочной характеристики и программы обработки данных находят массовую концентрацию аминокислот в анализируемом растворе.
Вычисление массовой доли аналита в анализируемой пробе гидролизата проводят для каждого из двух параллельных определений.
10 Обработка результатов
10.1 В соответствии с данными, полученными при анализе градуировочных растворов, создают таблицу пиков с использованием программного обеспечения. Расчеты содержания аминокислоты и площади пика выполняются системой обработки данных в автоматическом режиме.
10.2 Массовую долю индивидуальной аминокислоты X, мг/кг, вычисляют по формуле
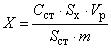 , (1)
, (1)
где - массовая концентрация индивидуальной аминокислоты в градуировочном растворе, мкг/см
;
- площадь пика индивидуальной аминокислоты в анализируемой пробе, усл. ед.;
- объем раствора для растворения аналита после пробоподготовки, см
;
- площадь пика индивидуальной аминокислоты в градуировочном растворе, усл. ед.;
т - масса пробы, г.
За окончательный результат принимают среднеарифметическое значение двух параллельных определений, округленное до второго десятичного знака.
Примечания
1 Результат выражают в мг/кг, что равнозначно получаемой по формуле (1) размерности мкг/г.
2 Для сопоставления полученной величины массовой доли аминокислоты с международными таблицами данных содержания аминокислот в белках полученный результат выражают в г/100 г белка. При этом содержание белка в анализируемой пробе предварительно определяют по ГОСТ 25011 (по методу Къельдаля).
Пример записи типичного аминокислотного состава белка животного происхождения приведен в приложении В.
11 Метрологические характеристики
11.1 Метрологические характеристики метода при доверительной вероятности Р=0,95 приведены в таблице 2.
Таблица 2
Наименование | Диапазон измерений массовой доли аминокислоты, мг/кг | Границы относительной погрешности | Предел | Предел |
Массовая доля аминокислоты | До 50 включ. | 27 |
|
|
Св. 50 до 1000 включ. | 16 |
|
| |
Примечание - |
|
Примечание - Нижний предел обнаружения аминокислот животного происхождения определяется индивидуальной чувствительностью применяемого датчика. Для использованных детекторов он соответствует концентрации (0,500±0,006) мкмоль/см в анализируемом растворе.
11.2 Расхождение между результатами двух параллельных определений, отражаемых в акте испытаний и выполненных одним оператором при анализе одной и той же пробы с использованием одних и тех же средств измерений и реактивов, не должно превышать предела повторяемости (сходимости) r, значения которого приведены в таблице 2.
В случае приемлемости результатов измерений при доверительной вероятности Р=0,95 должно соблюдаться условие
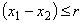 , (2)
, (2)
где и
- результаты параллельных измерений, мг/кг;
r - предел повторяемости, мг/кг.
11.3 Расхождение между результатами двух определений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости R, значения которого приведены в таблице 2.
В случае приемлемости результатов измерений при доверительной вероятности Р=0,95 должно соблюдаться условие
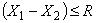 , (3)
, (3)
где и
- результаты двух определений, выполненных в разных лабораториях, мг/кг;
R - предел воспроизводимости, мг/кг.
11.4 Границы относительной погрешности (), находящиеся с доверительной вероятностью Р=0,95, при соблюдении условий настоящего стандарта, не должны превышать значений, приведенных в таблице 2.
12 Контроль точности результатов измерений
12.1 Процедуру контроля стабильности результатов определений (повторяемости, промежуточной прецизионности и погрешности) проводят в соответствии с порядком, установленным в лаборатории, по ГОСТ ИСО 5725-6.
12.2 Проверку приемлемости результатов определений, полученных в условиях повторяемости (сходимости), осуществляют в соответствии с требованиями ГОСТ ИСО 5725-2. Расхождение между результатами определений не должно превышать предела повторяемости (r). Значения r приведены в таблице 2.
12.3 Проверку приемлемости результатов определений, полученных в условиях воспроизводимости, проводят с учетом требований ГОСТ ИСО 5725-2. Расхождение между результатами определений, полученными двумя лабораториями, не должно превышать предела воспроизводимости (R). Значения R приведены в таблице 2.
Приложение А (справочное). Перечень и систематическое международное наименование аминокислот животного происхождения
Приложение А
(справочное)
А.1 Перечень и систематическое международное наименование аминокислот животного происхождения приведены в таблице А.1.
Таблица А.1
Наименование | Систематическое международное наименование | Обозначение | |
Глицин | Glycine | Гли | Gly |
Аланин | Alanine | Ала | Ala |
Валин* | Valine | Вал | Val |
Лейцин* | Leucine | Лей | Leu |
Изолейцин* | Isoleucine | Иле | lle |
Пролин | Proline | Про | Pro |
Фенилаланин* | Phenylalanine | Фен | Phe |
Тирозин | Tyrozine | Тир | Tyr |
Метионин* | Methionine | Мет | Met |
Цистеин | Cystein | Цис | Cys |
Аспарагиновая кислота | Aspartic acid | Асп | Asp |
Аспарагин | Asparagine | Асн | Asn |
Глутаминовая кислота | Glutamic acid | Глу | Glu |
Глутамин | Glutamine | Глн | Gln |
Лизин* | Lysine | Лиз | Lys |
Аргинин | Arginine | Apг | Arg |
Гистидин | Histidine | Гис | His |
Серин | Serine | Сер | Ser |
Треонин* | Threonine | Тре | Thr |
* Незаменимые аминокислоты. |
Примечание - Триптофан в аминокислотам анализе не определяют вследствие его разрушения кислотой. Глутамин определяется в составе глутаминовой кислоты, аспарагин - в составе аспарагиновой кислоты.
Приложение Б (справочное). Хроматограмма аминокислот с концентрацией 2 мкмоль/куб.см
Приложение Б
(справочное)
Хроматограмма аминокислот с концентрацией 2 мкмоль/см
Б.1 Хроматограмма аминокислот с концентрацией 2 мкмоль/см приведена на рисунке Б.1.
Рисунок Б.1 - Хроматограмма аминокислот с концентрацией 2 мкмоль/куб.см
|
Рисунок Б.1 - Хроматограмма аминокислот с концентрацией 2 мкмоль/см
Приложение В (справочное). Пример записи типичного аминокислотного состава животного белка
Приложение В
(справочное)
В.1 Пример записи типичного аминокислотного состава животного белка в г/100 г белка:
Asp - 9.2; Thr - 3,5; Ser - 3,6; Glu - 19,6; Pro - 3,7; Gly - 6,0; Ala - 5,2; Cys - 2,1; Val - 4,9; Met - 2,9; lley - 3,6; Ley - 6,2; Tyr - 3,9; Phe - 3,7; His - 3,8; Lys - 7,5; Arg - 7,7.
Всего 97,4 г/100 г белка.
Библиография
[1] | Патент RU N 128878 U1 | Устройство для гидролиза животного белка в составе пищевых продуктов |
УДК 547:637.5.04/.07:006.354 | МКС 67.120.10 |
Ключевые слова: мясо, мясные продукты, мясосодержащие продукты, белок, состав, аминокислоты, определение, хроматографический метод |
Электронный текст документа
и сверен по:
официальное издание
М.: Стандартинформ, 2017