ГОСТ Р ИСО 21535-2020
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Имплантаты хирургические неактивные
ИМПЛАНТАТЫ ДЛЯ ЗАМЕНЫ СУСТАВОВ
Специальные требования к имплантатам для протезирования тазобедренного сустава
Non-active surgical implants. Joint replacement implants. Specific requirements for hip-joint replacement implants
ОКС 11.040.40
Дата введения 2021-05-01
Предисловие
1 ПОДГОТОВЛЕН Обществом с ограниченной ответственностью "Центр сертификации и декларирования" (ООО "ЦСД") и Обществом с ограниченной ответственностью "ЦИТОпроект" (ООО "ЦИТОпроект") на основе официального перевода на русский язык англоязычной версии указанного в пункте 4 стандарта, который выполнен Федеральным государственным унитарным предприятием "Российский научно-технический центр по стандартизации, метрологии и оценке соответствия" (ФГУП "")
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 453 "Имплантаты в хирургии"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 6 ноября 2020 г. N 988-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 21535:2007* "Неактивные хирургические имплантаты. Имплантаты для замены суставов. Специальные требования к имплантатам для протезирования тазобедренного сустава", включая изменения и техническую поправку Amd. 1:2016 (ISO 21535:2007/Amd. 1:2016 "Non-active surgical implants - Joint replacement implants - Specific requirements for hip-joint replacement implants", IDT).
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты, сведения о которых приведены в дополнительном приложении ДА
5 ВЗАМЕН ГОСТ Р ИСО 21535-2013
Правила применения настоящего стандарта установлены в статье 26 Федерального закона от 29 июня 2015 г. N 162-ФЗ "О стандартизации в Российской Федерации". Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе "Национальные стандарты", а официальный текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
Введение
Международная организация по стандартизации (ИСО) является Всемирной федерацией национальных организаций по стандартизации (комитетов - членов ИСО). Разработку международных стандартов, как правило, осуществляют технические комитеты ИСО. Каждый комитет-член, заинтересованный в деятельности, для которой создан технический комитет, имеет право быть представленным в этом комитете. Международные правительственные и неправительственные организации, взаимодействующие с ИСО, также принимают участие в работах.
По вопросам стандартизации в области электротехники ИСО работает в тесном сотрудничестве с Международной электротехнической комиссией (МЭК).
Процедуры, использованные для разработки настоящего стандарта, и процедуры, предназначенные для его дальнейшего использования, представлены в Директивах ИСО/МЭК, часть 1, в частности: следует отметить различные критерии принятия для разных типов документов ИСО. Настоящий стандарт составлен в соответствии с редакционными правилами Директив ISO/IEC, часть 2 (см. www.iso.org/directives).
Необходимо учитывать, что некоторые элементы настоящего стандарта могут быть объектом патентных прав. ИСО не может нести ответственность за идентификацию одного или всех патентных прав. Подробная информация о патентных правах, выявленных при разработке настоящего стандарта, будет представлена во введении и/или в списке полученных патентных деклараций ИСО (см. www.iso.org/patents).
Любое торговое наименование, используемое в настоящем стандарте, является информацией, предоставленной для удобства пользователей, и не означает ее одобрения.
Для объяснения значения определенных терминов и выражений ИСО, относящихся к оценке соответствия, а также к информации о приверженности ИСО принципам ВТО в Технических барьерах в торговле (ТВТ) представлен ресурс URL: www.iso.org/iso/foreword.html.
Комитетом, ответственным за настоящий стандарт, является ISO/TC 150 "Имплантаты хирургические", подкомитет SC 4 "Заменители костей и суставов".
1 Область применения
Настоящий стандарт устанавливает специальные требования к имплантатам для протезирования тазобедренного сустава. В отношении безопасности настоящий стандарт устанавливает требования к показателям назначения, особенностям конструкции, материалам, оценке конструкции, производству, стерилизации, упаковке и информации, предоставляемой изготовителем, а также к методам испытаний.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты. Для датированных ссылок применяют только указанное издание ссылочного стандарта, для недатированных ссылок - последнее издание (включая все изменения).
ISО 7206-1, Iplants for surgery - Partial and total hip-joint prostheses - Part 1: Classification and designation of dimensions (Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 1. Классификация и обозначение размеров)
ISО 7206-2, Implants for surgery - Partial and total hip-joint prostheses - Part 2: Articulating surfaces made of metallic, ceramic and plastics materials (Импланты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 2. Суставные поверхности, изготовленные из металлических, керамических и полимерных материалов)
ISО 7206-4, Implants for surgery - Partial and total hip-joint prostheses - Part 4: Determination of endurance properties and performance of stemmed femoral components (Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 4. Определение прочности и эксплуатационных качеств бедренных компонентов с ножкой)
ISО 7206-6, Implants for surgery - Partial and total hip-joint prostheses - Part 6: Determination of endurance properties of head and neck region of stemmed femoral components (Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 6. Определение прочностных свойств области шейки и головки бедренных компонентов)
ISО 7206-10, Implants for surgery - Partial and total hip-joint prostheses - Part 10: Determination of resistance to static load of modular femoral heads (Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 10. Определение сопротивления статической нагрузке модульных бедренных головок)
ISО 14242-1, Implants for surgery - Wear of total hip-joint prostheses - Part 1: Loading and displacement parameters for wear-testing machines and corresponding environmental conditions for test (Имплантаты для хирургии. Износ тотальных эндопротезов тазобедренного сустава. Часть 1. Параметры нагружения и перемещения для испытательных машин и условия окружающей среды при испытании)
ISO 14242-2, Implants for surgery - Wear of total hip-joint prostheses - Part 2: Methods of measurement (Имплантаты для хирургии. Износ тотальных эндопротезов тазобедренного сустава. Часть 2. Методы измерений)
ISO 14242-3, Implants for surgery - Wear of total hip-joint prostheses - Part 3: Loading and displacement parameters for orbital bearing type wear testing machines and corresponding environmental conditions for test (Имплантаты для хирургии. Износ тотальных эндопротезов тазобедренного сустава. Часть 3. Параметры нагружения и перемещения машин для испытания на износ орбитальных опор и условия окружающей среды при испытании)
ISO 14630:2012, Non-active surgical implants - General requirements (Имплантаты хирургические неактивные. Общие требования)
ISO 21534:2007, Non-active surgical implants - Joint replacement implants - Particular requirements (Имплантаты хирургические неактивные. Имплантаты для замены суставов. Частные требования)
3 Термины и определения
В настоящем стандарте применены термины по ИСО 21534:2007 и ИСО 7206-1, а также следующие термины с соответствующими определениями:
3.1 вертлужный компонент: Имплантат, предназначенный для фиксации в подготовленной биологической вертлужной впадине.
Примечание - Этот компонент может иметь моноблочную или модульную конструкцию.
3.2 биполярная головка: Компонент протеза тазобедренного сустава, имеющий вогнутую (внутреннюю) поверхность, предназначенную для сочленения со сферической головкой бедренного компонента, и выпуклую (внешнюю) сферическую поверхность, предназначенную для сочленения с биологической вертлужной впадиной.
3.3 бедренный компонент: Элемент тотального или частичного протеза тазобедренного сустава, который предназначен для прикрепления к бедренной кости.
3.4 протезирование тазобедренного сустава, артропластика тазобедренного сустава: Имплантат, используемый для протезирования одной или обеих суставных поверхностей тазобедренного сустава.
3.5 модульный компонент: Бедренный или вертлужный компонент, который собирается пользователем из нескольких деталей.
3.6 моноблочный компонент: Бедренный или вертлужный компонент, который поставляется как единая конструкция.
3.7 частичное протезирование тазобедренного сустава, гемиартропластика тазобедренного сустава: Имплантат, состоящий из бедренного компонента, предназначенного для протезирования бедренной суставной поверхности тазобедренного сустава.
Примечание 1 - Имплантаты для частичного протезирования тазобедренного сустава могут иметь как биполярную, так и монополярную головку.
Примечание 2 - Этот компонент может иметь моноблочную или модульную конструкцию.
3.8 тотальное протезирование тазобедренного сустава, тотальная артропластика тазобедренного сустава: Имплантат, состоящий из бедренного и вертлужного компонентов, предназначенных для протезирования обеих суставных поверхностей тазобедренного сустава.
Примечание - Этот компонент может иметь моноблочную или модульную конструкцию.
3.9 монополярная головка: Головка бедренного компонента, предназначенная для сочленения с биологической вертлужной впадиной.
4 Показатели назначения
Требования раздела 4 ИСО 21534:2007 применяют совместно с указанными ниже требованиями.
Диапазон угловых движений между бедренным и вертлужным компонентами должен иметь следующие минимальные значения:
- 100° - при сгибании/разгибании;
- 60° - при отведении/приведении;
- 90° - при вращении внутрь/наружу.
Примечание - Метод, с помощью которого проводят данное измерение, описан в приложении А.
5 Особенности конструкции
5.1 Общие положения
Требования раздела 5 ИСО 21534:2007 применяют совместно с требованиями, установленными в 5.2 и 5.3.
5.2 Размеры и допуски
Примечание - Относительно требований к суставным поверхностям типа "металл по металлу" и "керамика по керамике" еще не получено достаточного количества информации о шероховатости поверхности и допусках на диаметр и размеры, чтобы предоставить спецификацию для этих параметров в настоящем стандарте.
5.2.1 Допуски и размеры конусных соединений
Необходимо учитывать, как минимум, следующие аспекты: диаметр, угол конусности, прямолинейности, округлости, микроскопическую и макроскопическую структуру поверхности.
В тех конструкциях, в которых использованы модульные бедренные компоненты, следует учитывать риск образования частиц износа и развития коррозии на поверхностях модульного компонента.
5.2.2 Допуски на диаметр суставных поверхностей
Допуски на диаметр суставных поверхностей металлических или керамических бедренных компонентов, предназначенных для использования с вертлужными компонентами из полиэтилена сверхвысокой молекулярной массы (СВМПЭ), должны соответствовать ИСО 7206-2.
5.2.3 Сферичность головок бедренных костей и полиэтиленовых компонентов вертлужной впадины
Для головок бедренных костей тотального эндопротезирования тазобедренного сустава и полиэтиленовых компонентов вертлужной впадины сферичность должна соответствовать требованиям, приведенным в ИСО 7206-2.
5.2.4 Поверхностная отделка головок бедренных костей и полиэтиленовых компонентов вертлужной впадины
Для головок бедренных костей тотального эндопротезирования тазобедренного сустава и полиэтиленовых компонентов вертлужной впадины отделка поверхности должна соответствовать требованиям, приведенным в ИСО 7206-2.
5.3 Толщина СВМПЭ в вертлужных компонентах и биполярных головках
5.3.1 Вертлужные компоненты
Для вертлужных компонентов с внешним диаметром 42 мм и более компонент, изготавливаемый из СВМПЭ, должен иметь следующую минимальную толщину нагружаемого сектора:
a) 5 мм - для компонентов с металлической или иной подложкой;
b) 6 мм - для компонентов без подложки.
5.3.2 Биполярные головки
Для биполярных головок с внешним диаметром (W)44 мм минимальная толщина выстилки из СВМПЭ должна составлять 5 мм.
Примечание - В тех случаях, когда размеры костей в той популяции, для которой предназначены эти имплантаты, требуют, чтобы диаметр вертлужного компонента составлял менее 42 мм, а диаметр биполярного компонента менее 44 мм, может потребоваться использовать значения толщины меньше указанных.
6 Материалы
Требования раздела 6 ИСО 21534:2007 применяют совместно с указанными ниже требованиями.
Нелегированный титан и титановые сплавы не следует использовать для суставных поверхностей тотальных протезов тазобедренного сустава, кроме тех случаев, когда проведена надлежащая обработка поверхности и подтверждена ее пригодность для использования в клинической практике.
7 Оценка конструкции
7.1 Общие положения
Требования раздела 7 ИСО 21534:2007 применяют совместно с указанными ниже требованиями. Возможны ситуации, когда одно или несколько испытаний, предусмотренных 7.2 ИСО 21534:2007, не требуются:
a) для каждого компонента среди линейки компонентов (в семействе продуктов);
b) в тех случаях, когда уже имеются результаты необходимого испытания, полученные для аналогичного или подобного компонента.
В этих случаях необходимо документально зафиксировать обоснование непрохождения конкретного испытания в отношении конкретного компонента.
7.2 Доклиническая оценка
7.2.1 Испытание бедренных компонентов на прочность
Испытание ножки бедренной кости эндопротеза тазобедренного сустава следует проводить в соответствии с эксплуатационными требованиями, приведенными в ИСО 7206-4.
7.2.2 Испытание прочности шейного отдела стволовых компонентов бедренной кости следует проводить в соответствии с эксплуатационными требованиями, приведенными в ИСО 7206-6.
7.2.3 Параметры фиксации бедренной головки
Применяют требования соответствующих пунктов ИСО 7206-10.
7.2.4 Испытание тотальных протезов тазобедренного сустава на износ
Характеристики износа при тотальных эндопротезах тазобедренного сустава, состоящих из бедренного компонента с неотъемлемой головкой или модульной головкой, сочленяющейся с металлическим, керамическим или СВМПЭ вертлужным компонентом, должны испытываться в соответствии с ИСО 14242-1 или ИСО 14242-3, а степень износа должна быть измерена в соответствии с ИСО 14242-2. Область шейки бедренных компонентов с ножкой должна испытываться и соответствовать эксплуатационным требованиям, приведенным в ИСО 7206-6.
Примечание - Для имитации неблагоприятных или других клинически значимых условий могут потребоваться дополнительные испытания на износ. Возможные методы испытаний включены в библиографию.
7.2.5 Минимальные и максимальные углы
Определение предусмотренных минимальных и максимальных углов между частями скелета, упоминаемых в перечислении а) раздела 4 ИСО 21534:2007, следует осуществлять в соответствии с процедурой, описанной в приложении А.
8 Производство
Требования раздела 8 ИСО 21534:2007 применяют совместно с указанными ниже требованиями:
- имплантаты, производимые из литейных кобальто-хромовых сплавов, при необходимости следует подвергать обработке раствором;
- любую проведенную термическую обработку следует документально фиксировать.
Примечание - Один сеанс удовлетворяющей требованиям термической обработки раствором позволяет удерживать литую заготовку на протяжении 4 ч при температуре 1200°С.
9 Стерилизация
Применяют требования раздела 9 ИСО 14630:2012.
10 Упаковка
Применяют требования раздела 10 ИСО 14630:2012.
11 Информация, предоставляемая производителем
11.1 Общие положения
Требования раздела 11 ИСО 14630:2012 и раздела 11 ИСО 21534:2007 применяют совместно с указанными ниже требованиями.
11.2 Размеры
На этикетке, листке-вкладыше с инструкцией или в руководстве по использованию должна быть указана следующая информация:
a) тип изделия;
b) номинальный диаметр головки (см. ИСО 7206-1) для моноблочного бедренного компонента протеза тазобедренного сустава или для модульного протеза головки бедренной кости (на этикетке, в листке-вкладыше с инструкцией и/или в руководстве по использованию);
c) номинальный диаметр (см. ИСО 7206-1) суставной поверхности вертлужного компонента (на этикетке, в листке-вкладыше с инструкцией и/или в руководстве по использованию);
d) символы, по которым следует ориентироваться при соединении головки и шейки модульного имплантата (в листке-вкладыше с инструкцией и/или в руководстве по использованию).
11.3 Структурная и функциональная совместимость компонентов
11.3.1 Для бедренных компонентов или модульных протезов головки бедренной кости, предназначенных для структурной и функциональной совместимости исключительно с определенными вертлужными чашками, на этикетке, в листке-вкладыше с инструкцией или в руководстве по использованию должна быть указана информация о совместимых вертлужных чашках.
11.3.2 Для вертлужных компонентов, предназначенных для структурной и функциональной совместимости исключительно с определенными бедренными компонентами, на этикетке, в листке-вкладыше с инструкцией или в руководстве по использованию должна быть указана информация о совместимых бедренных компонентах.
11.3.3 Для каждого бедренного компонента и протеза головки, имеющего модульную конструкцию, на этикетке, в листке-вкладыше с инструкцией или в руководстве по использованию должна быть указана информация о соответствующем компоненте, с которым они структурно и функционально совместимы.
Примечание - В большинстве случаев компоненты, произведенные одной компанией, могут быть несовместимыми с компонентами, произведенными другой компанией. Это относится, в частности, к модульным компонентам, которые имеют конусные соединения типа внешнего ("папа") или внутреннего ("мама") конуса.
11.4 Маркировка
11.4.1 На моноблочном бедренном компоненте должна быть маркировка с указанием номинального диаметра бедренной головки.
11.4.2 Маркировка (или маркировки), размещаемая(ые) на модульном протезе головки бедренной кости, должна(ы) указывать ее номинальный внешний диаметр и параметры соединения конуса и расточенного отверстия. Маркировка(и) должна(ы) легко читаться специалистом с нормальным или корригированным до нормального зрением.
11.4.3 На стержневой части модульного бедренного компонента имплантата, предназначенного для протезирования тазобедренного сустава и имеющего внешнее/внутреннее конусное соединение для модульного протеза головки, должна быть маркировка с указанием категории соединения (при условии, что это не нарушает предусмотренную функцию компонента). Маркировка должна быть нанесена на шейку бедренного компонента имплантата, предназначенного для протезирования тазобедренного сустава, для его идентификации или в иных целях, но только в том случае, если существуют доказательства того, что она не снижает предел прочности. Для имплантатов с модульными головками маркировку следует размещать на плоском участке проксимального конца той конической области, к которой подгоняется головка. Эта отметка должна легко читаться при осмотре невооруженным глазом или с помощью приспособлений для улучшения остроты зрения.
11.4.4 Вертлужный компонент, который имеет суставную поверхность, участвующую в формировании тотального эндопротеза тазобедренного сустава, должен иметь отметку, указывающую на номинальный диаметр суставной поверхности. Эта отметка должна легко читаться специалистом с нормальным или корригированным до нормального зрением.
11.5 Информация для пациента
Производитель должен включить в листок-вкладыш с инструкцией или в руководство по использованию, как минимум, следующее положение (или эквивалентную информацию): "Пациентов, которым устанавливают эндопротезы тазобедренного сустава, следует предупреждать, что срок службы имплантата может зависеть от их веса и уровня активности".
Приложение А
(справочное)
Оценка относительного углового движения компонентов
А.1 Закрепляют вертлужный компонент в соответствующем зажиме или другом фиксирующем приспособлении.
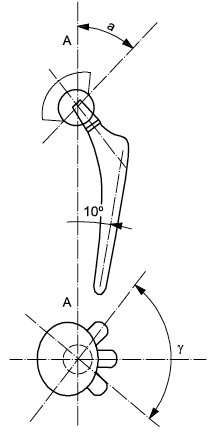
А.2 Закрепляют бедренный компонент, который может иметь интегральную либо модульную конструкцию, на испытательном стенде, таким образом, чтобы суставные поверхности бедренного и вертлужного компонентов соприкасались друг с другом и вращались вокруг осей, проходящих через центр суставной поверхности вертлужной впадины. Используя соответствующий гониометр или прибор для измерения углов, перемещают бедренный компонент рукой в плоскости его ножки и шейки до тех пор, пока шейка бедренного компонента не соприкоснется с вертлужной впадиной по ее медиальной поверхности, а затем по латеральной поверхности. Измеряют угол между двумя положениями с точностью ±1°, как показано на рисунке А.1 а). Этот угол
представляет собой угол отведения/приведения.
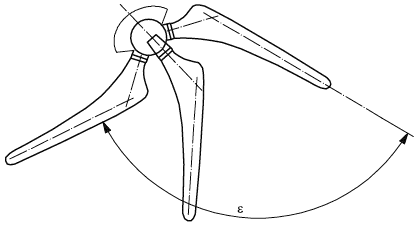
А.3 Повторяют движение, описанное в пункте А.2, в плоскости, проходящей через центр головки перпендикулярно плоскости стержня и шейки, как показано на рисунке А.1 b), и измеряют угол ![]() между двумя крайними положениями, изображенными на рисунке. Этот угол
между двумя крайними положениями, изображенными на рисунке. Этот угол ![]() представляет собой угол сгибания/разгибания.
представляет собой угол сгибания/разгибания.
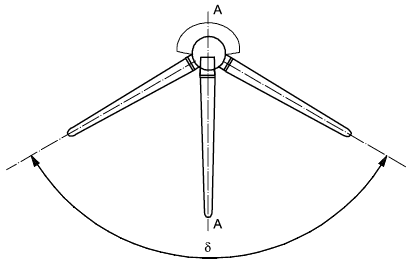
А.4 Исходно поместив вертлужный компонент в положение, изображенное на рисунках А.1 b) и А.1 с), вращают бедренный компонент вокруг оси АА сначала в одном, а затем в другом направлении и выполняют измерение угла , соответствующего диапазону свободного движения от одного упора к другому. Угол
представляет собой угол вращения внутрь/наружу.
А.5 Также возможно проведение оценки с помощью программного обеспечения CAD. На чертеже должны быть указаны углы и идентификационные сведения о компонентах (размер, длина шейки).
|
а) Протез тазобедренного сустава (отведение/приведение)
|
|
b) Протез тазобедренного сустава | с) Протез тазобедренного сустава |
- угол внутреннего/наружного вращения;
- угол отведения/приведения;
![]() - угол изгиба/удлинения а - установленный вертлужный компонент на 45° или угол, заданный производителем
- угол изгиба/удлинения а - установленный вертлужный компонент на 45° или угол, заданный производителем
Рисунок А.1 - Относительное угловое движение компонентов
Приложение ДА
(справочное)
Сведения о соответствии ссылочных международных стандартов национальным стандартам
Таблица ДА.1
Обозначение ссылочного международного стандарта | Степень соответствия | Обозначение и наименование соответствующего национального стандарта |
ISO 7206-1 | IDT | ГОСТ Р ИСО 7206-1-2005 "Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 1. Классификация и обозначение размеров" |
ISO 7206-2 | IDT | ГОСТ Р ИСО 7206-2-2013 "Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 2. Суставные поверхности, изготовленные из металлических, керамических и полимерных материалов" |
ISO 7206-4 | IDT | ГОСТ Р ИСО 7206-4-2012 "Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 4. Определение прочности и эксплуатационных качеств бедренных компонентов с ножкой" |
ISO 7206-6 | IDT | ГОСТ Р ИСО 7206-6-2012 "Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 6. Определение прочностных свойств области шейки и головки бедренных компонентов" |
ISO 7206-10 | IDT | ГОСТ Р ИСО 7206-10-2005 "Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 10. Определение сопротивления статической нагрузке модульных бедренных головок" |
ISO 14242-1 | IDT | ГОСТ Р ИСО 14242-1-2012 "Имплантаты для хирургии. Износ тотальных эндопротезов тазобедренного сустава. Часть 1. Параметры нагружения и перемещения для испытательных машин и условия окружающей среды при испытании" |
ISO 14242-2 | IDT | ГОСТ Р ИСО 14242-2-2013 "Имплантаты для хирургии. Износ тотальных эндопротезов тазобедренного сустава. Часть 2. Методы измерений" |
ISO 14242-3 | IDT | ГОСТ Р ИСО 14242-3-2013 "Имплантаты для хирургии. Износ тотальных эндопротезов тазобедренного сустава. Часть 1. Параметры нагружения и перемещения машин для испытания на износ орбитальных опор и условия окружающей среды при испытании" |
ISO 14630:2012 | IDT | ГОСТ Р ИСО 14630-2017 "Имплантаты хирургические неактивные. Общие требования" |
ISO 21534:2007 | IDT | ГОСТ Р ИСО 21534-2013 "Имплантаты хирургические неактивные. Имплантаты для замены суставов. Общие требования" |
Примечание - В настоящей таблице использовано следующее условное обозначение степени соответствия стандартов: | ||
Библиография
[1] | ASTM F3047M-15 Standard Guide for High Demand Hip Simulator Wear Testing of Hard-on-hard Articulations (Стандартное руководство по испытаниям на износ суставных поверхностей на высокоинтенсивном симуляторе тазобедренного сустава) |
УДК 617-089.844:006.354 | ОКС 11.040.40 |
Ключевые слова: неактивные хирургические имплантаты, протезирование тазобедренного сустава, специальные требования | |
Электронный текст документа
и сверен по:
, 2020