ГОСТ Р 50267.47-2004
(МЭК 60601-2-47-2001)
Группа P07
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Изделия медицинские электрические
Часть 2
ЧАСТНЫЕ ТРЕБОВАНИЯ БЕЗОПАСНОСТИ С УЧЕТОМ ОСНОВНЫХ ФУНКЦИОНАЛЬНЫХ ХАРАКТЕРИСТИК К АМБУЛАТОРНЫМ ЭЛЕКТРОКАРДИОГРАФИЧЕСКИМ СИСТЕМАМ
Medical electrical equipment. Part 2. Particular requirements for the safety, including essential performance, of ambulatory electrocardiographic systems
ОКС 11.040
ОКП 94 4110
Дата введения 2005-07-01
Предисловие
1 ПОДГОТОВЛЕН Закрытым акционерным обществом "ВНИИМП-ВИТА" на основе собственного аутентичного перевода стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 11 "Медицинские приборы и аппараты"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального Агентства по техническому регулированию и метрологии от 10 ноября 2004 г. N 67-ст
4 Настоящий стандарт является модифицированным по отношению к международному стандарту МЭК 60601-2-47-2001 "Изделия медицинские электрические. Часть 2. Частные требования безопасности с учетом основных функциональных характеристик к амбулаторным электрокардиографическим системам" (IEC 60601-2-47-2001 Medical electrical equipment. Part 2. Particular requirements for the safety, including essential performance, of ambulatory electrocardiographic systems) путем внесения технических отклонений, объяснение которых приведено во введении к настоящему частному стандарту
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему частному стандарту публикуется в указателе "Национальные стандарты", а текст этих изменений - в информационных указателях "Национальные стандарты". В случае пересмотра или отмены настоящего стандарта соответствующая информация будет опубликована в информационном указателе "Национальные стандарты"
Введение
Настоящий частный стандарт устанавливает требования безопасности к АМБУЛАТОРНЫМ ЭЛЕКТРОКАРДИОГРАФИЧЕСКИМ СИСТЕМАМ, изменяет и дополняет ГОСТ 30324.0-95 (далее - общий стандарт). Требования настоящего частного стандарта являются приоритетными по отношению к требованиям общего стандарта. Приложение АА включает в себя "Общие положения и обоснования" к некоторым требованиям настоящего частного стандарта. Предполагается, что обоснование указанных требований не только будет способствовать применению стандарта, но также с течением времени ускорит любой их пересмотр, обусловленный изменениями в клинической практике или вызванный новыми технологическими разработками. Вместе с тем данное приложение не является частью требований настоящего частного стандарта.
Знак звездочки (*), помещенный перед номером пункта или подпункта, указывает на то, что в приложении АА даны пояснения требований настоящего частного стандарта.
Настоящий частный стандарт является модифицированным по отношению к международному стандарту МЭК 60601-2-47-2001. При этом дополнительные слова, включенные в текст стандарта для учета потребностей национальной экономики Российской Федерации, заключены в рамки из тонких линий.
Текст приложения L "Нормативные ссылки" изложен в соответствии с ГОСТ Р 1.5-2002 и выделен вертикальной линией, расположенной слева от текста.
Сведения о соответствии ссылочных международных стандартов межгосударственным стандартам и национальным стандартам РФ приведены в дополнительном приложении ВВ. В тексте стандарта соответствующие ссылки выделены подчеркиванием сплошной горизонтальной линией.
РАЗДЕЛ ПЕРВЫЙ. ОБЩИЕ ПОЛОЖЕНИЯ
Применяют пункты общего стандарта, за исключением:
1 Область распространения и цель
Применяют пункт общего стандарта, за исключением:
1.1 Область распространения
Дополнение
Настоящий частный стандарт устанавливает требования безопасности к АМБУЛАТОРНЫМ ЭЛЕКТРОКАРДИОГРАФИЧЕСКИМ СИСТЕМАМ по 2.101 (далее - ИЗДЕЛИЕ).
Настоящий частный стандарт распространяется на изделия следующих категорий:
a) изделия, обеспечивающие непрерывную запись и непрерывный анализ потенциалов действия сердца - электрокардиосигнала (ЭКС) и обеспечивающие проведение повторных анализов полного ЭКС. Изделия хранят первичную запись ЭКС и первичный анализ, позволяя повторно проводить анализ в отдельном блоке системы.
Настоящий стандарт не устанавливает тип использованной среды для хранения ЭКС;
b) изделия, обеспечивающие непрерывный анализ и только фрагментарную или сжатую запись ЭКС без возможности проведения ее полного повторного анализа.
Требования безопасности настоящего стандарта распространяются на все типы изделий, подпадающих под одну из вышеупомянутых категорий.
Если амбулаторные электрокардиографические системы включают средства для автоматического анализа ЭКС, применяются минимальные требования по характеристикам измерения и анализа.
Настоящий частный стандарт не распространяется на системы, которые не осуществляют непрерывную запись и анализ ЭКС (например, регистраторы перемежающихся событий), а также на медицинские электрические изделия по ГОСТ 30324.25 и ГОСТ 30324.27.
1.2 Цель
Дополнение
Целью настоящего частного стандарта является установление частных требований безопасности к АМБУЛАТОРНЫМ ЭЛЕКТРОКАРДИОГРАФИЧЕСКИМ СИСТЕМАМ и требований к их основным характеристикам.
1.3 Частные стандарты
Дополнение
Нумерация разделов, пунктов и подпунктов настоящего частного стандарта соответствует нумерации общего стандарта. Изменение текста общего стандарта в настоящем частном стандарте осуществлено с использованием следующих слов:
"замена" - означает, что требования пункта или подпункта общего стандарта полностью заменены требованиями настоящего частного стандарта;
"дополнение" - означает, что требования настоящего частного стандарта дополняют требования общего стандарта;
"изменение" - означает, что требования пункта или подпункта общего стандарта изменены в соответствии с указаниями в настоящем частном стандарте;
"модификация" - означает, что требования пункта или подпункта общего стандарта частично изменены в соответствии с указаниями в настоящем частном стандарте.
Пункты и рисунки, которые дополняют пункты и рисунки общего стандарта, имеют нумерацию, начиная с цифры 101, дополнительные приложения обозначены буквами АА, ВВ и т.д., а дополнительные перечисления - аа), bb) и т.д.
Термин "настоящий стандарт" применен для ссылок на общий стандарт и настоящий частный стандарт, вместе взятые.
В случае отсутствия соответствующего раздела, пункта или подпункта в настоящем частном стандарте раздел, пункт или подпункт общего стандарта, даже если он не имеет прямого отношения, применим без изменений. Условие неприменимости любого раздела, пункта или подпункта общего стандарта оговорено в настоящем частном стандарте.
В настоящем частном стандарте термины набраны прописными буквами, методы испытаний - курсивом.
1.5 Дополнительные стандарты
Дополнение
ГОСТ Р 50267.0.2-95 Изделия медицинские электрические. Часть 1. Общие требования безопасности. 2. Электромагнитная совместимость. Требования и методы испытаний
2 Термины и определения
Применяют пункт общего стандарта, за исключением:
Дополнение
2.101 АМБУЛАТОРНАЯ ЭЛЕКТРОКАРДИОГРАФИЧЕСКАЯ СИСТЕМА (ИЗДЕЛИЕ) (AMBULATORY ELECTROCARDIOGRAPHIC SYSTEM (EQUIPMENT)
АМБУЛАТОРНЫЙ РЕГИСТРАТОР и УСТРОЙСТВО ВОСПРОИЗВЕДЕНИЯ, каждый из которых может осуществлять функцию анализа.
Примечание - Такое ИЗДЕЛИЕ часто относят к оборудованию для Холтеровского мониторирования по имени изобретателя доктора Нормана Холтера.
2.102 АМБУЛАТОРНЫЙ РЕГИСТРАТОР (AMBULATORY RECORDER)
Записывающее ИЗДЕЛИЕ, носимое ПАЦИЕНТОМ, включая ЭЛЕКТРОДЫ и кабели для записи или для записи и анализа потенциалов сердца.
2.103 УСТРОЙСТВО ВОСПРОИЗВЕДЕНИЯ (PLAYBACK EQUIPMENT)
УСТРОЙСТВО для отображения и документирования данных, загруженных от АМБУЛАТОРНОГО РЕГИСТРАТОРА.
Примечание - Это УСТРОЙСТВО обычно стационарное и включает компьютерные средства.
2.104 ЭЛЕКТРОКАРДИОГРАММА (ЭКГ) [ELECTROCARDIOGRAM (ECG)]
Видимая запись потенциалов действия сердца - электрокардиосигнала (ЭКС) (см. 2.101 ГОСТ 30324.25).
2.105 ОТВЕДЕНИЕ (LEAD)
Комбинация ЭЛЕКТРОДНЫХ СИГНАЛОВ (сигналов, снимаемых с соответствующего ЭЛЕКТРОДА ПАЦИЕНТА по конкретной методике съема), используемая для записи ЭКС.
Примеры
1 ОТВЕДЕНИЕ II по Эйтховену;
2 Униполярное грудное ОТВЕДЕНИЕ V5.
(См. 2.103 ГОСТ 30324.25).
2.106 ЭЛЕКТРОДЫ ПАЦИЕНТА (PATIENT ELECTRODE)
Контактные приспособления, прикрепляемые к определенным частям тела, используемые для снятия потенциалов сердца с последующим усилением и преобразованием (см. 2.104 ГОСТ 30324.25).
2.107 НЕЙТРАЛЬНЫЙ ЭЛЕКТРОД (NEUTRAL ELECTRODE)
Общая точка для дифференциальных усилителей и/или помехоподавляющих цепей, не участвующая в формировании любого отведения ЭКГ (см. 2.107 ГОСТ 30324.25).
2.108 КАБЕЛЬ ПАЦИЕНТА (PATIENT CABLE)
Многожильный кабель и соответствующий соединитель (и), служащие для присоединения ЭЛЕКТРОДОВ к АМБУЛАТОРНОМУ РЕГИСТРАТОРУ (см. 2.109 ГОСТ 30324.25).
2.109 ПРОВОД(А) КАБЕЛЯ ПАЦИЕНТА (ОТВЕДЕНИЯ) (LEAD WIRE(S)
Провод, соединяющий ЭЛЕКТРОД и АМБУЛАТОРНЫЙ РЕГИСТРАТОР.
2.110 РЕГИСТРАТОР НЕПРЕРЫВНОГО ДЕЙСТВИЯ (CONTINUOUS RECORDER)
ОБОРУДОВАНИЕ, которое выполняет непрерывную запись и (или) анализ ЭКГ.
5 Классификация
Применяют пункт общего стандарта, за исключением:
5.6
Изменение
Исключить все, кроме ИЗДЕЛИЯ с ПРОДОЛЖИТЕЛЬНЫМ РЕЖИМОМ РАБОТЫ.
6 Идентификация, маркировка и документация
Применяют пункт общего стандарта, за исключением:
6.1 Маркировка на наружной стороне ИЗДЕЛИЙ или их частей
Дополнение
аа) идентификация ПРОВОДА(ОВ) КАБЕЛЯ ПАЦИЕНТА (ОТВЕДЕНИЙ)
ПРОВОД(А) КАБЕЛЯ ПАЦИЕНТА (весь или частично) должен(ны) иметь нестираемую маркировку, выполненную таким образом, чтобы ПРОВОД(А) КАБЕЛЯ ПАЦИЕНТА можно было однозначно определить по обоим присоединительным ЭЛЕКТРОДАМ, он должен быть сконструирован и маркирован так, чтобы избежать неправильного подключения к АМБУЛАТОРНОМУ РЕГИСТРАТОРУ. Если используются независимые биполярные отведения, они должны быть четко обозначены на корпусе регистратора. ПРОВОД(А) КАБЕЛЯ ПАЦИЕНТА также должен иметь цветовую маркировку в соответствии с одной из схем цветового кодирования по таблице 101.
Таблица 101 - Цветовая маркировка ПРОВОДА КАБЕЛЯ ПАЦИЕНТА
Канал* | ЭЛЕКТРОД | Схема цветового кодирования | |
Код 1 | Код 2 | ||
Канал 1 | Положительный ЭЛЕКТРОД | Зеленый | Красный |
Отрицательный ЭЛЕКТРОД | Красный | Белый | |
Канал 2 | Положительный ЭЛЕКТРОД | Белый | Коричневый |
Отрицательный ЭЛЕКТРОД | Желтый | Черный | |
Канал 3 | Положительный ЭЛЕКТРОД | Оранжевый | Оранжевый |
Отрицательный ЭЛЕКТРОД | Голубой | Голубой | |
- | НЕЙТРАЛЬНЫЙ ЭЛЕКТРОД | Черный | Зеленый |
________________
Примечание - В таблице представлена предпочтительная маркировка полярностей, при этом в изделии могут быть отличия, которые должны быть маркированы должным образом. | |||
________________
* Канал - условное определение регистрирующего устройства для графического отображения различного сочетания ОТВЕДЕНИЙ.
6.8.2 Инструкция по эксплуатации
Дополнение
аа) Инструкция по эксплуатации должна содержать:
1) процедуры, необходимые для безопасной работы, на которые необходимо обратить внимание при наличии РАБОЧИХ ЧАСТЕЙ ТИПА В в отношении их риска, который может иметь место при неадекватной электрической установке;
2) указание на тип электрической установки, к которой может быть безопасно подключено ИЗДЕЛИЕ, включая подсоединение к любому ПРОВОДУ ВЫРАВНИВАНИЯ ПОТЕНЦИАЛОВ;
3) описание тех проводящих частей ЭЛЕКТРОДОВ и соответствующих соединителей РАБОЧИХ ЧАСТЕЙ ТИПА BF или РАБОЧИХ ЧАСТЕЙ ТИПА CF, включающих НЕЙТРАЛЬНЫЙ ЭЛЕКТРОД, которые не должны контактировать с другими проводящими частями, включая землю;
4) указание на возможный риск, вызванный суммированием ТОКОВ УТЕЧКИ, когда отдельные ИЗДЕЛИЯ электрически связаны между собой и/или подключены к многорозеточному удлинителю.
bb) Должны быть представлены четкие инструкции при использовании специальных типов аккумуляторов или процедуры зарядки аккумулятора с целью соответствия требованиям настоящего частного стандарта.
сс) Должны быть представлены четкие инструкции при использовании АМБУЛАТОРНОГО РЕГИСТРАТОРА во влажной окружающей среде.
dd) Маркировка ИЗДЕЛИЯ должна четко указывать, предназначено ли оно или нет для детей массой менее 10 кг.
ее) Изготовитель должен указать метод подсчета частоты сердечных сокращений.
ff) Изготовитель должен указать метод определения паузы.
gg) Если изделие предназначено для обнаружения и/или измерения сдвигов сегментов ST*, изготовитель должен указать в инструкции по эксплуатации или руководстве для врача следующее:
________________
* ST - составляющая зубцов комплекса р; Q; R; S; Т электрокардиосигнала (ЭКС).
- выполняется ли анализ сегментов ST по всем ОТВЕДЕНИЯМ с использованием каких-либо или всех калибровочных сигналов;
- существует ли выбираемый ОПЕРАТОРОМ критерий определения сдвигов сегментов ST (такой, как смещение и наклон этих параметров);
- насколько часто сдвиги сегментов ST суммируются в отчете (например, ежечасно) и сообщаются ли число приступов, типы приступов (повышение или снижение) и продолжительности приступов или представляется ли в отчете эта информация по каждому событию;
- сообщаются ли диапазоны частот сердечных сокращений, значения диапазонов смещений и/или наклона параметров в течение каждого приступа.
РАЗДЕЛ ВТОРОЙ. УСЛОВИЯ ОКРУЖАЮЩЕЙ СРЕДЫ
Применяют раздел общего стандарта, за исключением:
*10 Условия окружающей среды
10.2.1 Окружающая среда
Дополнение
Для АМБУЛАТОРНЫХ РЕГИСТРАТОРОВ:
a) Диапазон окружающей температуры от 10 °С до 45 °С.
b) Относительная влажность от 10% до 95%, без конденсации.
РАЗДЕЛ ТРЕТИЙ. ЗАЩИТА ОТ ОПАСНОСТЕЙ ПОРАЖЕНИЯ ЭЛЕКТРИЧЕСКИМ ТОКОМ
Применяют раздел общего стандарта, за исключением:
20 Электрическая прочность изоляции
Применяют пункт общего стандарта, за исключением:
20.2 Требования к ИЗДЕЛИЯМ с РАБОЧЕЙ ЧАСТЬЮ
Изменение
В-b Не применяют.
20.3 Значения испытательных напряжений
Дополнение
1) B-d Испытательное напряжение должно быть 1500 В (для КЛАССА I, КЛАССА II и ИЗДЕЛИЙ С ВНУТРЕННИМ ИСТОЧНИКОМ ЭЛЕКТРИЧЕСКОГО ПИТАНИЯ) между РАБОЧИМИ ЧАСТЯМИ ТИПА F и СИГНАЛЬНЫМ ВХОДОМ или СИГНАЛЬНЫМ ВЫХОДОМ. Это испытание не применяется, если входные/выходные части не могут быть подключены к внешнему ИЗДЕЛИЮ, в то время как устройство подключено к ПАЦИЕНТУ.
2) B-d Испытательное напряжение между РАБОЧИМИ ЧАСТЯМИ ТИПА F и КОРПУСОМ, если не считать СИГНАЛЬНЫЙ ВХОД, должно определяться с помощью НАПРЯЖЕНИЯ СЕТИ устройства и таблицы V общего стандарта. Требование общего стандарта для минимального питающего напряжения =250 В для ИЗДЕЛИЯ С ВНУТРЕННИМ ИСТОЧНИКОМ ЭЛЕКТРИЧЕСКОГО ПИТАНИЯ не применяется.
РАЗДЕЛ ЧЕТВЕРТЫЙ. ЗАЩИТА ОТ МЕХАНИЧЕСКИХ ОПАСНОСТЕЙ
Применяют раздел общего стандарта, за исключением:
21 Механическая прочность
*21.5
Замена
Получение данных с помощью АМБУЛАТОРНОГО РЕГИСТРАТОРА может быть прервано во время его удара, при этом удар не должен повлиять на нормальное получение данных, которое должно возобновиться в течение 60 с после завершения испытания.
Соответствие требованию проверяют следующим испытанием.
АМБУЛАТОРНЫЙ РЕГИСТРАТОР роняют с высоты 75 мм на доску из твердой древесины толщиной 50 мм (плотность древесины более 600 кг/м), ровно лежащую на твердом основании, таком как бетонированный пол, и находящуюся в прочном контакте с основанием по каждой поверхности, кромке и углу. Если АМБУЛАТОРНЫЙ РЕГИСТРАТОР обычно используется в сумке, тот же тип сумки используется и при испытании. АМБУЛАТОРНЫЙ РЕГИСТРАТОР не должен пострадать от удара, а должен возобновить получение обычных данных в течение 60 с после удара.
21.6
Замена
При транспортировании, хранении или в нерабочем состоянии АМБУЛАТОРНЫЙ РЕГИСТРАТОР не должен быть поврежден при падении с высоты 0,8 м ударом любой стороной, кромкой или углом о твердую поверхность (как указано выше, может быть использована сумка).
АМБУЛАТОРНЫЙ РЕГИСТРАТОР не должен получить явные повреждения при этом испытании и должен соответствовать требованиям настоящего частного стандарта.
Соответствие требованию проверяют следующим испытанием.
АМБУЛАТОРНЫЙ РЕГИСТРАТОР подвергают свободному падению по каждому из трех различных исходных положений с высоты 0,8 м на доску из твердой древесины толщиной 50 мм (например, твердая древесина плотностью более 600 кг/м), которая ровно лежит на твердом основании, таком как бетонный пол. Если АМБУЛАТОРНЫЙ РЕГИСТРАТОР обычно используется в сумке, тот же тип сумки может использоваться при испытании.
РАЗДЕЛ ПЯТЫЙ. ЗАЩИТА ОТ ОПАСНОСТЕЙ НЕЖЕЛАТЕЛЬНОГО ИЛИ ЧРЕЗМЕРНОГО ИЗЛУЧЕНИЯ
Применяют раздел общего стандарта, за исключением:
*36 Электромагнитная совместимость
Применяют ГОСТ Р 50267.0.2, за исключением:
36.201 ЭМИССИЯ
36.201.1 Радиочастотная ЭМИССИЯ (RF)
36.201.1.1
Замена
АМБУЛАТОРНЫЙ РЕГИСТРАТОР должен соответствовать требованиям ГОСТ Р 51318.11, группа 1, класс Б, а также ГОСТ Р 51318.22 (при необходимости).
36.201.1.7
Замена
ИЗДЕЛИЕ ИЛИ СИСТЕМА, СВЯЗАННЫЕ С ПАЦИЕНТОМ, должны испытываться вместе с КАБЕЛЯМИ ПАЦИЕНТА, ДАТЧИКАМИ и ЭЛЕКТРОДАМИ, присоединенными к ИЗДЕЛИЮ и оканчивающимися в нагрузке, имитирующей ПАЦИЕНТА (рисунки 101 и 102).
Сигнальные входные/выходные провода (если применимо) должны быть при испытании присоединены к ИЗДЕЛИЮ [см. 36.202.2.2, перечисление а) настоящего частного стандарта].
36.202 ПОМЕХОУСТОЙЧИВОСТЬ
Четвертый абзац
Дополнение
Примеры указаний возможных РИСКОВ включают изменения рабочего состояния, неисправимые нарушения или изменения хранимых данных.
*36.202.1 ЭЛЕКТРОСТАТИЧЕСКИЙ ЗАРЯД
Замена
Изделие и/или системы должны соответствовать ГОСТ Р 51317.4.2. Должен применяться уровень на напряжение ±6 кВ для контактного разряда в ДОСТУПНЫХ проводящих ЧАСТЯХ и на пластины связи. Дополнительно, уровень на напряжение ±8 кВ должен применяться для непроводящих ДОСТУПНЫХ ЧАСТЕЙ.
ИЗДЕЛИЕ после воздействия напряжения должно возвратиться к предыдущему рабочему режиму в течение 10 с без потери каких-либо хранимых данных.
*36.202.2 Устойчивость к излучаемым радиочастотным электромагнитным полям
36.202.2.1 Требования
Изменение
а) АМБУЛАТОРНЫЙ РЕГИСТРАТОР должен соответствовать ГОСТ Р 51317.4.3. Уровень радиочастотного поля должен быть 3 В/м.
36.202.2.2 Условия испытаний
Изменение
a) Должна быть использована 80%-ная амплитудная модуляция при единичной частоте модуляции в диапазоне от 1 до 5 Гц.
b) Провод ИЗДЕЛИЯ должен быть размещен безындуктивно и иметь общую длину до 1 м, а сигнальный провод (если применимо) и ПРОВОД ПИТАНИЯ (если применимо) должны быть установлены соответственно горизонтально и вертикально от ИЗДЕЛИЯ, как указано на рисунке 102.
c) Для ИЗДЕЛИЯ испытательная частота должна колебаться от 80 до 1000 МГц.
d) He применяют.
36.202.6 Магнитные поля
Дополнение
ИЗДЕЛИЕ должно быть три раза подвергнуто действию магнитного поля напряженностью 3 А/м на утроенной частоте сети. Требования настоящего частного стандарта по рабочим характеристикам должны быть выполнены и не должно быть потерь данных. См. также ГОСТ Р 50648.
РАЗДЕЛ ШЕСТОЙ. ЗАЩИТА ОТ ОПАСНОСТЕЙ ВОСПЛАМЕНЕНИЯ ГОРЮЧИХ СМЕСЕЙ АНЕСТЕТИКОВ
Применяют раздел общего стандарта.
РАЗДЕЛ СЕДЬМОЙ. ЗАЩИТА ОТ ЧРЕЗМЕРНЫХ ТЕМПЕРАТУР И ДРУГИХ ОПАСНОСТЕЙ
Применяют раздел общего стандарта.
РАЗДЕЛ ВОСЬМОЙ. ТОЧНОСТЬ РАБОЧИХ ХАРАКТЕРИСТИК И ЗАЩИТА ОТ ПРЕДСТАВЛЯЮЩИХ ОПАСНОСТЬ ВЫХОДНЫХ ХАРАКТЕРИСТИК
Применяют раздел общего стандарта, за исключением:
Дополнение
Примечание - Раздел восьмой настоящего частного стандарта носит справочно-информационный характер. |
50 Точность рабочих характеристик
Дополнение
*50.101 Автоматический анализ
ИЗДЕЛИЕ с встроенным автоматическим анализом должно отвечать требованиям настоящего раздела.
*50.101.1 Стандартные базы данных, используемые для оценки автоматических анализов
В настоящее время имеются четыре базы данных от трех источников для оценки носимых анализаторов ЭКС:
- База данных AHA: База данных американской ассоциации сердца (The American Heart Association) для оценки аритмии желудочков (80 записей по 30 мин каждая);
- База данных MIT-BIH: База данных по аритмиям Массачусетского технологического института - института Израильского госпиталя Beth (The Massachusetts Institute of Technology Beth Israel Hospital) (48 записей по 30 мин каждая);
- База данных NST: База данных Теста Шумового Стресса (Noise Stress Test) (12 записей по 30 мин каждая; поставляется с базой данных MIT);
- База данных CU: База данных по длительным аритмиям желудочков Крейгтоновского университета (The Creighton University) (35 записей по 8 мин каждая; поставляется с базой данных MIT).
Первые три базы данных состоят из оцифрованных выборок двухканальных Холтеровских записей, причем каждый кардиоцикл промаркирован. База данных CU содержит оцифрованные одноканальные записи ЭКС с промаркированными кардиоциклами. Это полный перечень баз данных, представляющих основу оценки и являющихся в настоящее время широко распространенными.
При отсутствии вышеуказанных баз данных у испытателей рекомендуется использовать отечественные базы данных и методику клинических испытаний, которые могут быть получены в Российском обществе холтеровского мониторирования и неинвазивной диагностики. Примечание - Российское общество Холтеровского мониторирования и неинвазивной диагностики при НИИ кардиологии им. А.Л.Мясникова, отдел новых методов диагностики. Москва, ул.3-я Черепковская, 15-а. |
*50.101.2 Требования к протоколам испытаний
50.101.2.1 Испытания следует проводить с использованием перечисленных баз данных.
Правильность обнаружения комплексов QRS* должна быть испытана с использованием баз данных AHA, MIT и NST.
________________
* QRS - составляющая зубцов комплекса р; Q; R; S; Т электрокардиосигнала.
Правильность обнаружения желудочковых экстрасистолий (VEB) должна быть испытана с использованием баз данных AHA, MIT и NST.
Если в ИЗДЕЛИИ заложено обнаружение эпизодов трепетания желудочков или фибрилляции (VF), то его способность осуществлять это должна быть проверена с использованием баз данных CU, AHA и MIT.
Если в ИЗДЕЛИИ заложено обнаружение наджелудочковых экстрасистолий (SVEB - наджелудочковое эктопическое сокращение) или трепетания предсердий (AF) или фибрилляции желудочков (VF), то его способность осуществлять это должна быть испытана с использованием баз данных MIT и NST.
50.101.2.2 Содержание каждого протокола испытаний
Для каждого протокола испытаний должны быть использованы следующие статистические данные:
- чувствительность (вероятность правильности обнаружения) комплексов QRS и специфичность (отсутствие ложных обнаружений) комплексов QRS;
- чувствительность (вероятность правильности обнаружения) желудочковых экстрасистолий VEB и специфичность (отсутствие ложных обнаружений) VEB.
В протоколе также должны быть следующие данные (если эти функции заявлены в ИЗДЕЛИИ):
- чувствительность эпизодов трепетания желудочков VF и специфичность VF;
- чувствительность наджелудочковых экстрасистолий SVEB и специфичность SVEB;
- чувствительность эпизодов трепетания предсердий AF и специфичность AF.
50.101.2.3 Оформление статистических отчетов
Основанная на отчетах по каждой обработанной записи общая сумма статистических данных для каждого испытуемого ИЗДЕЛИЯ должна быть представлена в табличной форме, как показано в таблицах 102 и 103. Символы и аббревиатуры, использованные в этих таблицах, следующие:
G - полная сумма статистических данных (по всем базам данных);
+Р=TN/(TN+FP) - специфичность или вероятность отсутствия ложного диагноза на контингенте здоровых или больных другой болезнью (т.е. специфичность, равная 1, - это вероятность ложного обнаружения);
R - используемые базы данных;
Se=ТР/(ТР+FN) - чувствительность или вероятность правильного обнаружения заболевания (т.е. вероятность отсутствия пропуска заболевания на контингенте больных, страдающих конкретно этим заболеванием);
VEB - желудочковая экстрасистолия (желудочковое эктопическое сокращение);
SVEB - наджелудочковая экстрасистолия (наджелудочковое эктопическое сокращение);
ТР - число правильных диагностических заключений о заболевании на контингенте, имеющем это заболевание;
TN - число правильных заключений об отсутствии заболевания на контингенте, не имеющем этого заболевания;
FP - число ложных обнаружений заболеваний на контингенте, не имеющем этого заболевания;
FN - число пропусков обнаружений заболеваний на контингенте больных данным заболеванием.
Таблица 102 - Наличие параметров в протоколах и используемые базы данных для анализаторов стандартного набора параметров
Статистические данные | База данных AHA | База данных MIT | База данных NST | База данных CU |
QRS Se (G) | R | R | R | - |
QRS+Р (G) | R | R | R | - |
VEB Se (G) | R | R | R | - |
VEB+Р (G) | R | R | R | - |
Se (G) пap VEB | R | R | - | R |
+P(G) пap VEB | R | R | - | R |
Se (G) коротких периодов VEB | R | R | - | R |
+Р (G) коротких периодов VEB | R | R | - | R |
Se (G) длинных периодов VEB | R | R | - | R |
+Р (G) длинных периодов VEB | R | R | - | R |
Таблица 103 - Наличие параметров в протоколах и используемые базы данных для анализаторов с дополнительным набором параметров
Статистические данные | База данных AHA | База данных MIT | База данных NST | База данных CU |
Эпизодическая Se (G) VF | R | R | - | R |
Эпизодическая +Р (G) VF | R | R | - | R |
SVEB Se (G) | - | R | R | - |
SVEB +Р (G) | - | R | R | - |
50.101.2.4 Методы испытаний
а) Использование баз данных
Каждая запись из базы данных должна вводиться в ИЗДЕЛИЕ непрерывно от начала до конца (то есть без перемотки или ускорения). Это требование применяется только к методу, по которому образцы ЭКГ вводятся в испытуемое ИЗДЕЛИЕ, оно не накладывает ограничения на метод, по которому ИЗДЕЛИЕ проводит анализ.
Если сигналы записей баз данных предварительно обработаны каким-либо способом перед их вводом в испытуемое изделие, эта предварительная подготовка должна быть раскрыта достаточно детально для контроля стороной, проводящей испытания.
Предварительная подготовка может включать (но не ограничивать):
- повторную выборку (т.е. смену частоты отсчетов в файлах баз данных);
- переформатирование (т.е. смену порядка байтов, образцовой точности или цифрового кодирования); изменение масштаба (изменение амплитуды сигнала, т.е. изменение усиления);
- перевод цифровых сигналов на аналоговые;
- фильтрацию программную или с помощью дополнительного компьютера, которая не употребляется при нормальном рабочем режиме испытуемого изделия.
Если оценка испытуемого изделия осуществляется с использованием сигналов, преобразованных в аналоговую форму и подаваемых в нормальные аналоговые входы изделия, то автоматическое управление чувствительностью, имеющееся у изделия (AGC), обеспечит регулировку усиления автоматически.
Если оценка испытуемого изделия осуществляется с использованием цифровых данных и автоматическое управление чувствительностью является частью аналогового внешнего интерфейса изделия, то изделие должно проверяться на возможность автоматического регулирования усиления с помощью альтернативного метода. Этот альтернативный метод обеспечивает режим испытания процедуры регулировки усиления на предварительной выборке сигналов, имеющейся в каждой базе данных, до работы с анализом каждой записи ЭКГ пациента. Испытание процедуры регулировки усиления должно информировать эксперта по оценке качества регулировки усиления в каждом или в обоих каналах ЭКГ. Эксперт, контролирующий работу регулировки усиления, должен отметить факт окончания процесса регулировки (например, получая сообщение: "изменения усиления нет") до начала подачи в изделие испытательной записи сигналов ЭКГ.
Для испытания качества анализатора используется метод "поциклового сравнения ЭКГ комплексов", описанный в перечислении с) настоящего подпункта. Метод обеспечивает получение QRS Se (чувствительность), QRS +P (специфичность), VEB Se, VEB +P и (если заявлено в документации на изделие) SVEB Se, SVEB +P. Порядок обработки данных, описанный в перечислении d) настоящего подпункта должен использоваться для получения Se и +P эпизодов VF (желудочковых фибрилляций) и AF (фибрилляций предсердий).
b) Использование обучающих (аннотационных) файлов
Протоколы испытаний, описанные в перечислениях с) и d) настоящего подпункта, требуют, чтобы для каждой записи выходные отчетные файлы изделия были записаны в том же формате, что и испытательные файлы баз данных. С целью сравнения испытательных и отчетных файлов должны использоваться программы на основе базы данных по аритмиям MIT-BIH на компакт-дисках (CD-ROM) (программы "bxb", "rxr", "epic", "mxm") или более поздние версии, реализованные МIТ, или должны использоваться программы с равноценными функциями и выходными сигналами. Изготовитель, использующий программы, отличающиеся от программ, реализованных МIТ, должен показать эквивалентность этих программ. Маркированные файлы, представленные в базах данных и использующиеся в качестве входных сигналов, не могут быть изменены каким-либо путем, за исключением тех (где применимо) уточненных маркированных файлов, которые получены от поставщиков баз данных при подтверждении эквивалентности.
Внутри испытательных файлов определены следующие маркеры сердечных комплексов:
N - любой комплекс, который не подпадает под категории S, V, F или Q, описанные ниже (нормальные кардиоциклы или кардиоциклы с блокадой ножки пучка ГИССА);
S - наджелудочковая экстрасистола (SVEB-наджелудочковое эктопическое сокращение): предсердное или AV-узловое преждевременное (функциональное) сокращение или выскальзывающее сокращение, или аберрантное (с отклонением от нормы) преждевременное предсердное сокращение;
V - желудочковая экстрасистола (VEB-желудочковое эктопическое сокращение): желудочковое преждевременное сокращение, желудочковое преждевременное сокращение типа "R-на-Т" или желудочковое выскальзывающее сокращение;
F - сливной комплекс (наложение желудочкового комплекса и комплекса нормального ритма);
Q - (Paced beat), стимулированный комплекс, слияние стимулированного комплекса с нормальным комплексом базового ритма или комплекс, который невозможно классифицировать.
Для облегчения процесса сравнения в перечислении с) настоящего подпункта определены дополнительные метки:
U - метка, которая маркирует сегмент нечитаемых данных.
Метки U появляются в базах данных, где комплексы сокращений не могут быть идентифицированы из-за чрезмерного шума или потерь сигнала по обоим каналам. В базе данных MIT пара меток U отмечает начало и конец каждого нечитаемого сегмента.
В базе данных AHA единичная метка U маркирует (приблизительный) центр каждого нечитаемого сегмента, начало которого устанавливается через 150 мс после предшествующей метки комплекса, а конец - за 150 мс перед меткой последующего комплекса.
При маркировке сегментов анализ, проводимый изделием, может приостанавливаться (прекращаться) из-за чрезмерного шума или потери сигнала, или по какой-либо другой причине. В этом случае изделие должно также вырабатывать метки U. Метки комплексов никогда не образуют пары с метками U в процессе поциклового сравнения.
Иногда возникают ложные комплексы (ложный положительный QRS), иногда теряются истинные комплексы (ложный отрицательный QRS). Для обеспечения процесса испытаний в испытательные файлы добавляются псевдометки, а в выходном файле ИЗДЕЛИЯ произвольно возникают ложные метки. Они используются в процессе проведения поциклового сравнения для получения необходимой статистики. Вводятся два типа меток:
Х - метка псевдосокращения, созданная внутри сегмента, помеченного как нечитаемого в испытательном файле базы данных;
О - метка псевдосокращения, созданная в остальных участках испытательного файла.
При поцикловом сравнении все метки объединяются в пары. Если испытательные файлы содержат псевдометки, которые не возникают в выходных файлах изделия, то подходящие метки О и Х отождествляются с псевдометками. Это соответствует определению ошибки QRS - ложному положительному или ложному отрицательному определению, в зависимости от наличия метки в испытательном файле. Все такие пары меток комплексов подсчитываются, включая и те, которые содержат метки О или X. Метки О и Х не используются при оценке точности выявления эпизодов нарушения ритма (run by run) [перечисление с) настоящего подпункта], включая оценки эпизодов VF и AF (фибрилляция желудочков и предсердий) [перечисление d) настоящего подпункта], так как для этих этапов нет необходимости объединять в пары отдельные метки комплексов.
В базах данных AHA и MIT следующие метки маркируют сегменты трепетания желудочков или фибрилляции предсердий:
[ - начало VF;
] - конец VF.
Комплекс продолжается между метками "[" и "]". Сегменты VF исключаются из процедуры поциклового сравнения комплексов.
В базе данных MIT используются дополнительные метки, отмечающие моменты изменения ритмов. Метки маркируют сегменты трепетания предсердий или фибрилляции желудочков (например AF, см. документацию, прилагаемую к каждой базе данных) и используются для оценки обнаружения AF. Метки комплексов никогда не образуют пары с метками ритмов.
с) Поцикловое сравнение комплексов
При сравнении комплексов справочные метки и метки, установленные изделием, подбираются попарно. При подборе абсолютная разница между временем конкретного комплекса по метке, установленной изделием, и временем, записанным в справочном файле, не должна превышать 150 мс. Если внутри окна не проведен подбор, то считается, что ожидаемый комплекс потерян или было специальное определение. Конечный результат сравнения по каждому комплексу представляет собой матрицу в соответствии с таблицей 104, каждый элемент которой - это точная итоговая сумма сведенных в пары меток комплексов соответствующего типа.
Таблица 104 - Матрица поциклового сравнения комплексов
Справочная метка | Метка, устанавливаемая изделием | ||||||
n | s | v | f | q | o | x | |
N | Nn | Ns | Nv | Nf | Nq | No | Nx |
S | Sn | Ss | Sv | Sf | Sq | So | Sx |
V | Vn | Vs | Vv | Vf | Vq | Vo | Vx |
F | Fn | Fs | Fv | Ff | Fq | Fo | Fx |
Q | Qn | Qs | Qv | Qf | Qo | Qx | |
O | On | Os | Ov | Of | Oq | - | - |
Х | Xn | Xs | Xv | Xf | Xq | - | - |
Поцикловое сравнение комплексов выполняют в соответствии со следующим методом:
1) Переменная величина устанавливается равной времени первой метки комплекса в испытательном файле после конца обучающего периода; переменная величина
устанавливается равной времени с первой метки комплекса, установленной изделием после конца обучающего периода. Все элементы матрицы устанавливаются на ноль.
Если значение величины находится в пределах 150 мс от начала испытательного сегмента, допустимо, чтобы интервал сравнения меток захватывал участок до начала испытательного сегмента. Если это имеет место, то утверждается совпадение (
относится к первому шагу поциклового сравнения до перехода ко второму шагу). С другой стороны, если значение величины
лежит в пределах 150 мс от начала сегмента испытания и при этом отсутствует тестовая метка справочного файла, то метка, установленная изделием, не учитывается (
относится ко времени следующей испытательной метки комплекса перед переходом ко второму шагу).
2) Должна рассматриваться одна из следующих ситуаций:
ситуация а). Если величина предшествует величине
, устанавливают величину
ко времени следующей испытательной метки комплекса (или ко времени за пределом окончания записи, если больше нет испытательных меток комплексов). Теперь существуют две возможности:
(i) Если значение величины ближе к значению величины
, а не величины
, и значение величины
лежит в пределах 150 мс от
(окно совпадения), то метки комплексов при указанных значениях величин
и
образуют пару. Переменная величина
устанавливается вновь на время следующей метки комплекса справочного испытательного файла.
(ii) В противном случае испытательная метка комплекса при величине отмечает псевдообнаружение. Эта дополнительная метка образует пары с О или Х "псевдометками комплексов". Переменная величина
вновь устанавливается до значения
.
ситуация b). Если величина не предшествует величине
, устанавливают величину
на время следующей метки комплекса справочного файла (или на время за пределами окончания записи, если больше не существует справочных меток комплексов). Тогда снова существуют две возможности:
(i) Если величина ближе к величине
, чем к величине
, и лежит в пределах 150 мс от величины
, то метки комплексов при величинах
и
образуют пару. Переменная величина
устанавливается равной времени следующей метки комплекса испытательного файла.
(ii) В противном случае изделие теряет комплекс при величине , и тогда используются "псевдометки комплексов" O или X. Переменная величина
устанавливается вновь на значение величины
.
ситуация с). Элемент матрицы, соответствующий паре меток комплексов, полученных для ситуации b), увеличивается на 1.
ситуация d). Ситуации b) и с) повторяют до тех пор, пока значения величин и
не выйдут за пределы окончания записи.
При построении матрицы применяемая процедура должна сохранять информацию во время сегментов, которые были промаркированы как нечитаемые или как VF в любом испытательном или выходном файле ИЗДЕЛИЯ. При нечитаемых сегментах используются псевдометки X; при всех других - псевдометки О. Метки комплексов, полученные в течение достоверных сегментов VF, не учитываются. Справочные метки комплексов, представленные в течение промаркированных изделием сегментов VF, образуют пары с псевдометками О и определяются подобно всем остальным потерянным комплексам. В принципе, нечитаемые сегменты или сегменты VF могут начинаться в течение периода обучения, а возможность этого должна быть принята во внимание компьютерной программой, разработанной для осуществления сравнений каждого комплекса.
Результаты сравнений каждого комплекса используют для получения QRS чувствительности и специфичности:
QTP=Nn+Ns+Nv+Nf+Nq+ | QFN=No+Nx; | ||||
Sn+Ss+Sv+Sf+Sq+ | So+Sx+ | ||||
Vn+Vs+Vv+Vf+Vq+ | Vo+Vx+ | ||||
Fn+Fs+Fv+Ff+Fq+ | Fo+Fx+ | ||||
Qn+Qs+Qv+Qf+Qq; | Qo+Qx; | ||||
QFP=On+Os+Ov+Of+Oq+Xn+Xs+Xv+Xf+Xq; | |||||
QRS Se=QTP/(QTP+QFN). | QRS+P=QTP/(QTP+QFP). | ||||
Результаты сравнений каждого комплекса используют для получения VEB чувствительности и специфичности:
VTP=Vv; | VFN=Vn+Vs+Vf+Vq+Vo+Vx; | ||||
VFP=Nv+Sv+Ov+Xv; | |||||
VEB Se=VTP/(VTP+VFN) | VEB+P=VTP/(VTP+VFP). | ||||
Отметим, что VTP и VFP не включают Fv или Qv, что не оказывает влияния на оценку за счет объединенных сливных желудочковых комплексов и сомнительных комплексов.
Чувствительность и специфичность SVEB определяют, как указано ниже:
SVTP=Ss; | SVFN=Sn+Sv+Sf+Sq+So+Sx; | |||
SVFP=Ns+Vs+Fs+Os+Xs; | ||||
SVEB Se=SVTP/(SVTP+SVFN) | SVEB+P=SVTP/(SVTP+SVFP). | |||
Отметим снова, что Qs исключается из SVTP и SVFP, поскольку это оказывает влияние на определение SVEB.
d) Сравнение VF и AF
Изделия, предназначенные для определения VF, также должны подвергаться испытанию. Это испытание требует получения выходных файлов ИЗДЕЛИЯ, содержащих (как минимум) промежутки времени, когда изделие определяло приступы VF, включая начало и конец. Частичное перекрытие существует в течение любого интервала, в котором и справочные, и выходные файлы ИЗДЕЛИЯ показывают, что VF прогрессирует. Каждый эпизод в справочном файле, для которого существует частичное перекрытие, с целью определения чувствительности приступа VF рассматривается как достоверный позитив; любые другие справочные эпизоды приступов рассматриваются как ложные негативы. Подобным образом каждый эпизод, промаркированный алгоритмом, для которого существование частичного перекрытия рассматривается для определения специфичности, можно считать как достоверный позитив. Любые другие промаркированные приступы (не имеющие перекрытия) рассматриваются как ложные позитивы.
Изделия, предназначенные для определения AF, также должны подвергаться испытанию. Это испытание осуществляют по такому же методу, что и в случае с VF, но с заменой на "AF" в описании, приведенном выше. Сегменты, промаркированные как трепетание предсердий в справочных аннотационных файлах, должны быть исключены из сравнения.
Исходя из числа достоверных позитивов ложные негативы и ложные позитивы получаются в соответствии с вышеприведенными методами, а чувствительность и специфичность приступов VF и AF определяют визуальным методом.
*50.101.3 Минимальные требования к отчету врача
Любые перечисленные ниже нарушения, определяемые ИЗДЕЛИЕМ, должны быть представлены в отчете. В отчете должны быть зарегистрированы все параметры, выбранные ОПЕРАТОРОМ, подведен итог по каждому пункту обследования в течение полных промежутков времени, определенных изготовителем, затем подведен итог по всей процедуре.
50.101.3.1 Частота сердечных сокращений
В отчете должны быть представлены наименьшая, средняя и наивысшая частоты сердечных сокращений. Итоговая информация должна также отражать общее число выявленных ударов сердца.
50.101.3.2 Наджелудочковая эктопия
Должны быть представлены в отчете общее число SVEB, единичных SVEB, парных SVEB, выбегов SVT и продолжительность некоторых форм SVT (любые суммы сокращений или время действия). Итоговая информация должна включать общее число каждого события, которое имело место в течение процедуры. В отчете должен быть подведен итог по каждому пункту по крайней мере за каждый час обследования и затем в конце дан итог всей процедуры.
50.101.3.3 Желудочковые экстрасистолии
В отчете должны быть представлены общее число желудочковых экстрасистолий (VEB), единичных VEB, парных VEB и выбегов трех или более VEB, а также продолжительность выбегов (число сокращений и/или продолжительность). При приступах желудочковой тахикардии для каждого приступа в отчете должны быть представлены частота и продолжительность (либо суммарное число комплексов и время действия). В отчете должно быть представлено количество минут (секунд, по выбору), которые были проанализированы по каждому каналу, а также количество времени, в течение которого анализ не проводился.
50.101.3.4 Данные по брадикардии
Требуется ежечасное представление общего числа приступов брадикардии, установленная частота их появления и продолжительность. В отчете приступы брадикардии должны быть представлены со следующими характеристиками: частота сердечных сокращений менее 50 в минуту за период 15 с или параметры, выбранные изготовителем, или параметры, определенные пользователем.
50.101.3.5 Паузы в сердечных сокращениях
В отчете должно быть представлено общее число пауз, выбранных ОПЕРАТОРОМ на основе абсолютной пороговой величины или выбранных изготовителем параметров. В отчете должны быть представлены также расположение и продолжительность самых длинных пауз.
50.101.3.6 Сдвиги сегментов ST
Если изготовитель заявил, что ИЗДЕЛИЕ способно определять и измерять сдвиги сегментов ST, соответствующие измерения (вместе с параметрами, заявленными изготовителем) должны быть приведены в отчете. Описание должно быть включено в ЭКСПЛУАТАЦИОННЫЕ ДОКУМЕНТЫ.
50.101.3.7 Распечатка ЭКГ на бумагу
Выбранные ОПЕРАТОРОМ скорость записи (25 мм/с) и чувствительность (мм/мВ) должны фиксироваться для каждого сообщения с целью удобства при проведении каждого клинического заключения. Должна отображаться любая заявленная конфигурация ОТВЕДЕНИЯ для каждого канала при каждой записи ЭКГ. Записи ЭКГ должны как минимум включать следующую информацию:
- время;
- частоту сердечных сокращений;
- аннотацию.
Дополнительно каждая "страница" записей ЭКГ должна содержать идентификацию ПАЦИЕНТА. "Страница" в настоящем контексте может быть представлена либо одноканальным графиком ЭКГ, выводимым с помощью ленточного регистратора, либо несколькими графиками на листах бумаги формата А.4. Калибровочный сигнал по каждому каналу должен быть представлен в каждой записи, включая метки, для которых был проведен анализ сегмента ST.
51 Защита от представляющих опасность выходных характеристик
*51.5 Неправильные выходные характеристики
Замена
*51.5.1 Динамический диапазон входного сигнала
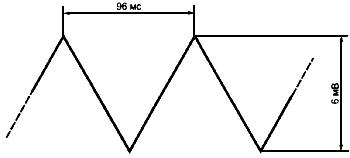
ИЗДЕЛИЕ должно регистрировать и отображать напряжения размахом 6 мВ для аналоговых регистраторов (при чувствительности 5 мм/мВ) при скорости изменения напряжения 125 мВ/с и при наличии на входе постоянного напряжения смещения ±300 мВ. Отображенный выходной сигнал не должен отличаться от входного сигнала более чем на 10% в диапазоне от 0,5 мВ и выше и не более чем на 50 мкВ - в диапазоне до 0,5 мВ.
Размах входного напряжения для аналоговых регистраторов должен быть 6 мВ.
Соответствие требованию проверяют следующим испытанием.
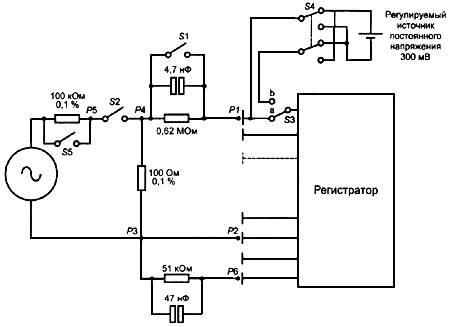
a) Устанавливают чувствительность 5 мм/мВ. Подают треугольный сигнал частотой 10,4 Гц и размахом 6 мВ (рисунок 103) в испытательную цепь (рисунок 104) с замкнутыми переключателям S1, S2 и переключателем S3 в положении а и при подключении положительного ЭЛЕКТРОДА ПАЦИЕНТА каждого канала к точке соединения Р1.
b) Подключают соединение отрицательного ЭЛЕКТРОДА ПАЦИЕНТА каждого канала через точку соединения Р2 к общему ПРОВОДУ ОТВЕДЕНИЯ через параллельное соединение сопротивления 51 кОм и конденсатора 47 нФ. Записывают треугольный сигнал.
c) Устанавливают переключатель S3 в положение b и используют переключатель S4 для подачи напряжения смещения 300 мВ, ждут 30 с и повторяют запись.
d) Оставляют переключатель S3 в положении b и используют переключатель S4 для изменения полярности напряжения смещения 300 мВ, ждут 30 с и повторяют запись.
e) Убеждаются, что размах отображаемого треугольного сигнала находится в пределах от 5,4 до 6,6 мВ.
ИЗДЕЛИЕ должно регистрировать и отображать напряжения размахом 10 мВ для цифровых регистраторов (при чувствительности 5 мм/мВ) и скорости напряжения не менее 125 мВ/с при наличии на входе постоянного напряжения смещения ±300 мВ. Отображенный выходной сигнал не должен отличаться от входного сигнала более чем на 10% в диапазоне от 0,5 мВ и выше и не более чем на 50 мкВ - в диапазоне до 0,5 мВ.
Размах входного напряжения для цифровых регистраторов должен быть 10 мВ.
Соответствие требованию проверяют следующим испытанием.
f) Устанавливают чувствительность 5 мм/мВ. Подают треугольный сигнал частотой 10,4 Гц и размахом 10 мВ (рисунок 103) в испытательную цепь (рисунок 104) с замкнутыми переключателями S1 и S2 и переключателем S3 в положении а и при подключении положительного ЭЛЕКТРОДА ПАЦИЕНТА каждого канала к точке соединения Р1.
g) Подключают соединение отрицательного ЭЛЕКТРОДА ПАЦИЕНТА каждого канала через точку соединения Р2 к общему ПРОВОДУ ОТВЕДЕНИЯ через параллельное соединение сопротивления 51 кОм и конденсатора 47 нФ. Записывают треугольный сигнал.
h) Устанавливают переключатель S3 в положение b и используют переключатель S4 для подачи напряжения смещения 300 мВ, ждут 30 с и повторяют запись.
i) Оставляют переключатель S3 в положении b и используют переключатель S4 для изменения полярности напряжения смещения 300 мВ, ждут 30 с и повторяют запись.
j) Убеждаются, что размах отображаемого треугольного сигнала находится в пределах от 9,0 до 11,0 мВ.
В качестве альтернативы применяют испытание синусоидальным сигналом 4 Гц непрерывным или состоящим из изолированных циклов, повторяющихся один раз в секунду, в соответствии с перечислениями f), g), h), i), j) настоящего пункта.
*51.5.2 Входной импеданс
Входной импеданс должен быть более 10 МОм на частоте, определенной при испытании для всех входных каналов. Это требование должно выполняться при наличии на входе постоянного напряжения смещения.
Соответствие требованию проверяют следующим испытанием.
a) Используют испытательную цепь, изображенную на рисунке 104.
b) Замыкают переключатели S1 и S2, размыкают переключатель S5, устанавливают переключатель S3 в положение а. Подают синусоидальный сигнал частотой 10 Гц, размахом 5 мВ на точки соединения Р1 и Р2.
c) Подключают соединения ЭЛЕКТРОДОВ ПАЦИЕНТА первого канала к точкам соединения Р1 и Р2. Все другие соединения ЭЛЕКТРОДОВ ПАЦИЕНТА подключают к точке соединения Р6.
d) Измеряют амплитуду выходного сигнала на УСТРОЙСТВЕ ВОСПРОИЗВЕДЕНИЯ изготовителя.
e) Размыкают переключатель S1 и измеряют изменения амплитуды выходного сигнала. Амплитуда установившегося выходного сигнала не должна уменьшаться более чем на 6%.
f) Повторяют испытание с напряжениями смещения плюс 300 мВ и минус 300 мВ.
g) Повторяют все эти испытания для всех других каналов ЭКГ.
*51.5.3 Подавление синфазной помехи
Подавление синфазной помехи должно быть не менее 60 дБ для синусоидального сигнала при частоте ПИТАЮЩЕЙ СЕТИ и не менее 45 дБ - при удвоенной частоте ПИТАЮЩЕЙ СЕТИ. Подавление синфазной помехи определяют как отношение значения размаха напряжения с частотой ПИТАЮЩЕЙ СЕТИ, подаваемого на вход синфазно, к значению размаха отображаемого сигнала в каждом канале ЭКГ.
Соответствие требованию проверяют следующим испытанием.
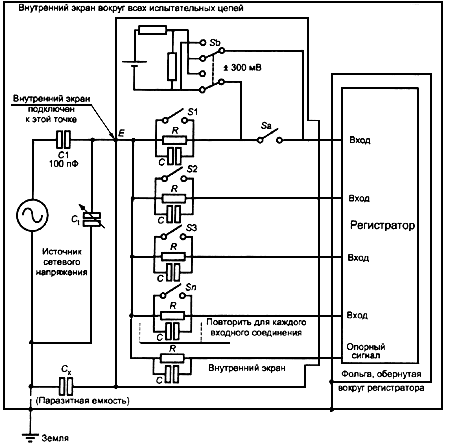
Применяют испытательную цепь, изображенную на рисунке 105.
a) Используют рекомендуемые изготовителем КАБЕЛИ ПАЦИЕНТА или равноценные им. Накладывают на испытуемое ИЗДЕЛИЕ проводящую фольгу и подсоединяют ее к земле. Фольга должна полностью покрывать ИЗДЕЛИЕ, за исключением входов КАБЕЛЕЙ ПАЦИЕНТА, и должна соответствовать профилю ИЗДЕЛИЯ. Зазор между фольгой и изделием не должен превышать 3 мм. КАБЕЛИ ПАЦИЕНТА должны быть обернуты по всей длине в подобный экран из фольги, подключенный к точке подачи напряжения ПИТАЮЩЕЙ СЕТИ (точка Е). К этой же точке должны быть подключены экран, в котором размещены резистивно-конденсаторные цепи, источник постоянного напряжения смещения и переключатели. ИЗДЕЛИЕ и измерительные цепи помещают в наружный экран, соединенный с землей. Устанавливают сигнал помехи на частоте ПИТАЮЩЕЙ СЕТИ. Узкополосные режекторные фильтры на частоте питания в ИЗДЕЛИИ должны быть отключены, даже если компьютерная программа не позволяет ПОЛЬЗОВАТЕЛЮ сделать это.
b) Каждое ОТВЕДЕНИЕ ЭЛЕКТРОДОВ ПАЦИЕНТА подключают к точке Е последовательно: с сопротивлением 51 кОм, конденсатором 47 нФ и переключателем, соединенными параллельно. Подключают НЕЙТРАЛЬНЫЙ ЭЛЕКТРОД, если имеется, через сопротивление 51 кОм, соединенное параллельно с конденсатором 47 нФ, к этой же точке Е. Подают испытательный сигнал помехи в точку Е через конденсатор 100 пФ. Нижнюю поверхность генератора заземляют. Переключатели на участке цепи от S1 до Sn включительно должны быть разомкнуты, переключатель Sa замкнут. Регулируют конденсатор до тех пор, пока:
![]() =100 пФ.
=100 пФ.
Эта регулировка должна быть проделана, когда испытуемое ИЗДЕЛИЕ полностью удалено из испытательной установки, а КАБЕЛИ ПАЦИЕНТА, фольга вокруг КАБЕЛЕЙ ПАЦИЕНТА и измерительные цепи расположены внутри заземленного внешнего экрана в положениях, которые они будут занимать при испытании ИЗДЕЛИЯ. Внешний экран должен находиться в положении, в котором будет использоваться при текущих испытаниях. Результирующее испытательное напряжение на конденсаторе , будет составлять
значения сигнала генератора. Открывают внешний экран, подключают ИЗДЕЛИЕ, закрывают внешний экран и записывают сигнал.
с) Повторяют испытание с постоянным напряжением смещения плюс 300 мВ и минус 300 мВ путем открывания переключателя Sa и переключений переключателя Sb в каждое положение. Повторяют испытание с последовательным смещением по каждому входу.
d) Повторяют испытания с замкнутыми переключателями от S1 до Sn no очереди при двойной частоте ПИТАЮЩЕЙ СЕТИ.
Измеренный размах выходного сигнала в течение каждого периода испытаний не должен превышать 4 мВ при размахе напряжения на входе 4 В на частоте ПИТАЮЩЕЙ СЕТИ. На двойной частоте ПИТАЮЩЕЙ СЕТИ измеренный размах выходного сигнала в течение каждого периода испытаний не должен превышать 4 мВ при размахе напряжения на входе 1,422 В.
*51.5.4 Погрешность чувствительности
Выходной сигнал при всех возможных установках чувствительности не должен отличаться от входного сигнала в пределах ±10%.
Соответствие требованию проверяют следующим испытанием.
Подают синусоидальный сигнал частотой 5 Гц и размахом 2 мВ на все входные каналы ЭКГ. Выходной сигнал должен соответствовать вышеуказанным требованиям при каждой возможной установке чувствительности.
*51.5.5 Стабильность чувствительности
Спустя одну минуту после включения ИЗДЕЛИЯ изменение чувствительности не должно превышать 3% в течение 24 ч (при неизменных условиях окружающей среды).
Соответствие требованию проверяют следующим испытанием.
Подают синусоидальный сигнал частотой 5 Гц и размахом 2 мВ на все входные каналы ЭКГ в течение 24 ч. При каждой возможной установке чувствительности проверяют, что выходной сигнал соответствует требованиям в любой момент времени в течение первого часа (проверяют через 1 мин, 2 мин, 5 мин, 10 мин, 20 мин, 30 мин, 45 мин и 60 мин) и один раз в течение каждого последующего часа до истечения 24 ч.
*51.5.6 Калибровка амплитуды
С целью калибровки системы калибровочный сигнал, эквивалентный напряжению (1,0±0,05) мВ на входах ЭКГ, должен быть использован для аналоговых систем. Сигнал может иметь форму ступеньки или импульса с временем нарастания менее 5 мс (время нарастания амплитуды калибровочного сигнала от 10% до 90%).
Соответствие требованию определяют осмотром.
*51.5.7 Требования к шумам системы
Размах напряжения внутренних шумов, приведенных к входу и регистрируемых на выходе системы, не должен превышать 50 мкВ в течение любых 10 с, когда все входы через сопротивление 51 кОм, установленное параллельно конденсатору 47 нФ, последовательно соединены с каждым подсоединением ЭЛЕКТРОДА ПАЦИЕНТА. Любые узкополосные режекторные фильтры на частоте ПИТАЮЩЕЙ СЕТИ, если имеются, должны быть включены в течение этого испытания на соответствующей частоте ПИТАЮЩЕЙ СЕТИ.
Соответствие требованию проверяют следующим испытанием.
Включают последовательно в каждое подсоединение ЭЛЕКТРОДА ПАЦИЕНТА сопротивление 51 кОм, установленное параллельно конденсатору 47 нФ, как показано на рисунке 105, затем соединяют все подсоединения ЭЛЕКТРОДОВ ПАЦИЕНТА, включая подсоединение правой ноги, вместе. В этом испытании не подключают генератор входных сигналов и конденсатор 100 пФ. При максимальной чувствительности осуществляют запись в течение 2 мин. Запись, полученную в течение первых 10 с и последних 10 с, во внимание не принимают. Разделяют оставшиеся 100 с на интервалы по 10 с каждый и проверяют затем в каждом интервале уровни шума на выходе. Размах напряжения внутренних шумов должен находиться в пределах допуска по крайней мере в девяти из десяти интервалов.
*51.5.8 Взаимовлияние между каналами
Взаимовлияние между каналами ИЗДЕЛИЯ не должно приводить в любом канале к возникновению выходного сигнала размахом более 0,2 мВ.
Соответствие требованию проверяют следующим испытанием.
а) Подключают АМБУЛАТОРНЫЙ РЕГИСТРАТОР к испытательной цепи, изображенной на рисунке 104, с закрытыми переключателями S1 и S2, открытым S5, переключателем S3 в положении а, положительные ЭЛЕКТРОДЫ ПАЦИЕНТА всех каналов подключают к точке соединения Р1.
b) Подключают общий ЭЛЕКТРОД ПАЦИЕНТА каждого канала через точку соединения Р2 к общему ПРОВОДУ ОТВЕДЕНИЯ через сопротивление 51 кОм, включенное параллельно конденсатору 47 нФ.
c) Регулируют сигнал генератора с целью получения между точками соединения Р1 и Р2 синусоидального сигнала размахом 4 мВ и частотой 10 Гц. Записывают сигнал по крайней мере в течение 10 с.
d) Отсоединяют все, кроме одного, положительные ЭЛЕКТРОДЫ ПАЦИЕНТА от точки соединения Р1 и подключают к точке соединения Р2. Записывают сигнал по крайней мере в течение 10 с.
e) Повторяют это для оставшихся каналов, подключая к точке соединения Р1 за один раз только один положительный ЭЛЕКТРОД ПАЦИЕНТА.
Размах выходных сигналов каналов, положительные ЭЛЕКТРОДЫ ПАЦИЕНТА которых подключены к точке соединения Р2, не должен превышать 0,2 мВ.
*51.5.9 Частотная характеристика
ИЗДЕЛИЕ должно соответствовать следующим требованиям:
a) Отклик АМБУЛАТОРНОГО РЕГИСТРАТОРА на прямоугольный импульс 3 мВ, 100 мс не должен приводить к смещению базовой линии после действия импульса относительно базовой линии перед действием импульса более чем на 0,1 мВ. Спад вершины импульса должен быть менее 0,3 мВ/с. Выброс переднего фронта импульса должен быть менее 10%.
Кроме того:
b) Неравномерность амплитудно-частотной характеристики в диапазоне частот от 0,67 до 40 Гц должна быть в пределах от плюс 40% до минус 30% (от плюс 3 дБ до минус 3 дБ) относительно частоты 5 Гц.
Если в ИЗДЕЛИИ изготовителем предусмотрена возможность измерения сегмента ST, нижняя граничная частота должна быть не более 0,05 Гц для фильтра верхних частот первого порядка или его функционального эквивалента.
Если изготовитель отметил, что ИЗДЕЛИЕ имеет возможность записи ЭКГ у грудных детей массой менее 10 кг, верхняя граничная частота должна быть не менее 55 Гц.
Или:
c) Отклики на пачки треугольных импульсов 1,5 мВ, 40 мс, которые имитируют серии узких R-зубцов ЭКС, должны быть в пределах от 60% до 110% относительно отклика на действие пачки треугольных импульсов 1,5 мВ, 200 мс.
Если изготовитель отметил, что ИЗДЕЛИЕ имеет возможность записи ЭКГ у грудных детей массой менее 10 кг, отклик на треугольные импульсы 1,5 мВ, 40 мс должен быть в пределах от 80% до 100% относительно отклика на треугольные импульсы 1,5 мВ, 200 мс.
Соответствие требованиям проверяют следующими испытаниями.
Системным входом является ЭЛЕКТРОД ПАЦИЕНТА; выход измеряют по записи ЭКГ на системной твердой копии.
a) Записывают по крайней мере в течение 20 с нулевую (базовую) линию и затем одиночный прямоугольный импульс 3 мВ, 100 мс. Продолжают запись нулевой линии по крайней мере в течение следующих 20 с.
b) С помощью испытательной цепи, изображенной на рисунке 104, записывают по крайней мере в течение 5 с синусоидальный сигнал размахом 2 мВ, частотой 0,67 Гц. Повторяют это для частот 1 Гц, 2 Гц, 5 Гц, 10 Гц, 20 Гц и 40 Гц.
Если в ИЗДЕЛИИ изготовителем предусмотрена возможность измерения сегмента ST, проводят вышеуказанные испытания при низких частотах от 0,67 до 0,05 Гц или применяют эквивалентные методы.
Если изготовитель отметил, что ИЗДЕЛИЕ имеет возможность записи ЭКГ у грудных детей массой менее 10 кг, проводят вышеуказанные серии испытаний при верхних частотах от 40 до 55 Гц.
c) Записывают по крайней мере в течение 5 с пачку треугольных импульсов 1,5 мВ, длительностью 200 мс с частотой повторения 1 Гц. Затем уменьшают длительность треугольных импульсов до 40 мс. Проводят запись в течение 2 мин, изменяя медленно частоту повторения от 60 до 70 импульсов в минуту, чтобы обеспечить получение всей огибающей амплитуд.
Проверяют с помощью следующих измерений записи на твердой копии:
a) Базовая линия после подачи прямоугольного импульса 3 мВ относительно положения базовой линии до подачи прямоугольного импульса смещается не более чем на 0,1 мВ. Спад вершины импульса не превышает 0,3 мВ/с.
b) Размах сигнала на частотах 0,67 Гц, 1 Гц, 2 Гц, 10 Гц, 20 Гц, 40 Гц находится между 70% и 140% от размаха сигнала на частоте 5 Гц.
Если в ИЗДЕЛИИ изготовителем предусмотрена возможность измерения сегмента ST, заменяют нижнюю граничную частоту 0,67 Гц на 0,05 Гц или ее функциональным эквивалентом.
Если изготовитель отметил, что ИЗДЕЛИЕ имеет возможность записи ЭКГ у грудных детей массой менее 10 кг, заменяют верхнюю граничную частоту 40 Гц на 55 Гц.
с) Наименьший пик пачки треугольных импульсов 1,5 мВ, 40 мс составляет не менее 60% наибольшего пика пачки треугольных импульсов 1,5 мВ, 200 мс.
Если изготовитель отметил, что ИЗДЕЛИЕ имеет возможность записи ЭКГ у грудных детей массой менее 10 кг, наименьший пик пачки треугольных импульсов 1,5 мВ, 40 мс составляет не менее 80% наибольшего пика пачки треугольных импульсов 1,5 мВ, 200 мс.
*51.5.10 Минимальный регистрируемый сигнал
Синусоидальный сигнал частотой 10 Гц и размахом 50 мкВ должен быть различим на записи при скорости развертки 25 мм/с и установке чувствительности 10 мм/мВ.
Соответствие требованию проверяют измерением.
*51.5.11 Функционирование при наличии импульсов кардиостимулятора
Если изготовитель отметил, что в АМБУЛАТОРНОМ РЕГИСТРАТОРЕ имеется возможность записи сигнала ЭКГ при наличии импульсов имплантированного кардиостимулятора, то на функционирование ИЗДЕЛИЯ не должна оказывать неблагоприятное воздействие работа имплантированного кардиостимулятора.
Соответствие требованию проверяют следующим испытанием.
a) Подключают ИЗДЕЛИЕ к цепи, как показано на рисунке 106, с присоединением положительного ЭЛЕКТРОДА ПАЦИЕНТА каждого канала к точке соединения Р1 и присоединением отрицательного ЭЛЕКТРОДА и общего ЭЛЕКТРОДА - к точке соединения Р2.
b) Регулируют генератор синусоидального сигнала таким образом, чтобы на сопротивлении 111 Ом был синусоидальный сигнал частотой 10 Гц и размахом (2,0±0,2) мВ. Генератор импульсов на сопротивлении 111 Ом добавляет импульсы (200±25) мВ длительностью (1,0±0,1) мс и временем нарастания 100 мкс с частотой повторения 100 импульсов/мин.
c) Осуществляют запись по крайней мере в течение 30 с.
d) Меняют местами присоединения положительных и отрицательных ЭЛЕКТРОДОВ по перечислению а) и повторяют запись.
e) Убеждаются при воспроизведении входного сигнала по перечислению b), что для всех импульсов высота второго пика синусоидального сигнала после импульса не отличается от высоты пика синусоидального сигнала непосредственно перед импульсом более чем на 0,2 мВ.
Если изготовитель отметил, что ИЗДЕЛИЕ имеет возможность записи деятельности имплантированного кардиостимулятора, оно должно проводить видимую запись импульсов кардиостимулятора с амплитудами между 2 мВ и 200 мВ, длительностями между 0,1 мс и 2,0 мс и временем нарастания менее 100 мкс.
Соответствие требованию проверяют следующим испытанием.
Испытания должны быть проведены с использованием четырех различных импульсов, имеющих время нарастания менее 100 мкс: первый импульс имеет амплитуду 2 мВ и длительность 2 мс; второй импульс имеет амплитуду 200 мВ и длительность 2 мс; третий импульс имеет амплитуду 20 мВ и длительность 0,1 мс; четвертый импульс имеет амплитуду 2 мВ и длительность 0,1 с.
Осуществляют запись по крайней мере в течение 30 с с установкой выхода синусоидального генератора по перечислению b) настоящего подпункта и частотой повторения 100 импульсов/мин, затем проверяют, чтобы для каждого импульса метка по крайней мере высотой 2 мм была распечатана на твердой копии при той же частоте повторения и том же интервале между импульсами, что и у импульсов на входе в ИЗДЕЛИЕ.
*51.5.12 Точность измерения времени
Полная погрешность в течение 24 ч не должна превышать 30 с.
Соответствие требованию проверяют следующим испытанием.
ИЗДЕЛИЕ осуществляет запись сигнала от имитатора ЭКГ или работает в режиме калибровки в течение 24 ч. При отсчетах времени испытания 1 ч ±1 с, 8 ч ±1 с и 23 ч ±1 с в запись вводят сигнальную метку события. Это может быть обеспечено посредством радиосигналов точного времени. Рассматривают полный протокол и проверяют, что метки событий соответствуют фактическому времени 1-го, 8-го и 23-го часа ведения протокола с отклонением не более 30 с.
*51.5.13 Стандартная сетка твердой копии
Кроме случаев, показанных ниже, твердая копия должна быть разлинована делениями в 1,0 мм вдоль горизонтальной (время) и вертикальной (напряжение) осей. Каждая пятая начерченная линия должна быть выделена. Погрешность нанесения линий должна быть в пределах ±2% при условиях влажности по 10.2.1. Если масштабные коэффициенты менее или равны 6,25 мм/с и 5 мм/мВ (например для максимальной подробности), допускается не использовать сетчатые начерченные линии.
Соответствие требованию проверяют измерением и следующим испытанием.
Используя увеличительное стекло с разрешающей способностью по крайней мере 0,05 мм, измеряют начерченные линии в трех следующих местоположениях на семисантиметровой ленте бумаги для записи: в верхнем левом углу, в середине и нижнем правом углу. В каждом местоположении промежутки между каждой десятой линией внутри квадрата (20х20) мм должны быть в пределах ±2% (±0,2 мм).
*51.5.14 Переключение и установка чувствительности
Установленная чувствительность должна быть распечатана на принтере. Аналоговые системы должны распечатывать на принтере калибровочный импульс.
Соответствие требованию проверяют осмотром распечатки.
*51.5.15 Временное выравнивание
Когда по всем каналам установлена одна и та же полоса пропускания, то временная асимметрия между каналами, за исключением указанного ниже, должна быть в пределах ±20 мс или ±0,5 мм (при масштабе 25 мм/с по оси времени). Это применяется ко всей системе и всем отдельным частям (АМБУЛАТОРНЫЙ РЕГИСТРАТОР, УСТРОЙСТВО ВОСПРОИЗВЕДЕНИЯ и т.д.).
Если асимметрия превышает вышеупомянутый предел, то должно быть включено в запись соответствующее предупреждение о том, что временное выравнивание отсутствует.
Соответствие требованию проверяют следующим испытанием.
a) Подключают АМБУЛАТОРНЫЙ РЕГИСТРАТОР к испытательной цепи, изображенной на рисунке 104. Переключатели S1 и S2 замкнуты, переключатель S3 находится в положении а, переключатель S5 разомкнут. Подключают все положительные присоединения ОТВЕДЕНИЙ к точке соединения Р1 и все отрицательные присоединения ОТВЕДЕНИЙ к точке соединения Р2. Источник сигнала регулируется так, чтобы обеспечить между точками соединения Р1 и Р2 пачки прямоугольных импульсов с амплитудой (1,0±0,5) мВ, длительностью 200 мс, передним и задним фронтами менее 1,0 мс, частотой повторения 1 Гц.
b) Если АМБУЛАТОРНЫЙ РЕГИСТРАТОР или УСТРОЙСТВО ВОСПРОИЗВЕДЕНИЯ имеют переключаемые фильтры, их регулируют так, чтобы все каналы имели одну и ту же полосу пропускания.
c) Записывают по крайней мере в течение 1 ч импульсы по всем каналам АМБУЛАТОРНОГО РЕГИСТРАТОРА. Распечатывают (или выводят на дисплей) в масштабе 25 мм/с и 10 мм/мВ сигналы по крайней мере по двум каналам одновременно. Проверяют, что временной сдвиг по переднему и заднему фронтам сигнала между каждыми каналами менее 20 мс (0,5 мм). Проводят это измерение в трех отдельных точках по каждому каналу в течение 1 ч записи. Повторяют это испытание для всех скоростей развертки, имеющихся в УСТРОЙСТВЕ ВОСПРОИЗВЕДЕНИЯ.
d) Если измеренная асимметрия превышает 20 мс (0,5 мм), то проверяют, чтобы предупреждение было распечатано или отображено на дисплее с помощью УСТРОЙСТВА ВОСПРОИЗВЕДЕНИЯ.
РАЗДЕЛ ДЕВЯТЫЙ. НЕНОРМАЛЬНАЯ РАБОТА И УСЛОВИЯ НАРУШЕНИЯ; ИСПЫТАНИЯ НА ВОЗДЕЙСТВИЕ ВНЕШНИХ ФАКТОРОВ
Применяют раздел общего стандарта.
РАЗДЕЛ ДЕСЯТЫЙ. ТРЕБОВАНИЯ К КОНСТРУКЦИИ
Применяют раздел общего стандарта, за исключением:
*56 Компоненты и общая компоновка
*56.7 Батареи
с) Состояние батареи
Замена
АМБУЛАТОРНЫЕ РЕГИСТРАТОРЫ должны соответствовать следующим требованиям:
АМБУЛАТОРНЫЕ РЕГИСТРАТОРЫ должны иметь средства отображения степени разряда ВНУТРЕННЕГО ИСТОЧНИКА ЭЛЕКТРИЧЕСКОГО ПИТАНИЯ, при котором ИЗДЕЛИЕ не соответствует требованиям настоящего частного стандарта.
Соответствие требованию проверяют осмотром и освидетельствованием.
Дополнение
*56.7.101 Время, в течение которого осуществляется мониторинг и сохранение данных
*56.7.101.1 Время, в течение которого осуществляется мониторинг
а) РЕГИСТРАТОРЫ НЕПРЕРЫВНОГО ДЕЙСТВИЯ должны иметь возможность при полностью заряженном ВНУТРЕННЕМ ИСТОЧНИКЕ ЭЛЕКТРИЧЕСКОГО ПИТАНИЯ, как указано изготовителем, осуществлять непрерывный мониторинг по крайней мере в течение 24 ч.
Соответствие требованию проверяют проведением испытаний, как указано в 51.5.12 при записи сигнала от имитатора ЭКГ.
*56.7.101.2 Сохранение данных
АМБУЛАТОРНЫЕ РЕГИСТРАТОРЫ, использующие средства поддержки энергонезависимой памяти, должны иметь возможность сохранения запомненной информации без какого-либо внешнего питания по крайней мере в течение 72 ч после окончания мониторинга.
Соответствие требованию проверяют следующим образом:
a) Испытывают ИЗДЕЛИЕ, как указано в 56.7.101.1, перечисление а).
b) Выдерживают ИЗДЕЛИЕ в течение 72 ч после записи при температуре 25 °С и влажности 70%.
c) Считывают запись после выдержки и проверяют, что изменения данных отсутствуют.
Размеры в метрах

1 - ШНУР ПИТАНИЯ; 2 - сигнальный провод; 3 - стол, изготовленный из изолирующего материала; 4 - испытуемое ИЗДЕЛИЕ; 5 - КАБЕЛЬ ПАЦИЕНТА; 6 - нагрузка, имитирующая ПАЦИЕНТА (сопротивление 51 кОм, включенное параллельно конденсатору 47 нФ); 7 - металлическая пластина
- конденсатор 220 пФ;
- сопротивление 510 Ом.
и
, соединенные последовательно, имитируют руку
Рисунок 101 - Установка для испытания эмиссионных излучений (36.201.1)
Размеры в метрах
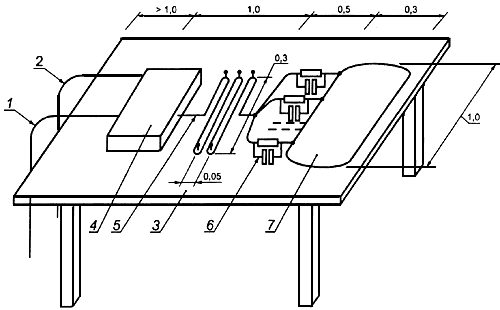
1 - ШНУР ПИТАНИЯ; 2 - сигнальный провод; 3 - стол, изготовленный из изолирующего материала; 4 - испытуемое ИЗДЕЛИЕ; 5 - КАБЕЛЬ ПАЦИЕНТА; 6 - нагрузка, имитирующая ПАЦИЕНТА (сопротивление 51 кОм, включенное параллельно конденсатору 47 нФ); 7 - металлическая пластина
Рисунок 102 -Установка для испытаний на излучение и защищенность от излучения (36.201.1 и 36.202.2)
Рисунок 103 - Сигнал для испытания динамического диапазона входных сигналов (51.5.1)
![]() - переключатели;
- переключатели;![]() - точки соединения
- точки соединения
Рисунок 104 - Общая испытательная цепь (51.5)
- сопротивление 51 кОм;
- конденсатор 47 нФ;
- регулируемый конденсатор
Рисунок 105 - Цепь для испытания подавления синфазной помехи (51.5.3)
Рисунок 106 - Цепь для испытания на устойчивость при действии импульса кардиостимулятора (51.5.11)
Приложение L
(обязательное)
Нормативные ссылки
Дополнение В настоящем стандарте использованы ссылки на следующие стандарты: ГОСТ 30324.0-95/ГОСТ Р 50267.0-92 Изделия медицинские электрические. Часть 1. Общие требования безопасности ГОСТ 30324.25-95/ГОСТ Р 50267.25-94 Изделия медицинские электрические. Часть 2. Частные требования безопасности к электрокардиографам ГОСТ 30324.27-95/ГОСТ Р 50267.27-95 Изделия медицинские электрические. Часть 2. Частные требования безопасности к электрокардиографическим мониторам ГОСТ Р 50267.0.2-95 Изделия медицинские электрические. Часть 1. Общие требования безопасности. 2. Электромагнитная совместимость. Требования и методы испытаний ГОСТ Р 50648-94 Совместимость технических средств электромагнитная. Устойчивость к магнитному полю промышленной частоты. Технические требования и методы испытаний ГОСТ Р 51317.4.2-99 Совместимость технических средств электромагнитная. Устойчивость к электростатическим разрядам. Требования и методы испытаний ГОСТ Р 51317.4.3-99 Совместимость технических средств электромагнитная. Устойчивость к радиочастотному электромагнитному полю. Требования и методы испытаний ГОСТ Р 51318.11-99 Совместимость технических средств электромагнитная. Радиопомехи индустриальные от промышленных, научных, медицинских и бытовых (ПНМБ) высокочастотных устройств. Нормы и методы испытаний |
При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов по указателю "Национальные стандарты", составленному по состоянию на 1 января текущего года, и по соответствующим информационным указателям, опубликованным в текущем году. Если ссылочный документ заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться замененным (измененным) стандартом. Если ссылочный документ отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
Приложение АА
(справочное)
Общие положения и обоснования
В настоящем приложении представлено краткое обоснование важнейших требований настоящего частного стандарта. Понимание обоснований основных требований рассматривается как существенный момент для надлежащего применения стандарта. Кроме того, предполагается, что в результате изменений в клинической практике и в технологии обоснования настоящих требований будут облегчать в будущем любой пересмотр стандарта, который обусловлен этими усовершенствованиями.
10 Условия окружающей среды
Поскольку АМБУЛАТОРНЫЕ РЕГИСТРАТОРЫ могут применяться вне медицинских кабинетов, их использование предполагает расширенные диапазоны температуры и влажности. Установленные требования охватывают большинство условий окружающей среды, которые могут встретиться при практическом использовании.
Не существует установленных требований для типов магнитной ленты и твердотельной памяти, так как оба типа этих изделий используются в одной и той же окружающей среде.
21.5
Другие стандарты, относящиеся к испытаниям на удар АМБУЛАТОРНОГО РЕГИСТРАТОРА, носимого ПАЦИЕНТОМ, устанавливали плотность древесины более 700 кг/м. Практика использования твердой древесины свидетельствует о том, что такая плотность недостижима. Поэтому в настоящем частном стандарте установлена более низкая плотность древесины. Опыт показывает, что выбранная плотность древесины вполне пригодна для испытаний.
36 Электромагнитная совместимость
Наблюдается растущий интерес к электромагнитной совместимости медицинских ИЗДЕЛИЙ. Дополнительный стандарт ГОСТ Р 50267.0.2 отражает этот интерес и обеспечивает общее руководство по применению требований электромагнитной совместимости.
В результате того, что АМБУЛАТОРНЫЕ РЕГИСТРАТОРЫ связаны с ПАЦИЕНТОМ и обязаны точно выполнять свои функции в разнообразных местах, где электромагнитная окружающая среда неизвестна или меняется в широких пределах, представляется возможным распространить общие требования ГОСТ Р 50267.0.2 с целью обеспечения обоснованной гарантии хорошей и безопасной работы ИЗДЕЛИЯ.
36.202.1 Электростатический разряд
Установленное в настоящем частном стандарте значение 6 кВ выбрано потому, что оно представляет собой значение разряда, которое встречается повсеместно. Одновременно учитывается, что такое изделие находится в постоянном контакте с ПАЦИЕНТАМИ и может быть подвержено действию еще больших электростатических разрядов.
36.202.2 Излучаемые радиочастотные электромагнитные поля
Исследование отдельных ПАЦИЕНТОВ может происходить в окружающей среде, имеющей необыкновенно высокие уровни электромагнитных полей. Чтобы избежать неправильных записей, такие ПАЦИЕНТЫ должны быть предупреждены врачом о том, что эти ИЗДЕЛИЯ не должны подвергаться действию таких высоких уровней полей.
Частота модуляции 10,4 Гц выбрана потому, что она находится в пределах полосы пропускания ИЗДЕЛИЯ и близка к частоте максимальной мощности в частотном спектре комплекса QRS.
50 Точность рабочих характеристик
50.101 Автоматический анализ
Достоверная оценка должна быть воспроизводимой. По этой причине оценки ИЗДЕЛИЙ осуществляются без использования вмешательства оператора, что обеспечивает воспроизводимую оценку. При вмешательстве оператора достигаются более точные результаты для ИЗДЕЛИЙ. Таким образом, если оценки осуществляются путем измерений при вмешательстве человека и улучшаются только за счет настойчивости и опыта ОПЕРАТОРА, то результаты испытаний не представляют воспроизводимого значения величины и такие оценки не признаются.
Широко распространена практика передачи оцифрованного ЭКС из базы данных непосредственно в программу анализа. Это обеспечивает получение точных и воспроизводимых результатов. Допустимо осуществлять испытания программы анализа на некотором испытательном стенде, если порт программы анализа ИЗДЕЛИЯ проверен отдельно.
АМБУЛАТОРНЫЕ ЭЛЕКТРОКАРДИОГРАФИЧЕСКИЕ СИСТЕМЫ часто создаются для обеспечения оптимальных характеристик и эксплуатируются квалифицированным персоналом, который взаимодействует с программой. Оценки таких систем настоящим стандартом не рассматриваются.
Полное раскрытие процедуры формирования выходных аннотированных файлов ИЗДЕЛИЯ дает возможность независимому (постороннему) эксперту использовать процедуру проверки с применением необходимого контроля результатов испытаний. Это также дает возможность эксперту использовать (по выбору) необходимые дополнительные данные испытаний.
Развитие методологии происходит в сочетании ИЗДЕЛИЯ и его интерфейса. В принципе, интерфейс может включать существенные программные компоненты для обработки выходных сигналов ИЗДЕЛИЯ, тем самым улучшая его указанные характеристики. Неполное раскрытие возможностей интерфейса будет являться сдерживающим фактором его использования для целей, отличных от прямого преобразования выходных сигналов ИЗДЕЛИЯ в стандартные маркированные файлы.
50.101.1 Использование стандартных баз данных
В настоящее время широко используются четыре стандартные базы данных для оценки АМБУЛАТОРНЫХ ЭЛЕКТРОКАРДИОГРАФИЧЕСКИХ СИСТЕМ от трех источников:
- База данных AHA: База данных американской ассоциации сердца (The American Heart Association) для оценки аритмии желудочков (80 записей по 30 мин каждая);
- База данных MIT: База данных по аритмиям Массачусетского технологического института - Израильского госпиталя Beth (The Massachusetts Institute of Technology-Beth Israel Hospital) (48 записей по 30 мин каждая);
- База данных NST: База данных для испытаний шумового стресса (12 записей по 30 мин каждая; поставляется с базой данных MIT);
- База данных CU: База данных по длительным аритмиям желудочков Крейгтоновского университета (The Creighton University (35 записей по 8 мин каждая; поставляется с базой данных MIT).
Первые три базы данных состоят из оцифрованных выборок двухканальных Холтеровских записей, причем каждый ЭКС-комплекс промаркирован. База данных CU содержит оцифрованные одноканальные записи ЭКС с промаркированными изменениями комплексов. Это полный перечень баз данных, которые представляют основу оценки и являются в настоящее время широко распространенными.
Эти базы данных можно получить через:
ECRI, 5200 Butler Pike, Plymouth Meeting, PA 19462, USA (База данных AHA).
Распространитель базы данных MIT - BIN; MIT Room 20A113,77 Massachusetts Avenue; Cambridge; MA 02139; USA (базы данных MIT, ESC, NST и CU).
Вне пределов Северной Америки базу данных ESC можно получить из Института CNR клинической физиологии компьютерной лаборатории. Via Trieste, 41, 56100 Pisa, Италия.
Поскольку технические характеристики в значительной степени зависят от характеристик отдельных анализируемых ЭКС, процедура оценок проходит с использованием стандартных записей, при этом результаты таких оценок обеспечивают возможность сравнения ИЗДЕЛИЙ и их стандартных технических характеристик. Такие стандартные записи позволяют изготовителю испытывать каждую базу данных ПАЦИЕНТА со всеми тремя стандартными усилениями (5, 10, 20 мм/мВ) по обоим каналам ЭКГ и видеть, какая установка усиления дает "наилучшие" результаты. Стандартные записи позволяют изготовителю изменять установки усиления вручную. Это приближает использование функции автоматического управления усилением в большинстве АМБУЛАТОРНЫХ ЭЛЕКТРОКАРДИОГРАФИЧЕСКИХ СИСТЕМ.
Исключение записей с кардиостимулированными комплексами разрешено только для ИЗДЕЛИЙ, которые не предназначены для анализа аналоговых записей ЭКГ с кардиостимуляцией. Это основано на том, что записи на магнитных лентах не воспроизводят артефакты кардиостимулятора с достаточной точностью, позволяющей использование общепринятых технологий распознавания этих артефактов в реальных сигналах. Однако цифровые базы данных воспроизводят аналоговые сигналы с высокой точностью, обеспечивающей использование технологий распознавания артефактов кардиостимулятора с помощью ИЗДЕЛИЙ, предназначенных для анализа аналоговых регистраторов ЭКГ.
Для большинства ИЗДЕЛИЙ требуется определенное количество времени для изучения основного ритма. По этой причине период изучения 5 мин размещен в начале каждой записи и исключен из статистики оцениваемых характеристик. Если используется увеличенная версия базы данных AHA (содержащая 2,5 ч неаннотированных сигналов в записи, предшествующей периоду испытания 30 мин), только последние 35 мин каждой записи (стандартной эквивалентной версии) могут быть применены к испытуемому ИЗДЕЛИЮ.
Для сравнения каждого комплекса необходимы четкие комплексы QRS, которые отсутствуют при наличии эпизодов VF, промаркированных метками ритма в справочных аннотационных файлах и исключенных из поциклового сравнения. С другой стороны, данные сегменты включены в испытания последовательного обнаружения VEB и SVEB и VF.
50.101.2 Требования к протоколам испытаний
Отдельные вопросы не могут быть должным образом разрешены с использованием существующей методологии испытаний.
Сфера действия и многообразие VF в базах данных AHA и MIT недостаточны для использования этих баз данных в качестве заменителей базы данных CU с целью оценки возможности определения VF ИЗДЕЛИЕМ. Оценка определения VF с использованием 80 записей базы данных AHA и 48 записей базы данных MIT должна дополнять требуемую оценку с помощью базы данных CU, хотя база данных CU не содержит достаточного количества сигналов, способных вызвать ложные определения VF.
Документ ЕС 38:1998 ANSI/AAMI обеспечивает дальнейшее руководство по оценке программы анализа (особенно для выбегов эктопических сокращений) (particularly for runs of ectopic beats).
50.101.3 Минимальные требования к отчету врача
Приступы тахикардии, брадикардии, эктопии и сдвиги сегмента ST должны быть приняты во внимание врачом, оказывающим помощь ПАЦИЕНТУ. Так как спортсмены на длинные дистанции (бегуны, пловцы, мотоциклисты) часто могут иметь частоту сердечных сокращений менее 50 ударов/мин, важно предоставить возможность ОПЕРАТОРУ отбирать параметры так, чтобы в таких случаях не делать ложного диагноза сердечной патологии. Представление возможности ОПЕРАТОРУ отбирать параметры может быть также полезным для анализа сегментов ST.
51 Защита от представляющих опасность выходных характеристик
51.5 Неправильные выходные характеристики
51.5.1 Динамический диапазон входных сигналов
Интерпретации ЭКГ обычно не включают анализ QRS по мелким морфологическим деталям, поэтому динамический диапазон входных сигналов ±3 мВ и скорость изменения напряжения до 125 мВ/с вполне достаточны. В то же время скорость изменения напряжения для диагностических ЭЛЕКТРОКАРДИОГРАФОВ и мониторов сердечной деятельности установлена 320 мВ/с, а рекомендациями отчета AHA 1985 г. [1] данное требование для амбулаторных электрокардиографов составляет 75 мВ/с. Максимальная скорость изменения напряжения синусоидального сигнала равна размаху сигнала, умноженному на частоту и на число . Синусоидальный сигнал с размахом 6 мВ и частотой 6,7 Гц имеет максимальную скорость изменения напряжения 126,66 мВ/с.
Кроме того, важно, чтобы РЕГИСТРАТОРЫ были работоспособны при наличии на входе постоянного напряжения смещения. Данное требование изначально возникло в связи с наличием больших напряжений поляризации ЭЛЕКТРОДОВ. Требование в этой части для поляризации, которая бывает на ЭЛЕКТРОДЕ, устанавливается ±300 мВ.
51.5.2 Входной импеданс
Требование к входному импедансу устанавливается исходя из уровня импеданса кожа-ЭЛЕКТРОД в диапазоне частот сигналов ЭКГ. Если используются стандартные ЭЛЕКТРОДЫ ЭКГ, то системы измерения должны иметь достаточно высокий входной импеданс, чтобы все измерения проводить без существенных ошибок.
Промышленность способна легко удовлетворить эти требования. Несмотря на продолжающееся развитие ЭЛЕКТРОДОВ с предварительно наносимыми гелями, что привело к значительному снижению импеданса, необходимо ориентироваться на наихудшие случаи использования ЭЛЕКТРОДОВ старого типа. Использование современных ЭЛЕКТРОДОВ, уменьшающих импеданс, снизит в дальнейшем небольшое число объектов, чей чрезмерный импеданс ЭЛЕКТРОД-кожа вызывает ошибку измерения.
Импедансы кожа-ЭЛЕКТРОД уменьшаются с увеличением частоты и времени после наложения ЭЛЕКТРОДА. Метод испытания имитирует частотно-зависимое снижение импеданса посредством конденсатора 4,7 нФ, включенного параллельно с сопротивлением 0,62 МОм. При 10 Гц импеданс этой цепи составляет приблизительно 610 кОм. Следовательно, ИЗДЕЛИЕ, у которого входной импеданс при 10 Гц составляет 9,55 МОм или более, выдержит это испытание.
51.5.3 Подавление синфазной помехи
Метод нормирования и измерения подавления синфазной помехи, установленный настоящим частным стандартом, определяет худшее, а не нормальное значение емкости относительно земли в зависимости от емкости ПАЦИЕНТА относительно АМБУЛАТОРНОГО РЕГИСТРАТОРА. Требование 60 дБ на частоте сети представляется заниженным, так как при практическом применении определяющей является емкость между АМБУЛАТОРНЫМ РЕГИСТРАТОРОМ и ПАЦИЕНТОМ, что может привести к значительно большему подавлению синфазной помехи. Измерения на частоте второй гармоники осуществляются по причине искажения формы напряжения питания, которое имеет место, например, вследствие работы контроллеров с тиристорами и электронного оборудования с емкостными сетевыми фильтрами.
Регистратор обертывают заземленной фольгой для стабилизации емкости АМБУЛАТОРНОГО РЕГИСТРАТОРА относительно земли. Испытательные цепи и КАБЕЛЬ ПАЦИЕНТА экранируют для устранения влияния паразитной емкости этих элементов относительно земли. Кроме того, вся испытательная установка защищена внешним заземленным экраном для стабилизации паразитной емкости .
Остается единственный фактор, который будет влиять на результаты - это конструкция конкретного АМБУЛАТОРНОГО РЕГИСТРАТОРА, его размеры и расстояния между внутренней цепью и внешней оболочкой из фольги (то есть толщина изолированной оболочки). Чем выше результирующая емкость РЕГИСТРАТОРА относительно оболочки из фольги, тем больше трудностей в обеспечении соответствия требованиям настоящего стандарта по этой методологии проведения испытаний. С другой стороны, экранирование испытательных цепей и КАБЕЛЯ ПАЦИЕНТА дает возможность обеспечения по соответствию требований к подавлению синфазной помехи.
Для проверки подавления синфазной помехи ИЗДЕЛИЕМ необходимо отключить узкополосный режекторный фильтр ПИТАЮЩЕЙ СЕТИ, если он имеется. Если этого не сделать, то будет проверена главным образом режекция этого узкополосного режекторного фильтра. Желательно, чтобы было достигнуто хорошее подавление синфазной помехи на частотах, отличных от частоты ПИТАЮЩЕЙ СЕТИ.
51.5.4 Точность чувствительности
Значение чувствительности 10 мм/мВ отражает хорошо обоснованное соглашение [1]. Для гарантии безопасности и эффективности дополнительные установки не требуются. Однако выходные сигналы при всех других имеющихся установках чувствительности должны быть в разумных пределах, близких к их номинальным значениям.
51.5.5 Стабильность чувствительности
Для обеспечения гарантии непротиворечивой интерпретации стабильность чувствительности особенно важна для амбулаторного оборудования, так как типовой период мониторинга составляет 24 ч и более. Изменения сигналов ЭКГ, которые не являются результатом физиологических или патофизиологических изменений, должны быть сведены к минимуму. Установленные настоящим частным стандартом пределы представляют консенсус по отношению к достижимым на практике уровням стабильности.
51.5.6 Калибровка амплитуды
Стандартизированное напряжение обеспечивает привязку к абсолютному значению напряжения для аналоговых систем. Это особенно важно для точного измерения уровней сегментов ST, сдвиг которых, равный 1 мм (0,1 мВ), может указывать разницу между нормальной и ишемической реполяризацией. Анализ сегментов ST был основным в системах визуальной оценки и все больше и больше внедряется в более автоматизированные цифровые амбулаторные системы ЭКГ.
Аналоговые средства подвержены значительно большим изменениям чувствительности, чем цифровые. Поэтому в аналоговых системах, использующих съемные носители информации, обычно используются калибровочные импульсы для регулировки чувствительности воспроизводящего устройства, за счет чего обеспечивается необходимая точность чувствительности всей системы.
Пределы ошибки, составляющие не более 5%, представляют приемлемую норму.
51.5.7 Требования к шумам системы
Шум в электрокардиографических записях относится к одному из наиболее вредных постоянных факторов, препятствующих получению чистого, обеспечивающего постановку диагноза, сигнала. Данная проблема, однако, часто является следствием внешних помех (электромагнитных), движений ПАЦИЕНТА (миографических сигналов), нарушения техники наложения ЭЛЕКТРОДОВ или нарушения техники соединения проводов. Большинство изготовителей прикладывают к ИЗДЕЛИЮ руководства для обеспечения надлежащих технических приемов измерения ЭКГ. Экранированные провода, так же как и высокий входной импеданс и подавление синфазной помехи, смягчают некоторые проблемы шума. Устройства активного подавления синфазных помех в цепи НЕЙТРАЛЬНОГО ЭЛЕКТРОДА обеспечивают дополнительное подавление синфазной помехи, что в конечном итоге снижает шум в системе.
51.5.8 Взаимовлияние каналов
Максимальный уровень взаимовлияния каналов определяется требованиями точности постановки диагноза с одной стороны и дополнительными затратами на подавление шума с другой стороны. Установленный уровень вполне достаточен для диагностики и экономически оправдан на практике.
51.5.9 Частотная характеристика
Полный набор параметров частотной характеристики должен включать и фазовые искажения, которые наиболее существенны на низких частотах. Наиболее простым методом их проверки является воздействие импульсным напряжением. Испытания на высоких частотах не проводятся, так как измерение сдвига фазы на частотах свыше 25 Гц затруднительно при скорости развертки 25 мм/с, а на частоте 40 Гц для обеспечения точных измерений требуется скорость развертки 400 мм/с.
На практике фазовая характеристика фильтра верхних частот с граничной частотой 0,05 Гц считается приемлемой. Смещение базовой линии, происходящее сразу после действия импульсов, соответствует фильтру верхних частот 0,05 Гц. Требование к крутизне 0,30 мВ/с означает, что при стандартной чувствительности и скорости развертки изменение типичного интервала ST, равного 100 мс, составит 0,3 мм и не будет клинически значимым, особенно если типичный комплекс QRS будет иметь площадь около 0,1 мВ·с (сравните с 0,3 мВ·с).
Требование к верхней граничной частоте 40 Гц установлено исходя из двух соображений. Во-первых, из основных целей амбулаторного электрокардиографа (которые состоят в: [] - определении ритмов и [
] - выявлении смещений сегментов ST, необходимых для определения приступов ишемии), которые могут быть в достаточной мере достигнуты в полосе до 40 Гц. Во-вторых, из постоянной проблемы высокочастотного шума, вызванного частотой питающей сети и мышечными артефактами, которые можно уменьшить при полосе пропускания 40 Гц.
Настоящий стандарт предлагает методы испытаний для оценки как частотной характеристики, так и способности АМБУЛАТОРНЫХ ЭЛЕКТРОКАРДИОГРАФИЧЕСКИХ ИЗДЕЛИЙ воспроизводить ЭКГ-подобные сигналы, такие как треугольный сигнал, имитирующий R-зубец. Допущение 40%-ного уменьшения амплитуды треугольного входного сигнала согласовывается с ожидаемым уменьшением, вызванным ограничением при цифровой дискретизации сигнала, когда на одном канале при 24-часовой регистрации запоминается примерно 10 миллионов отсчетов. Испытание импульсного отклика также применяется для имитации R-зубца и определения смещения базовой линии после воздействия импульса, что при реальном входном ЭКС может привести к артефактным смещениям сегмента ST и ложным интерпретациям о наличии ишемии.
Требование к нижней граничной частоте 0,67 Гц основано на данных о частоте сердечных сокращений из исследований Simonson*. Эти исследования показывают, что частота сердечных сокращений 44 удара/мин встречается у 99% взрослых с изменением отдельных интервалов RR менее 126 мс. Таким образом, нижняя граница 40 ударов/мин (0,67 Гц) существует у 99% взрослых в 90% времени исследования. Bailey и др. использовали эти данные для обоснования нижней граничной частоты 0,67 Гц в рекомендациях AHA 1990 г.
________________
* Simonson Е. Differentiation between normal and abnormal in electrocardiography. St. Louis: C.V.MosbyCo., 1961.
Simonson, Е. et. al. Variability of the electrocardiogram in normal young men. Am Heart, 1949, vol.38.
Уменьшение нижней граничной частоты приблизительно от 0,2 до 0,3 Гц наблюдается у аналогичных РЕГИСТРАТОРОВ с магнитной лентой. Выбор в качестве верхнего предела точности частотного отклика плюс 3 дБ допускает это увеличение.
51.5.10 Минимальный регистрируемый сигнал
Ясно различимое отображение сигнала 50 мкВ увеличивает вероятность распознавания Р-волн, очень важных для диагностики.
51.5.11 Функционирование при наличии импульсов кардиостимулятора
ПАЦИЕНТЫ, имеющие кардиостимуляторы с большими амплитудами импульсов на поверхности тела, распространены среди населения, диагностируемого с помощью амбулаторных ЭКГ. В связи с этим запись ЭКГ осуществляется ИЗДЕЛИЯМИ, подходящими для использования у таких ПАЦИЕНТОВ, и функции которых не должны нарушаться при наличии импульсных сигналов кардиостимулятора.
Если изготовитель заявил, что ИЗДЕЛИЕ имеет возможность записи импульсов кардиостимулятора, необходимо проведение испытаний с использованием четырех различных импульсов для охвата диапазона возможных амплитуд импульсов кардиостимулятора на поверхности съема ЭКС.
51.5.12 Точность измерения времени
Связь времени возникновения внешнего события (например, применение лекарств, наличие симптомов, физическая активность) и комплексов ЭКС ПАЦИЕНТОВ существенна для клинической интерпретации. Так как записанные ЭКС анализируются в ретроспективе, записывающее ИЗДЕЛИЕ и система должны обеспечивать механизм точной индикации фактического времени наступления события совместно с сигналами ЭКС на дисплее и на принтере. Общее требование для точности ±30 с в течение 24 ч гарантирует, что разница между фактическим временем наступления события и записанным временем наступления события достаточно мала для учета клинической корреляции и интерпретации сопутствующих комплексов ЭКС.
51.5.13 Стандарт на координатную сетку твердой копии
Прямолинейная координатная сетка с временной осью 25 мм/с и осью напряжения 10 мм/мВ была в электрокардиографии традиционной. Выделение каждой пятой линии упрощает измерения времени и напряжения.
Рисунок сетки может быть предварительно напечатан на обычной бумаге или может быть распечатан с помощью того же печатающего устройства, используемого для печати ЭКГ (например, лазерных принтеров). Установленная максимальная ошибка ±2% обеспечивает достаточную точность клинических измерений и является достижимой. Изменения влажности будут проявляться в расширении и сжатии бумажных волокон. Ошибки измерения и влажность учитываются установленным допуском ±2%.
51.5.14 Установки чувствительности и переключения
Изменения амплитуды в записанных ЭКГ ПАЦИЕНТОВ (вследствие физиологических факторов или расположения ОТВЕДЕНИЙ) служат основанием выбора различных масштабных коэффициентов. Традиционно использовался НОМИНАЛЬНЫЙ масштабный коэффициент 10 мм/мВ. Дополнительные установки чувствительности 5 мм/мВ и 20 мм/мВ соответствуют рекомендациям IEC и AHA. Другие установки чувствительности (например, 40 мм/мВ и 2,5 мм/мВ) могут быть даны изготовителем в качестве опций. Плавная регулировка чувствительности, как правило, нежелательна.
Отображение калибровочного импульса ЭКГ на дисплее обеспечивает ОПЕРАТОРА средствами проверки амплитуды воспроизведенной ЭКГ.
51.5.15 Временное выравнивание
Клиническая расшифровка записанных ЭКГ требует визуализации комплекса ЭКГ в различных отведениях. Определенные детали, такие как импульсы кардиостимулятора, видны только в одном отведении. Параллельный анализ ЭКГ по двум (или более) каналам требует, чтобы межканальная асимметрия была достаточно небольшой, чтобы не оказывать влияния на интерпретацию ЭКГ. Ошибка асимметрии, равная ±0,5 мм, соответствует максимальной временной асимметрии, равной ±20 мс (при шкале 25 мм/с). Этот допуск указывает практический уровень ошибок измерения, а также отклонения в записывающем и ВОСПРОИЗВОДЯЩЕМ ИЗДЕЛИЯХ, происходящие из-за недостаточного выравнивания магнитных записывающих головок, эффекта детонации магнитной ленты и/или из-за асимметрии аналогово-цифрового преобразования.
56.7 Батареи
В зависимости от заложенной функции в некоторых изделиях используется более одного ВНУТРЕННЕГО ИСТОЧНИКА ЭЛЕКТРИЧЕСКОГО ПИТАНИЯ (например, батарея для специальной памяти). Если функция любого ВНУТРЕННЕГО ИСТОЧНИКА ЭЛЕКТРИЧЕСКОГО ПИТАНИЯ состоит в обеспечении безопасной работы в соответствии с настоящим частным стандартом (что включает точность данных и автоматического анализа), то необходима индикация состояния каждого ВНУТРЕННЕГО ИСТОЧНИКА ЭЛЕКТРИЧЕСКОГО ПИТАНИЯ, чтобы ОПЕРАТОР мог вовремя заменить или зарядить батарею перед установкой изделия на ПАЦИЕНТА.
Исходя из особенностей применения АМБУЛАТОРНОГО РЕГИСТРАТОРА (мониторинг деятельности сердца в течение 24 ч или более в отсутствие специализированного персонала) необходимо контролировать состояние каждого внутреннего источника электрического питания в течение периода мониторинга, для того чтобы избежать обработки и анализа (или в реальном времени или после мониторинга) искаженных или неточных данных.
56.7.101 Время мониторинга и сохранение данных
56.7.101.1 Время мониторинга
Минимальное время записи амбулаторных ЭКГ меняется в зависимости от типа исследования. Часто встречающиеся события могут определяться с помощью коротких периодов записей, тогда как для событий, встречающихся не часто, а изредка, требуется продолжительная запись. Для большинства клинических применений рекомендован минимальный период - 24 ч. Этот период включает суточную изменчивость процессов, определяющих деятельность сердца. Он создает возможность определения большинства приступов перемежающихся аритмий в течение фаз бодрствования и сна с распознаванием времени изменения частоты и обеспечением соответствующей защиты от эффектов неустойчивой работы регистратора.
56.7.101.2 Сохранение данных
Требования сохранения данных в течение 72 ч основаны на допущении, что записи должны быть сохранены по крайней мере в течение выходных дней, что является распространенной ситуацией на практике.
Алфавитный указатель терминов
Термин | Пункт соответствующего стандарта | Обозначение ссылочного межгосударственного и национального стандартов |
АМБУЛАТОРНЫЙ РЕГИСТРАТОР | 2.102 | ГОСТ Р 50267.47 |
АМБУЛАТОРНАЯ ЭЛЕКТРОКАРДИОГРАФИЧЕСКАЯ СИСТЕМА (ИЗДЕЛИЕ) | 2.101 | ГОСТ Р 50267.47 |
ВНУТРЕННИЙ ИСТОЧНИК ЭЛЕКТРИЧЕСКОГО ПИТАНИЯ | 2.1.9 | ГОСТ 30324.0 |
ВХОД СИГНАЛЬНЫЙ | 2.1.18 | ГОСТ 30324.0 |
ДОКУМЕНТЫ ЭКСПЛУАТАЦИОННЫЕ | 2.1.4 | ГОСТ 30324.0 |
ИЗДЕЛИЕ С ВНУТРЕННИМ ИСТОЧНИКОМ ПИТАНИЯ | 2.2.29 | ГОСТ 30324.0 |
КАБЕЛЬ ПАЦИЕНТА | 2.108 | ГОСТ Р 50267.47 |
КОРПУС | 2.1.6 | ГОСТ 30324.0 |
НАПРЯЖЕНИЕ СЕТЕВОЕ | 2.4.2 | ГОСТ 30324.0 |
ОПАСНОСТЬ | 2.12.18 | ГОСТ 30324.0 |
ОПЕРАТОР | 2.12.17 | ГОСТ 30324.0 |
ОТВЕДЕНИЕ | 2.105 | ГОСТ Р 50267.47 |
ПАЦИЕНТ | 2.12.4 | ГОСТ 30324.0 |
ПРОВОД ВЫРАВНИВАНИЯ ПОТЕНЦИАЛОВ | 2.6.6 | ГОСТ 30324.0 |
ПРОВОД ОТВЕДЕНИЯ | 2.109 | ГОСТ Р 50267.47 |
РЕГИСТРАТОР НЕПРЕРЫВНОГО ДЕЙСТВИЯ | 2.110 | ГОСТ Р 50267.47 |
СЕТЬ ПИТАЮЩАЯ | 2.12.10 | ГОСТ 30324.0 |
ТОК УТЕЧКИ | 2.5.3 | ГОСТ 30324.0 |
УСТРОЙСТВО ВОСПРОИЗВЕДЕНИЯ | 2.103 | ГОСТ Р 50267.47 |
ЧАСТЬ ДОСТУПНАЯ | 2.1.22 | ГОСТ 30324.0 |
ЧАСТЬ РАБОЧАЯ | 2.1.5 | ГОСТ 30324.0 |
ЧАСТЬ РАБОЧАЯ ТИПА В | 2.1.24 | ГОСТ 30324.0 |
ЧАСТЬ РАБОЧАЯ ТИПА BF | 2.1.25 | ГОСТ 30324.0 |
ЧАСТЬ РАБОЧАЯ ТИПА CF | 2.1.26 | ГОСТ 30324.0 |
ЧАСТЬ РАБОЧАЯ ТИПА F | 2.1.7 | ГОСТ 30324.0 |
ШНУР ПИТАНИЯ | 2.7.17 | ГОСТ 30324.0 |
ЭЛЕКТРОД | 2.104 | ГОСТ 30324.25 |
ЭЛЕКТРОД НЕЙТРАЛЬНЫЙ | 2.107 | ГОСТ 50267.47 |
ЭЛЕКТРОДЫ ПАЦИЕНТА | 2.106 | ГОСТ 50267.47 |
ЭЛЕКТРОКАРДИОГРАММА (ЭКГ) | 2.101 | ГОСТ 30324.25 |
Приложение ВВ
(обязательное)
Сведения о соответствии ссылочных международных стандартов межгосударственным стандартам и национальным стандартам РФ, использованным в настоящем стандарте в качестве нормативных ссылок
Таблица ВВ.1
Обозначение ссылочного межгосударственного стандарта и национального стандарта РФ | Обозначение и наименование ссылочного международного стандарта и условное обозначение степени его соответствия ссылочному межгосударственному стандарту и национальному стандарту РФ |
ГОСТ 30324.0-95 | МЭК 60601-1:1998 "Изделия медицинские электрические. Часть 1. Общие требования безопасности" (MOD) |
ГОСТ Р 50267.0.2-95 | МЭК 60601-1-2:1993 "Изделия медицинские электрические. Часть 1. Общие требования безопасности. 2. Электромагнитная совместимость. Требования и методы испытаний" (MOD) |
ГОСТ 30324.25-95 | МЭК 60601-2-25:1993 "Изделия медицинские электрические. Часть 2. Частные требования безопасности к электрокардиографам" (IDT) |
ГОСТ 30324.27-95 | МЭК 60601-2-27:1993 "Изделия медицинские электрические. Часть 2. Частные требования безопасности к электрокардиографическим мониторам" (MOD) |
ГОСТ Р 50648-94 | МЭК 61000-4-8:1993 "Электромагнитная совместимость. Часть 4. Испытание и методы измерения. Раздел 8. Испытание на иммунитет силового, частотного, магнитного поля. Основная публикация ЭМС" (MOD) |
ГОСТ Р 51317.4.2-99 | МЭК 61000-4-2:1995 "Электромагнитная совместимость. Часть 4. Методики испытаний и измерений. Раздел 2. Испытание на невосприимчивость к электростатическому разряду" (MOD) |
ГОСТ Р 51317.4.3-99 | МЭК 61000-4-3:1995 "Электромагнитная совместимость. Часть 4. Методики испытаний и измерений. Раздел 3. Испытание на невосприимчивость к воздействию электромагнитного поля с излучением на радиочастотах" (MOD) |
ГОСТ Р 51318.11-99 | СИСПР 11:1997 "Совместимость технических средств электромагнитная. Радиопомехи индустриальные от промышленных, научных, медицинских и бытовых (ПНМБ) высокочастотных устройств. Нормы и методы испытаний" (IDT) |
ГОСТ Р 51318.22-99 | СИСПР 22:1997 "Совместимость технических средств электромагнитная. Радиопомехи индустриальные от оборудования информационных технологий. Нормы и методы испытаний" (IDT) |
Примечание - В настоящей таблице использованы следующие условные обозначения степени соответствия стандартов: - IDT - идентичные стандарты; - MOD - модифицированные стандарты. | |
Библиография
[1] SHEFFIELD, L.T., et al. Recommendations for standards of instrumentation and practice in the use of ambulatory electrocardiography. (AHA special report from the task force of the Committee on Electrocardiography and Cardiac Electrophysiology of the Council on Clinical Cardiology). Circulation, 1985, vol.71, pp.626A-636A
Текст документа сверен по:
М.: ИПК Издательство стандартов, 2004