ГОСТ Р ИСО 21535-2013
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ИМПЛАНТАТЫ ХИРУРГИЧЕСКИЕ НЕАКТИВНЫЕ.
ИМПЛАНТАТЫ ДЛЯ ЗАМЕНЫ СУСТАВОВ.
СПЕЦИАЛЬНЫЕ ТРЕБОВАНИЯ К ИМПЛАНТАТАМ ДЛЯ ПРОТЕЗИРОВАНИЯ ТАЗОБЕДРЕННОГО СУСТАВА
Non-active surgical implants. Joint replacement implants. Specific requirements for hip-joint replacement implants
ОКС 11.040.40
ОКП 93 9800
Дата введения 2014-11-01
Предисловие
1 ПОДГОТОВЛЕН Обществом с ограниченной ответственностью "ЦИТОпроект" (ООО "ЦИТОпроект") на основе собственного аутентичного перевода стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 453 "Имплантаты в хирургии"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 7 мая 2013 г. N 86-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 21535:2007* "Неактивные хирургические имплантаты. Имплантаты для замены суставов. Специальные требования к имплантатам для протезирования тазобедренного сустава" (ISO 21535:2007 "Non-active surgical implants - Joint replacement implants - Specific requirements for hip-joint replacement implants").
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе "Национальные стандарты", а официальный текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (gost.ru)
Введение
Существуют три уровня международных стандартов, в которых рассматриваются требования к неактивным хирургическим имплантатам. Они перечислены ниже (уровень 1 является наивысшим):
- уровень 1: общие требования к неактивным хирургическим имплантатам и инструментарию, используемому для их установки;
- уровень 2: частные требования к семействам неактивных хирургических имплантатов;
- уровень 3: специальные требования к отдельным типам неактивных хирургических имплантатов.
Настоящий международный стандарт является стандартом уровня 3 и содержит требования, применимые конкретно к протезам тазобедренного сустава.
Международный стандарт ИСО 14630 уровня 1 содержит требования ко всем неактивным хирургическим имплантатам. При этом дополнительные требования будут установлены в стандартах уровней 2 и 3. Стандарты уровня 2 применимы к более ограниченным наборам или семействам имплантатов, например, к имплантатам, предназначенным для применения в остеосинтезе, сердечно-сосудистой хирургии или протезировании суставов.
Для того, чтобы охватить все требования, рекомендуется начать рассмотрение со стандарта наиболее низкого уровня.
1 Область действия
Настоящий стандарт устанавливает специальные требования к имплантатам для протезирования тазобедренного сустава. В отношении безопасности настоящий стандарт устанавливает требования к показателям назначения, особенностям конструкции, материалам, оценке конструкции, производству, стерилизации, упаковке и информации, поставляемой изготовителем, а также к методам испытаний.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты*:
_______________
* Таблицу соответствия национальных стандартов международным см. по ссылке. - .
ИСО 7206-1 Имплантаты для хирургии. Частичные и полные протезы тазобедренных суставов. Часть 1. Классификация и обозначение размеров
ИСО 7206-2:1996 Имплантаты для хирургии. Частичные и полные протезы тазобедренных суставов. Часть 2. Суставные поверхности из металлических, керамических и пластмассовых материалов
ИСО 7206-4 Имплантаты для хирургии. Частичные и полные протезы тазобедренных суставов. Часть 4. Определение характеристик долговечности стержневых бедренных элементов
ИСО 7206-6:1992 Имплантаты для хирургии. Частичные и полные протезы тазобедренных суставов. Часть 6. Определение характеристик долговечности в зоне головки и шейки стержневых бедренных элементов
ИСО 7206-10 Имплантаты для хирургии. Частичные и полные протезы тазобедренных суставов. Часть 10. Определение стойкости к статической нагрузке модульных суставных бедренных головок
ИСО 14630 Имплантаты хирургические неактивные. Общие требования
ИСО 21534:2007 Неактивные хирургические имплантаты. Имплантаты для замены суставов. Частные требования
3 Термины и определения
В настоящем документе применены термины по ИСО 21534 и ИСО 7206-1, а также следующие с соответствующими определениями:
3.1 Вертлужный компонент
Имплантат, предназначенный для фиксации в подготовленной биологической вертлужной впадине.
Примечание - Этот компонент может иметь моноблочную или модульную конструкцию.
3.2 Биполярная головка
Компонент протеза тазобедренного сустава, имеющий вогнутую (внутреннюю) поверхность, предназначенную для сочленения со сферической головкой бедренного компонента, и выпуклую (внешнюю) сферическую поверхность, предназначенную для сочленения с биологической вертлужной впадиной.
3.3 Бедренный компонент
Элемент тотального или частичного протеза тазобедренного сустава, который предназначен для прикрепления к бедренной кости.
3.4 Протезирование тазобедренного сустава
Артропластика тазобедренного сустава
Имплантат, используемый для протезирования одной или обеих суставных поверхностей тазобедренного сустава.
3.5 Модульный компонент
Бедренный или вертлужный компонент, который собирается пользователем из ряда деталей.
3.6 Моноблочный компонент
Бедренный или вертлужный компонент, который поставляется как единая конструкция.
3.7 Частичное протезирование тазобедренного сустава
Гемиартропластика тазобедренного сустава
Имплантат, состоящий из бедренного компонента, предназначенного для протезирования бедренной суставной поверхности тазобедренного сустава.
Примечание 1 - Имплантаты для частичного протезирования тазобедренного сустава могут иметь как биполярную, так и монополярную головку.
Примечание 2 - Этот компонент может иметь моноблочную или модульную конструкцию.
3.8 Тотальное протезирование тазобедренного сустава
Тотальная артропластика тазобедренного сустава
Имплантат, состоящий из бедренного и вертлужного компонентов, предназначенных для протезирования обеих суставных поверхностей тазобедренного сустава.
Примечание - Этот компонент может иметь моноблочную или модульную конструкцию.
3.9 Монополярная головка
Головка бедренного компонента, предназначенная для сочленения с биологической вертлужной впадиной.
4 Показатели назначения
Требования пункта 4 стандарта ИСО 21534 применяются совместно с указанными ниже требованиями.
Диапазон угловых движений между бедренным и вертлужным компонентами должен иметь следующие минимальные значения:
- 100° при сгибании/разгибании;
- 60° при отведении/приведении;
- 90° при ротации внутрь/кнаружи.
Примечание - Метод, с помощью которого можно провести это измерение, описан в Приложении А.
5 Особенности конструкции
5.1 Общие требования
Требования пункта 5 стандарта ИСО 21534 применяются совместно с указанными ниже требованиями, установленными в пунктах 5.2 и 5.3.
5.2 Размеры и допуски
Примечание - Относительно требований к суставным поверхностям типа "металл-по-металлу" и "керамика-по-керамике" пока еще не получено достаточного количества информации о шероховатости поверхности и допусках на диаметр и размеры, чтобы предоставить спецификацию для этих параметров в данном издании настоящего стандарта.
5.2.1 Допуски и размеры конусных соединений
Следует уделить особое внимание, как минимум, следующим аспектам: диаметру, углу конусности, прямолинейности, округлости, микроскопической и макроскопической структуре поверхности.
В конструкциях, где используются модульные бедренные компоненты, следует учитывать риск образования частиц износа и развития коррозии на поверхностях модульного компонента.
5.2.2 Допуски на диаметр суставных поверхностей
Допуски на диаметр суставных поверхностей металлических или керамических бедренных компонентов, предназначенных для использования с вертлужными компонентами из сверхвысокомолекулярного полиэтилена (СВМПЭ), должны соответствовать стандарту ИСО 7206-2, пункты 4.1.3 и 4.2.3 соответственно.
Примечание - Требования к сферичности и шероховатости для изделий из СВМПЭ, контактирующих с металлом или керамикой, изложены в ИСО 7206-2.
5.3 Толщина СВМПЭ в вертлужных компонентах и биполярных головках
5.3.1 Вертлужные компоненты
Для вертлужных компонентов с внешним диаметром 42 мм и больше компонент, изготавливаемый из СВМПЭ, должен иметь следующую минимальную толщину нагружаемого сектора:
а) 5 мм - для компонентов с металлической или иной подложкой;
б) 6 мм - для компонентов без подложки.
5.3.2 Биполярные головки
Для биполярных головок с внешним диметром (W) 44 мм минимальная толщина выстилки из СВМПЭ должна составлять 5 мм.
Примечание - В тех случаях, когда размеры костей в популяции, для которой предназначены эти имплантаты, требуют, чтобы диаметр вертлужного компонента составлял менее 42 мм, а диаметр биполярного компонента - менее 44 мм, может потребоваться использовать значения толщины меньше указанных.
6 Материалы
Требования пункта 6 стандарта ИСО 21534 применяются совместно с указанными ниже требованиями.
Нелегированный титан и титановые сплавы не следует использовать для суставных поверхностей тотальных протезов тазобедренного сустава, кроме случаев, когда проведена надлежащая обработка поверхности и подтверждена ее пригодность для использования в клинической практике.
7 Оценка конструкции
7.1 Общие требования
Требования пункта 7 стандарта ИСО 21534 применяются совместно с указанными ниже требованиями. Возможны ситуации, когда одно или несколько испытаний, предусмотренных пунктом 7.2 ИСО 21534, не требуются:
а) для каждого компонента среди линейки компонентов (в семействе продуктов);
б) в тех случаях, когда уже имеются результаты необходимого испытания, полученные для аналогичного или похожего компонента.
В этих случаях необходимо документально зафиксировать обоснование невыполнения любого конкретного испытания в отношении любого конкретного компонента.
7.2 Доклиническая оценка
7.2.1 Испытание бедренных компонентов на прочность
Испытание бедренных компонентов имплантатов, используемых для тотального протезирования тазобедренного сустава, осуществляется в соответствии с ИСО 7206-4. Результаты испытания следует зафиксировать.
Примечание - В настоящее время идет работа по созданию пересмотренной версии ИСО 7206-4, включающей набор испытаний, предусмотренных стандартом ИСО 7206-8, и описывающей контролируемые параметры для циклических испытаний, предназначенных для оценки прочности бедренных компонентов с тремя различными диапазонами длины ножки.
7.2.2 Прочность в зоне головки и шейки бедренных компонентов с ножкой
Испытание в зоне головки и шейки бедренных компонентов с ножкой проводится в соответствии с пунктом 7.2 ИСО 7206-6.
7.2.3 Параметры фиксации головки
Применяются требования соответствующих пунктов ИСО 7206-10.
7.2.4 Испытание тотальных протезов тазобедренного сустава на износ
Параметры износа тотальных протезов тазобедренного сустава, состоящих из бедренного компонента с интегральной или модульной головкой, сочленяющейся с металлическим, керамическим или изготовленным из СВМПЭ вертлужным компонентом, оцениваются с помощью контролируемой валидированной процедуры с документальной регистрацией полученных результатов.
7.2.5 Минимальные и максимальные углы
Определение предусмотренных минимальных и максимальных углов между частями скелета, упоминаемых в пункте 4а) стандарта ИСО 21534, следует осуществлять в соответствии с процедурой, описанной в Приложении А.
8 Производство
Требования пункта 8 стандарта ИСО 21534 применяются совместно с указанными ниже требованиями:
- имплантаты, производимые из литейных кобальто-хромовых сплавов, при необходимости должны подвергаться обработке на твердый раствор;
- любую проведенную термическую обработку необходимо документально зафиксировать.
Примечание - Один сеанс удовлетворяющей требованиям термической обработки с образованием твердого раствора позволяет удерживать литую заготовку на протяжении 4 часов при температуре 1200°С.
9 Стерилизация
Применяются требования пункта 9 стандарта ИСО 14630.
10 Упаковка
Применяются требования пункта 10 стандарта ИСО 14630.
11 Информация, предоставляемая производителем
11.1 Общие требования
Требования пункта 11 стандарта ИСО 14630 и пункта 11 стандарта ИСО 21534 применяются совместно с указанными ниже требованиями.
11.2 Размеры
На этикетке, листке-вкладыше с инструкцией или в руководстве по использованию должна быть указана следующая информация:
а) тип изделия;
б) номинальный диаметр головки (см. ИСО 7206-1) для моноблочного бедренного компонента протеза тазобедренного сустава или для модульного протеза головки бедренной кости (на этикетке, в листке-вкладыше с инструкцией и/или в Руководстве по использованию);
в) номинальный диаметр (см. ИСО 7206-1) суставной поверхности вертлужного компонента (на этикетке, в листке-вкладыше с инструкцией и/или в Руководстве по использованию);
г) символы, по которым следует ориентироваться при соединении головки и шейки модульного имплантата (в листке-вкладыше с инструкцией и/или в Руководстве по использованию).
11.3 Структурная и функциональная совместимость компонентов
11.3.1 Для бедренных компонентов или модульных протезов головки бедренной кости, предназначенных для структурной и функциональной совместимости исключительно с определенными вертлужными чашами, на этикетке, в листке-вкладыше с инструкцией или в Руководстве по использованию должна быть указана информация о совместимых вертлужных чашах.
11.3.2 Для вертлужных компонентов, предназначенных для структурной и функциональной совместимости исключительно с определенными бедренными компонентами, на этикетке, в листке-вкладыше с инструкцией или в Руководстве по использованию должна быть указана информация о совместимых бедренных компонентах.
11.3.3 Для каждого бедренного компонента и протеза головки, имеющего модульную конструкцию, на этикетке, в листке-вкладыше с инструкцией или в Руководстве по использованию должна быть указана информация о соответствующем компоненте, с которым они структурно и функционально совместимы.
Примечание - В большинстве случаев компоненты, произведенные одной компанией, могут быть несовместимыми с компонентами, произведенными другой компанией. Это относится, в частности, к модульным компонентам, которые имеют конусные соединения типа внешнего ("папа") или внутреннего ("мама") конуса.
11.4 Маркировка
11.4.1 На моноблочном бедренном компоненте должна иметься маркировка с указанием номинального диаметра бедренной головки.
11.4.2 Маркировка (или маркировки), размещаемая на модульном протезе головки бедренной кости, должна указывать ее номинальный внешний диаметр и параметры соединения конуса и расточенного отверстия. Эти маркировки должны легко читаться специалистом с нормальным или корригированным до нормального зрением.
11.4.3 На стержневой части модульного бедренного компонента имплантата, предназначенного для протезирования тазобедренного сустава и имеющего внешнее/внутреннее конусное соединение для модульного протеза головки, должна иметься маркировка с указанием категории соединения (при условии, что это не нарушает предусмотренную функцию компонента). Маркировка в области шейки бедренного компонента имплантата, предназначенного для протезирования тазобедренного сустава, наносится для его идентификации или в иных целях, но только в том случае, если существуют доказательства того, что она не снижает предел прочности. Для имплантатов с модульными головками маркировку следует размещать на плоском участке проксимального конца конической области, к которой подгоняется головка. Эта отметка должна легко читаться при осмотре невооруженным глазом или с помощью приспособлений для улучшения остроты зрения.
11.4.4 Вертлужный компонент, который имеет суставную поверхность, участвующую в формировании тотального протеза тазобедренного сустава, должен иметь отметку, указывающую на номинальный диаметр суставной поверхности. Эта отметка должна легко читаться специалистом с нормальным или корригированным до нормального зрением.
11.5 Информация для пациента
Производитель должен включить в листок-вкладыш с инструкцией или в Руководство по использованию, как минимум, следующее положение (или эквивалентную информацию):
"Пациентов, которым устанавливаются эндопротезы тазобедренного сустава, следует предупреждать, что срок службы имплантата может зависеть от их веса и уровня активности".
Приложение А
(справочное)
Оценка относительного углового движения компонентов
А.1 Закрепляют вертлужный компонент в соответствующем зажиме или другом фиксирующем приспособлении.
А.2 Закрепляют бедренный компонент, который может иметь интегральную либо модульную конструкцию, на испытательном стенде, так чтобы суставные поверхности бедренного и вертлужного компонентов соприкасались друг с другом и вращались вокруг осей, проходящих через центр суставной поверхности вертлужной впадины. Используя соответствующий гониометр или прибор для измерения углов, перемещают бедренный компонент рукой в плоскости его ножки и шейки до тех пор, пока шейка бедренного компонента соприкоснется с вертлужной впадиной по ее медиальной поверхности, а затем - по латеральной поверхности. Измеряют угол () между двумя положениями с точностью ±1°, как показано на рисунке А.1 а). Этот угол (
) представляет собой угол отведения/приведения.
А.3 Повторяют движение, описанное в пункте А.2, в плоскости, проходящей через центр головки перпендикулярно плоскости стержня и шейки, как показано на рисунке А.1 б), и измеряют угол () между двумя крайними положениями, изображенными на рисунке. Этот угол (
) представляет собой угол сгибания/разгибания.
А.4 Исходно поместив вертлужный компонент в положение, изображенное на рисунках А.1 б) и А.1 в), вращают бедренный компонент вокруг оси АА сначала в одном, а затем в другом направлении, и выполняют измерение угла (), соответствующего диапазону свободного движения от одного упора к другому. Угол (
) представляет собой угол ротации внутрь/кнаружи.
А.5 Также возможно проведение оценки с помощью программного обеспечения CAD. На чертеже должны быть указаны углы и идентификационные сведения о компонентах (размер, длина шейки).
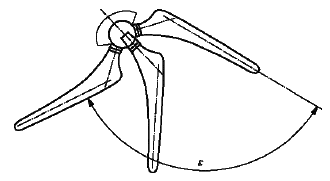
а) Протез тазобедренного сустава - отведение/приведение
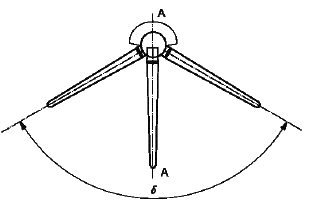
б) Протез тазобедренного сустава - сгибание/разгибание
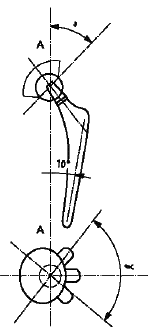
в) Протез тазобедренного сустава - ротация внутрь/кнаружи
Условные обозначения
- угол ротации внутрь/кнаружи;
- угол отведения/приведения;
- угол сгибания/разгибания;
установите вертлужный компонент под углом 45° либо под углом, который задан производителем.
Рисунок А.1 - Относительные угловые движения компонентов
Библиография
[1] ИСО 7206-8 Имплантаты для хирургии. Частичные и тотальные протезы бедренного сустава. Часть 8. Методы определения прочности бедренных компонентов с ножкой.
[2] ИСО/TR 9325 Имплантаты для хирургии. Частичные и тотальные протезы бедренного сустава. Рекомендации для устройств имитации, предназначенных для оценки протезов тазобедренного сустава.
[3] ИСО/TR 9326 Имплантаты для хирургии. Частичные и тотальные протезы бедренного сустава. Руководство по лабораторной оценке изменений формы опорных поверхностей.
[4] ИСО 14242-1 Имплантаты для хирургии. Износ тотальных протезов тазобедренного сустава. Часть 1. Параметры нагружения и смещения для аппаратов для испытания на износ и соответствующие условия окружающей среды для испытаний.
[5] ИСО 14242-2 Имплантаты для хирургии. Износ тотальных протезов тазобедренного сустава. Часть 2. Методы измерения.
Приложение ДА
Сведения о соответствии национальных стандартов Российской Федерации ссылочным международным стандартам
Таблица ДА.1
Обозначение ссылочного международного стандарта | Степень соответствия | Обозначение и наименование соответствующего национального стандарта |
ИСО 7206-1:1995 | IDT | ГОСТ Р ИСО 7206-1-2005 "Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 1. Классификация и обозначение размеров" |
ИСО 7206-2:1996 | IDT | ГОСТ Р ИСО 7206-2-2005 "Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 2. Суставные поверхности, изготовленные из металлических, керамических и полимерных материалов" |
ИСО 7206-4:2010 | IDT | ГОСТ Р ИСО 7206-4-2012 "Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 4. Определение прочности и эксплуатационных качеств бедренных компонентов с ножкой" |
ИСО 7206-6:1992 | IDT | ГОСТ Р ИСО 7206-6-2012 "Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 6. Определение прочностных свойств области шейки и головки бедренных компонентов" |
ИСО 7206-10:2003 | IDT | ГОСТ Р ИСО 7206-10-2005 "Имплантаты для хирургии. Эндопротезы тазобедренного сустава частичные и тотальные. Часть 10. Определение сопротивления статистической нагрузке модульных бедренных головок" |
ИСО 14630:2008 | IDT | ГОСТ Р ИСО 14630-2011 "Имплантаты хирургические неактивные. Общие требования" |
ИСО 21534:2007 | IDT | ГОСТ Р ИСО 21534-2013 "Имплантаты хирургические неактивные. Имплантаты для замены суставов. Частные требования" |
Примечание - В настоящей таблице использовано следующее условное обозначение степени соответствия стандартов: | ||
УДК 616-089.843:006.354 | ОКС 11.040.40 | ОКП 93 9800 |
Ключевые слова: неактивные хирургические имплантаты, протезирование тазобедренного сустава, специальные требования | ||
Электронный текст документа
и сверен по:
, 2014

