ГОСТ Р 56430-2015/GHTF/SG3/N18:2010
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Система менеджмента качества
ИЗДЕЛИЯ МЕДИЦИНСКИЕ
Руководство по корректирующим и предупреждающим действиям и связанным процессам системы менеджмента качества
Quality management system. Medical devices. Guidance on corrective action and preventive action and related QMS processes
ОКС 03.120.10
11.040.01
ОКП 94 000
Дата введения 2016-07-01
Предисловие
1 ПОДГОТОВЛЕН Обществом с ограниченной ответственностью "МЕДИТЕСТ" (ООО "МЕДИТЕСТ") на основе собственного аутентичного перевода на русский язык международного документа, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 436 "Управление качеством медицинских изделий"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 10 июня 2015 г. N 633-ст
4 Настоящий стандарт идентичен по отношению к международному документу Целевой группы по глобальной гармонизации (Global Harmonization Task Force, GHTF) GHTF/SG3/N18:2010* "Система менеджмента качества. Изделия медицинские. Руководство по корректирующим и предупреждающим действиям и связанным процессам системы менеджмента качества" (GHTF/SG3/N18:2010 "Quality management system - Medical devices - Guidance on corrective action and preventive action and related QMS processes")
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января предыдущего года) информационном указателе "Национальные стандарты", а официальный текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
Введение
Настоящий стандарт разработан Целевой группой по глобальной гармонизации (GHTF) - добровольным сообществом, состоящим из представителей регулирующих органов медицинской промышленности. Настоящий стандарт не предназначен как обязательное руководство для использования его в регулировании медицинских изделий.
Настоящий стандарт предназначен для изготовителей медицинских изделий и регулирующих органов. Он также может быть использован для образовательных целей, но не предназначен для использования его для оценки или аудита на соответствие нормативным требованиям. Ожидается, что пользователь настоящего стандарта знаком с нормативными требованиями к системе менеджмента качества (СМК) в промышленности медицинских изделий.
Для целей настоящего стандарта предполагается, что изготовитель медицинского изделия имеет СМК, которая требует от изготовителя документирования ряда процессов, с целью обеспечения того, чтобы медицинские изделия, выпускаемые в обращение, являются безопасными и результативными. Например, такие требования включены в ИСО 13485 "Изделия медицинские. Системы менеджмента качества. Системные требования для целей регулирования", "Постановление министерства Японии по стандартам по контролю за производством и контролю за качеством медицинских изделий и изделий для in vitro диагностики (MHLW Постановление Министерства N 169)", "Предписание для Систем качества FDA
21 CFR Часть 820" или требования к системам качества соответствующих европейских директив по медицинским изделиям.
________________
Министерство Японии по здравоохранению, труду и благосостоянию.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (США).
Для этих целей изготовитель должен устанавливать процессы и определять соответствующие меры управления для мониторинга выявления несоответствий и потенциальных несоответствий и их анализа. Кроме того, изготовитель должен разработать процедуры, определяющие, когда и как должны быть предприняты коррекции, корректирующие или предупреждающие действия. Эти действия должны быть адекватны риску возникновения несоответствия или потенциального несоответствия.
Термины, примененные в настоящем стандарте, касающиеся рисков, менеджмента рисков и связанной с ними терминологией, определены в ИСО 14971 "Изделия медицинские. Применение менеджмента риска для медицинских изделий".
Сокращение "САРА" не будет использоваться в настоящем стандарте, так как понятие корректирующих и предупреждающих действий было неправильно интерпретировано, предполагая, что предупреждающие действия требуются для каждого корректирующего действия.
В рамках настоящего стандарта рассматривается процесс получения информации из различных "активных" и "пассивных" источников, которые будут иметь основу для корректирующих или предупреждающих действий.
Изготовитель должен обосновать выбор типа источников данных, на основании которых будут определены корректирующие или предупреждающие действия.
Независимо от характера источника данных, дальнейшая оценка и последующее расследование являются идентичными, включая этапы расследования, выявления причин, определение необходимых последующих действий, верификацию их реализации и оценку результативности.
Настоящий стандарт включает описание процессов измерения, анализа и улучшения в виде полных и интегрированных процессов.
1 Область применения
Настоящий стандарт содержит рекомендации для установления адекватных процессов измерения, анализа и улучшения в системе менеджмента качества, связанных с коррекцией и/или корректирующими действиями в случае выявления несоответствий или предупреждающих действий для потенциальных несоответствий системы, процессов или продукции.
2 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями. В скобках даны ссылки на пункты ИСО 9000.
2.1 коррекция (correction): Действие, предпринятое для устранения обнаруженного несоответствия (3.6.2).
Примечания
1 Коррекция может осуществляться в сочетании с корректирующим действием (3.6.5).
2 Коррекция может включать в себя, например, переделку (3.6.7) или снижение градации (3.6.8).
2.2 корректирующее действие (action corrective): Действие, предпринятое для устранения причины обнаруженного несоответствия (3.6.2) или другой нежелательной ситуации.
Примечания
1 У несоответствия может быть несколько причин.
2 Корректирующее действие предпринимается для предотвращения повторного возникновения события, тогда как предупреждающее действие (3.6.4) - для предотвращения возникновения события.
3 Существует различие между коррекцией (3.6.6) и корректирующим действием.
2.3 источники получения данных (data sources): Процессы внутри системы менеджмента качества, позволяющие получать качественную информацию, которая может быть использована для идентификации несоответствий или потенциальных несоответствий.
2.4 разрешение на отклонение (concession): Разрешение на использование или выпуск продукции, которая не соответствует установленным требованиям (3.6.11).
2.5 предупреждающее действие (preventive action): Действие, предпринятое для устранения причины потенциального несоответствия (3.6.2) или другой потенциально нежелательной ситуации.
Примечания
1 У потенциального несоответствия может быть несколько причин.
2 Предупреждающее действие предпринимается для предотвращения возникновения события, тогда как корректирующее действие (3.6.5) - для предотвращения повторного возникновения события.
2.6 несоответствие (nonconformity): Невыполнение требования (3.1.2).
2.7 верификация (verification): Подтверждение на основе представления объективных свидетельств (3.8.1) того, что установленные требования (3.1.2) были выполнены.
Примечания
1 Термин "верифицировано" используется для обозначения соответствующего статуса.
2 Деятельность по подтверждению может включать:
- осуществление альтернативных расчетов;
- сравнение научной и технической документации (3.7.3) по новому проекту с аналогичной документацией по апробированному проекту;
- проведение испытаний (3.8.3) и демонстраций;
- анализ документов до их выпуска.
2.8 валидация (validation): Подтверждение на основе представления объективных свидетельств (3.8.1) того, что требования (3.1.2), предназначенные для конкретного использования или применения, выполнены.
Примечания
1 Термин "подтверждено" используется для обозначения соответствующего статуса.
2 Условия применения могут быть реальными или смоделированными.
3 Общий обзор
Изготовитель отвечает за внедрение и поддержание СМК, которая позволяет организации производить безопасные и результативные медицинские изделия, отвечающие требованиям потребителей и нормативным требованиям.
Несоответствие, как это определено в 2.6, является невыполнением требования. Важно понимать, что требования могут относиться к продукции, процессу или СМК.
Когда несоответствие идентифицировано, изготовитель должен определить его значимость, связанные риски и вероятность его повторения.
После того, как это было сделано, изготовитель может принять решение о том, что несоответствие имеет незначительные риски или вряд ли повторится. В таких случаях изготовитель может решить провести только коррекцию.
Если несоответствие повторяется в СМК, в процессе производства или после того как медицинское изделие было поставлено потребителю, это признак того, что соответствующие действия могут быть необходимы. В любом случае СМК требует, чтобы корректирующие действия проводились с целью предотвращения повторения несоответствия. Корректирующие действия могут быть как простыми, как переподготовка сотрудников, так и более сложными, как реинжиниринг производственного процесса.
Изготовитель может столкнуться с ситуациями, которые на самом деле не являлись причиной несоответствий, но могли создать их в будущем. Такие ситуации могут потребовать принятия предупреждающих действий. Например, анализ трендов производства или приемо-сдаточных испытаний показывает, что процесс приближается к предельным значениям и требуется пересмотр параметров приемки продукции или технологических параметров производства (процессов, оборудования или производственных объектов). Эти изменения могут представлять собой предупреждающие действия. Предупреждающие действия не должны включать такие корректировки, которые бы предназначались для увеличения номинальных значений в диапазоне регулирования производственных процессов.
Меры, принятые для устранения выявленных несоответствий в рамках одной СМК (независимо от того, предпринимались ли действия в более чем на одной производственной площадке или филиалах, функционирующих в рамках этой СМК), будут рассматриваться как корректирующие действия. Тем не менее, подобные действия, применяемые в другой СМК (независимо от того, распространяется ли она на эту площадку или филиал, или организацию в целом), в которых еще не возникали подобные несоответствия, будут рассматриваться как предупреждающие.
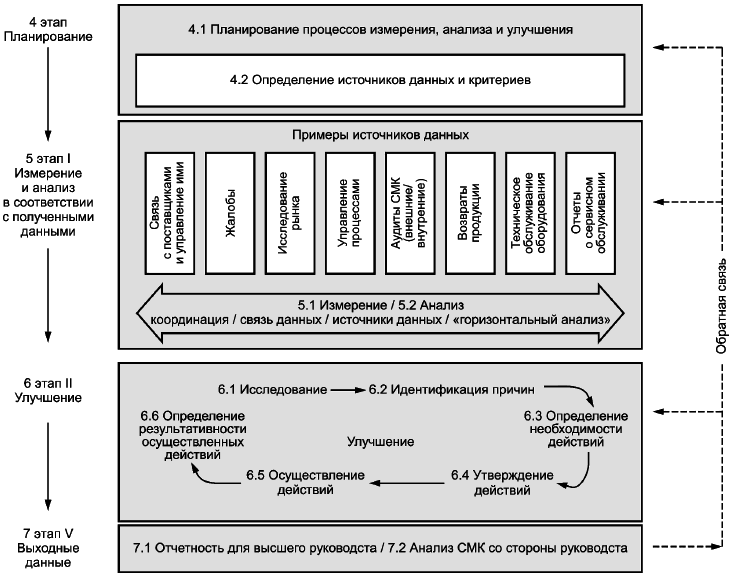
На рисунке 1 показаны типичные этапы, которые необходимо учитывать при планировании, осуществлении и поддержании результативности процессов измерения, анализа, улучшения и ответственности высшего руководства. В приложении A представлен перечень возможных мероприятий, соответствующих этапам на рисунке 1.
В качестве проверки результативности определенных процессов, высшее руководство должно регулярно пересматривать выходы процессов и актуализировать их по мере необходимости.
Рисунок 1 - Процессы измерения, анализа и улучшения
Документированные процедуры, требования и записи должны быть определены изготовителем для обеспечения и демонстрации результативного планирования, функционирования и управления процессами. Документированные свидетельства принятия решений и осуществления каких-либо действий должны являться частью СМК.
4 Этап I. Планирование
Планирование включает определение процессов и связанных с ними ресурсов для удовлетворения конкретных целей. Факторы, которые следует учитывать на этапе планирования должны быть согласованы с общим бизнес-планом изготовителя, включающие предполагаемое использование изделия, анализ рынка, обратную связь от потребителей, а также нормативные требования.
Должно быть определено участие высшего руководства (например, анализ, утверждение) на соответствующих уровнях в случаях выявления несоответствий или потенциальных несоответствий. Высшее руководство должно обеспечить, чтобы критерии измерений и источники данных были определены и доведены до сведения всей организации.
4.1 Планирование процессов измерения, анализа и улучшения
Факторы, которые следует учитывать в ходе планирования должны быть согласованы с общим бизнес-планом изготовителя и, как минимум, должны включать в себя тип производимого изделия, предназначенные рынки и потребителей, и нормативные требования. В рамках планирования высшее руководство должно определить процессы, критически важные для деятельности, влияющей на качество и нормативные требования, и выбирать соответствующие источники данных для измерения, анализа и содействовать улучшению по мере необходимости.
В процессе планирования измерения и анализа, изготовитель должен учитывать источники данных, измерение элементов данных в пределах каждого источника данных, включая периодичность мониторинга и анализа, которые должны быть осуществлены по каждому источнику данных, или нескольким источникам данных.
Измерение элементов данных должно быть осуществлено таким образом, чтобы обеспечивать изготовителя результативной управленческой деятельностью и поддерживать результативность СМК. Каждый из элементов данных должен быть определен, запланирован в соответствии с конкретными требованиями для измерения, которые периодически подвергаются мониторингу.
Область применения СМК и область применения процессов измерения, анализа и улучшения определяют, является ли источник данных активным (корректирующие действия) или пассивным (предупреждающие действия).
Этапы планирования должны обеспечивать следующее:
- определение соответствующих внутренних и внешних источников данных, являющихся индикаторами процесса и эксплуатационных характеристик изделия;
- обеспечение адекватными ресурсами и установление ответственности и полномочий для того, чтобы осуществить необходимые действия. Ресурсы могут включать в себя технических экспертов, испытательные лаборатории, данные, инфраструктуру, обучение и т.д.;
- определение требований для каждого идентифицированного источника данных, включая ограничения, критерии приемлемости, критерии развития, механизмов отчетности о несоответствиях или потенциальных несоответствиях;
- анализ элементов данных в пределах источников данных;
- взаимосвязь и анализ данных, полученных из источников данных.
Для каждого элемента данных должны быть определены отдельные критерии, однако критерии могут быть определены и для комбинации элементов данных. Критерии должны быть количественными, когда это возможно, чтобы максимально обеспечить согласованность и воспроизводимость для последующего анализа. Если критерии и данные являются качественными, то субъективность должна быть устранена или сведена к минимуму.
Критерии приемлемости должны быть основаны на данных системы менеджмента качества, продукции и процессов, спецификаций или требований, которые обычно определяются в ходе проектирования и разработки. Это включает в себя процессы проектирования, разработку и поддержание процессов производства, доставки, обслуживания и процессов монтажа.
Критерии развития, используемые для целей реализации процесса улучшения (см. раздел 6) могут быть представлены в виде уровней действий, триггерных точек, порогов и т.д., и их необходимо документировать. Эти критерии развития включают в себя определенные уровни действий общего характера, а также конкретные действия в рамках деятельности по управлению рисками. В частности, критерии должны быть установлены для конкретных случаев. Например, в случае инцидента, который привел к летальному исходу или серьезным травмам, следует приступить к немедленным действиям в рамках этапа улучшения (см. раздел 6).
Для новых технологий и существующих, но с новым подходом применения, первоначальные критерии развития иногда трудно определить в рамках процесса мониторинга. Поэтому изготовитель должен планировать ресурсы для анализа информации, чтобы подтвердить первоначальные предположения и установить или пересмотреть критерии развития.
Планирование должно предусматривать подтверждение того, что критерии приемлемости и развития, механизмы отчетности о несоответствиях или потенциальных несоответствиях, по-прежнему соответствуют ранее определенным источникам и элементам данных. Там, где должны быть определены новые источники данных, следует подтвердить, что они были выявлены и их критерии определены.
4.2 Определение источников данных и критериев
Изготовитель должен определить и документировать соответствующие источники данных и элементы данных, как внутренние, так и внешние по отношению к организации. Элементы данных должны предоставлять информацию о несоответствиях, потенциальных несоответствиях и результативности процессов в определенных источниках данных.
Примерами источников данных могут являться:
- нормативные требования;
- анализ со стороны руководства;
- поставщики (взаимодействие/управление);
- жалобы/обращения;
- отчеты о неблагоприятных событиях;
- мониторинг процессов;
- готовая продукция;
- аудиты (внутренние/внешние);
- отзывы о продукции;
- статистика по комплектующим;
- отчеты по обслуживанию;
- возвраты продукции;
- исследование рынка/клиентуры;
- научная литература;
- источники СМИ;
- процессы жизненного цикла продукции (проектирование, закупки, производство и обслуживание, обратная связь от потребителей);
- менеджмент рисков.
Дополнительные примеры элементов данных приведены в приложении B.
Когда проблема выявляется из одного источника данных, изготовителю необходимо проанализировать аналогичную информацию из других источников данных. Более того, также следует анализировать информацию, полученную из внешних источников данных. Получение информации из нескольких источников данных в результате приведет к комплексной оценке данных. Это поможет изготовителю лучше определить необходимые меры.
5 Этап II. Измерение и анализ с помощью источников данных
После того, как были определены источники данных, элементы данных и критерии приемлемости, как часть процесса планирования, изготовитель должен осуществлять процессы измерения, мониторинга и анализа, чтобы подтвердить соответствие или выявить несоответствие.
Программное обеспечение, используемое при измерении, мониторинге и анализе, будь то приобретенное или специально разработанное, должно быть валидировано для использования его по назначению.
Например, опросы клиентов, проводимые отделом маркетинга, показали, что существует общее недовольство относительно упаковки продукта X. При дальнейшем расследовании (внутри этого источника данных и среди других источников), например, данными из жалоб, возвратам продукции, отчетам и др., стало очевидно, что существует вероятность возникновения несоответствий: небезопасного использования или повреждения изделия в результате использования текущего варианта упаковки. В результате этого анализа на стадии III (см. раздел 6) было определено, что в данном случае целесообразно осуществить предупреждающие действия.
5.1 Измерение
В рамках настоящего стандарта, измерение представляет собой набор операций для определения значения элемента данных (количество, качество).
Данные, полученные по результатам измерений продукции, процессов и СМК, накапливаются на протяжении всего жизненного цикла изделия. Изготовитель должен определить, например частоту измерения, величину точности и достоверности данных. Изготовитель также должен убедиться, что собранные текущие данные являются актуальными.
Данные результатов измерений должны быть сохранены в виде записей. Изготовитель должен сохранять данные в виде, позволяющем их извлекать, при этом данные должны являться подходящими для анализа и отвечающими как СМК, так и нормативным требованиям.
Мониторинг является систематическим и регулярным сбором результатов измерений. Изготовитель должен определить на этапе планирования, какие, когда и каким образом собранные данные должны быть проверены. Полученные данные должны быть таковыми, чтобы они смогли быть проанализированы для дальнейших действий. Мониторинг данных может быть непрерывным или периодическим, в зависимости от типа источника данных и элементов данных. Процессы мониторинга должны периодически пересматриваться для целей их дальнейшей пригодности.
5.2 Анализ
В настоящем стандарте анализ представляет собой систематический сбор данных и их оценивание посредством измерений для формирования заключений.
Изготовитель должен иметь документированные процедуры для анализа данных в соответствии с критериями, установленными в 4.1. Анализ необходимо проводить с целью выявления несоответствий или потенциальных несоответствий или с целью определения области, где необходимо инициировать дальнейшее расследование. Кроме того, анализ используется для демонстрации пригодности и результативности продукции, процессов и СМК. Анализ может быть выполнен с использованием аналитических инструментов, групп экспертов, владельцев процессов или с помощью независимого анализа. Результаты анализа должны быть задокументированы.
После того, как определено, что необходимо измерять, должны быть определены статистические методы для идентификации области изменчивости и тем самым помочь изготовителю поддерживать или повышать результативность и эффективность. Эти методы также способствуют лучшему использованию имеющихся данных для оказания помощи в принятии решений. Статистические методы оказывают помощь в выявлении, оценке, анализе, интерпретации и моделировании изменчивости.
Для анализа несоответствия могут быть применены как статистические, так и нестатистические методы.
Примеры статистических методов:
- графики статистического управления процессами;
- анализ Парето;
- тренды данных;
- линейный и нелинейный регрессионный анализ;
- опытно-конструкторские (DOE - планирование эксперимента) и анализ отклонений;
- графические методы (гистограммы, диаграммы рассеяния и т.д.).
Примеры нестатистических методов:
- анализ СМК со стороны руководства;
- результаты совещаний по качеству;
- комиссии по надежности (внутренние/внешние);
- анализ видов и последствий отказов (FMEA);
- анализ древа неисправностей (FTA).
Анализ, как правило, проводится в нескольких различных точках (во времени и/или на организационном уровне). Например, определенный объем анализа и возможности расследования отказов (где есть доказательства несоответствия) будет необходим для каждого источника данных.
В дополнение к анализу из источников данных необходимо определить уровень анализа между источниками данных, чтобы определить степень и значимость несоответствия или потенциального несоответствия. Связь данных из различных источников данных называется "горизонтальный анализ". С помощью горизонтального анализа можно:
- определить, что предложенное действие, исходя из анализа источника данных, является достаточным, без дальнейших дополнительных действий в этапе III (см. раздел 6); или,
- предоставить информацию о необходимости дополнительных действий на этапе III (см. раздел 6), независимо от того, выявил ли анализ источников данных несоответствия или потенциальные несоответствия.
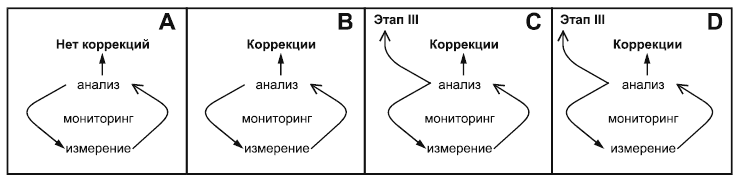
Варианты выходных данных измерения и анализа приведены на рисунке 2.
Рисунок 2 - Выходы измерения и анализа
В представленном ниже примере приведена более подробная информация, разъясняющая рисунок 2. Каждый вариант, показывающий различные выходы результатов измерения и анализа, описывается на основе приведенного ниже примера.
Пример - В процессе проектирования и разработки не были выполнены требования к составу документации. Недостающая документация включала в себя замену одного поставщика электронной платы на другого. Требование заключалось в документировании наименования поставщика и его регистрационного номера в итоговом отчете.




Документированные процедуры должны четко разграничить и определить, когда требуется переход на этап III.
Обычно изготовители имеют в наличии организационные группы или связанные процессы из основных источников данных (например, обработка жалоб, информация о несоответствиях, материалы наблюдательных советов, процессы управления изменениями). В рамках этих групп или процессов определенные виды деятельности, отраженные на рисунке 2, могут быть реализованы без дальнейших действий на этапе III.
Однако могут иметь место определенные события, действия по которым, в связи со значимостью риска, могут перейти на этап III без замедления. В случае выявления потенциального несоответствия, последующие действия также могут переходить на этап III (см. раздел 6) для осуществления необходимых действий по предотвращению возникновения потенциального несоответствия.
В случае невозможности коррекции, или, если коррекция может быть принята в группах или процессах, необходим мониторинг и анализ источников данных (например, в тренде), для определения того, какая накопленная информация может потребоваться на этапе III. Всякий раз, когда проблема переходит на этап III, любая информация, полученная в рамках, определяемых деятельностью этих групп или процессов, должна быть использована в какой-либо деятельности этапа III, например, "расследование" (см. 6.1) или "определение действий" (см. 6.3).
6 Этап III. Улучшение
Этап "улучшение" в виде корректирующих или предупреждающих действий предназначен для устранения или смягчения последствий несоответствия или потенциального несоответствия.
Деятельность по улучшению зависит от конкретного несоответствия или потенциального несоответствия. Все предыдущие данные этапа II должны быть использованы в качестве входных данных в процессах этапа III.
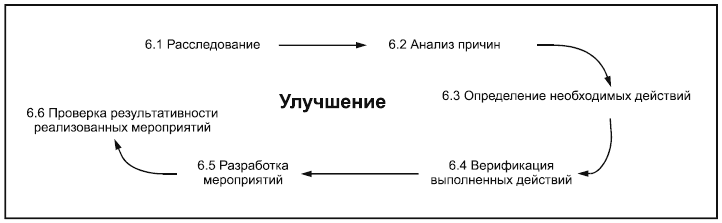
Этап "улучшение" и мероприятия, приведенные на рисунке 3, должны быть задокументированы. Улучшение обычно включает следующие виды деятельности, которые изготовитель будет осуществлять последовательно или иногда одновременно:
- всестороннее расследование отчетов о несоответствиях;
- глубокий анализ причин возникновения несоответствий;
- определение необходимых действий;
- верификация выполнения этих действий;
- разработка мероприятий;
- проверка результативности реализованных мероприятий.
6.1 Расследование
Цель расследования заключается в идентификации основной причины существующих или, по возможности, потенциальных несоответствий, а также в выработке рекомендации для решения проблемы. Масштаб/рамки расследования должны быть соизмеримы с риском выявленного несоответствия.
Рисунок 3 - Этап III. Улучшение
Практика показывает, что документально план должен быть разработан до начала проведения расследования (см. приложение D). План должен включать:
- описание несоответствия, выраженное в виде постановки задачи;
- область расследования;
- группа по расследованию, и обязанности членов группы;
- описание деятельности, которая должна быть выполнена;
- ресурсы;
- методы и средства;
- временные рамки.
Из информации, полученной в ходе всего процесса, постановка задачи может быть пересмотрена и уточнена в зависимости от обстоятельств.
Расследование должно:
- определить степень несоответствия или потенциального несоответствия;
- принимать во внимание, что есть, вероятно, несколько причин события; следовательно, расследование не должно быть прекращено досрочно;
- отличать симптомы несоответствия от истинных причин его возникновения и требовать устранения первопричины, а не только симптомов;
- определить конечную точку расследования. Чрезмерно исчерпывающее расследование может являться неоправданной отсрочкой осуществления коррекции несоответствия или понести дополнительное увеличение затрат. (Например, если устранить 80% выявленных причин, то вполне вероятно, что значительные причины были устранены (метод Парето));
- принять во внимание выходные данные менеджмента риска;
- согласовать вид и форму доказательств. Например, доказательства должны включать следующую информацию:
a) тяжесть;
b) вероятность наступления события;
c) анализ последствий, вытекающих из события.
Для облегчения анализа расследование должно предусматривать сбор данных и основываться на любом анализе, оценках и расследованиях, которые были ранее осуществлены (см. раздел 5). Лицам, осуществляющим расследование, потребуется идентифицировать, определить и затем документировать наблюдаемые замечания/несоответствия или уже известные причины, чтобы гарантировать понимание контекста и масштаба расследования. Также необходимо:
- проанализировать и уточнить полученную информацию;
- провести анализ любой дополнительной информации, полученной с помощью горизонтального анализа;
- рассмотреть, является ли это системной или несистемной проблемой;
- собрать дополнительные доказательства, если это необходимо;
- провести опрос владельцев процессов/операторов или других заинтересованных сторон;
- провести анализ документов;
- проверить объекты или аспекты окружающей среды.
Должны быть проанализированы предыдущие расследования с целью определения является ли данное событие новым или повторяющимся, когда, например, ранее реализованные действия явились нерезультативными. Следующие вопросы помогут принять решение:
- Несоответствие получено из одного источника данных?
- Соотносится ли данное несоответствие с несоответствиями, полученными из других источников данных?
- Идентифицирует ли несоответствие несколько источников данных?
- Оказывают ли влияние на расследуемую проблему другие несоответствия?
Многие из инструментов, которые используются в расследованиях, основаны на причинно-следственной связи между событием и симптом этого события. Чтобы убедиться, что выявлены именно причины, а не симптомы, необходимо следующее:
- четкое описание причины и ее влияние. Также должна быть описана связь между причиной и нежелательным результатом;
- каждое описание причины также должно включать условия, способствующие возникновению нежелательного эффекта.
Бездействие может рассматриваться как причина только в случае, если существует требование какого-либо действия. Требование действия может быть определено в процедуре, регламенте, стандартах, руководящих принципах или другого разумно ожидаемого действия.
Некоторые из наиболее распространенных инструментов и методов включают следующее:
- причинно-следственные диаграммы;
- метод "5 почему";
- схемы Парето;
- причинно-следственные диаграммы "рыбий скелет" Исикавы;
- анализ изменений;
- методы анализа рисков;
- метод "Да/Нет".
Итогом расследования должно быть следующее:
- четко определенная постановка задачи;
- информация, которая была собрана, проанализирована и/или оценена;
- результаты анализа/оценивания информации;
- идентификация причин(ы) или способствующих факторов;
- действия в отношении причин(ы) или способствующих факторов.
6.2 Определение основных причин
Причины или факторы, способствующие возникновению несоответствия или потенциального несоответствия, должны быть незамедлительно выявлены, чтобы могли быть приняты корректирующие действия для предотвращения повторения события или предупреждающие действия для предотвращения его возникновения. Процесс определения основных причин следует начинать с выхода(ов) расследования (см. 6.1).
При оценке соответствующих данных, необходимо учитывать следующее:
- систематическое накопление причинно-следственных выводов, документально подтвержденных данных;
- оценка значимых или скрытых причин и их влияние на проблему;
- уверенность, что идентифицируются причины, а не симптомы;
- проверка более одной первопричины (анализ других процессов в случае необходимости). Причины или способствующие факторы возникновения несоответствий или потенциальных несоответствий могут включать следующее:
- отказ или неисправность: поступающих материалов, процессов, инструментов, оборудования или производственных объектов, в которых выпускается продукция, хранение и использование, в том числе оборудование и систем в нем;
- неадекватные или отсутствующие процедуры и документация;
- несоблюдение процедур;
- неадекватное управление процессом;
- несоответствующее планирование;
- недостаток обучения;
- неадекватные условия труда;
- недостаточные ресурсы (человеческие или материальные);
- изменчивость процесса.
Для получения дополнительной информации по аспектам, которые будут рассмотрены при выполнении анализа основных причин, см. приложение C.
Результатом анализа основной причины должно являться четкое изложение фундаментальной причины возникновения несоответствия (см. приложение D).
6.3 Определение действий
Когда причина(ы) определена(ы), изготовитель должен определить и задокументировать необходимые коррекции и/или корректирующие действия или предупреждающие действия. Эти действия должны быть проанализированы с целью обеспечения того, что идентифицированы все необходимые действия. Анализ может быть полезен для процессного подхода. В случае необходимости решения относительно управления продукцией также должны быть документированы.
Возможно получение следующих результатов, которые должны быть задокументированы: Не требуется никаких дополнительных действий (при условии, что отсутствуют вопросы, связанные с безопасностью или регулирующими требованиями):
a) продолжается непрерывный мониторинг;
b) принимается решение об отклонении и продолжается мониторинг.
Коррекции
Коррекция может быть необходима, чтобы сделать первые корректировки с целью решения вопросов безопасности или снижения риска (например, прекращение выпуска, приостановка отгрузки/поставки, предоставление пояснительных уведомлений). Эта деятельность проводится до завершения расследования и выявления причины. Однако после проведения расследования и определения основных причин, могут потребоваться необходимые дополнительные и/или, возможно, иные коррекции.
Корректирующие действия
Корректирующие действия должны решать системные проблемы. Например, изменение процедуры и обучение персонала пересмотренной процедуре само по себе не всегда может быть целесообразным или достаточным для решения системных(ой) проблем(ы).
Предупреждающие действия
Разработка предупреждающих действий не предполагает наличие ранее выявленных несоответствий.
В результате этой деятельности, перечень действий должен быть задокументирован. Он может включать:
- подробное описание осуществления работ;
- анализ регулирующих требований (лицензирование, сертификация и т.д.);
- функции и обязанности лиц, связанных с выполнением действий;
- определение необходимых ресурсов (например, информационное обеспечение, инфраструктура, производственная среда);
- протоколы верификации и/или валидации с критериями приемлемости;
- график выполнения работ, включая временную последовательность;
- методы или данные для определения результативности с критериями приемлемости;
- идентификацию начальной точки мониторинга и конечной точки в виде коррекций и/или корректирующих действий или предупреждающих действий, как было изложено выше.
6.4 Верификация действий
Перед осуществлением действий, которые были определены, изготовитель должен верифицировать идентифицированные действия и утвердить их реализацию. Кроме того может дополнительно потребоваться валидация или ревалидация, там, где меняются потребности пользователей или предполагаемое использование и будет необходима валидация процесса проектирования.
Деятельность по верификации должна обеспечить, чтобы все элементы предлагаемого действия (документация, обучение и т.д.) будут удовлетворять требованиям предполагаемого действия. Эти мероприятия должны быть выполнены лицами, которые компетентны в процессе проектирования или процессе, который является предметом корректирующих или предупреждающих действий. Верификация предупреждающего действия может быть достигнута путем создания условий, в которых можно соответствующую ситуацию подтвердить, и при этом несоответствие не возникает.
С помощью валидации деятельности накапливаются данные и информация, которые подтверждают вероятность результативности корректирующих действий для исключения несоответствия или предлагаемого несоответствия.
Примеры вопросов, которые будут рассмотрены при планировании верификации/валидации, включают в себя:
- Устранит ли действие выявленную причину?
- Охватывает ли действие все необходимые процессы/продукцию?
- Влияет ли отрицательно действие на готовую продукцию?
- Можно ли завершить действия в соответствии с запланированным графиком (ресурсы, сырье/материалы, логистика, связь и т.д.)?
- Является ли действие соизмеримым со степенью ранее установленных рисков?
- Возникнут ли новые риски или несоответствия после этих действий?
6.5 Осуществление действий
Следующие элементы, которые могут быть затронуты при осуществлении действий, и которые должны быть задокументированы:
- принимающие участие стороны;
- материалы;
- процессы;
- обучение;
- коммуникации;
- инструменты;
- временные рамки осуществления действий.
Также необходимо верифицировать, что осуществление всех действий завершено.
6.6 Определение результативности осуществленных действий
Изготовитель должен накапливать данные, связанные с результативностью, в течение всего времени осуществления действий (примеры приведены в приложении D).
Высшее руководство должно обеспечить проведение анализа и свое участие в нем с целью подтверждения того, что предпринятые действия были результативными, а новые вопросы или проблемы не возникают. Следующие вопросы должны быть рассмотрены на соответствующих этапах осуществления действий и включены в окончательный анализ:
- существующая проблема была всесторонне рассмотрена?
- определена ли степень проблемы (например, диапазон выпускаемых изделий, информация от пациентов, процессы, производственные линии, оператор)?
- выявлены ли первопричины/способствующие факторы этой проблемы и решены ли они?
- определены ли действия, направленные на улучшение? Запланированы ли они, задокументированы, верифицируются и осуществляются ли?
Если изготовитель считает действия нерезультативными, он должен повторно инициировать деятельность этапа III (см. раздел 6). Если изготовитель считает действия нерезультативными или в ходе осуществления действий возникают новые проблемы или несоответствия, то он должен перейти к действиям этапа II (см. раздел 5).
7 Этап IV. Входные данные для высшего руководства
Высшее руководство на разных уровнях организации должно быть вовлечено в каждое действие улучшения; либо посредством утверждения действий или отчетности.
Отчет для высшего руководства является основным механизмом, чтобы гарантировать, что система менеджмента качества в целом является результативной.
7.1 Отчет для высшего руководства
Изготовитель должен иметь механизм/процедуру, который оперативно реагировал бы на вопросы, связанные с безопасностью или другие проблемы в управлении с высоким риском. Эти вопросы могут быть идентифицированы в источниках данных, фазах улучшения (см. раздел 6), или возникать из источников, внешних по отношению к системе менеджмента качества. В дополнение к этому оперативному механизму, изготовитель должен определить обязанности высшего руководства и сотрудников (например, владельцев процессов) касательно процессов измерения, анализа и улучшения процессов, чтобы гарантировать, что процессы и реализуемые действия, результативны. Для этого в данном механизме должно быть предусмотрено управление на разных уровнях, чтобы получать актуальную информацию или данные:
- из деятельности по измерению и анализу из отдельных источников данных;
- расследований, действий, осуществления и т.д. из процессов улучшения.
7.2 Анализ со стороны руководства
Изготовитель должен иметь процедуры для получения входных данных для анализа со стороны руководства, включая соответствующую информацию процессов улучшения, таких как действия по улучшению (корректирующие и/или предупреждающие действия), а также важных изменений.
Изготовитель должен определить, какие данные должны быть представлены для анализа со стороны руководства. Данные должны учитывать специфику целей в области качества изготовителя и анализироваться на регулярной основе. Простое предоставление ряда мероприятий по улучшению или данных о том, какое количество действий по улучшению было включено в анализ со стороны руководства, не является достаточным для оценки результативности процессов.
В анализ должна быть включена оценка любых возможностей для улучшения продукции, процессов системы менеджмента качества или самой организации в целом.
Выходными данными анализа могут являться выделение дополнительных ресурсов или персонала в ту или иную области, проект или производство продукции, в которых анализ выявил проблемы, связанные с невыполнением требований клиентов, регулирующих требований, требований безопасности и ожидания необходимой результативности.
Приложение A
(справочное)
Примеры этапов деятельности
Перечень возможной деятельности на соответствующих этапах приведен на рисунке 1.
Ниже приведены примеры из основных пунктов настоящего стандарта. Они не предназначены в качестве обязательных и не должны использоваться в качестве таковых, но могут быть использованы как примеры взаимосвязи этапов и деятельности описанных в настоящем стандарте. Приведенные в скобках номера пунктов/видов деятельности не означают строгой последовательности - некоторые могут выполняться параллельно.
Таблица A.1
Этап | Деятельность |
Планирование | 1 Определение всех источников данных (внутренних/внешних) по типу продукции (4.1) |
Измерение и анализ с помощью источников данных | 7 Измерение и анализ всех источников данных, в которых возникают несоответствия и потенциальные несоответствия (5, 5.1 и 5.2) |
Расследование | 10 Определение объема и необходимых выходных данных по расследованию (6.1) |
Входные данные для высшего руководства | 17 Формирование отчета по расследованию и выходных данных для высшего руководства (7.1) |
* Шаги 20-22 не описаны в настоящем стандарте, но добавлены в эту таблицу в качестве напоминания об общих управленческих функциях в этой области СМК. | |
Приложение B
(справочное)
Примеры источников данных и элементов данных
Примеры источников данных и элементов данных приведены в таблице B.1, но не ограничиваются этой таблицей.
Таблица B.1
Источники данных | Элементы данных |
Регулирующие требования | Результаты проверок регулирующими органами |
Анализ СМК со стороны высшего руководства | Выходные данные отчета по анализу высшего руководства |
Управление поставщиками | Количество поставок |
Работа с жалобами/обращениями | Количество |
Отчет о неблагоприятных событиях | События |
Управление процессами | По видам продукции |
Готовая продукция | Результаты проверок и протоколы испытаний |
Аудиты СМК (внутренние/внешние) | Наблюдения (количество, категории, корпоративная политика, регулирующие требования, важность, другое) |
Отзывы о продукции | Своевременное реагирование на отзывы |
Статистика по комплектующим | Периодичность замены |
Отчеты по обслуживанию | Отчеты по монтажу |
Возврат продукции | Количество |
Исследование рынка/клиентов | Требования потребителей |
Научная литература | Научные работы |
Средства массовой информации | Статьи в профессиональных журналах |
Жизненный цикл продукции (проектирование, закупка, производство и обслуживание, обратная связь от потребителей | Результаты анализа проектирования и разработки |
Менеджмент риска | Опубликованные отчеты/литературные данные о нежелательных событиях с аналогичной продукцией |
Приложение C
(справочное)
Примеры факторов, способствующих возникновению несоответствий
Примеры возможных способствующих факторов, которые рассматриваются при выполнении анализа основных причин:
Материалы:
- несоответствующее сырье (сырье сделано не в соответствии со спецификацией);
- проблема связанных партий;
- проблема проектирования (неправильно выбрано сырье для продукции, неправильные спецификации);
- проблема поставщика (отсутствие управления поставщиками, отсутствие альтернативного поставщика);
- нехватка сырья.
Машины/оборудование:
- неправильный выбор инструмента;
- недостаточное техническое обслуживание или проектирование - калибровка;
- оборудование эксплуатировалось не в соответствии с рекомендациями изготовителя;
- поврежденное оборудование или инструмент;
- заканчивается срок эксплуатации;
- человеческая ошибка - недостаточная подготовка.
Производственная среда:
- не правильно организовано рабочее место;
- не осуществляется контроль соблюдения режима - температуры, влажности, давления, чистоты;
- несоответствующее планирование работы.
Менеджмент:
- недостаточное участие в управлении;
- стресс;
- человеческий фактор;
- отсутствие ограждений опасных объектов;
- было ли извещено руководство/предприняло ли оно меры.
Методы:
- нечеткие процедуры;
- неследование на практике предписанной методологии;
- плохие коммуникации.
Система менеджмента:
- недостаточное обучение или образование;
- плохое вовлечение сотрудников;
- плохое распознавание опасности;
- предыдущие опасности не устранены.
Измерение, мониторинг и улучшение:
- неадекватные процессы измерения и улучшения.
Приложение D
(справочное)
Примеры документирования процессов улучшения
Таблица D.1 представляет собой руководство для документирования различных требований процессов улучшения.
Таблица D.1
Необходимые действия | Примеры документирования | |
Формулировка проблемы | - Четкое определение формулировки проблемы. | В ходе процесса испытаний готовой продукции, два изделия из 30 были признаны несоответствующими требованиям проектного документа N 123456, пересмотр А. Примечание 2.1 в тексте проектного документа N 123456 требует, чтобы шероховатость поверхности была максимум 32 мкдюйма по всей внешней поверхности. Два несоответствующих изделия имели шероховатость поверхности выше максимальной: |
Коррекции | Основные примеры: | Поставщик был уведомлен о проблеме. |
Расследования | - Определение проблемы (актуализация/уточнение, если была выявлена новая информация). | Рассмотрен источник проблемы. Последующее расследование подтвердило, что проблема была ограничена поставщиком N 678. Все дополнительное количество доступного компонента было проверено в соответствии с планом проверки (95/95) и не было обнаружено никаких проблем. |
Идентификация причин несоответствий | Результатом анализа первопричин должно быть четкое изложение самых основных причин, приводящих к несоответствию | Был сделан вывод, что причиной появления этого несоответствия явились неадекватные процедуры у поставщика |
Планирование деятельности | Укажите: | Корректирующее действие: поставщик добавил в документированные процедуры требования к технологической линии по параметрам обрабатываемой поверхностей |
Верификация деятельности | Деятельность по верификации должна обеспечить, чтобы все элементы предложенного действия (документации, обучение и т. д.) удовлетворяла требованиям предлагаемого действия. | Общие примеры приведены ниже. Фактическая документация должна быть более конкретной: |
Верификация результативности | Методы или данные для определения результативности с критериями приемлемости: | "X" месяцев после внедрения: |
УДК 006.83:006.354 | ОКС 03.120.10 | ОКП 94 000 |
11.040.01 | ||
Ключевые слова: изделия медицинские, система менеджмента качества, корректирующие и предупреждающие действия, связанные процессы СМК | ||
Электронный текст документа
и сверен по:
, 2015