ГОСТ Р 53773-2010
Группа Н59
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПРОДУКЦИЯ СОКОВАЯ
Методы определения антоцианинов
Juice products. Methods for determination of Anthocyanins
ОКС 67.080,
67.050
ОКСТУ 9109
Дата введения 2011-01-01
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. N 184-ФЗ "О техническом регулировании", а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 РАЗРАБОТАН Некоммерческой организацией "Российский союз производителей соков" (НО "РСПС") при участии НИИ питания Российской Академии медицинских наук (НИИ питания РАМН)
2 ВНЕСЕН Подкомитетом "Соки фруктовые и овощные, нектары, сокосодержащие напитки и морсы" Технического комитета по стандартизации ТК 93 "Продукты переработки фруктов, овощей и грибов"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 24 февраля 2010 г. N 21-ст
4 В настоящем стандарте учтены основные положения международного стандарта CODEX-STAN 247-2005* "Общий стандарт на фруктовые соки и нектары" (CODEX-STAN 247-2005 "Codex general standard for fruit juices and nectars") в части методов анализа и отбора проб соковой продукции;
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
в части качественного определения антоцианинов учтены основные нормативные положения документа IFU Метод 71:1998 "Определение антоцианинов методом высокоэффективной жидкостной хроматографии" (Международная федерация производителей фруктовых соков) [IFU-Analyses No. 71 "Anthocyanins by HPLС" (International Federation of Fruit Juice Produces)]
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячно издаваемых информационных указателях "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
1 Область применения
Настоящий стандарт распространяется на фруктовые соки и нектары, фруктовые концентрированные соки, фруктовые пюре и концентрированные пюре, морсы и концентрированные морсы, сокосодержащие напитки, соковую продукцию обогащенную и для детского питания (далее - соковая продукция) и устанавливает следующие методы определения антоцианинов:
- метод высокоэффективной жидкостной хроматографии (далее - ВЭЖХ) для качественного определения антоцианинов в соковой продукции;
- метод рН-дифференциальной спектрофотометрии для определения массовой концентрации (массовой доли) суммы антоцианинов в соковой продукции. Нижний предел измерений массовой концентрации (массовой доли) суммы антоцианинов составляет 5 мг/дм (млн
). Верхний предел измерений массовой концентрации (массовой доли) 5000 мг/дм
(млн
).
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р ИСО 5725-1-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения
ГОСТ Р ИСО 5725-2-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
ГОСТ Р 51652-2000 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.018-93 Система стандартов безопасности труда. Пожаровзрывобезопасность статического электричества. Общие требования
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 199-78 Реактивы. Натрий уксуснокислый 3-водный. Технические условия
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ 4234-77 Реактивы. Калий хлористый. Технические условия
ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 24104-2001 Весы лабораторные. Общие технические требования*
________________
* С 1 января 2010 г. действует ГОСТ Р 53228-2008 в части вновь разрабатываемых и модернизируемых весов; с 1 января 2013 г. - в части весов, разработанных до 1 января 2010 г.
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26313-84 Продукты переработки плодов и овощей. Правила приемки, методы отбора проб
ГОСТ 26671-85 Продукты переработки плодов и овощей, консервы мясные и мясорастительные. Подготовка проб для лабораторных анализов
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание - При использовании настоящего стандарта целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодно издаваемому указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применен следующий термин с соответствующим определением:
3.1 антоцианины: Водорастворимые растительные пигменты, обусловливающие красную, синюю и фиолетовую окраску фруктов, относящиеся к классу флавоноидов и представляющие собой гликозиды антоцианидинов.
Примечание - Структура основных антоцианидинов, входящих в состав природных антоцианинов, приведена в приложении А (см. рисунок А.1).
4 Отбор и подготовка проб
4.1 Отбор проб - по ГОСТ 26313, подготовка проб - по ГОСТ 26671.
5 Метод высокоэффективной жидкостной хроматографии (ВЭЖХ)
5.1 Сущность метода ВЭЖХ
Метод обращенно-фазовой ВЭЖХ с фотометрическим детектированием при 518 нм обеспечивает разделение и качественное определение антоцианинов в соковой продукции, имеющей красную, синюю и фиолетовую окраску, с целью установления таких нарушений, как добавление экстрактов и соков из других окрашенных фруктов и овощей и (или) избыточное разбавление соковой продукции.
Полученные хроматограммы сравнивают с хроматограммами аутентичных фруктовых соков и данными таблицы Б.2 приложения Б.
5.2 Средства измерений, вспомогательное оборудование, посуда, реактивы, материалы
5.2.1 Хроматограф жидкостный высокоэффективный со спектрофотометрическим детектором (рабочий диапазон длин волн поглощения от 200 до 600 нм) и программно-аппаратным комплексом сбора и обработки результатов типа "Millenium 2000".
5.2.2 Колонка аналитическая длиной 250 мм и внутренним диаметром 4,6 мм, заполненная октадецилсиликагелем размером частиц 5 мкм.
5.2.3 Шприц для ВЭЖХ вместимостью 10 и 20 мкл.
5.2.4 Весы лабораторные по ГОСТ 24104 с пределами абсолютной погрешности однократного взвешивания ±0,1 мг.
5.2.5 Фильтры мембранные с диаметром пор 0,2 и 0,45 мкм для фильтрования подвижной фазы и проб.
5.2.6 рН-метр с диапазоном измерений рН от 2 до 18; погрешность измерений ±0,01 ед. рН.
5.2.7 Пипетки градуированные 1-2-1, 1-2-2, 1-2-5, 1-2-1 и 1-2-25 2-го класса точности по ГОСТ 29227.
5.2.8 Колбы мерные вместимостью 25, 100 см с одной отметкой по ГОСТ 1770.
5.2.9 Емкости для жидких проб (виалы) вместимостью 2-6 см.
5.2.10 Центрифуга лабораторная с фактором разделения (g-фактор) 800-1000.
5.2.11 Посуда лабораторная стеклянная по ГОСТ 25336:
воронки лабораторные,
стаканы вместимостью 50, 100 и 1000 см.
5.2.12 Вода дистиллированная по ГОСТ 6709.
5.2.13 Спирт этиловый ректификованный по ГОСТ Р 51652.
5.2.14 Ацетонитрил для ВЭЖХ по [1].
5.2.15 Кислота ортофосфорная по ГОСТ 6552.
Допускается применение других средств измерений, вспомогательного оборудования, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающим необходимую точность измерения, а также реактивов и материалов по качеству не хуже вышеуказанных.
5.3 Подготовка к проведению определения
5.3.1 Подготовка проб для хроматографического определения
Для качественного определения антоцианинов в концентрированных соках и пюре взвешивают 1 г пробы с записью результата до третьего знака после запятой и пробу разбавляют в 5 см дистиллированной воды (пюре и соковую продукцию с высоким содержанием растворимых сухих веществ разбавляют дистиллированной водой в соотношении от 1:2 до 1:5). Подготовленную пробу для удаления мутной взвеси центрифугируют и фильтруют через мембранный фильтр с диаметром пор 0,2 мкм.
Для качественного определения антоцианинов в другой соковой продукции, а также в соках прямого отжима 1 г пробы без предварительного разбавления центрифугируют и фильтруют через мембранный фильтр с диаметром пор 0,45 мкм.
При суммарном содержании антоцианинов в соке менее 0,1% пробу фильтруют через мембранный фильтр, не разбавляя.
5.3.2 Приготовление подвижной фазы для жидкостной хроматографии
Готовят раствор ортофосфорной кислоты с рН=2,1. Для этого в дистиллированную воду по каплям добавляют концентрированную ортофосфорную кислоту (см. 5.2.15), рН контролируют с помощью рН-метра. Полученный раствор ортофосфорной кислоты смешивают с ацетонитрилом в соотношении 88:12 в процентах по объему. Подвижную фазу фильтруют под вакуумом через мембранный фильтр с диаметром пор 0,45 мкм.
Срок хранения подвижной фазы - одна неделя при хранении в плотно укупоренной посуде.
5.3.3 Выполнение измерений
Условия хроматографического анализа:
колонка аналитическая длиной 250 мм и внутренним диаметром 4,6 мм, заполненная октадецилсиликагелем размером частиц 5 мкм;
температура колонки: 35 °С;
детектирование: фотометрический детектор с длиной волны 518 нм;
скорость подачи элюента: 1,0 см/мин;
объем вводимой пробы: 10-20 мкл.
Градиентное элюирование:
ортофосфорная кислота с рН=2,1 (см. 5.3.2) в соотношении с ацетонитрилом (см. 5.2.14) в соответствии с таблицей 1.
Таблица 1 - Состав подвижной фазы
Длительность, мин | Ортофосфорная кислота, % по объему | Ацетонитрил, % по объему | Тип градиента |
0 | 88 | 12 | Линейный |
20 | 75 | 25 | Линейный |
30 | 60 | 40 | Линейный |
Хроматографическая система (обращенно-фазовая колонка в качестве неподвижной фазы и градиент водного раствора ортофосфорной кислоты и ацетонитрила) должна обеспечивать разделение основных пиков антоцианинов, приведенных в таблице Б.1 приложения Б.
Примечание - Пример разделения пиков антоцианинов сока черной смородины приведен на рисунке Б.1 приложения Б. Хроматографическая система должна обеспечивать разделение на четыре основных пика для сока черной смородины, причем пики 2 и 3 должны разделяться полностью (до нулевой линии).
5.4 Обработка и оформление результатов
Идентификацию пиков проводят путем сравнения с хроматограммами соковой продукции из фруктов с известным составом пигментов антоцианина и с таблицей Б.2 приложения Б.
Содержание индивидуальных пигментов, выраженное в относительных единицах - процентах, определяют как отношение площади хроматографического пика к сумме площадей всех идентифицированных пиков антоцианинов.
Систематизированные данные, характеризующие порядок выхода наиболее распространенных антоцианинов в соковой продукции из фруктов и их примерный состав, приведены в таблице Б.2 приложения Б.
6 Метод рН-дифференциальной спектрофотометрии
6.1 Сущность метода рН-дифференциальной спектрофотометрии
Метод основан на применении рН-дифференциальной спектрофотометрии. Суммарную массовую концентрацию (массовую долю) антоцианинов в соковой продукции определяют на основе изменения поглощения света с длиной волны 510 нм при изменении кислотности растворов соковой продукции с рН от 1 до 4,4.
6.2 Средства измерений, вспомогательные устройства, материалы, реактивы
6.2.1 Спектрофотометр СФ-26, СФ-46 или подобный, позволяющий проводить измерения при длинах волн от 200 до 900 нм, допустимая абсолютная погрешность измерения коэффициента пропускания - не более 1%.
6.2.2 Кюветы кварцевые для спектрофотометрии с длиной оптического пути 10 мм.
6.2.3 Установка ультразвуковая с частотой ультразвука 43-45 кГц.
6.2.4 Аппарат для встряхивания проб по [2].
6.2.5 Весы лабораторные по ГОСТ 24104 с пределами абсолютной погрешности однократного взвешивания ±0,1 мг.
6.2.6 Весы лабораторные по ГОСТ 24104 с пределами абсолютной погрешности однократного взвешивания ±0,5 мг.
6.2.7 рН-метр с диапазоном измерений рН от 2 до 18; погрешность измерений ±0,01 ед. рН;
6.2.8 Фильтры мембранные с диаметром пор 0,45 мкм.
6.2.9 Центрифуга лабораторная с фактором разделения (g-фактор) 800-1000.
6.2.10 Колбы мерные наливные 2-50-2, 2-100-2, 2-250-2 по ГОСТ 1770.
6.2.11 Пипетки 4-1-2 или 5-1-2, 4-2-10 или 5-2-10, 4-2-25 или 5-2-25 по ГОСТ 29227.
6.2.12 Вода дистиллированная по ГОСТ 6709.
6.2.13 Цианидин-3-О-глюкозид, содержание основного вещества не менее 95%.
6.2.14 Спирт этиловый ректификованный по ГОСТ Р 51652.
6.2.15 Ацетонитрил для ВЭЖХ по [1].
6.2.16 Натрий уксуснокислый по ГОСТ 199, ч.д.а.
6.2.17 Калий хлористый по ГОСТ 4234, ч.д.а.
6.2.18 Кислота соляная по ГОСТ 3118.
Допускается применение других средств измерений, вспомогательного оборудования, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающим необходимую точность измерения, а также реактивов и материалов по качеству не хуже вышеуказанных.
6.3 Проведение измерений
6.3.1 Условия проведения измерений
Измерения проводят в следующих лабораторных условиях:
температура окружающего воздуха | (25±5) °С; |
атмосферное давление | (97±10) кПа; |
относительная влажность | (65±15)%; |
частота переменного тока | (50±5) Гц; |
напряжение в сети | (220±10) В. |
6.3.2 Подготовка к проведению определения методом рН-дифференциальной спектрофотометрии
6.3.2.1 Подготовка буферных растворов
а) Подготовка буферного раствора c рН=1,0
Для приготовления буферного раствора c рН=1,0 помещают 1,49 г хлористого калия KCl в мерную колбу вместимостью 100 см, доводят до метки дистиллированной водой и тщательно перемешивают.
Для приготовления раствора соляной кислоты молярной концентрации (HCl)=0,2 моль/дм
в мерную колбу вместимостью 100 см
помещают 75 см
дистиллированной воды, осторожно приливают 1,7 см
концентрированной соляной кислоты HCl, доводят до метки дистиллированной водой и тщательно перемешивают.
Затем в стакане вместимостью 100 см смешивают 25 см
полученного раствора KCl с 67 см
раствора HCl молярной концентрации 0,2 моль/дм
. При необходимости значение рН полученного буферного раствора доводят до 1,0 концентрированной соляной кислотой.
б) Подготовка буферного раствора c рН=4,5
Для приготовления буферного раствора c рН=4,5 растворяют 1,64 г уксуснокислого натрия, помещают в мерную колбу вместимостью 100 см, доводят до метки дистиллированной водой и тщательно перемешивают. Доводят значение рН раствора до 4,5 концентрированной соляной кислотой.
Срок хранения буферных растворов - не более 3 мес.
6.3.2.2 Подготовка проб для анализа
а) Определение массовой концентрации суммы антоцианинов в соковой продукции, не содержащей нерастворимые в воде вещества, проводят следующим образом. В две мерные колбы вместимостью 25 см каждая помещают по 1 см
пробы и доводят до метки буферными растворами c pH 1,0 и 4,5, приготовленными в соответствии с 6.3.2.1. Растворы перемешивают, выдерживают в течение 15 мин и проводят измерение оптической плотности при длинах волн 510 и 700 нм. Измерение оптической плотности при 700 нм проводят для установления величины поглощения света посторонними примесями в анализируемой соковой продукции.
б) Определение массовой концентрации суммы антоцианинов в соковой продукции, содержащей нерастворимые в воде вещества, проводят следующим образом. 15 см пробы предварительно гомогенизируют, а затем центрифугируют по 6.2.9 с фактором разделения не менее 990 g в течение 20 мин.
Получают осветленную пробу. После этого в две мерные колбы, вместимостью 25 см каждая, помещают по 1 см
осветленной пробы и доводят до метки буферными растворами с pH 1,0 и 4,5, приготовленными в соответствии с 6.3.2.1. Растворы перемешивают, выдерживают в течение 15 мин и проводят измерение оптической плотности при длинах волн 510 и 700 нм. Измерение оптической плотности при 700 нм проводят для установления величины поглощения света посторонними примесями в анализируемой соковой продукции.
в) Определение массовой доли суммы антоцианинов в концентрированных соках проводят после предварительного разбавления пробы дистиллированной водой весовым методом в соотношении 1:5.
Для этого на лабораторных весах по ГОСТ 24104 в колбе вместимостью 25 см взвешивают 5 г концентрированного сока с записью результата до третьего знака после запятой, прибавляют дистиллированную воду до метки и тщательно перемешивают. Затем в две мерные колбы вместимостью по 25 см
(
) отбирают по 1 см
приготовленного раствора и доводят их до метки буферными растворами c pH 1,0 и 4,5, приготовленными по 6.3.2.1 (соотношение двух взятых объемов 25 см
и 1 см
составляет величину разведения (
), используемую при расчете массовой доли антоцианинов по формуле 4).
Растворы перемешивают и выдерживают в течение 15 мин до начала измерений и проводят измерение оптической плотности при длинах волн 510 и 700 нм.
г) Подготовку проб по 6.3.2.2 а) и б) проводят с целью определения массовой концентрации суммы антоцианинов, а по 6.3.2.2 в) - с целью определения их массовой доли.
6.3.2.3 Значения оптической плотности должны находиться в пределах 0,2-1,0.
Для проб соковой продукции, приготовленных по 6.3.2.2 в), имеющих значения оптической плотности раствора более 1,0, повышают величину разведения (). Для проб соковой продукции, приготовленных по 6.3.2.2 б), увеличивают объем буферных растворов.
Для проб соковой продукции, приготовленных по 6.3.2.2 в), имеющих значения оптической плотности раствора менее 0,2, уменьшают величину разведения (). Для проб соковой продукции, приготовленных по 6.3.2.2 б), имеющих значения оптической плотности раствора менее 0,2, увеличивают объем анализируемой пробы.
6.3.3 Выполнение спектрофотометрических измерений
Измерения оптической плотности подготовленных проб проводят на спектрофотометре при длинах волн 510 и 700 нм. Измеряемой величиной является разность в оптической плотности растворов с рН 1,0 и 4,5 при длинах волн 510 и 700 нм, которая пропорциональна массовой концентрации (массовой доле) антоцианинов в исследуемом растворе. Пробы анализируют два раза в условиях повторяемости в соответствии с требованиями ГОСТ Р ИСО 5725-1 (подраздел 3.14) и ГОСТ Р ИСО 5725-2.
6.4 Обработка результатов спектрофотометрических измерений
6.4.1 Вычисления массовой концентрации суммы антоцианинов проводят до третьего десятичного знака в следующем порядке.
Оптическую плотность суммы антоцианинов рассчитывают как разность оптических плотностей растворов при разных длинах волн и значениях pH по формуле
![]() . (1)
. (1)
Массовую концентрацию суммы антоцианинов , мг/дм
, рассчитывают в пересчете на цианидин-3-глюкозид по формуле
![]() , (2)
, (2)
где - измеренная оптическая плотность суммы антоцианинов;
![]() - молекулярная масса цианидин-3-глюкозида, равная 449,2 г/моль;
- молекулярная масса цианидин-3-глюкозида, равная 449,2 г/моль;
- вместимость мерной колбы, взятой для разбавления, см
;
- объем пробы, отобранный для анализа, см
;
- молярный коэффициент экстинкции цианидин-3-глюкозида, равный 26900 [моль·см/дм
]
;
- длина оптического пути кюветы, равная 1 см.
6.4.2 Вычисления массовой доли суммы антоцианинов проводят до третьего десятичного знака в следующем порядке.
Оптическую плотность суммы антоцианинов рассчитывают как разность оптических плотностей растворов при разных длинах волн и значениях pH по формуле
![]() . (3)
. (3)
Массовую долю суммы антоцианинов , млн
, в пересчете на цианидин-3-глюкозид рассчитывают по формуле
![]() , (4)
, (4)
где - измеренная оптическая плотность суммы антоцианинов;
![]() - молекулярная масса цианидин-3-глюкозида, равная 449,2 г/моль;
- молекулярная масса цианидин-3-глюкозида, равная 449,2 г/моль;
- величина разведения по 6.3.2.2 в);
- объем буферного раствора, см
, по 6.3.2.2 в);
- молярный коэффициент экстинкции цианидин-3-глюкозида, равный 26900 [моль·см/дм
]
;
- длина оптического пути кюветы, равная 1 см;
![]() - масса анализируемой пробы, г.
- масса анализируемой пробы, г.
Расхождение между двумя параллельными определениями (в процентах от среднего значения), выполненными в условиях повторяемости, не должно превышать предела повторяемости (сходимости) , приведенного в таблице 2 при вероятности
0,95.
При соблюдении этого условия за окончательный результат определения принимают среднеарифметическое значение результатов двух параллельных определений , округленное до второго десятичного знака.
Границы относительной погрешности определения массовой концентрации (массовой доли) суммы антоцианинов , %, при соблюдении условий, регламентированных настоящим методом, при вероятности
0,95 не должны превышать значений, приведенных в таблице 2.
Таблица 2 - Основные метрологические характеристики метода определения массовой концентрации или массовой доли суммы антоцианинов
Метрологическая характеристика ( | Значение показателя при диапазонах измерений массовой концентрации (массовой доли), мг/дм | ||
От 5 до 100 включ.* | Св. 100 до1000 включ.** | Св. 1000 до 5000 включ.*** | |
Предел повторяемости (сходимости) | 14 | 9 | 8 |
Предел воспроизводимости | 19 | 14 | 10 |
Граница относительной погрешности | 14 | 10 | 7 |
Предел обнаружения метода, мг/дм | 1,0 | ||
* Исследования проводились на образцах клубники, выращенной в средней полосе Российской Федерации. ** Исследования проводились на образцах клюквы, выращенной в Российской Федерации. *** Исследования проводились на образцах черной смородины, выращенной в средней полосе Российской Федерации. | |||
Если массовая концентрация (массовая доля) суммы антоцианинов превышает 5000 мг/дм(млн
), то определение массовой концентрации (массовой доли) суммы антоцианинов проводят после разбавления пробы.
В заключение результат массовой концентрации (массовой доли) суммы антоцианинов представляют в следующем виде:
![]() , (5)
, (5)
где - среднее значение результатов двух параллельных определений, мг/дм
(млн
);
- границы абсолютной погрешности определений, мг/дм
(млн
), рассчитанные по формуле
![]() , (6)
, (6)
где - значение относительной погрешности метода приведено в таблице 2, %.
6.5 Контроль точности результатов определения
6.5.1 Оперативный контроль повторяемости результатов определения
Оперативный контроль повторяемости результатов определения массовой концентрации (массовой доли) антоцианинов проводят при получении каждого результата определения путем сравнения расхождения между результатами двух параллельных определений (в процентах от среднего значения) с пределом повторяемости (сходимости), приведенным в таблице 2.
Повторяемость результатов признают удовлетворительной при условии
. ![]() . (7)
. (7)
При превышении предела повторяемости (сходимости) определение повторяют. При повторном превышении указанного предела выясняют причины, приводящие к неудовлетворительным результатам, их устраняют и определение повторяют.
6.5.2 Оперативный контроль воспроизводимости результатов определения
Абсолютное расхождение между результатами двух независимых определений, которые получены в условиях воспроизводимости (одна и та же методика, идентичный объект определения, разные лаборатории, разные операторы, различное оборудование), не должно превышать предела воспроизводимости, приведенного в таблице 2. При превышении указанного предела воспроизводимости контрольное определение повторяют. При повторном превышении указанного предела воспроизводимости выясняют причины, приводящие к неудовлетворительным результатам, и устраняют их.
6.5.3 Оперативный контроль погрешности (точности) результатов определения
Для проведения оперативного контроля погрешности определение проводят в пробах, объем или масса которых должна соответствовать удвоенному их количеству, необходимому для проведения определения. Пробу делят на две равные части. В одну из них добавляют стандартный раствор цианидин-3-глюкозида в таких количествах, чтобы добавка составляла 50%-150% исходного содержания компонента в пробе, но не превышала верхней границы диапазона определения массовой концентрации или массовой доли компонента с учетом границ погрешности определения (см. таблицу 2). В обеих частях пробы проводят определение в соответствии с требованиями настоящего стандарта.
Результаты контрольных определений признают удовлетворительными, если погрешность определения массовой концентрации (массовой доли) цианидина-3-глюкозида в добавке не превышает норматива оперативного контроля погрешности (точности), то есть выполняется условие
![]() , (8)
, (8)
где - среднее значение двух определений массовой концентрации (массовой доли) цианидина-3-глюкозида в пробе с добавкой, мг/дм
(млн
);
- среднее значение двух определений массовой концентрации (массовой доли) цианидина-3-глюкозида в пробе без внесения добавки, мг/дм
(млн
);
- значение добавки цианидина-3-глюкозида, мг/дм
(млн
);
- норматив оперативного контроля погрешности, мг/дм
(млн
).
При проведении внутрилабораторного контроля (0,90) значение
рассчитывают по формуле
![]() . (9)
. (9)
При проведении внешнего контроля (0,95) значение
рассчитывают по формуле
![]() , (10)
, (10)
где - границы относительной погрешности определения массовой концентрации (массовой доли) цианидина-3-глюкозида, указанные в таблице 2.
При превышении норматива оперативного контроля погрешности проводят повторные контрольные определения. При повторном превышении указанного норматива выясняют причины, приводящие к неудовлетворительным результатам, и устраняют их.
Периодичность контроля погрешности (точности) устанавливается самой лабораторией с учетом фактического состояния работ. При замене оборудования, колонок, реактивов или при построении новой градуировочной зависимости проведение оперативного контроля погрешности обязательно.
7 Требования безопасности
7.1 Условия безопасного проведения работ
При работе с химическими реактивами следует соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005 и ГОСТ 12.1.007. При подготовке проб к анализу и выполнении измерений с использованием жидкостного хроматографа соблюдают правила пожаровзрывобезопасности по ГОСТ 12.1.018, по электробезопасности - по ГОСТ 12.1.019, и инструкции по эксплуатации прибора.
7.2 Требования к квалификации оператора
К выполнению измерений, обработке и оформлению результатов допускаются инженер-химик, техник или лаборант, имеющие высшее или среднее специальное образование, опыт работы в химической лаборатории и изучившие инструкцию по эксплуатации метода высокоэффективной жидкостной хроматографии. Первое применение метода высокоэффективной жидкостной хроматографии в лаборатории следует проводить под руководством специалиста, владеющего теорией метода высокоэффективной жидкостной хроматографии и имеющего практические навыки в этой области.
Приложение А
(справочное)
Структура основных антоцианидинов, входящих в состав природных антоцианинов
А.1 Общая структура антоцианидинов приведена на рисунке А.1.
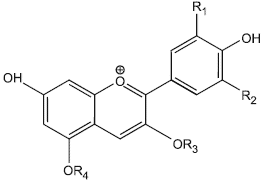
Рисунок А.1 - Общая структура антоцианидинов
Примечание - Конкретный вид антоцианидина зависит от состава радикалов R, R
, приведенных в таблице А.1.
Таблица А.1 - Виды антоцианидинов в зависимости от состава радикалов
Вид антоцианидина | Состав радикалов | Сокращенное наименование | |
R | R | ||
Пеларгонидин | Н | Н | Pgd |
Цианидин | ОН | Н | Cyd |
Пеонидин | ОСН | Н | Pnd |
Дельфинидин | ОН | ОН | Dpd |
Петунидин | ОСН | ОН | Ptd |
Мальвидин | ОСН | ОСН | Mvd |
Примечание - R | |||
Приложение Б
(справочное)
Систематизированные литературные и экспериментальные данные по порядку выхода наиболее распространенных антоцианинов фруктов и их примерному составу
Б.1 Порядок элюирования индивидуальных антоцианинов, их сокращенное и полное наименования приведены в таблице Б.1.
Таблица Б.1 - Порядок элюирования индивидуальных антоцианинов, их сокращенное и полное наименования
N | Наименование антоцианинов | |
сокращенное | полное | |
1 | Dpd-3,5-diglu | Дельфинидин-3,5-диглюкозид |
2 | Cyd-3,5-diglu | Цианидин-3,5-диглюкозид |
3 | Dpd-3-samb | Дельфинидин-3-самбубиозид |
4 | Dpd-3-gal | Дельфинидин-3-галактозид |
5 | Dpd-3-glu | Дельфинидин-3-глюкозид |
6 | Cyd-3-sop | Цианидин-3-софорозид |
7 | Cyd-3-glu-rut | Цианидин-3-гликорутинозид |
8 | Dpd-3-rut | Дельфинидин-3-рутинозид |
9 | Cyd-3-gal | Цианидин-3-галактозид |
10 | Dpd-3-ara | Дельфинидин-3-арабинозид |
11 | Cyd-3-samb | Цианидин-3-самбубиозид |
12 | Cyd-3-glu | Цианидин-3-глюкозид |
13 | Cyd-3-xyl-rut | Цианидин-3-ксилозорутинозид |
14 | Cyd-3-rut | Цианидин-3-рутинозид |
15 | Ptd-3-gal | Петунидин-3-галактозид |
16 | Cyd-3-ara | Цианидин-3-арабинозид |
17 | Ptd-3-glu | Петунидин-3-глюкозид |
18 | Pgd-3-glu | Пеларгонидин-3-глюкозид |
19 | Pnd-3-gal | Пеонидин-3-галактозид |
20 | Pgd-3-ara | Пеларгонидин-3-арабинозид |
21 | Pnd-3-glu | Пеонидин-3-глюкозид |
22 | Mvd-3-glu | Мальвидин-3-глюкозид |
23 | Pnd-3-ara | Пеонидин-3-арабинозид |
Пример хроматограммы сока черной смородины приведен на рисунке Б.1.
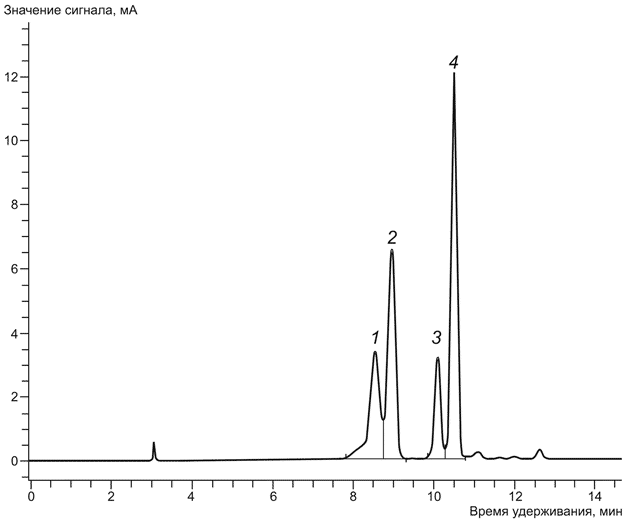
1 - Dpd-3-glu (дельфинидин-3-глюкозид); 2 - Dpd-3-rut (дельфинидин-3-рутинозид); 3 - Cyd-3-glu (цианидин-3-глюкозид); 4 - Cyd-3-rut (цианидин-3-рутинозид)
Рисунок Б.1 - Пример хроматограммы сока черной смородины (происхождение - Россия, 2007 год, исследования НИИ питания РАМН)
Примечание - Хроматографическая система должна обеспечивать разделение четырех основных пиков, причем пики 2 и 3 должны разделяться полностью (до нулевой линии).
Б.2 Примерный состав основных антоцианинов фруктов приведен в таблице Б.2.
Таблица Б.2 - Примерный состав основных антоцианинов фруктов
Наименование фрукта | Относительное содержание антоцианинов, % | ||||||||||||||||||||||
Dpd-3,5-diglu | Cyd-3,5-diglu | Dpd-3-gal | Cyd-3-samb | Dpd-3-glu | Cyd-3-sop | Cyd-3-glu-rut | Dpd-3-rut | Cyd-3-gal | Dpd-3-ara | Cyd-3-samb | Cyd-3-glu | Cyd-3-xyl-rut | Cyd-3-rut | Ptd-3-gal | Cyd-3-ara | Ptd-3-glu | Pgd-3-glu | Pnd-3-gal | Pgd-3-ara | Pnd-3-glu | Mvd-3-glu | Pnd-3-ara | |
Гранат | 0-15 | 0-15 | - | - | 15-45 | - | - | - | - | - | - | 15-45 | - | - | - | - | - | - | - | - | - | - | - |
Гибискус | - | - | - | - | - | - | - | - | - | - | Более 45 | - | - | - | - | - | - | - | - | - | - | - | - |
Черника | - | - | 0-15 | - | 0-15 | - | - | - | 0-15 | 0-15 | - | 15-45 | - | - | 0-15 | 0-15 | 0-15 | - | - | - | 0-15 | 0-15 | - |
Красный виноград | - | - | - | - | 15-45 | - | - | - | - | - | - | 0-15 | - | - | - | - | 15-45 | - | - | - | 0-15 | Более 45 | - |
Черная смородина | - | - | - | - | 15-45 | - | - | 15-45 | - | - | - | 0-15 | - | 15- 45 | - | - | - | - | - | - | - | - | - |
Красная смородина | - | - | - | - | - | 0-15 | 0-15 | - | - | - | - | 0-15 | Более 45 | 0-15 | - | - | - | - | - | - | - | - | - |
Слива | - | - | - | - | - | - | - | - | - | - | - | Более 45 | - | Более 45 | - | - | - | - | - | - | - | - | - |
Клюква | - | - | - | - | - | - | - | - | 15-45 | - | - | 0-15 | - | - | - | 15-45 | - | - | 15-45 | - | 0-15 | - | 15-45 |
Клубника | - | - | - | - | - | - | - | - | - | - | - | 0-15 | - | - | - | - | - | Более 45 | - | 0-15 | - | - | - |
Черешня | - | - | - | - | - | 15-45 | - | - | - | - | - | Более 45 | - | 15-45 | - | - | - | - | - | - | - | - | - |
Вишня | - | - | - | - | - | 0-15 | Более 45 | - | - | - | - | 0-15 | - | 15- 45 | - | - | - | - | - | - | - | - | - |
Малина | - | - | - | - | - | 15-45 | 0-15 | - | - | - | - | 15-45 | - | 0-15 | - | - | - | - | - | - | - | - | - |
Ежевика | - | - | - | - | - | - | - | - | - | - | - | Более 45 | - | - | - | - | - | - | - | - | 0-15 | - | - |
Брусника | - | - | - | - | - | - | - | - | Более 45 | - | - | 0-15 | - | - | - | 0- 15 | - | - | - | - | - | - | - |
Бузина | - | - | - | - | - | - | - | - | - | - | Более 45 | - | - | - | - | - | - | - | - | - | - | - | - |
Черноплод- | - | - | - | - | - | - | - | - | Более 45 | - | - | 0-15 | - | - | - | 15- 45 | - | - | - | - | 0-15 | - | - |
Крыжовник черный | - | - | - | - | - | - | - | 0-15 | - | - | - | 0-15 | - | Более 45 | - | - | - | - | - | - | - | - | - |
Калина | - | - | - | - | - | - | - | - | Более 45 | 0-15 | - | - | - | - | - | - | - | - | - | - | - | - | - |
Ирга | - | - | - | - | - | - | - | - | Более 45 | - | - | 15- 45 | - | - | - | - | 0-15 | - | - | - | - | - | - |
Библиография
[1] ТУ 6-09-3534-74* Ацетонитрил для ВЭЖХ
[2] ТУ 64-1-2451-78* Аппарат для встряхивания проб
________________
* Документ в информационных продуктах не содержится. За информацией о документе Вы можете обратиться в Службу поддержки пользователей. - .
Электронный текст документа
и сверен по:
, 2010

