ГОСТ 31982-2012
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ, КОРМА, ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕ
Метод определения содержания бета-адреностимуляторов с помощью газовой хроматографии с масс-спектрометрическим детектором
Food products, feeds, food raw materials. Method of determination of -agonists by Gas chromatography. Mass spectrometry
МКС 65.120
67.050
67.120
Дата введения 2014-07-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным бюджетным учреждением "Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов" (ФГБУ "ВГНКИ"), Федеральным государственным бюджетным учреждением "Центральная научно-методическая ветеринарная лаборатория" (ФГБУ "ЦНМВЛ")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 3 декабря 2012 г. N 54-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
Таджикистан | TJ | Таджикстандарт |
Узбекистан | UZ | Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 27 июня 2013 г. N 241-ст введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2014 г.
5 Стандарт подготовлен на основе ГОСТ Р 54032-2010
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
ВНЕСЕНА поправка, опубликованная в ИУС N 2, 2020 год
Поправка внесена изготовителем базы данных
1 Область применения
1 Область применения
Настоящий стандарт распространяется на продукты пищевые в части мяса и мясных продуктов, включая мясо и продукты из мяса птицы, комбикорма и продовольственное сырье и устанавливает метод газовой хроматографии с масс-спектрометрическим детектором (далее по тексту - ГХ-МС) для идентификации и количественного определения бета-адреностимуляторов.
Диапазон измерений от 0,1 до 100,0 мкг/кг.
Примечание - Метод может быть использован для определения содержания бета-адреностимуляторов в физиологических жидкостях, шерсти и органах животных.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.018-93 Система стандартов безопасности труда. Пожаровзрывобезопасность статического электричества. Общие требования
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 12.2.085-2002 Сосуды, работающие под давлением. Клапаны предохранительные. Требования безопасности
ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
ГОСТ 9293-74 Азот газообразный и жидкий. Технические условия
ГОСТ 9805-84 Спирт изопропиловый. Технические условия
ГОСТ 13496.0-80 Комбикорма, сырье. Методы отбора проб
ГОСТ 13867-68 Продукты химические. Обозначение чистоты
ГОСТ 22300-76 Реактивы. Эфиры этиловый и бутиловый уксусной кислоты. Технические условия
ГОСТ 24104-2001 Весы лабораторные. Общие технические требования
ГОСТ 24147-80 Аммиак водный особой чистоты. Технические условия
ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Сущность метода
Идентификацию и количественное определение бета-адреностимуляторов методом ГХ-МС проводят с использованием стандартных образцов бета-адреностимуляторов.
Количественное определение бета-адреностимуляторов проводят методом внутреннего стандарта по площади пика идентифицированных соединений относительно градуировочной зависимости, полученной при анализе градуировочных растворов известных соединений в аналогичных условиях.
4 Условия выполнения измерений
При определении содержания бета-адреностимуляторов в лаборатории должны быть соблюдены следующие условия:
- температура окружающего воздуха | от 10 °С до 30 °С; |
- атмосферное давление | от 84 до 106 кПа; |
- напряжение в электросети | (220±20) В; |
- частота тока в электросети | от 49 до 51 Гц; |
- относительная влажность воздуха | от 30% до 80%. |
Хроматографические измерения проводят в условиях, указанных инструкцией по эксплуатации соответствующего прибора.
5 Средства измерений, вспомогательное оборудование, посуда, реактивы и материалы
5.1 Для определения содержания бета-адреностимуляторов применяют следующие средства измерений, вспомогательное оборудование и материалы:
- хромато-масс-спектрометр, позволяющий проводить измерения в диапазоне от 45 до 650 атомных единиц массы (а.е.м.), с разрешением по шкале масс не более 1,0 а.е.м. и чувствительностью в режиме ионизации электронным ударом: при инжекции в колонку 2 пг гексахлорбензола (сканирование в диапазоне от 45 до 350 а.е.м. за 1 с) отношение сигнал/шум на молекулярном ионе с m/z 284 не менее 10/1;
- колонку кварцевую капиллярную 30 м0,25 мм
0,25 мкм с индексом полярности неподвижной жидкой фазы от пяти до 30;
- компьютер с установленным программным обеспечением для управления хромато-масс-спектрометром и обработки результатов измерений;
- автосамплер для газового хроматографа;
- пипетки одноканальные переменного объема 10-100 мм, 40-200 мм
, 200-1000 мм
, 1-5 см
с допустимой относительной погрешностью дозирования по метанолу не более 2% (Transferpettor Brand, Германия)*;
- весы класса точности I и класса точности II с дискретностью от счета 0,01 мг, поверочным делением
 по ГОСТ 24104;
по ГОСТ 24104;
- модуль термостатируемый нагревательный с системой отдувки растворителей инертным газом и максимальной температурой термостатирования 250 °С;
- измельчитель-гомогенизатор лабораторный;
- гомогенизатор лабораторный конфигурации ротор-статор;
- испаритель ротационный со скоростью вращения от 20 до 280 об/мин и температурным диапазоном нагревательной бани от 30 °С до 100 °С;
- центрифугу лабораторную рефрижераторную со скоростью вращения ротора не менее 3500 об/с и диапазоном рабочих температур от минус 10 °С до 25 °С, с адаптерами для пробирок вместимостью 15, 50 см и микроцентрифужных пробирок вместимостью 1,5 см
;
- картридж для твердофазной экстракции объемом не менее 6 см, заполненный обращенно-фазным сорбентом С 18 с размером диаметра частиц не более 50 мкм;
- устройство вакуумное для твердофазной экстракции;
- флаконы стеклянные вместимостью 4 см с завинчивающимися крышками и тефлоновыми прокладками;
- флаконы стеклянные вместимостью 40 см с завинчивающимися крышками и тефлоновыми прокладками;
- флаконы стеклянные вместимостью 2 см с завинчивающимися
, тефлоновыми прокладками и вставками объемом 100 мм
;
_______________
Текст документа соответствует оригиналу. - .
- колбы мерные стеклянные 2-10-2, 2-100-2, 2-1000-2 по ГОСТ 1770;
- колбы стеклянные П-2-100-32 ТС по ГОСТ 25336;
- баню ультразвуковую с рабочей частотой не менее 20 кГц и объемом не менее 1 дм;
- шейкер вортексного типа движения, с амплитудой встряхивания 5 мм;
- шейкер орбитального типа движения с максимальной частотой вращения 1000 об/мин;
- рН-метр с набором электродов с пределами абсолютной погрешности измерений ±0,01 ед. рН;
- фильтры мембранные с размером диаметра пор не более 0,45 мкм;
- шкаф сушильный лабораторный с автоматическим регулированием температуры в рабочем пространстве от 25 °С до 300 °С.
_______________
* Указанные материалы являются рекомендуемыми к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
5.2 При выполнении измерений применяют следующие реактивы и материалы:
- гелий газообразный (сжатый) высокой чистоты, марка 6.0;
- азот газообразный особой чистоты по ГОСТ 9293;
- фермент протеолитический Subtilisine A (Sigma, Германия, N Р-5380)*;
- кислоту уксусную по ГОСТ 61, х.ч.;
- кислоту соляную по ГОСТ 3118, х.ч.;
- кислоту хлорную 65%-ную, х.ч.;
- кальций хлористый двухводный, х.ч.;
- аммиак водный по ГОСТ 24147,о.с.ч.;
- кислоту метилборную, х.ч.;
- N-метил-N-триметилсилил-трифторацетамид (МСТФА) (Sigma, Германия, N М-7891)*;
- триметилйодсилан (ТМИС) (Aldrich, Германия, N 19,552-9)*;
- дитиоэритритол (ДТЭ), х.ч.;
- N,N-бис-триметилсилилтрифторацетамид (БСТФА) (Sigma, Германия, N Т-5634)*;
- триметилхлорсилан (ТМХС) (Sigma, Германия, N Т-4252)*;
- эфир метил-трет-бутиловый для хроматографии;
- н-Гексан х.ч.;
- калия гидроокись по ГОСТ 24363, х.ч.;
- натрия гидроокись по ГОСТ 4328, х.ч.;
- метанол-яд по ГОСТ 6995;
- этанол абсолютный, х.ч.;
- сок пищеварительный Helix pomatia (Merck, Германия, N 1.04114)*;
- воду деионизованную;
- спирт изопропиловый по ГОСТ 9805, о.с.ч.;
- эфир этиловый уксусной кислоты по ГОСТ 22300, х.ч.;
- сорбент Bondesil С18 40 мкм (Varian, США, N 12213012)*;
- твин 20 (Sigma, Германия, N Р-2287)*;
- натрий хлористый по ГОСТ 4233, х.ч.;
- калий фосфорнокислый однозамещенный по ГОСТ 4198;
- натрий уксуснокислый, х.ч.;
- трис(гидроксиметил)-аминометан, х.ч.
Все реактивы должны относиться к подгруппе чистоты 2 х.ч. или 3 ч.д.а по ГОСТ 13867.
_______________
* Указанные материалы являются рекомендуемыми к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
5.3 Для определения содержания бета-адреностимуляторов применяют следующие стандартные образцы:
- цимбутерол - d9 массовой долей основного вещества не менее 98,0% (RIKILT*, Wageningen UR)**;
- цимбутерол массовой долей основного вещества не менее 98,0% (RIKILT, Wageningen UR)**;
- кленбутерол - d6 массовой долей основного вещества не менее 98,0% (RIKILT, Wageningen UR)**;
- кленбутерол массовой долей основного вещества не менее 99,0% (Boehringer, Ingelheim)**;
- сальбутамол - d6 массовой долей основного вещества не менее 98,0% (RIKILT, Wageningen UR)**;
- сальбутамол массовой долей основного вещества не менее 98,0% (SIGMA, Deisenhofen)**;
- мапентерол массовой долей основного вещества не менее 99,0% (RIKILT, Wageningen UR)**;
- мапентерол - d11 массовой долей основного вещества не менее 98,0% (RIKILT, Wageningen UR)**;
- тербуталин массовой долей основного вещества не менее 99,0% (SIGMA, Deisenhofen)**;
- тербуталин - d9 массовой долей основного вещества не менее 98,0% (RIKILT, Wageningen UR)**;
- стандартные образцы с аттестованной массовой долей кленбутерола и сальбутамола:
1) лиофилизованная моча (IRMM***, BCR-504)**;
2) лиофилизованная печень, чистый образец (IRMM, BCR-648)**;
3) лиофилизованная печень (IRMM, BCR-649)**.
Допускается применение других средств измерений, вспомогательного оборудования, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающим необходимую точность измерения, а также реактивов и материалов по качеству не хуже вышеуказанных.
_______________
* Институт пищевой безопасности, расположенный в Нидерландах.
** Указанные стандартные образцы являются рекомендуемыми к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
*** Институт референтных материалов и измерений, расположенный в Бельгии.
6 Подготовка к проведению измерений
6.1 Приготовление растворов
6.1.1 Приготовление трис-буфера молярной концентрации 0,2 моль/дм
и рН 8,0
В мерную колбу вместимостью 1000 см вносят 24,2 г трис(гидроксиметил)-аминометана и 14,7 г кальция хлористого двухводного, растворяют в 800 см
деионизованной воды, измеряют рН, доводят значение рН до (8,0±0,1) соляной кислотой молярной концентрации
1 моль/дм
(6.1.13) и доводят объем раствора до метки деионизованной водой.
Срок хранения раствора при температуре от 2 °С до 4 °С - не более 1 мес.
(Поправка. ИУС N 2-2020).
6.1.2 Приготовление фосфатного буферного раствора молярной концентрации 0,1 моль/дм
и рН 5,0
В мерную колбу вместимостью 1000 см вносят 13,6 г калия фосфорнокислого однозамещенного, растворяют в 900 см
деионизованной воды, измеряют рН, доводят значение рН до (5,0±0,1) соляной кислотой молярной концентрации
1 моль/дм
(6.1.13) и доводят объем до метки деионизованной водой.
Срок хранения раствора при температуре от 2 °С до 4 °С - не более 3 мес.
(Поправка. ИУС N 2-2020).
6.1.3 Приготовление фосфатного буферного раствора молярной концентрации 0,1 моль/дм
и рН 6,0
В мерную колбу вместимостью 1000 см вносят 13,6 г калия фосфорнокислого однозамещенного, растворяют в 900 см
деионизованной воды, измеряют рН, доводят значение рН до (6,0±0,1) соляной кислотой молярной концентрации
1 моль/дм
(6.1.13) и доводят объем до метки деионизованной водой.
Срок хранения раствора при температуре от 2 °С до 4 °С - не более 3 мес.
(Поправка. ИУС N 2-2020).
6.1.4 Приготовление ацетатного буферного раствора молярной концентрации 0,2 моль/дм
В мерную колбу вместимостью 1000 см вносят 16,4 г натрия уксуснокислого, растворяют в 900 см
деионизованной воды, измеряют рН, доводят значение рН до (5,0±0,1) концентрированной уксусной кислотой и доводят объем раствора до метки деионизованной водой.
Срок хранения раствора при температуре от 2 °С до 4 °С - не более 1 мес.
6.1.5 Приготовление растворов для дериватизации
Для приготовления раствора МСТФА/ТМИС/ДТЭ смешивают 1000 мм МСТФА и 5 мм
ТМИС во флаконе вместимостью 2 см
, добавляют к полученному раствору 2 мг ДТЭ.
Срок хранения раствора при температуре от 2 °С до 4 °С - не более 1 нед.
Для приготовления раствора БСТФА/ТМХС смешивают 1000 мм БСТФА и 10 мм
ТМХС во флаконе вместимостью 2 см
.
Срок хранения раствора при температуре от 2 °С до 4 °С - не более 1 нед.
6.1.6 Приготовление раствора аммиака в изопропиловом спирте
Во флакон вместимостью 40 см вносят 15 см
изопропилового спирта, приливают 0,45 см
аммиака и помещают раствор на 1 мин на ультразвуковую баню.
Раствор используют свежеприготовленным.
6.1.7 Приготовление раствора этилового эфира уксусной кислоты и метилборной кислоты
Для приготовления раствора смешивают 0,02 см метилборной кислоты и 10 см
этилового эфира уксусной кислоты в мерной колбе вместимостью 10 см
.
Раствор используют свежеприготовленным.
6.1.8 Приготовление раствора гидроокиси калия молярной концентрации 1 моль/дм
В мерную колбу вместимостью 1000 см вносят 56,1 г гидроокиси калия, растворяют в 900 см
деионизованной воды и доводят объем раствора до метки деионизованной водой.
Срок хранения раствора при комнатной температуре - не более 1 мес.
6.1.9 Приготовление раствора гидроокиси натрия молярной концентрации 10 моль/дм
В мерную колбу вместимостью 1000 см вносят 400,0 г гидроокиси натрия, растворяют в 600 см
деионизованной воды и доводят объем раствора до метки деионизованной водой.
Срок хранения раствора при комнатной температуре - не более 1 мес.
6.1.10 Приготовление раствора гидроокиси натрия молярной концентрации 2 моль/дм
В мерную колбу вместимостью 1000 см вносят 84,0 г натрия гидроокиси, растворяют в деионизированной воде и доводят объем до метки дистиллированной водой.
Срок хранения раствора при комнатной температуре в сосуде из полимерных материалов - не более 1 мес.
6.1.11 Приготовление раствора соляной кислоты молярной концентрации 0,01 моль/дм
В мерную колбу вместимостью 100 см приливают 50 см
деионизованной воды, 0,1 см
концентрированной соляной кислоты и доводят объем раствора до метки деионизованной водой.
Срок хранения раствора при комнатной температуре - не более 1 мес.
6.1.12 Приготовление 25%-ного раствора соляной кислоты
В мерную колбу вместимостью 100 см приливают 44 см
деионизованной воды, затем осторожно вносят 56 см
концентрированной соляной кислоты.
Срок хранения раствора при комнатной температуре - не более 1 мес.
6.1.13 Приготовление раствора соляной кислоты молярной концентрации 1 моль/дм
В мерную колбу вместимостью 1000 см приливают 500 см
деионизованной воды, вносят 81 см
концентрированной соляной кислоты и доводят объем до метки деионизованной водой.
Срок хранения раствора при комнатной температуре - не более 1 мес.
6.1.14 Приготовление растворов внутреннего стандарта массовой концентрации 0,1 мкг/см
В мерную колбу вместимостью 100 см вносят 1 мг стандартного образца дейтрированных производных, приливают 80 см
этанола, перемешивают и помещают раствор на 1 мин на ультразвуковую баню, затем доводят объем до метки этанолом. В мерную колбу вместимостью 10 см
пипеточным дозатором вносят 0,1 см
приготовленного раствора и доводят объем до метки этанолом.
Срок хранения раствора при температуре не выше минус 18 °С - не более 12 мес.
6.1.15 Приготовление стандартного раствора бета-адреностимуляторов
В мерную колбу вместимостью 100 см вносят 10 мг каждого стандартного образца, приливают 80 см
этанола, перемешивают и помещают раствор на 1 мин на ультразвуковую баню, затем доводят объем до метки этанолом.
Массовая концентрация каждого соединения в растворе должна составлять 0,1 мг/см
.
Срок хранения раствора при температуре не выше минус 18 °С - не более 12 мес.
6.1.16 Приготовление стандартного раствора бета-адреностимуляторов
В мерную колбу вместимостью 10 см пипеточным дозатором вносят 0,1 см
стандартного раствора
(6.1.15) и доводят объем до метки этанолом.
Массовая концентрация каждого соединения в растворе должна составлять 1000 нг/см
.
Срок хранения раствора при температуре от 2 °С до 4 °С - не более 4 мес.
6.1.17 Приготовление стандартного раствора бета-адреностимуляторов
В мерную колбу вместимостью 10 см пипеточным дозатором вносят 1 см
стандартного раствора
(6.1.16) и доводят объем до метки этанолом.
Массовая концентрация каждого соединения в растворе должна составлять 100 нг/см
.
Срок хранения раствора при температуре от 2 °С до 4 °С - не более 4 мес.
6.1.18 Приготовление стандартного раствора бета-адреностимуляторов
В мерную колбу вместимостью 10 см пипеточным дозатором вносят 1 см
стандартного раствора
(6.1.17) и доводят объем до метки этанолом.
Массовая концентрация каждого соединения в растворе должна составлять 10 нг/см
.
Срок хранения раствора при температуре от 2 °С до 4 °С - не более 4 мес.
6.1.19 Приготовление стандартного раствора бета-адреностимуляторов
В мерную колбу вместимостью 10 см пипеточным дозатором вносят 5 см
стандартного раствора
(6.1.18) и доводят объем до метки этанолом.
Массовая концентрация каждого соединения в растворе должна составлять 5 нг/см
.
Срок хранения раствора при температуре от 2 °С до 4 °С - не более 4 мес.
6.1.20 Приготовление градуировочных растворов бета-адреностимуляторов
Для приготовления градуировочного раствора массовой концентрацией 0,1 нг/см к сухому остатку после упаривания матрицы вносят 0,02 см
стандартного раствора
(6.1.19), приливают 0,1 см
раствора внутреннего стандарта (6.1.14). Затем пипеточным дозатором вносят 0,88 см
этанола, переносят на шейкер и гомогенизируют. Затем помещают на центрифугу и центрифугируют при 15000 об/мин в течение 10 мин при температуре 10 °С.
Для приготовления градуировочного раствора массовой концентрацией 0,5 нг/см используют стандартный раствор
(6.1.19).
Для приготовления градуировочного раствора массовой концентрацией 1 нг/см используют стандартный раствор
(6.1.18).
Для приготовления градуировочного раствора массовой концентрацией 10 нг/см используют стандартный раствор
(6.1.17).
Для приготовления градуировочного раствора массовой концентрацией 100 нг/см используют стандартный раствор
(6.1.16).
К сухому остатку после упаривания чистой пробы исследуемого типа матриц вносят 0,1 см соответствующего стандартного раствора, приливают 0,1 см
раствора внутреннего стандарта (6.1.14). Затем пипеточным дозатором вносят 0,8 см
этанола, переносят на шейкер и гомогенизируют. Затем помещают на центрифугу и центрифугируют при 15000 об/мин в течение 10 мин при температуре 10 °С.
Приготовленные градуировочные растворы и растворы внутренних стандартов хранят в морозильнике при температуре не выше минус 20 °С. Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 30 мин.
6.2 Подготовка хромато-масс-спектрометра к выполнению измерений
Подготовку хромато-масс-спектрометра к работе осуществляют в соответствии с техническим руководством по эксплуатации прибора.
6.3 Подготовка газового хроматографа к выполнению измерений
6.3.1 Подготовку газового хроматографа к работе осуществляют в соответствии с техническим руководством по эксплуатации прибора. Для получения градуировочных характеристик устанавливают параметры газового хроматографа в соответствии с 6.4.1.
6.3.2 Для получения градуировочных данных используют градуировочные растворы бета-адреностимуляторов и растворы их дейтерированных производных в соответствии с таблицей 1, внесенные в заведомо чистые пробы анализируемого типа матриц (растворы бета-адреностимуляторов и их дейтерированные производные вносят в матрицу перед этапом дериватизации). В качестве внутреннего стандарта используют дейтерированные производные определяемых бета-адреностимуляторов. Для каждого бета-адреностимулятора используется соответствующее дейтерированное производное.
Таблица 1 - Массовая концентрация бета-адреностимуляторов в градуировочных растворах
Наименование бета-адреностимулятора | Градуировочный уровень | ||||
N 1 | N 2 | N 3 | N 4 | N 5 | |
Массовая концентрация, нг/см | |||||
Нативные бета-адреностимуляторы | |||||
Кленбутерол | 0,1 | 0,5 | 1 | 10 | 100 |
Сальбутамол | 0,1 | 0,5 | 1 | 10 | 100 |
Мапентерол | 0,1 | 0,5 | 1 | 10 | 100 |
Цимбутерол | 0,1 | 0,5 | 1 | 10 | 100 |
Тербуталин | 0,1 | 0,5 | 1 | 10 | 100 |
Изотопно-меченые бета-адреностимуляторы/внутренний стандарт | |||||
Кленбутерол-d6 | 10 | 10 | 10 | 10 | 10 |
Сальбутамол-d6 | 10 | 10 | 10 | 10 | 10 |
Мапентерол-d11 | 10 | 10 | 10 | 10 | 10 |
Цимбутерол-d9 | 10 | 10 | 10 | 10 | 10 |
Тербуталин-d9 | 10 | 10 | 10 | 10 | 10 |
6.3.3 При установлении градуировочной характеристики используют не менее трех уровней массовой концентрации градуировочных растворов в диапазоне определяемого бета-адреностимулятора массовой концентрации от 1 до 100 нг/см. В инжектор хроматографа вводят каждый градуировочный раствор не менее двух раз.
С помощью компьютерной системы обработки данных устанавливают градуировочную характеристику для площади пика методом внутреннего стандарта для каждого бета-адреностимулятора.
Коэффициент отклика для
-го бета-адреностимулятора рассчитывают по формуле
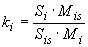 , (1)
, (1)
где - площадь пика
-го бета-адреностимулятора в градуировочном растворе;
- массовая концентрация внутреннего стандарта в градуировочном растворе, нг/см
;
- площадь пика внутреннего стандарта в градуировочном растворе;
- массовая концентрация
-го бета-адреностимулятора в градуировочном растворе, нг/см
.
Проверяют приемлемость полученных значений коэффициента отклика для каждого бета-адреностимулятора анализируемых градуировочных уровней, используя неравенство
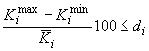 , (2)
, (2)
где 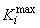 - максимальное значение
- максимальное значение -го коэффициента отклика;
- минимальное значение
-го коэффициента отклика;
- среднее значение
-го коэффициента отклика;
- относительная разность коэффициентов отклика.
Значения (
0,95) не должны превышать: 5% (
3) или 4% (
2), где
- число параллельных определений
-го коэффициента отклика для каждого градуировочного уровня.
6.3.4 При отсутствии дейтерированных производных бета-адреностимуляторов используют метод абсолютной градуировки. Градуировочные растворы бета-адреностимуляторов (не менее трех уровней массовой концентрации от 1 до 100 нг/см на пробу) вносят в заведомо чистые матрицы на стадии внесения внутреннего стандарта так же, как для метода с дейтерированными производными. Каждый градуировочный уровень анализируют не менее двух раз.
6.3.5 Расчеты коэффициента отклика и площади пика выполняют с помощью системы обработки данных в автоматическом режиме.
6.3.6 Градуировочную характеристику считают приемлемой, если рассчитанное программным обеспечением значение квадрата коэффициента корреляции для каждого бета-адреностимулятора 0,98, а значение "Accuracy" для каждой точки градуировочной кривой находится в диапазоне 80%-120%.
6.3.7 Построение новой градуировочной кривой проводят после каждого включения газового хроматографа (остановка работы для сервисного обслуживания или текущей профилактики).
6.4 Условия хроматографических измерений
6.4.1 Газовый хроматограф с масс-спектрометрическим детектором включают в соответствии с руководством (инструкцией) по эксплуатации и устанавливают параметры, рекомендуемые изготовителем капиллярных колонок. Например, для кварцевой капиллярной колонки 30 м0,25 мм
0,25 мкм применяют следующие хроматографические условия:
- газ-носитель - гелий;
- скорость потока газа-носителя 0,8 см/мин;
- температура инжектора 280 °С;
- инжектор в режиме без деления потока;
- температурная программа колонки:
начальная температура 100 °С в течение 0,5 мин;
программируемый нагрев от 100 °С до 200 °С со скоростью 25,0 °С/мин;
программируемый нагрев от 200 °С до 225 °С со скоростью 4,0 °С/мин;
программируемый нагрев от 225 °С до 270 °С со скоростью 20,0 °С/мин;
- изотерма при температуре 270 °С до 20 мин;
- время анализа 20 мин;
- объем пробы от 1 до 5 мм.
Допускается использование других хроматографических условий, обеспечивающих разделение компонентов пробы.
6.4.2 Градуировку и настройку масс-спектрометрического детектора в режиме электронной ионизации и тандемной масс-спектрометрии проводят согласно инструкции по эксплуатации прибора.
7 Отбор проб
7.1 Отбор проб
7.1.1 Отбор проб мяса и мясных продуктов, включая мясо и продукты из мяса птицы - по [1].
7.1.2 Объем отбираемых проб мочи должен быть не менее 40 см.
Объем отбираемых проб желчи должен быть не менее 30 см.
Масса отбираемых проб пигментированной шерсти - не менее 10 г.
Отобранные пробы мочи и желчи при отсутствии возможности испытания в день отбора замораживают при температуре минус 20 °С.
7.1.3 Отбор проб комбикормов - по ГОСТ 13496.0.
7.2 Подготовка проб
7.2.1 Обработка проб органов, тканей, мочи, желчи, шерсти животных и кормов
7.2.1.1 100 г мышечной ткани, предварительно очищенной от грубой соединительной ткани, измельчают на гомогенизаторе и взвешивают на весах по 10,0 г гомогенизированной пробы в двух флаконах вместимостью по 40 см. Во флаконы добавляют 20 см
трис-буфера (6.1.1), 10 мг протеолитического фермента и пипеточным дозатором вносят по 50 мм
раствора дейтерированных стандартных образцов массовой концентрации 10 нг/см
.
Флаконы закрывают крышкой с тефлоновой прокладкой и помещают на нагревательный модуль с магнитной мешалкой при температуре 55 °С на 3 ч. Затем флаконы с полученным гидролизатом охлаждают до комнатной температуры, измеряют рН и, при необходимости, доводят значение рН до 5,0 хлорной кислотой. Флаконы с пробами помещают на центрифугу и центрифугируют при 3000 об/мин в течение 20 мин при температуре 4 °С. Полученный супернатант переносят в стеклянные флаконы вместимостью по 40 см. Осадок повторно экстрагируют 5 см
фосфатного буферного раствора (6.1.2). Полученные гидролизаты объединяют, измеряют рН и, при необходимости, доводят значение рН до 6,0 хлорной кислотой, помещают на центрифугу и центрифугируют при 3000 об/мин в течение 20 мин, фильтруют через мембранный фильтр.
7.2.1.2 Пробу печени или почек измельчают на гомогенизаторе и взвешивают на весах по 10,0 г гомогенизированной пробы в двух флаконах вместимостью 40 см. Во флаконы добавляют по 20 см
фосфатного буферного раствора (6.1.2), измеряют рН и, при необходимости, доводят значение рН до 5,0 раствором гидроокиси калия (6.1.8) молярной концентрации
1 моль/дм
или 25%-ным водным раствором соляной кислоты (6.1.12). Пипеточным дозатором вносят по 50 мм
смеси дейтерированных стандартных образцов массовой концентрации 10 нг/см
и ставят флаконы на ультразвуковую баню на 20 мин при температуре 40 °С. Затем пробы переносят на шейкер, гомогенизируют 30 сек и охлаждают до комнатной температуры. Флаконы с пробами помещают на центрифугу и центрифугируют при 3000 об/мин в течение 10 мин при температуре 4 °С. Затем во флаконы приливают 5 см
фосфатного буферного раствора (6.1.2), экстрагируют 30 сек на шейкере и центрифугируют. Экстракты объединяют, измеряют рН и, при необходимости, доводят значение рН до 5,0 раствором гидроокиси калия молярной концентрации
1 моль/дм
(6.1.8) или 25%-ным водным раствором соляной кислоты (6.1.12). Пипеточным дозатором в экстракты вносят по 50 мм
пищеварительного сока Helix pomatia, помещают на нагревательный модуль с магнитной мешалкой при температуре 40 °С на 15 ч. После гидролиза пробу охлаждают до комнатной температуры, измеряют рН и, при необходимости, доводят значение рН до 6,0 25%-ным водным раствором соляной кислоты (6.1.12). Гидролизат центрифугируют и фильтруют через мембранный фильтр.
7.2.1.3 Во флакон вносят 10 см мочи, 10 см
ацетатного буферного раствора (6.1.4), 50 мм
пищеварительного сока Helix pomatia, измеряют рН и, при необходимости, доводят значение рН до 5,0 раствором гидроокиси калия молярной концентрации
1 моль/дм
(6.1.8) или 25%-ным водным раствором соляной кислоты (6.1.12). Пипеточным дозатором вносят по 50 мм
смеси дейтерированных стандартных образцов массовой концентрации 10 нг/см
и ставят флаконы на нагревательный модуль при температуре 40 °С на 15 ч для ферментативного гидролиза коньюгатов. Гидролизат охлаждают до комнатной температуры, измеряют рН и, при необходимости, доводят значение рН до 6,0 25%-ным водным раствором соляной кислоты (6.1.12), фильтруют через мембранный фильтр.
(Поправка. ИУС N 2-2020).
7.2.1.4 Во флакон вносят 5 см желчи, 15 см
ацетатного буферного раствора (6.1.4), 100 мм
пищеварительного сока Helix pomatia. Далее проводят обработку пробы в соответствии с 7.2.1.3.
(Поправка. ИУС N 2-2020).
7.2.1.5 Сетчатку отделяют от глазного яблока, помещают во флакон вместимостью 40 см и взвешивают на весах. На каждые 50 мг сетчатки добавляют 1 см
фосфатного буферного раствора (6.1.2). Затем гомогенизируют 30 сек на гомогенизаторе конфигурации ротор-статор. Во флаконы вместимостью 40 см
вносят по 1 см
гомогенизированной пробы и добавляют по 9 см
ацетатного буферного раствора (6.1.4). Пипеточным дозатором вносят 50 мм
пищеварительного сока Helix pomatia и по 50 мм
смеси дейтерированных стандартных образцов массовой концентрации
10 нг/см
. Закрывают флаконы крышкой с тефлоновой прокладкой и помещают на нагревательный модуль с магнитной мешалкой на 15 ч при температуре 40 °С. Полученный гидролизат охлаждают до комнатной температуры, измеряют рН и, при необходимости, доводят значение рН до 6,0 раствором гидроокиси натрия молярной концентрации
10 моль/дм
(6.1.9). Флаконы с пробами помещают на центрифугу и центрифугируют при 3000 об/мин в течение 10 мин при температуре 4 °С. Гидролизат фильтруют через мембранный фильтр.
7.2.1.6 100 г кормов измельчают на гомогенизаторе и взвешивают на весах по 10,0 г гомогенизированной пробы в двух флаконах вместимостью 40 см. Во флаконы добавляют 25 см
соляной кислоты молярной концентрацией
0,01 моль/дм
(6.1.11). Пипеточным дозатором вносят по 50 мм
смеси дейтерированных стандартных образцов массовой концентрации 10 нг/см
. Флаконы помещают в шейкер на 30 мин, а затем центрифугируют. Надосадочный слой переносят во флакон вместимостью 40 см
, добавляют 5 см
н-Гексана, экстрагируют два раза по 2 мин, отбрасывая гексановые фракции. Измеряют рН водного остатка и, при необходимости, доводят значение рН до 6,0 раствором гидроокиси натрия молярной концентрации
10 моль/дм
(6.1.9), помещают на центрифугу и центрифугируют при 3000 об/мин в течение 10 мин при температуре 4 °С. Экстракт фильтруют через мембранный фильтр.
7.2.1.7 10 г пигментированной шерсти промывают 0,2%-ным водным раствором твин 20 и деионизованной водой, высушивают в сушильном шкафу при температуре 40 °С и измельчают ножницами на отрезки размером от 1 до 2 мм. Измельченную шерсть взвешивают на весах и по 1,0 г помещают в два флакона вместимостью 40 см. Во флаконы добавляют по 20 см
раствора гидроокиси натрия молярной концентрациии
2 моль/дм
(6.1.10). Затем во флаконы вносят пипеточным дозатором по 50 мм
смеси дейтерированных стандартных образцов массовой концентрации
10 нг/см
.
Флаконы ставят на нагревательный модуль с магнитной мешалкой на 1 ч при температуре 85 °С. Затем охлаждают до комнатной температуры, добавляют 10 см метил-третбутилового эфира, экстрагируют два раза по 5 мин, собирая эфирную фракцию в выпарительную колбу вместимостью 100 см
. Для полного отделения метил-третбутилового эфира флаконы помещают на центрифугу и центрифугируют при 3000 об/мин в течение 5 мин. Затем во флаконы вносят по 5 г натрия хлористого, перемешивают и повторно экстрагируют дважды по 5 мин с 10 см
смеси этилового эфира уксусной кислоты и изопропилового спирта в соотношении 60:40. Объединенные экстракты упаривают на ротационном испарителе при температуре не выше 40 °С. К сухому остатку приливают 10 см
фосфатного буферного раствора (6.1.3) и помещают на 1 мин на ультразвуковую баню. Экстракт фильтруют через мембранный фильтр.
7.3 Очистка подготовленных проб методом твердофазной экстракции (ТФЭ)
Картриджи для твердофазной экстракции вместимостью 6 см с 0,5 г сорбента С18 40 мкм кондиционируют на вакуумном устройстве для ТФЭ, пропуская последовательно: 4 см
метанола, 1 см
деионизованной воды, 3 см
фосфатного буферного раствора молярной концентрации
0,1 моль/дм
(6.1.3). Пропускают через картридж пробу, полученную в соответствии с 7.2.1.1-7.2.1.7, в фосфатном буфере (на всех этапах ТФЭ, кроме этапов сушки, вакуум не применяют). Промывают картридж последовательно два раза по 2 см
фосфатным буферным раствором, 1 см
раствором уксусной кислоты молярной концентрации
1 моль/дм
и затем сушат картридж в вакууме 20 мин. Далее промывают картридж 2 см
метанола и снова сушат в вакууме 10 мин. Элюируют аналиты раствором аммиака в изопропиловом спирте (6.1.6). Упаривают элюат на ротационном испарителе при температуре не выше 45 °С. Остаток перерастворяют в 1 см
абсолютного этанола и переносят во флакон вместимостью 4 см
. Упаривают этанол досуха в токе азота на нагревательном модуле при температуре от 35 °С до 40 °С и не менее 1 ч.
Каждую новую партию сорбента необходимо тестировать по описанной процедуре ТФЭ. При тестировании используют стандартные растворы бета-адреностимуляторов известной молярной концентрации в фосфатном буферном растворе (6.1.3). Модифицируют только два этапа: объем метанола на стадии промывки сорбента (критично для анилиновых бета-адреностимуляторов) и объем элюирующего раствора на последней стадии (критично для бета-адреностимуляторов фенольного типа).
(Поправка. ИУС N 2-2020).
8 Порядок выполнения измерений
8.1 Дериватизация бета-адреностимуляторов
8.1.1 Для получения триметилсилиловых производных бета-адреностимуляторов к сухому остатку после ТФЭ очистки по 7.3 пипеточным дозатором приливают 50 мм смеси МСТФА/ТМИС/ДТЭ (6.1.5). Помещают флаконы в нагревательный модуль на 60 мин при температуре 60 °С. По истечении указанного времени реакционную смесь охлаждают до комнатной температуры, переносят в стеклянные флаконы вместимостью 2 см
с вставками на 100 мм
и используют для ГХ-МС анализа.
8.1.2 Для двухстадийной дериватизации к сухому остатку после ТФЭ очистки пипеточным дозатором приливают 50 мм раствора метилборной кислоты в этиловом эфире уксусной кислоты (6.1.7). Полученную реакционную смесь выдерживают при комнатной температуре 20 мин. По истечении указанного времени от 1 мм
до 2 мм
реакционной смеси вводят в хромато-масс-спектрометр. Получают хроматограмму циклических метилборатов.
Затем реакционную смесь упаривают досуха и к сухому остатку добавляют 50 мм раствора БСТФА/ТМХС (6.1.5). Полученную реакционную смесь помещают в нагревательный модуль при температуре 60 °С на 30 мин. По истечении указанного времени реакционную смесь охлаждают до комнатной температуры, переносят в стеклянные флаконы вместимостью 2 см
с вставками на 100 мм
и используют для ГХ-МС анализа.
8.2 ГХ-МС анализ
8.2.1 В инжектор хроматографа вводят по 1-5 мм анализируемой пробы и проводят анализ в условиях, указанных в 6.4. Проводят не менее двух определений для каждой анализируемой пробы.
(Поправка. ИУС N 2-2020).
8.2.2 Времена удерживания бета-адреностимуляторов определяют при анализе градуировочных растворов. Времена удерживания идентифицированных бета-адреностимуляторов в анализируемой пробе не должны отличаться от времен удерживания бета-адреностимуляторов в градуировочном растворе не более чем на 2,5%.
8.2.3 Данные о диагностических ионах триметилсилиловых производных бета-адреностимуляторов приведены в таблице 2.
Таблица 2 - Диагностические ионы триметилсилиловых производных бета-адреностимуляторов
Наименование бета-адреностимулятора | Диагностические ионы | |||
Кленбутерол | 1 | 276 | 348 | 86/262/243/333 |
Кленбутерол-d6 | 1 | 282 | 354 | 92/262/246/339 |
Кленбутерол | 2 | 276 | 420 | 86/300/335/405 |
Кленбутерол-d6 | 2 | 282 | 426 | 92/300/335/411 |
Сальбутамол | 3 | 239 | 455 | 86/294/369/440 |
Сальбутамол-d6 | 3 | 245 | 461 | 92/295/369/446 |
Тербуталин | 3 | 225 | 442 | 86/356/371/426 |
Мапентерол | 1 | 324 | 396 | 100/277/291/296 |
Мапентерол | 2 | 324 | 468 | 100/364/369/453 |
Цимбутерол | 1 | 233 | 305 | 86/200/219/234 |
Цимбутерол-d9 | 1 | 242 | 314 | 95/206/219/234 |
Цимбутерол | 2 | 233 | 377 | 86/272/291/362 |
Цимбутерол-d9 | 2 | 242 | 386 | 95/278/291/371 |
Примечание - В таблице использованы следующие условные обозначения: |
8.2.4 Данные о диагностических ионах метилборатов бета-адреностимуляторов приведены в таблице 3.
Таблица 3 - Диагностические ионы метилборатов бета-адреностимуляторов
Наименование бета-адреностимулятора | Диагностические ионы | |||
Кленбутерол | 1 | 276 | 300 | 243/245/285/287 |
Кпенбутерол-d6 | 1 | 282 | 306 | 246/248/288/290 |
Сальбутамол | 2 | 239 | 287 | 229/230/271/272 |
Сальбутамол-d6 | 2 | 245 | 293 | 232/233/274/275 |
Мапентерол | 1 | 324 | 348 | 277/279/291/319 |
Цимбутерол | 1 | 233 | 257 | 158/200/241/242 |
Цимбутерол-d9 | 1 | 242 | 266 | 159/206/247/248 |
Примечание - В таблице использованы следующие условные обозначения: |
9 Обработка результатов ГХ-МС анализа
9.1 В соответствии с данными, полученными при анализе градуировочных растворов, оформляют таблицу пиков с использованием программного обеспечения хромато-масс-спектрометра. Метод обработки хроматограммы - внутренний стандарт.
Содержание -го бета-адреностимулятора в анализируемой пробе
, мкг/кг, рассчитывают по формуле
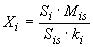 , (3)
, (3)
где - площадь пика
-го бета-адреностимулятора в анализируемой пробе;
- содержание внутреннего стандарта в анализируемой пробе, мкг/кг;
- площадь пика внутреннего стандарта в анализируемой пробе;
- коэффициент отклика для
-го бета-адреностимулятора.
9.1.1 Расчеты количества бета-адреностимулятора и площади пика выполняются системой обработки данных в автоматическом режиме.
9.1.2 Результаты измерений округляют до второго десятичного знака и выражают в мкг/кг.
За результат измерений содержания -го бета-адреностимулятора принимают среднеарифметическое результатов двух параллельных определений, если выполняется условие приемлемости:
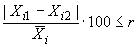 , (4)
, (4)
где и
- результаты двух параллельных определений содержания
-го бета-адреностимулятора, выполненных в условиях повторяемости, мкг/кг;
- среднеарифметическое значение результатов двух параллельных определений,
и
, мкг/кг;
- предел повторяемости, значение которого приведено в таблице 7, %.
9.1.3 Для целей количественного и подтверждающего анализа допускается проведение измерений в различных режимах тандемной масс-спектрометрии, позволяющих получить требуемое количество подтверждающих критериев. При количественном анализе допускается проведение измерения по одному наиболее интенсивному иону в соответствии с требованиями, указанными в 8.2. Подтверждающий анализ проводят при наличии не менее четырех диагностических критериев, полученных для силированных производных или метилборатов, в соответствии с требованиями, указанными в 8.2.
9.2 Идентификацию бета-адреностимуляторов и их количественное определение проводят с соблюдением следующих условий для масс-спектрометрического детектирования:
- молекулярный ион используют для идентификации, если присутствует в масс-спектре с относительной интенсивностью не менее 10%;
- относительная ионная интенсивность каждого из диагностических ионов должна быть не менее 10%;
- соотношение сигнал/шум для каждого диагностического иона должно быть не менее 3/1.
Относительные интенсивности детектированных ионов, выраженные как процент от интенсивности самого интенсивного иона, должны соответствовать таковым из градуировочного раствора, в сопоставимых массовых концентрациях, измеренные при тех же самых условиях, в пределах допустимых отклонений, указанных в таблице 4.
Таблица 4 - Максимально допустимые отклонения для относительных ионных интенсивностей
Относительная интенсивность | ЭИ-ГХ-МС (относительная), % | ГХ-МС | ||||
Св. | 50 | ±10 | ±20 | |||
" | 20 | до | 50 | включ. | ±15 | ±25 |
От | 10 | " | 20 | " | ±20 | ±30 |
Менее 10 | ±50 | ±50 |
При проведении подтверждающего анализа число диагностических ионов для каждого из масс-спектрометрических методов определяют с учетом идентифицирующих критериев.
Для подтверждения каждого из бета-адреностимуляторов необходимы минимум четыре идентифицирующих критерия. В таблице 5 приведено количество идентифицирующих критериев в зависимости от используемых масс-спектрометрических методов.
Таблица 5 - Отношение между масс-спектрометрическими методами и количеством полученных идентифицирующих критериев
Масс-спектрометрические методы | Количество идентифицирующих критериев, полученных на диагностический ион |
Масс-спектрометрия низкого разрешения (HP) | 1,0 |
НР-МС | 1,0 |
НР-МС | 1,5 |
Масс-спектрометрия высокого разрешения (ВР) | 2,0 |
ВР-МС | 2,0 |
ВР-МС | 2,5 |
В таблице 6 показаны примеры числа идентифицирующих критериев ( - целое число), полученных для различных масс-спектрометрических методов.
Таблица 6 - Примеры расчета идентифицирующих критериев
Методы ГХ-МС анализа | Число диагностических ионов | Количество идентифицирующих критериев |
ГХ-МС (ЭИ или ХИ) | ||
ГХ-МС (ЭИ или ХИ) | 2 (Производное А) + 2 (Производное Б) | 4 |
2 производных | ||
ГХ-МС-МС | 1 предшественник и 2 дочерних | 4 |
ГХ-МС-МС | 2 предшественника, каждый с 1 дочерним | 5 |
10 Метрологические характеристики
Значения допускаемой относительной расширенной неопределенности , % (при коэффициенте охвата
2) измерений содержания индивидуальных бета-адреностимуляторов по установленному в настоящем стандарте методу приведены в таблице 7.
Таблица 7 - Метрологические характеристики метода
Диапазон измерений содержаний бета-адреностимуляторов, мкг/кг | Относительная расширенная неопределенность | Предел повторяемости, при | ||||
От | 0,10 | до | 1,00 | включ. | 25 | 15 |
Св. | 1,00 | " | 10,00 | " | 15 | 10 |
" | 10,00 | 10 | 5 |
Фактические значения расширенной неопределенности , мкг/кг (при коэффициенте охвата
2) результатов, полученных при определении содержания индивидуальных бета-адреностимуляторов и признанных приемлемыми (8.1.2), рассчитываются по формуле (7).
11 Оформление результатов измерений
Результат анализа в документах, предусматривающих его использование, представляют в виде
 , (5)
, (5)
где - окончательный результат определения содержания бета-адреностимулятора, мкг/кг;
- среднеарифметическое двух параллельных определений содержания
-го бета-адреностимулятора в анализируемой пробе, выполненных в условиях повторяемости, мкг/кг;
- расширенная неопределенность (при коэффициенте охвата
2) определения содержания
-го бета-адреностимулятора, определяемая по формуле 7, мкг/кг.
12 Контроль точности измерений
12.1 Контроль стабильности градуировочной характеристики проводят не реже одного раза в пять дней. Повторно анализируют образцы для градуировки хроматографа по 6.4 и определяют коэффициенты отклика для каждого бета-адреностимулятора (два параллельных определения) в тех же условиях, в которых была установлена градуировочная характеристика. Градуировочную характеристику признают стабильной, если коэффициент отклика для каждого из двух параллельных определений отличается от значения, установленного при градуировке, не более чем на 10%. Если градуировочная характеристика нестабильна, градуировку хроматографа проводят повторно.
12.2 Контроль смещения результатов измерений с помощью стандартных образцов проводят не реже одного раза в месяц. С использованием стандартной процедуры подготовки проб проводят анализ стандартных образцов в соответствии с разделом 7 и получают результат измерений содержания -го бета-адреностимулятора (
, мкг/кг). Результаты измерений признают удовлетворительными при выполнении неравенства
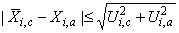 , (6)*
, (6)*
_______________
* Формула 6. (Поправка. ИУС N 2-2020).
где - содержание
-го бета-адреностимулятора в анализируемом стандартном образце, мкг/кг;
- аттестованное значение содержания
-го бета-адреностимулятора в стандартном образце, мкг/кг;
- расширенная неопределенность (при коэффициенте охвата
2) результата измерений содержания
-го бета-адреностимулятора, полученного при соблюдении требований настоящего стандарта, мкг/кг, рассчитывается по формуле
 , (7)
, (7)
где - расширенная неопределенность (при коэффициенте охвата
2) аттестованного содержания
-го бета-адреностимулятора в аттестованном стандартном образце в соответствии с паспортом (сертификатом) на конкретный стандартный образец, мкг/кг.
13 Требования безопасности
13.1 Используемые в работе реактивы относятся к веществам 1-го и 2-го класса опасности по ГОСТ 12.1.007, при работе с ними необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
13.2 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией.
13.3 Операции по приготовлению и дозированию градуировочных растворов следует проводить под тягой в вытяжном шкафу.
13.4 При проведении испытаний следует соблюдать ГОСТ 12.2.085 и правила устройства и безопасной эксплуатации сосудов, работающих под давлением, действующие на территории государства, принявшего стандарт.
13.5 При выполнении измерений на хромато-масс-спектрометре следует соблюдать правила электробезопасности в соответствии с ГОСТ 12.1.019, пожаровзрывобезопасности по ГОСТ 12.1.018 и инструкцией по эксплуатации прибора.
13.6 К выполнению измерений методом газовой хроматографии допускаются лица, владеющие техникой ГХ-МС и изучившие инструкции по эксплуатации применяемой аппаратуры.
Библиография
[1] | ISO 17604:2003* | Microbiology of food and animal feeding stuffs - Carcass sampling for microbiological analysis (Микробиология пищевых продуктов и кормов для животных. Отбор проб с туши для микробиологического анализа) |
________________ |
Редакция документа с учетом
изменений и дополнений подготовлена
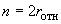 , %
, %
