ГОСТ 31480-2012
Группа С19
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
КОМБИКОРМА, КОМБИКОРМОВОЕ СЫРЬЕ
Определение содержания аминокислот (лизина, метионина, треонина, цистина и триптофана) методом капиллярного электрофореза
Mixed fodders, raw mixed fodders. Determination of aminoacids (lysine, methionine, threonine, cystine and triptophane) content by method of capillary electrophoresis
МКС 65.120
Дата введения 2013-07-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Открытым акционерным обществом "Всероссийский научно-исследовательский институт комбикормовой промышленности" (ОАО "ВНИИКП"), Научно-производственной фирмой аналитического приборостроения "Люмэкс" (НПФ АП "Люмэкс"), Федеральным государственным учреждением "Ленинградская межобластная ветеринарная лаборатория" (ФГУ ЛМВЛ)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 23-24 мая 2012 г. N 41)
За принятие проголосовали:
Краткое наименование страны | Код страны | Сокращенное наименование национального органа по стандартизации |
Азербайджан | AZ | Азгосстандарт |
Армения | AM | Минторгэкономразвития |
Кыргызстан | KG | Кыргызстандарт |
Российская Федерация | RU | Росстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 28 сентября 2012 г. N 465-ст межгосударственный стандарт ГОСТ 31480-2012 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2013 г.
5 Настоящий стандарт подготовлен на основе применения ГОСТ Р 52347-2005
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта публикуется в указателе "Национальные стандарты".
Информация об изменениях к настоящему стандарту публикуется в указателе "Национальные стандарты", а текст изменений - в информационных указателях "Национальные стандарты". В случае пересмотра или отмены настоящего стандарта соответствующая информация будет опубликована в информационном указателе "Национальные стандарты"
ВНЕСЕНА поправка, опубликованная в ИУС N 6, 2018 год
Поправка внесена изготовителем базы данных
1 Область применения
1 Область применения
Настоящий стандарт распространяется на комбикорма и комбикормовое сырье и устанавливает экспрессный метод определения содержания аминокислот: лизина, метионина, треонина, цистина и триптофана с помощью капиллярного электрофореза.
Метод основан на разделении в кварцевом капилляре под действием электрического поля ионных форм аминокислот и на их детектировании по собственному поглощению в ультрафиолетовой (УФ) области.
Идентификацию и количественное определение анализируемых аминокислот проводят с помощью установленного программного обеспечения.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.018-93 Система стандартов безопасности труда. Пожаровзрывобезопасность статического электричества. Общие требования
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
________________
* На территории Российской Федерации документ не действует. Действует ГОСТ Р 12.1.019-2009, здесь и далее по тексту. - .
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ 4107-78 Реактивы. Бария гидроокись 8-водная. Технические условия
ГОСТ 4199-76 Реактивы. Натрий тетраборнокислый 10-водный. Технические условия
ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
ГОСТ 4328-77 Натрия гидроокись. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 10521-78 Реактивы. Кислота бензойная. Технические условия
ГОСТ 13496.0-80* Комбикорма, сырье. Методы отбора проб
________________
* На территории Российской Федерации документ не действует. Действует ГОСТ Р ИСО 6497-2011, здесь и далее по тексту. - .
ГОСТ 13586.3-83 Зерно. Правила приемки и методы отбора проб
ГОСТ 13979.0-86 Жмыхи, шроты и горчичный порошок. Правила приемки и методы отбора проб
ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия
ГОСТ 17083-87 Электротепловентиляторы бытовые. Общие технические условия
ГОСТ 17681-82 Мука животного происхождения. Методы испытаний
ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия
ГОСТ 21400-75 Стекло химико-лабораторное. Технические требования. Методы испытаний
ГОСТ 24104-2001* Весы лабораторные. Общие технические требования
________________
* На территории Российской Федерации документ не действует. Действует ГОСТ Р 53228-2008, здесь и далее по тексту. - .
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 27262-87* Корма растительного происхождения. Методы отбора проб
________________
* На территории Российской Федерации документ не действует. Действует ГОСТ Р ИСО 6497-2011, здесь и далее по тексту. - .
ГОСТ 27668-88 Мука и отруби. Приемка и методы отбора проб
ГОСТ 29169-91 (ИСО 648-77) Посуда лабораторная стеклянная. Пипетки с одной отметкой
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов по указателю "Национальные стандарты", составленному по состоянию на 1 января текущего года, и по соответствующим информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Диапазоны измерений содержания аминокислот и метрологические характеристики метода
Диапазоны измерений содержания аминокислот (АК) и значения показателей повторяемости, воспроизводимости и точности приведены в таблице 1 (при вероятности =0,95).
Таблица 1
Наименование определяемого компонента и диапазон измерений | Показатель повторяемости (относительное среднеквадратичное отклонение повторяемости) | Показатель воспроизводимости (относительное среднеквадратичное отклонение воспроизводимости) | Показатель точности (границы относительной погрешности) |
Лизин, %: | |||
от 0,25 до 1,0 включ. | 20 | 25 | 50 |
св. 1,0 " 2,5 " | 15 | 20 | 40 |
" 2,5 " 10 " | 10 | 14 | 28 |
Метионин, %: | |||
от 0,3 до 1,0 включ. | 20 | 25 | 50 |
св. 1,0 " 3,0 " | 15 | 20 | 40 |
Треонин, %: | |||
от 0,25 до 1,0 включ. | 20 | 25 | 50 |
св. 1,0 " 3,0 " | 15 | 18 | 36 |
Цистин, %: | |||
от 0,2 до 2,0 включ. | 20 | 25 | 50 |
Триптофан, %: | |||
от 0,1 до 2,0 включ. | 11 | 15 | 30 |
(Поправка. ИУС N 6-2018).
4 Требования техники безопасности
4.1 При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007, требования пожарной безопасности по ГОСТ 12.1.004, ГОСТ 12.1.018 и электробезопасности при работе с электроустановками по ГОСТ 12.1.019.
4.2 Помещение, в котором проводят измерения, должно быть снабжено приточно-вытяжной вентиляцией. Работу с реактивами необходимо проводить в вытяжном шкафу.
4.3 При работе с концентрированными кислотами и щелочами необходимо использовать резиновые перчатки.
5 Отбор и подготовка проб к выполнению измерений
5.1 Отбор проб - по ГОСТ 13496.0, ГОСТ 13586.3, ГОСТ 13979.0, ГОСТ 17681, ГОСТ 27262, ГОСТ 27668.
5.2 Подготовка пробы к анализу - с использованием сита с отверстиями диаметром 1 мм по нормативным документам государств, принявших стандарт.
6 Определение содержания лизина, метионина, треонина и цистина
6.1 Средства измерений, оборудование, материалы и реактивы
Система капиллярного электрофореза с диапазоном изменения рабочего напряжения от 1 до 25 кВ, системой поддержания рабочей температуры капилляра, спектрофотометрическим детектором, предназначенным для регистрации оптического поглощения в области 190-200 нм, снабженная кварцевым капилляром (эффективная длина 65 см, внутренний диаметр 0,05 мм), типа "Капель-105".
Программно-аппаратный комплекс для сбора и обработки хроматографических данных типа "МультиХром для Windows", версия не ниже 1.5.
Весы лабораторные по ГОСТ 24104 с пределом допускаемой абсолютной погрешности однократного взвешивания не более ±0,001 и ±0,02 г.
Холодильник бытовой по ГОСТ 16317 любой марки.
рН-метр лабораторный (основная погрешность измерения не более ±0,05 ед. pH).
Центрифуга лабораторная марки ШХ 2.779.040 со скоростью вращения не менее 6000 об/мин.
Шкаф сушильный лабораторный с терморегулятором, обеспечивающим поддержание температуры (110±2) °С.
Электроплитка бытовая по ГОСТ 14919.
Вентилятор по ГОСТ 17083.
Эксикатор по ГОСТ 25336.
Баня водяная с регулятором нагрева.
Бутыли из полиэтилена с плотно завинчивающейся крышкой вместимостью 10, 20, 100, 500 и 1000 см.
Колбы конические со шлифом -1-25(1000)-14/23(19/26, 24/29) по ГОСТ 25336.
Колбы мерные 1(2)-25(50, 100, 1000)-2 по ГОСТ 1770.
Пипетки градуированные 1(2, 3, 5)-1(1а, 2, 2а)-2-1(5, 10) по ГОСТ 29227.
Пипетки с одной отметкой 1 (2)-2-1(5, 10, 20) по ГОСТ 29169.
Микродозаторы переменного объема 5-50, 50-200, 200-1000 мм и с пределом допускаемой погрешности измерения не более ±5% по нормативным документам государств, принявших стандарт.
Пробирки П2Т-25ТС по ГОСТ 25336.
Пробирки для микропроб однократного применения (типа Эппендорфа) вместимостью 1,5 см по нормативным документам государств, принявших стандарт.
Стаканчики для взвешивания (бюксы) СВ-14/8 (19/9, 24/10, 34/12) по ГОСТ 25336.
Воронки В-25(36)-36(80) ХС по ГОСТ 25336.
Ампулы стеклянные с перетяжкой вместимостью 20 см из стекла по ГОСТ 21400.
Виалы стеклянные с герметично завинчивающейся крышкой вместимостью 15 см для кислотного гидролиза.
Фильтры целлюлозно-ацетатные (размер пор 0,2 мкм, диаметр 25 мм).
Фильтры обеззоленные "синяя лента" по нормативным документам государств, принявших стандарт.
Натрия гидроокись по ГОСТ 4328, раствор молярной концентрации (NaOH)=0,5 моль/дм
.
L-лизин моногидрохлорид, L-метионин, L-цистин, L-треонин, L-аргинин квалификации не ниже ч., "Флука", Швейцария (допускается использовать D-, а также смесь DL-аминокислот).
Кислота соляная по ГОСТ 3118, растворы молярных концентраций (HCI)=1 моль/дм
,
(HCI)=0,1 моль/дм
,
(HCI)=6 моль/дм
.
-циклодекстрин, "Флука", Швейцария.
Натрий тетраборнокислый, стандарт-титр.
Натрий тетраборнокислый 10-водный по ГОСТ 4199, растворы молярных концентраций (Na
B
O
·10H
O)=0,05 моль/дм
и
(Na
B
O
·10H
O)=0,02 моль/дм
.
Кислота бензойная по ГОСТ 10521.
Вода дистиллированная по ГОСТ 6709.
Примечания
1 Допускается применение средств измерений и оборудования с такими же или лучшими метрологическими и техническими характеристиками, а также материалов и реактивов по качеству не ниже вышеуказанных.
2 Все реактивы должны быть квалификации х.ч. или ч.д.а.
3 Требования к обработке посуды и использованию оснастки, необходимой для выполнения измерений, в соответствии с приложением А.
6.2 Подготовка к проведению измерений
6.2.1 Приготовление вспомогательных растворов
6.2.1.1 Приготовление раствора соляной кислоты молярной концентрации (HCI)=1 моль/дм
8,3 см концентрированной соляной кислоты помещают в мерную колбу вместимостью 100 см
и доводят объем раствора до метки дистиллированной водой. Возможно использование стандарт-титра соляной кислоты. Срок хранения не ограничен при комнатной температуре.
6.2.1.2 Приготовление раствора гидроокиси натрия молярной концентрации (NaOH)=0,5 моль/дм
Навеску гидроокиси натрия массой 2,000 г помещают в мерную колбу вместимостью 100 см, растворяют в 50-60 см
дистиллированной воды и доводят объем раствора в колбе до метки дистиллированной водой. Раствор хранят в емкости из полиэтилена с плотно завинчивающейся крышкой не более 2 мес при комнатной температуре.
Растворы по 6.2.1.1 и 6.2.1.2 предназначены только для промывок капилляра.
6.2.1.3 Приготовление раствора тетраборнокислого натрия молярной концентрации (Na
B
O
·10H
O)=0,05 моль/дм
Раствор готовят из стандарт-титра по прилагаемой к нему инструкции и хранят в полиэтиленовой посуде, закрыв пробкой. Срок хранения раствора - 2 мес при комнатной температуре.
Примечание - При отсутствии стандарт-титра раствор готовят из 10-водного тетраборнокислого натрия. Для этого навеску препарата массой 19,071 г растворяют в мерной колбе вместимостью 1 дм в свежепрокипяченной и охлажденной без доступа воздуха дистиллированной воде. pH раствора при 20 °С должен быть 9,22±0,10.
6.2.1.4 Приготовление раствора соляной кислоты молярной концентрации (HCI)=6 моль/дм
100 см концентрированной соляной кислоты смешивают с равным объемом дистиллированной воды. Срок хранения не ограничен при комнатной температуре. Раствор используют для гидролиза проб.
6.2.1.5 Приготовление раствора соляной кислоты молярной концентрации (HCI)=0,1 моль/дм
Раствор готовят из стандарт-титра по прилагаемой к нему инструкции. Срок хранения не ограничен при комнатной температуре.
6.2.2 Приготовление буферных растворов
6.2.2.1 Приготовление рабочего буферного раствора молярной концентрации тетраборнокислого натрия (Na
B
O
·10H
O)=0,02 моль/дм
20 см раствора тетраборнокислого натрия, приготовленного по 6.2.1.3, помещают в мерную колбу вместимостью 50 см
и доводят объем в колбе до метки дистиллированной водой. Раствор тщательно перемешивают и используют:
- для кондиционирования капилляра;
- для хранения капилляра в нерабочее время;
- в качестве ведущего электролита (рабочего буферного раствора) для определения лизина, треонина и цистина;
- для приготовления ведущего электролита при определении метионина.
6.2.2.2 Приготовление рабочего буферного раствора для определения метионина
Навеску -циклодекстрина массой 0,114 г растворяют в пробирке в 10 см
раствора тетраборнокислого натрия молярной концентрации
(Na
B
O
·10H
O)=0,02 моль/дм
(см. 6.2.2.1). Полученную смесь закрывают пробкой и слегка нагревают на водяной бане при температуре от 50 °С до 70 °С до полного растворения
-циклодекстрина. Хранят в сосуде из полиэтилена не более 14 сут при температуре не ниже 18 °С.
6.2.2.3 Подготовка буферных растворов для проведения измерений
Непосредственно перед началом проведения измерений рабочие буферные растворы необходимо:
- профильтровать через ацетатно-целлюлозный фильтр, отбросив первые порции фильтрата (1-2 см);
- дегазировать центрифугированием. Для этого в пробирки Эппендорфа помещают 0,5 см соответствующего раствора (см. 6.2.2.1 или 6.2.2.2), плотно закрывают пробками и центрифугируют в течение 2 мин при скорости вращения 6000 об/мин.
6.2.3 Приготовление градуировочных растворов аминокислот (АК)
6.2.3.1 Приготовление запасных растворов АК массовыми концентрациями, г/дм:
- лизина - 2,50;
- метионина и треонина - 1,00;
- цистина - 0,50;
- аргинина - 1,00.
Для приготовления растворов лизина, метионина, треонина и аргинина необходимую навеску каждой АК (см. таблицу 2) помещают в отдельную мерную колбу вместимостью 100 см, растворяют в дистиллированной воде и доводят объем раствора в колбе до метки дистиллированной водой.
Таблица 2
Аминокислота | Навеска, г | Концентрация, г/дм |
L-лизин моногидрохлорид* | 0,3124 | 2,50 |
L-метионин | 0,1000 | 1,00 |
L-треонин | 0,1000 | 1,00 |
L-цистин | 0,0500 | 0,50 |
L-аргинин | 0,1000 | 1,00 |
* В случае L-лизина дигидрохлорида величина навески 0,3747 г; L-лизина моногидрата величина навески 0,2808 г. |
Для приготовления раствора цистина навеску массой 0,050 г помещают в мерную колбу вместимостью 100 см, растворяют в 10 см
раствора соляной кислоты молярной концентрации
(HCI)=0,1 моль/дм
(см. 6.2.1.5), доводят объем раствора в колбе до метки дистиллированной водой и тщательно перемешивают.
Срок хранения запасных растворов АК в герметично закрытой посуде - 6 мес при температуре от 4 °С до 6 °С.
6.2.3.2 Приготовление запасного раствора бензойной кислоты массовой концентрации 1,00 г/дм
Навеску бензойной кислоты массой 0,100 г помещают в мерную колбу вместимостью 100 см, растворяют в 20 см
раствора тетраборнокислого натрия молярной концентрации 0,05 моль/дм
(см. 6.2.1.3), доводят объем раствора в колбе до метки дистиллированной водой и перемешивают. Срок хранения - 6 мес при комнатной температуре.
6.2.3.3 Приготовление рабочего раствора бензойной кислоты массовой концентрации 5 мг/дм
В мерную колбу вместимостью 100 см помещают 0,5 см
запасного раствора бензойной кислоты массовой концентрации 1,00 г/дм
(см. 6.2.3.2), доводят объем раствора в колбе до метки дистиллированной водой и перемешивают. Срок хранения - 1 мес при комнатной температуре.
6.2.3.4 Приготовление смешанного раствора аргинина и бензойной кислоты
В мерную колбу вместимостью 25 см помещают 5 см
раствора аргинина (см. 6.2.3.1) и 0,625 см
запасного раствора бензойной кислоты (см. 6.2.3.2), доводят объем раствора в колбе до метки дистиллированной водой и перемешивают. Массовые концентрации компонентов составляют: аргинина - 200 мг/дм
, бензойной кислоты - 25 мг/дм
.
Срок хранения - 3 мес при температуре от 4 °С до 6 °С.
6.2.3.5 Приготовление исходной градуировочной смеси N 1
В полиэтиленовом сосуде вместимостью 20 см смешивают по 2 см
запасных растворов лизина, метионина, треонина и цистина (см. 6.2.3.1) и раствора аргинина с бензойной кислотой (см. 6.2.3.4). Массовые концентрации компонентов в растворе, мг/дм
:
- лизина - 500;
- метионина - 200;
- треонина - 200;
- цистина -100;
- аргинина - 40;
- бензойной кислоты - 5.
Срок хранения смеси в герметично закрытой посуде в холодильнике - 1 мес при температуре от 4 °С до 6 °С.
6.2.3.6 Приготовление рабочей градуировочной смеси N 2
В полиэтиленовом сосуде вместимостью 10 см смешивают 1 см
смеси N 1 (см. 6.2.3.5), 0,8 см
смешанного раствора (см. 6.2.3.4) и 3,2 см
дистиллированной воды. Массовые концентрации компонентов в смеси, мг/дм
:
- лизина -100;
- метионина - 40;
- треонина - 40;
- цистина - 20;
- аргинина - 40;
- бензойной кислоты - 5.
Примечания
1 Аргинин введен в состав смеси из-за частичного наложения пиков лизина и аргинина, чтобы нивелировать влияние несимметричности пиков. Бензойная кислота может служить внутренним стандартом и одновременно реперным пиком, облегчающим разметку электрофореграмм.
2 Допускается применение рабочих градуировочных смесей с другими концентрациями АК, при этом массовая концентрация бензойной кислоты должна быть 5 мг/дм.
6.2.4 Подготовка капилляра к работе
6.2.4.1 Подготовка нового капилляра к работе
Подготовку нового капилляра к работе проводят в соответствии с руководством по эксплуатации системы капиллярного электрофореза.
Примечание - Необходимо следить за уровнем жидкости в пробирке для слива. Не допускается перетекание жидкости из пробирки в прибор!
6.2.4.2 Ежедневная подготовка капилляра к работе
Если капилляр оставляли на ночь заполненным дистиллированной водой, то перед работой его необходимо промыть раствором соляной кислоты в течение 10 мин (см. 6.2.1.1), дистиллированной водой в течение 3 мин, раствором гидроокиси натрия в течение не менее 10 мин (см. 6.2.1.2), снова дистиллированной водой 3 мин и затем рабочим буферным раствором (см. 6.2.2.1) в течение 10 мин в условиях, предусмотренных таблицей 3 для режима "Анализ". Затем следует проконтролировать состояние капилляра, проанализировав рабочую градуировочную смесь N 2 (см. 6.2.3.6) с использованием существующей градуировки по 6.2.5.
При этом в первую очередь обращают внимание на воспроизводимость по времени выхода. Если время выхода определяемых компонентов отличается более чем на 5%, капилляр промывают рабочим буферным раствором повторно и снова проверяют стабильность градуировочной характеристики. Если время выхода совпадает, то проверяют найденные концентрации компонентов по 6.2.5.
В том случае, если накануне в капилляре был оставлен раствор ведущего электролита, его не промывают соляной кислотой и гидроокисью натрия. Растворы ведущего электролита в рабочих и промывочных пробирках заменяют свежими порциями и промывают капилляр только раствором ведущего электролита, после чего контролируют стабильность градуировочной характеристики.
6.2.4.3 Хранение капилляра
Порядок хранения капилляра при перерывах в работе зависит от интенсивности использования прибора
При ежедневной работе рекомендуется после окончания последнего анализа промыть капилляр раствором тетраборнокислого натрия молярной концентрации (Na
B
O
·10H
O)=0,02 моль/дм
(см. 6.2.2.1) в течение 10-15 мин и оставить на ночь заполненным этим же раствором.
При перерывах в работе на 2-7 сут капилляр следует промыть дистиллированной водой и оставить заполненным ею же.
При перерывах на срок более недели капилляр необходимо после тщательной промывки дистиллированной водой высушить и оставить в сухом состоянии. В этом случае для восстановления работоспособности капилляра его нужно подготовить к работе как новый капилляр.
6.2.5 Градуировка системы
Градуировку системы капиллярного электрофореза проводят способом одного эталона для каждого из двух условий проведения анализа в соответствии с процедурой, описанной в 6.3.2.
С этой целью не менее трех раз анализируют рабочую градуировочную смесь N 2 в условиях, рекомендованных при определении метионина, аналогичную процедуру осуществляют в условиях, рекомендованных при определении остальных трех аминокислот. Полученные электрофореграммы обрабатываются в соответствии с процедурой градуировки, описанной в руководстве пользователя программы обработки данных ("МультиХром" или аналогичной) и рассчитывают средние величины градуировочных коэффициентов и их среднеквадратичные отклонения (СКО). Градуировку следует считать успешной, если величины СКО не превышают 5%. Выбраковку неудовлетворительных градуировочных точек проводят в том случае, если отклонение площади пика и одновременно времени выхода пика данного компонента превышает 5% среднеарифметических значений.
6.2.6 Контроль стабильности градуировочной характеристики
Каждый раз перед началом проведения измерений необходимо после подготовки капилляра проанализировать рабочую градуировочную смесь N 2. При этом в рабочем журнале фиксируют время выхода определяемых компонентов и их массовые концентрации, рассчитанные по существующей градуировочной характеристике. Градуировку признают стабильной, если отклонение найденных массовых концентраций от заданных значений не превышает 5% для метионина и цистина и 10% для лизина и треонина. В противном случае анализируют рабочую градуировочную смесь N 2 еще два раза. При повторных отклонениях, превышающих указанные нормативы, градуировку системы проводят заново, начиная с приготовления нового раствора рабочей градуировочной смеси N 2.
6.3 Проведение измерений
6.3.1 Проведение гидролиза и получение испытуемого раствора
Навеску исследуемого продукта массой 0,1000 г помещают в стеклянную виалу или ампулу с перетяжкой, добавляют 10 см раствора соляной кислоты молярной концентрации
(HCI)=6 моль/дм
(см. 6.2.1.4). При гидролизе в стеклянной ампуле ее запаивают в пламени газовой горелки в месте перетяжки. Виалу с плотно завинченной крышкой или запаянную ампулу помещают в эксикатор, который ставят в сушильный шкаф на 14-16 ч при температуре 110 °С (оставляют на ночь).
По окончании гидролиза виалу или ампулу вынимают из эксикатора и охлаждают до комнатной температуры. Содержимое слегка перемешивают и фильтруют в коническую колбу со шлифом вместимостью 25 см, отбирают в стеклянную бюксу 1 см
фильтрата и выпаривают досуха в потоке теплого воздуха вентилятора. Бюксу охлаждают при комнатной температуре, сухой остаток растворяют в 1 см
дистиллированной воды (испытуемый раствор).
В зависимости от объекта исследования и предполагаемого содержания АК проводят разбавление испытуемого раствора дистиллированной водой. Рекомендуемые разбавления: для зерновых культур в два раза (соотношение объемов испытуемого раствора и воды 1:1), для продуктов растительного (жмых, шрот) и животного происхождения, а также комбикормов в пять раз (соотношение объемов испытуемого раствора и воды 1:4). Отбор испытуемого раствора и воды производят с помощью микродозаторов или градуированных пипеток.
Критерием оптимальности разбавления является то, что концентрация АК в разбавленном испытуемом растворе не должна превышать их значений в рабочей градуировочной смеси N 2.
0,5 см полученного раствора помещают в пробирку Эппендорфа, центрифугируют для дегазации при 6000 об/мин в течение 5 мин (рабочий испытуемый раствор) и используют для электрофоретического анализа.
Примечание - При возникновении затруднений в разметке пиков АК на электрофореграмме сухой остаток растворяют в 1 см раствора бензойной кислоты массовой концентрации 5 мг/дм
. Разбавление испытуемого раствора проводят раствором бензойной кислоты массовой концентрации 5 мг/дм
(см. 6.2.3.3).
6.3.2 Анализ рабочего испытуемого раствора
Анализ рабочего испытуемого раствора проводят дважды: для определения лизина, треонина и цистина - в среде буферного раствора тетраборнокислого натрия (см. 6.2.2.1) при температуре 20 °С, для определения метионина - в среде буферного раствора тетраборнокислого натрия с добавкой -циклодекстрина (см. 6.2.2.2) при температуре 40 °С. При анализе серии проб рационально проанализировать их сначала при одном составе буфера, а затем, поменяв буфер и температуру, проанализировать те же растворы повторно. Рекомендуемые условия анализа приведены в таблице 3.
Таблица 3 - Условия проведения анализа методом капиллярного электрофореза
Параметр | Определение лизина, треонина и цистина | Определение метионина |
Длина волны, нм | 190-200 нм (конкретное значение устанавливается для каждого прибора по методике, приведенной в приложении Б) | |
Ввод пробы | Пневматический (давление 30 мбар, время 15 с) | |
Режим анализа | Напряжение плюс 20 кВ, время 17 мин (при определении метионина время анализа можно сократить до 10 мин) | |
Рабочий буферный раствор | По 6.2.2.1 | По 6.2.2.2 |
Температура, °С | 20 | 40 |
На электрофореграмме определяемые АК расположены в следующей последовательности: лизин, метионин, треонин, цистин.
6.3.3 Обработка электрофореграмм
По окончании анализа необходимо исправить автоматическую разметку пиков, удалить лишние пики, проверить настройку отчета, обратив особое внимание на то, чтобы метод расчета был установлен "Заказной", и распечатать отчет. Если для какой-либо АК измеренное значение концентрации превосходит ее массовую концентрацию в рабочей градуировочной смеси N 2, то анализ необходимо повторить по 6.3.1, увеличив разбавление испытуемого раствора.
6.4 Обработка результатов измерений
6.4.1 Массовую долю АК , %, вычисляют по формуле
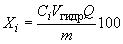 , (1)
, (1)
где - массовая концентрация
-АК, измеренная по 6.3.3, мг/дм
;
- объем гидролизата, 0,01 дм
;
- коэффициент разбавления, равный отношению общего объема испытуемого раствора, полученного после разбавления, к объему взятой для разбавления части;
- масса навески, мг;
100 - коэффициент пересчета в проценты.
6.4.2 Вычисления выполняют до третьего десятичного знака с последующим округлением результатов до второго десятичного знака.
6.5 Оформление результатов измерений
При анализе каждой пробы выполняют два параллельных определения, начиная со взятия навески испытуемой пробы. Если расхождение между результатами параллельных определений не превышает допустимое 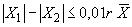 , где
, где ,
,
- результат первого и второго параллельных определений и их среднеарифметическое значение соответственно, то среднеарифметическое значение принимают за результат анализа. В противном случае получают еще два результата определений и вычисляют окончательный результат анализа пробы в соответствии с [1].
Значения повторяемости и воспроизводимости
приведены в таблице 4.
Таблица 4
Наименование определяемого компонента и диапазон измерений | Предел повторяемости (относительное значение допускаемого расхождения между двумя результатами параллельных определений) | Предел воспроизводимости (относительное значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях) |
Лизин, %: | ||
от 0,25 до 1,0 включ. | 56 | 70 |
св. 1,0 " 2,5 " | 42 | 56 |
" 2,5 " 10 " | 28 | 39 |
Метионин, %: | ||
от 0,3 до 1,0 включ. | 56 | 70 |
св. 1,0 " 3,0 " | 42 | 56 |
Треонин, %: | ||
от 0,25 до 1,0 включ. | 56 | 70 |
св. 1,0 " 3,0 " | 42 | 50 |
Цистин, %: | ||
от 0,2 до 2,0 включ. | 56 | 70 |
(Поправка. ИУС N 6-2018).
По полученному результату анализа и значению относительной погрешности () (см. таблицу 1) рассчитывают абсолютную погрешность по формуле
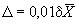 , (2)
, (2)
где - среднеарифметическое значение результатов двух параллельных определений.
Результат измерения представляют в виде 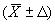 , %. Допускается представление результата в виде
, %. Допускается представление результата в виде 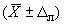 , %, где
, %, где - значение характеристики погрешности результатов измерений, установленное при реализации методики в конкретной лаборатории и обеспечиваемое контролем стабильности результатов измерений, при условии
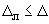 .
.
7 Определение содержания триптофана
7.1 Средства измерения, оборудование, материалы и реактивы
Для проведения измерения дополнительно к указанным в 6.1 должны применяться:
стаканы В(Н)-1-1000ТС по ГОСТ 25336;
колбы с тубусом вместимостью 1000 см по ГОСТ 25336;
воронка Бюхнера по ГОСТ 9147;
кислота серная по ГОСТ 4204, раствор молярной концентрации (H
SO
)=2 моль/дм
;
спирт этиловый ректификованный по ГОСТ 18300;
индикатор метиловый красный;
бария гидроокись 8-водная по ГОСТ 4107;
стандарт триптофана (в форме DL- или L-оптического изомера), сухое вещество, квалификации не ниже ч., "Флука", Швейцария.
Примечание - Требования к обработке посуды и использованию оснастки, необходимой для выполнения измерений, - в соответствии с приложением А.
7.2 Подготовка к измерению
7.2.1 Приготовление раствора соляной кислоты молярной концентрации (HCI)=1 моль/дм
- по 6.2.1.1.
7.2.2 Приготовление раствора гидроокиси натрия молярной концентрации (NaOH)=0,5 моль/дм
- по 6.2.1.2.
7.2.3 Приготовление насыщенного раствора гидроокиси бария для гидролиза
Навеску 8-водного кристаллогидрата гидроокиси бария массой 480 г помещают в химический стакан вместимостью 1000 см, добавляют 780 см
дистиллированной воды и осторожно нагревают до насыщения при температуре от 75 °С до 80 °С. Горячий раствор фильтруют через обеззоленный фильтр "синяя лента" с помощью воронки Бюхнера и колбы с тубусом и переливают в емкость из термостойкого стекла для хранения.
Раствор в горячем виде (нагревают до растворения осадка) применяют на стадии гидролиза проб. При отборе аликвотной порции горячего раствора необходимо использовать стеклянные пипетки или одноразовые полипропиленовые наконечники от микродозаторов (последние меняют после каждого отбора горячего раствора гидроокиси натрия).
7.2.4 Приготовление раствора серной кислоты молярной концентрации (H
SO
)=2 моль/дм
5,5 см концентрированной серной кислоты помещают в мерную колбу вместимостью 50 см
с 10-15 см
дистиллированной воды, доводят до метки дистиллированной водой и перемешивают. Раствор используют для нейтрализации, срок хранения не ограничен при комнатной температуре.
7.2.5 Приготовление раствора метилового красного массовой концентрации 0,5 мг/см
50 мг метилового красного помещают в мерную колбу вместимостью 100 см, приливают 30 см
этилового спирта, доводят до метки дистиллированной водой и тщательно перемешивают. Хранят в стеклянной посуде. Срок хранения не ограничен при комнатной температуре.
7.2.6 Приготовление раствора тетраборнокислого натрия молярной концентрации (Na
B
O
·10H
O)=0,05 моль/дм
- по 6.2.1.3.
7.2.7 Приготовление раствора тетраборнокислого натрия молярной концентрации (Na
B
O
·10H
O)=0,02 моль/дм
- по 6.2.2.1.
Раствор тщательно перемешивают и используют:
- для кондиционирования капилляра;
- для хранения капилляра в нерабочее время;
- в качестве раствора ведущего электролита (рабочего буферного раствора).
7.2.7.1 Подготовка рабочего буферного раствора - по 6.2.2.3.
7.2.8 Приготовление градуировочных растворов
7.2.8.1 Приготовление запасного раствора триптофана массовой концентрации 1,0 мг/см
Навеску триптофана массой 100 мг помещают в мерную колбу вместимостью 100 см, приливают 30-40 см
дистиллированной воды, перемешивают до полного растворения (при необходимости нагревают на водяной бане). Объем в колбе доводят до метки дистиллированной водой и снова перемешивают. Срок хранения в герметично закрытой посуде в холодильнике - 2 мес при температуре от 4 °С до 6 °С.
7.2.8.2 Приготовление запасного раствора триптофана массовой концентрации 0,1 мг/см
5 см запасного раствора триптофана массовой концентрации 1,0 мг/см
(см. 7.2.8.1) помещают в мерную колбу вместимостью 50 см
, доводят дистиллированной водой до метки и перемешивают. Срок хранения в герметично закрытой посуде в холодильнике - 2 мес при температуре от 4 °С до 6 °С.
7.2.8.3 Приготовление градуировочного раствора триптофана массовой концентрации 5 мг/дм
2,5 см запасного раствора триптофана массовой концентрации 0,1 мг/см
(см. 7.2.8.2) помещают в мерную колбу вместимостью 50 см
, доводят дистиллированной водой до метки и перемешивают. Срок хранения в герметично закрытой посуде в холодильнике - 14 сут при температуре от 4 °С до 6 °С.
Для построения градуировочного графика приготовленный раствор анализируют по 7.2.10.
7.2.9 Подготовка капилляра к работе
7.2.9.1 Подготовка нового капилляра к работе - по 6.2.4.1.
7.2.9.2 Ежедневная подготовка капилляра к работе
Если капилляр оставляли на ночь заполненным дистиллированной водой, то перед работой его необходимо промыть гидроокисью натрия (см. 6.2.1.2) и дистиллированной водой по 5 мин и затем раствором ведущего электролита в течение времени, предусмотренного методикой для режима "Анализ". Далее надо проверить состояние капилляра, проанализировав градуировочный раствор триптофана (см. 7.2.8.3). При этом в первую очередь обращают внимание на воспроизводимость времени выхода, а затем - на стабильность градуировочной характеристики.
В том случае, если накануне капилляр был оставлен заполненным раствором ведущего электролита, его не промывают гидроокисью натрия. Растворы ведущего электролита в рабочих и промывочных пробирках заменяют свежими порциями и промывают капилляр только раствором ведущего электролита, после чего контролируют стабильность градуировочной характеристики.
7.2.9.3 Хранение капилляра
При ежедневной работе рекомендуется после окончания последнего анализа промыть капилляр раствором тетраборнокислого натрия молярной концентрации (Na
B
O
·10H
O)=0,02 моль/дм
(см. 6.2.2.1) в течение 10-15 мин и оставить на ночь заполненным этим же раствором.
Примечание - При работе с реальными пробами на электрофореграмме могут наблюдаться дрейф базовой линии, появление ступеней и смещение времен выхода компонентов, что связано с возможным мешающим влиянием матричных компонентов или примесей. В этом случае рекомендуется по окончании работы промыть капилляр дистиллированной водой в течение 2 мин, раствором соляной кислоты (см. 6.2.1.1) - 10 мин, дистиллированной водой - 5 мин, гидроокисью натрия (см. 6.2.1.2) - 10 мин, дистиллированной водой - 5 мин, буферным раствором - 5 мин и оставить на ночь заполненным этим же раствором.
7.2.10 Градуировка системы и контроль стабильности градуировочной характеристики
Градуировку системы капиллярного электрофореза проводят методом одного эталона, анализируя не менее трех раз градуировочный раствор триптофана (см. 7.2.8.3).
7.2.10.1 Ввод градуировочных растворов
Предварительно необходимо промыть капилляр свежей порцией рабочего буферного раствора (см. 7.2.7.1), после чего запустить и перевести в режим ожидания программу "МультиХром".
Рекомендуемые параметры ввода: давление 30 мбар, время ввода 5 с, напряжение 0 кВ.
7.2.10.2 Анализ градуировочных растворов
Рекомендуемые параметры анализа: рабочая длина волны 219 нм; напряжение плюс 20 кВ; температура 40 °С; время анализа 8 мин.
Уровни жидкости в пробирках с буферным раствором на входе и выходе капилляра должны быть одинаковыми, поэтому необходимо через 7-10 анализов пробирки на входе и выходе заново наполнять свежими порциями буферного раствора одинакового объема.
7.2.10.3 Построение градуировочной зависимости
Электрофореграммы, полученные по 7.2.10.2, обрабатывают в соответствии с процедурой градуировки, описанной в руководстве пользователя программы обработки данных ("МультиХром" или аналогичной). С помощью программы рассчитывают среднюю величину градуировочного коэффициента и СКО имеющейся выборки. Градуировку следует считать успешной, если величина СКО не превышает 5%. В противном случае градуировочный раствор анализируют еще несколько раз, дополняя градуировочную таблицу до получения указанной величины СКО. Выбраковку неудовлетворительных градуировочных точек проводят в том случае, если отклонение площади пика и одновременно времени выхода пика триптофана превышает 5% средних значений.
Следует обращать внимание на правильность автоматической разметки начала и конца пика триптофана и при необходимости дополнительно пользоваться ручной разметкой.
7.2.10.4 Контроль стабильности градуировочной характеристики
Контроль стабильности градуировочной характеристики проводят непосредственно перед измерениями испытуемых растворов путем записи электрофореграммы градуировочного раствора (см. 7.2.8.3).
Градуировку признают стабильной, если отклонение найденной массовой концентрации от заданного значения не превышает 5%. В противном случае анализируют градуировочный раствор еще два раза. При повторных отклонениях, превышающих указанные нормативы хотя бы один раз, градуировку системы проводят заново, начиная с приготовления нового запасного раствора (см. 7.2.8.1).
7.3 Проведение испытания
7.3.1 Проведение гидролиза и получение испытуемого раствора
Навеску исследуемого продукта массой 0,1000 г помещают в стеклянную виалу или ампулу с перетяжкой (см. 6.3.1), добавляют 5 см раствора гидроокиси бария (см. 7.2.3). Виалу с плотно завинченной крышкой или запаянную ампулу помещают в эксикатор, который ставят в сушильный шкаф на 14-16 ч при температуре 110 °С (оставляют на ночь).
По окончании гидролиза горячий гидролизат из виалы или ампулы количественно переносят в мерную колбу вместимостью 100 см, в которую предварительно помещено 40-50 см
дистиллированной воды, добавляют 1-3 капли индикатора метилового красного (см. 7.2.5) и нейтрализуют раствор, добавив сначала 3,5 см
раствора серной кислоты (см. 7.2.4), а затем добавляют раствор серной кислоты по каплям до перехода окраски из желтой в розовую. Затем доводят объем раствора до метки дистиллированной водой, перемешивают, оставляют на 10-15 мин до просветления раствора над осадком сульфата бария. 1,0 см
полученного раствора помещают в пробирку Эппендорфа, центрифугируют 2-3 мин при 6000 об/мин, после чего 0,5 см
раствора переносят в сухую пробирку Эппендорфа и используют для анализа (испытуемый раствор).
7.3.2 Анализ испытуемого раствора
Для каждой пробы записывают не менее двух электрофореграмм. Параметры ввода и анализа испытуемого раствора - по 7.2.10.1, 7.2.10.2. По окончании анализа проверяют правильность идентификации и разметки пиков, после чего формируют отчет с указанием метода расчета "Заказной".
Примечание - На электрофореграмме пробы могут наблюдаться пики, соответствующие другим аминокислотам, в частности метионину, поведение которого в рамках данной методики не рассматривается, поскольку известно, что происходит частичная потеря этой аминокислоты при щелочном гидролизе. Показано отсутствие мешающего влияния сопутствующих аминокислот количественному определению триптофана.
7.4 Обработка результатов
7.4.1 Массовую долю триптофана , %, вычисляют по формуле
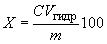 , (3)
, (3)
где - массовая концентрация триптофана в испытуемом растворе, измеренная по 7.3.2, мг/дм
;
- объем испытуемого раствора, 0,1 дм
;
- масса навески, 100 мг;
100 - коэффициент пересчета в проценты.
7.4.2 Вычисления выполняют с точностью до третьего десятичного знака с последующим округлением результатов до второго десятичного знака.
7.5 Оформление результатов
При анализе каждой пробы выполняют два параллельных определения, начиная со взятия навески испытуемой пробы. Если расхождение между результатами параллельных определений не превышает допустимое 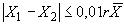 , где
, где ,
,
- результат первого и второго параллельных определений и их среднеарифметическое значение соответственно, то среднеарифметическое значение принимают за результат анализа. В противном случае получают еще два результата определений и вычисляют окончательный результат анализа пробы по [1].
Значения повторяемости и воспроизводимости
приведены в таблице 5.
Таблица 5
Диапазон измерений, % | Предел повторяемости (относительное значение допускаемого расхождения между двумя результатами параллельных определений) | Предел воспроизводимости (относительное значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях) |
От 0,1 до 2,0 включ. | 31 | 42 |
(Поправка. ИУС N 6-2018).
По полученному результату анализа и значению относительной погрешности () (см. таблицу 1) рассчитывают абсолютную погрешность по формуле
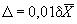 , (4)
, (4)
где - среднеарифметическое значение результатов двух параллельных определений.
Результат измерения представляют в виде 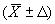 , %. Допускается представление результата в виде
, %. Допускается представление результата в виде 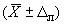 , %, где
, %, где - значение характеристики погрешности результатов измерений, установленное при реализации методики в конкретной лаборатории и обеспечиваемое контролем стабильности результатов измерений, при условии
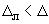 .
.
8 Контроль качества результатов измерений
8.1 Контроль качества результатов измерений предусматривает:
- контроль исполнителем процедуры выполнения измерений на основе оценки погрешности измерений при реализации отдельной контрольной процедуры;
- контроль стабильности результатов измерений на основе контроля стабильности СКО повторяемости, СКО промежуточной (внутрилабораторной) прецизионности и погрешности.
8.2 Контроль исполнителем процедуры выполнения измерений проводят с использованием образцов для контроля. В качестве таких образцов применяют (в порядке понижения приоритетности) стандартные образцы состава анализируемой продукции; образцы, для которых содержание анализируемых компонентов установлено на основании межлабораторного сличительного эксперимента; образцы, для которых содержание аминокислот установлено в данной лаборатории стандартизованными методами; образцы, многократно проанализированные в лаборатории данным методом.
Сравнивают результат контрольной процедуры с нормативом контроля
. Результат контрольной процедуры вычисляют по формуле
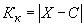 , (5)
, (5)
где - опорное (аттестованное) значение, %;
- результат измерения содержания аминокислот в образце для контроля, %.
В качестве норматива контроля принимают значение характеристики погрешности измерений, установленное в лаборатории при реализации методики (
, %); если эти значения еще не установлены (например, при освоении методики), то вместо
используют значение
. Качество контрольной процедуры признают удовлетворительным, если
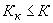 . При невыполнении этого неравенства процедуру контроля повторяют. При повторном неудовлетворительном результате находят и устраняют причины, приводящие к неудовлетворительным результатам.
. При невыполнении этого неравенства процедуру контроля повторяют. При повторном неудовлетворительном результате находят и устраняют причины, приводящие к неудовлетворительным результатам.
Периодичность контроля исполнителем процедуры выполнения измерений на основе оценки погрешности измерений при реализации отдельной контрольной процедуры, а также реализуемые процедуры контроля стабильности результатов измерений регламентируют в руководстве по качеству лаборатории*.
________________
* Документ в информационных продуктах не содержится. За информацией о документе Вы можете обратиться в Службу поддержки пользователей. - .
8.3 Расхождение между результатами, полученными в двух лабораториях, не должно превышать предела воспроизводимости (см. таблицу 5). При выполнении этого условия приемлемы оба результата измерений, и в качестве окончательного может быть использовано их среднее значение.
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений по [1].
Приложение А (обязательное). Требования к обработке посуды и использованию оснастки, необходимой для выполнения измерений
Приложение А
(обязательное)
При выполнении измерений массовой доли АК необходимо тщательно соблюдать чистоту химической посуды, руководствуясь следующими правилами.
А.1 Необходимо иметь отдельный набор посуды, который используют только для определения аминокислот.
А.2 Для мытья химической посуды разрешается использовать концентрированную серную кислоту или концентрированную азотную кислоту. Категорически запрещается использовать для мытья щелочь, хромовую смесь. Посуду многократно ополаскивают дистиллированной водой.
А.3 Категорически запрещается при работе с пробами применять насадки к дозатору, которые использовали для приготовления градуировочных смесей.
А.4 Для каждого раствора необходимо использовать свой наконечник. Раствор из колбы наливают в стаканчик или одноразовую пробирку и из него отбирают аликвотную порцию. Запрещается погружать насадку во весь объем раствора во избежание загрязнения.
А.5 Насадки для дозаторов и пробирки для анализа можно использовать неоднократно. Для этого их выдерживают в дистиллированной воде в течение суток, многократно ополаскивают, затем кипятят на плитке в дистиллированной воде в течение часа, далее высушивают на воздухе. Желательно пробирки и насадки, используемые для концентрированных растворов и для растворов малых концентраций, обрабатывать отдельно.
А.6 Виалы, крышки и прокладки после гидролиза моют с помощью ерша водопроводной водой, затем виалы заливают на 30 мин соляной кислотой (1:1), споласкивают водопроводной, а затем дистиллированной водой и сушат.
Приложение Б (рекомендуемое). Методика определения оптимальной рабочей длины волны при анализе аминокислот
Приложение Б
(рекомендуемое)
Для определения аминокислот желательно выбирать наименьшую длину волны, т.к. интенсивность поглощения тем больше, чем короче длина волны (в спектральной области 190-200 нм). С другой стороны, при уменьшении длины волны уменьшается как интенсивность светового потока лампы, так и чувствительность фотоприемника. В результате возрастает шум базовой линии электрофореграммы, который ограничивает нижний предел определяемых концентраций. В связи с этим для каждого прибора должна быть экспериментально определена оптимальная рабочая длина волны, при которой достигается максимальное соотношение полезного аналитического сигнала (высоты пика) и размаха шумовой характеристики, на фоне которой необходимо надежно выделять пик искомого компонента при его минимальной концентрации.
После проведения автоматической градуировки монохроматора и приготовления растворов проводят анализ рабочей градуировочной смеси N 2 по принятой процедуре при различных длинах волн от 190 до 200 нм с шагом 2 нм. Концентрацию аминокислот в смеси выбирают так, чтобы на электрофореграмме без изменения масштаба можно было бы измерить как высоты пиков, так и размах шумовой дорожки. Далее вычисляют для каждой длины волны отношение высоты пика к размаху шумовой дорожки (от минимума до максимума). Оптимальной длиной волны считают ту, при которой величина этого отношения имеет максимальное значение.
Библиография
[1] ИСО 5725-6:94 | Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике |
Электронный текст документа
и сверен по:
официальное издание
М.: Стандартинформ, 2012
Редакция документа с учетом
изменений и дополнений подготовлена

