ГОСТ 31483-2012
Группа С19
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРЕМИКСЫ
Определение содержания витаминов: B (тиаминхлорида), B
(рибофлавина), B
(пантотеновой кислоты), B
(никотиновой кислоты и никотинамида), B
(пиридоксина), B
(фолиевой кислоты), C (аскорбиновой кислоты) методом капиллярного электрофореза
Premixes. Determination of vitamins: B (thiaminchloride), B
(riboflavin), B
(pantothenic acid), B
(nicotinic acid and nicotinamide), B
(pyridoxine), B
(folic acid), C (ascorbic acid) content by method of capillary electrophoresis
МКС 65.120
Дата введения 2013-07-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Открытым акционерным обществом "Всероссийский научно-исследовательский институт комбикормовой промышленности" (ОАО "ВНИИКП"), Научно-производственной фирмой аналитического приборостроения "Люмэкс" (НПФ АП "Люмэкс")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол N 41 от 23-24 мая 2012 г.)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны | Сокращенное наименование национального органа по стандартизации |
Азербайджан | AZ | Азгосстандарт |
Армения | AM | Минэкономикии Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Кыргызстан | KG | Кыргызстандарт |
Российская Федерация | RU | Росстандарт |
Таджикистан | TJ | Таджикстандарт |
(Поправка. ИУС N 6-2019).
4 Приказом Федерального агентства по техническому регулированию и метрологии от 8 октября 2012 г. N 471-ст межгосударственный стандарт ГОСТ 31483-2012 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2013 г.
5 Стандарт подготовлен на основе применения ГОСТ Р 52741-2007
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта публикуется в указателе "Национальные стандарты".
Информация об изменениях к настоящему стандарту публикуется в указателе "Национальные стандарты", а текст изменений - в информационных указателях "Национальные стандарты". В случае пересмотра или отмены настоящего стандарта соответствующая информация будет опубликована в информационном указателе "Национальные стандарты"
ВНЕСЕНА поправка, опубликованная в ИУС N 6, 2019 год с учетом уточнения, опубликованного в ИУС 11-2019
Поправка внесена изготовителем базы данных
1 Область применения
1 Область применения
Настоящий стандарт распространяется на премиксы и устанавливает метод капиллярного электрофореза для определения содержания водорастворимых витаминов: B (тиаминхлорида), B
(рибофлавина), B
(пантотеновой кислоты), B
(никотиновой кислоты и никотинамида), B
(пиридоксина), B
(фолиевой кислоты), С (аскорбиновой кислоты).
В зависимости от состава анализируемой пробы и точности измерений используют два варианта метода капиллярного электрофореза:
- метод капиллярного зонного электрофореза (далее - КЗЭ); не применяют для определения витамина B в форме никотинамида и для определения витамина B
(рибофлавина) из-за большой погрешности;
- метод мицеллярной электрокинетической хроматографии (далее - МЭКХ); не применяют для определения витамина B (тиаминхлорида) из-за большой погрешности.
Идентификацию и количественное определение анализируемых витаминов проводят с помощью установленного программного обеспечения.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.018-93 Система стандартов безопасности труда. Пожаровзрывобезопасность статического электричества. Общие требования
ГОСТ 12.1.019-79* Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
________________
* На территории Российской Федерации документ не действует. Действует ГОСТ Р 12.1.019-2009, здесь и далее по тексту. - .
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ 4199-76 Реактивы. Натрий тетраборнокислый 10-водный. Технические условия
ГОСТ 4328-77 Натрия гидроокись. Технические условия
ГОСТ 5644-75 Сульфит натрия безводный. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9656-75 Реактивы. Кислота борная. Технические условия
ГОСТ 13496.0-80* Комбикорма, сырье. Методы отбора проб
________________
* На территории Российской Федерации документ не действует. Действует ГОСТ Р ИСО 6497-2011, здесь и далее по тексту. - .
ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия
ГОСТ 22180-76 Кислота щавелевая. Технические условия
ГОСТ 24104-2001* Весы лабораторные. Общие технические требования
________________
* На территории Российской Федерации документ не действует. Действует ГОСТ Р 53228-2008 , здесь и далее по тексту. - .
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов по указателю "Национальные стандарты", составленному по состоянию на 1 января текущего года, и по соответствующим информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Диапазоны измерений содержания витаминов и метрологические характеристики метода для двух вариантов
Диапазоны измерений содержания витаминов и значения показателей повторяемости, воспроизводимости и точности при вероятности 0,95 приведены в таблице 1.
Таблица 1
Наименование определяемого компонента и диапазон измерений, г/кг | Вариант метода капиллярного электрофореза | Показатель повторяемости (относительное среднеквадратичное отклонение повторяемости) | Показатель воспроизводимости (относительное среднеквадратичное отклонение воспроизводимости) | Показатель точности (границы относительной погрешности) |
| КЗЭ | 6 | 10 | 20 |
МЭКХ | 11 | 17 | 34 | |
| КЗЭ | 10 | 21 | 42 |
МЭКХ | 8 | 14 | 28 | |
| КЗЭ, МЭКХ | 5 | 10 | 20 |
| КЗЭ, МЭКХ | 5 | 9 | 18 |
| МЭКХ | 9 | 14 | 28 |
| КЗЭ, МЭКХ | 6 | 10 | 20 |
| КЗЭ, МЭКХ | 7 | 10 | 20 |
C (аскорбиновая кислота) от 2,0 до 50,0 включ. | КЗЭ, МЭКХ | 7 | 17 | 34 |
4 Требования техники безопасности
4.1 При проведении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007, требования пожарной безопасности по ГОСТ 12.1.004, ГОСТ 12.1.018 и требования электробезопасности при работе с электроустановками по ГОСТ 12.1.019.
4.2 Помещение, в котором проводят измерения, должно быть снабжено приточно-вытяжной вентиляцией. Работу с реактивами необходимо проводить в вытяжном шкафу.
4.3 При работе с концентрированными кислотами и щелочами и при приготовлении растворов витаминов необходимо использовать респираторы и резиновые перчатки.
5 Отбор и подготовка проб
5.1 Отбор проб - по ГОСТ 13496.0.
5.2 Подготовка пробы к анализу - по [1].
6 Определение содержания витаминов
6.1 Средства измерений, оборудование, материалы и реактивы
Система капиллярного электрофореза, снабженная кварцевым капилляром (полная длина 75 см, эффективная длина 65 см, внутренний диаметр 50 мкм), типа "Капель-105" с версией ПЗУ 5.16.6.
Весы лабораторные по ГОСТ 24104 с пределом допускаемой абсолютной погрешности однократного взвешивания не более ±0,001 и ±0,02 г.
Холодильник бытовой по ГОСТ 16317 любой марки.
рН-метр лабораторный (основная погрешность измерения - не более ±0,05 ед. рН).
Центрифуга лабораторная марки ШХ 2.779.040 со скоростью вращения не менее 5000 об/мин.
Шкаф сушильный лабораторный с терморегулятором, обеспечивающим поддержание температуры (150±2) °С.
Электроплитка бытовая по ГОСТ 14919.
Устройство перемешивающее по техническому документу.
Баня водяная с регулятором нагрева.
Пробирки центрифужные полипропиленовые.
Микродозаторы переменного объема 10-100 мм, 100-1000 мм
,1000-5000 мм
и с пределом допускаемой погрешности измерения не более ±5% по техническому документу.
Наконечники полипропиленовые для микродозаторов вместимостью 0,3 см; 1,0 см
и 5,0 см
.
Пробирки для микропроб однократного применения (типа Эппендорфа) вместимостью 1,5 см по техническому документу.
Сосуды из темного стекла с герметично завинчивающимися крышками и тефлоновыми прокладками вместимостью 10-40 см для приготовления запасных растворов витаминов.
Колбы плоскодонные с притертыми пробками Кн-2-50-18 (22) по ГОСТ 25336.
Стаканы химические В-1-100(150, 250) ТС по ГОСТ 25336.
Колбы мерные 2-25(50, 100)-2 по ГОСТ 1770.
Цилиндры 1(3)-10(25) по ГОСТ 1770.
Пипетки градуированные 1(2,3,5)-1(1а,2,2а)-2-1(5,10) по ГОСТ 29227.
Фильтры целлюлозно-ацетатные, размер пор 0,2 мкм, диаметр 25 мм.
Насадки для фильтров.
Натрия гидроокись по ГОСТ 4328, раствор молярной концентрации 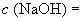 0,5 моль/дм
0,5 моль/дм.
Кислота соляная по ГОСТ 3118, растворы молярных концентраций 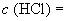 6 моль/дм
6 моль/дм,
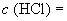 1 моль/дм
1 моль/дм,
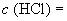 0,2 моль/дм
0,2 моль/дм, объемной концентрации 1%.
Кислота борная по ГОСТ 9656, раствор молярной концентрации 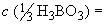 0,2 моль/дм
0,2 моль/дм.
Натрия сульфит безводный по ГОСТ 5644, раствор молярной концентрации 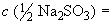 0,1 моль/дм
0,1 моль/дм.
Кислота щавелевая по ГОСТ 22180 или кислота щавелевая 2-водная, раствор с массовой долей 1%.
Натрий тетраборнокислый, стандарт-титр или натрий тетраборнокислый 10-водный по ГОСТ 4199, растворы молярных концентраций 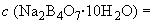 0,05 моль/дм
0,05 моль/дм и
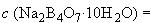 0,01 моль/дм
0,01 моль/дм.
Натрия додецилсульфат, фирма "Fluka" (кат. N 71729).
Витамин B (тиаминхлорид гидрохлорид), фирма "ICN" (кат. N 103028).
Витамин B (рибофлавин), фирма "ICN" (кат. N 102813).
Витамин B (DL-пантотеновая кислота, кальциевая соль), фирма "Sigma" (кат. N 9153).
Витамин B (никотиновая кислота), фирма "ICN" (кат. N 102446).
Витамин B (никотинамид), фирма "ICN" (кат. N 102447).
Витамин B (пиридоксин гидрохлорид), фирма "ICN" (кат. N 102777).
Витамин B (фолиевая кислота), фирма "ICN" (кат. N 101725).
Витамин C (L-аскорбиновая кислота), фирма "ICN" (кат. N 100769).
Вода дистиллированная по ГОСТ 6709.
Примечания
1 Допускается применение средств измерений и оборудования с такими же или лучшими метрологическимии техническими характеристиками, а также материалов и реактивов, по качеству не ниже вышеуказанных.
2 Все реактивы должны быть квалификации х. ч. или ч. д. а.
6.2 Подготовка к проведению измерений
6.2.1 Приготовление вспомогательных растворов
6.2.1.1 Приготовление раствора соляной кислоты молярной концентрации 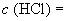 6 моль/дм
6 моль/дм
50 см концентрированной соляной кислоты смешивают в химическом стакане вместимостью 200 см
с 50 см
дистиллированной воды. Смесь переносят в стеклянную емкость с притертой пробкой для хранения. Срок хранения не ограничен.
6.2.1.2 Приготовление раствора соляной кислоты молярной концентрации 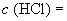 1 моль/дм
1 моль/дм
17 см раствора соляной кислоты, приготовленного по 6.2.1.1, смешивают в химическом стакане вместимостью 200 см
с 83 см
дистиллированной воды. Смесь переносят в стеклянную емкость с притертой пробкой для хранения. Срок хранения не ограничен.
6.2.1.3 Приготовление раствора гидроокиси натрия молярной концентрации 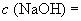 0,5 моль/дм
0,5 моль/дм
Навеску гидроокиси натрия массой 2,000 г растворяют в мерной колбе вместимостью 100 см с 50-60 см
дистиллированной воды и объем в колбе доводят дистиллированной водой до метки. Раствор перемешивают и хранят в емкости из полиэтилена с плотно завинчивающейся крышкой. Срок хранения - 2 мес.
Примечание - Растворы по 6.2.1.2-6.2.1.3 предназначены только для промывок капилляра.
6.2.1.4 Приготовление раствора борной кислоты молярной концентрации 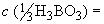 0,2 моль/дм
0,2 моль/дм
Навеску борной кислоты массой 1,236 г растворяют в мерной колбе вместимостью 100 см в 50-60 см
дистиллированной воды, доводят объем раствора в колбе до метки дистиллированной водой и перемешивают. Раствор хранят в емкости из полиэтилена с плотно завинчивающейся крышкой. Срок хранения - 2 мес.
6.2.1.5 Приготовление раствора соляной кислоты объемной концентрации 1%
3 см раствора соляной кислоты, приготовленной по 6.2.1.1, растворяют в 98 см
дистиллированной воды в стеклянной емкости вместимостью 100-150 см
и тщательно перемешивают. Раствор хранят в стеклянной емкости с притертой пробкой. Срок хранения не ограничен.
6.2.1.6 Приготовление раствора щавелевой кислоты с массовой долей 1%
Навеску безводной щавелевой кислоты массой 1,000 г или 2-водной щавелевой кислоты массой 1,400 г растворяют в мерной колбе вместимостью 100 см в дистиллированной воде, доводят объем раствора в колбе до метки дистиллированной водой и перемешивают. Раствор хранят в стеклянной емкости с притертой пробкой. Срок хранения не ограничен.
6.2.1.7 Приготовление раствора тетраборнокислого натрия молярной концентрации 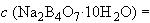 0,05 моль/дм
0,05 моль/дм
Раствор готовят из стандарт-титра по прилагаемой к нему инструкции и хранят в полиэтиленовой емкости с плотно завинчивающейся крышкой. Срок хранения - 2 мес.
Примечание - При отсутствии стандарт-титра раствор готовят из 10-водного тетраборнокислого натрия. Для этого навеску препарата массой 19,071 г растворяют в мерной колбе вместимостью 1 дм в свежепрокипяченной и охлажденной без доступа воздуха дистиллированной воде. рН раствора при 20 °С должен быть 9,22±0,10.
6.2.1.8 Приготовление раствора тетраборнокислого натрия молярной концентрации 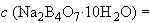 0,01 моль/дм
0,01 моль/дм
20 см раствора тетраборнокислого натрия, приготовленного по 6.2.1.7, помещают в мерную колбу вместимостью 100 см
, доводят объем в колбе до метки дистиллированной водой и тщательно перемешивают. Раствор хранят в полиэтиленовой емкости с плотно завинчивающейся крышкой. Срок хранения - 2 мес.
6.2.1.9 Приготовление ведущего электролита N 1
40 см тетраборнокислого натрия, приготовленного по 6.2.1.7, помещают в химический стакан вместимостью 100 см
, добавляют 20 см
раствора борной кислоты (см. 6.2.1.4) и тщательно перемешивают. Раствор хранят в стеклянной емкости с притертой пробкой. Срок хранения - 2 мес.
6.2.1.10 Приготовление ведущего электролита N 2
Навеску додецилсульфата натрия массой 0,576 г помещают в мерную колбу вместимостью 25 см, добавляют 15-17 см
ведущего электролита N 1 (см. 6.2.1.9) и перемешивают. Доводят объем в колбе до метки этим же раствором, снова перемешивают. Раствор хранят в стеклянной емкости с притертой пробкой. Срок хранения - 1 мес.
6.2.1.11 Подготовка растворов ведущих электролитов для проведения измерений
Непосредственно перед началом измерений растворы ведущих электролитов необходимо:
- профильтровать через ацетатно-целлюлозный фильтр, отбросив первые порции фильтрата (1-1,5 см);
- дегазировать центрифугированием в течение 3-5 мин при скорости вращения 5000 об/мин.
6.2.1.12 Приготовление раствора сульфита натрия молярной концентрации 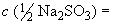 0,1 моль/дм
0,1 моль/дм
Навеску безводного сульфита натрия массой 0,630 г помещают в мерную колбу вместимостью 50 см, добавляют 20-30 см
дистиллированной воды, перемешивают до полного растворения препарата и доводят объем раствора в колбе дистиллированной водой до метки.
Раствор используют только в день приготовления, поэтому указанный выше объем (50 см) не является строго определенным. Его изменяют в зависимости от интенсивности использования раствора в течение предстоящего рабочего дня.
6.2.1.13 Приготовление экстрагирующего раствора для получения вытяжки витаминов из испытуемых проб
Раствор тетраборнокислого натрия (см. 6.2.1.7) смешивают с раствором сульфита натрия (см. 6.2.1.12) в соотношении 3:2 в химическом стакане вместимостью 250 см. Раствор хранят в стеклянной емкости с притертой пробкой и используют только в день приготовления.
6.2.2 Подготовка капилляра к работе
6.2.2.1 Подготовка нового капилляра к работе
Подготовку нового капилляра к работе проводят в соответствии с руководством по эксплуатации системы капиллярного электрофореза.
Примечание - Необходимо следить за уровнем жидкости в пробирке для слива. Не допускается перетекание жидкости из пробирки в прибор!
6.2.2.2 Ежедневная подготовка капилляра к работе
Если капилляр оставляли на ночь заполненным дистиллированной водой, то перед работой его необходимо промыть раствором гидроокиси натрия (см. 6.2.1.3) и дистиллированной водой по 5 мин, затем раствором соответствующего ведущего электролита в течение времени, предусмотренного методикой для режима "Анализ".
В том случае, если накануне в капилляре был оставлен раствор ведущего электролита, то на следующий день в зависимости от предстоящего метода определения витаминов капилляр промывают следующим образом:
- при работе методом зонного электрофореза - свежей порцией ведущего электролита (см. 6.2.1.9) в течение 10-15 мин без напряжения;
- при работе методом мицеллярной электрокинетической хроматографии следует проводить последовательную промывку дистиллированной водой, раствором гидроокиси натрия (см. 6.2.1.3) и снова дистиллированной водой по 5 мин, а затем ведущим электролитом (см. 6.2.1.10) в течение 10-15 мин без напряжения.
Во всех случаях далее следует проверять состояние капилляра, проанализировав контрольный раствор (см. 6.2.3.6). При этом в первую очередь обращают внимание на стабильность времени выхода, а затем на стабильность градуировочной характеристики (см. 6.2.5).
Если проверка стабильности градуировочной характеристики неудовлетворительная, то следует промыть капилляр соответствующим ведущим электролитом под напряжением 25 кВ в течение 5-10 мин и повторить проверку стабильности градуировочной характеристики.
Между анализами капилляр промывают соответствующим ведущим электролитом в течение 3 мин.
После работы с испытуемыми образцами в конце рабочего дня необходимо проводить последовательную промывку капилляра дистиллированной водой в течение 10 мин, раствором соляной кислоты (см. 6.2.1.2) и дистиллированной водой по 5 мин, а затем раствором гидроокиси натрия (см. 6.2.1.3) и дистиллированной водой по 10 мин.
При определении витаминов методом МЭКХ капилляр оставляют на ночь заполненным дистиллированной водой.
При определении витаминов методом КЗЭ капилляр промывают ведущим электролитом N 1 (см. 6.2.1.9) в течение 10-15 мин и оставляют на ночь с этим же раствором.
Примечание - При работе с испытуемыми пробами на электрофореграмме может наблюдаться дрейф базовой линии, появление ступеней и смещение времени выхода компонентов, что связано с возможным мешающим влиянием матричных компонентов или примесей. В этом случае рекомендуется:
- во время проведения анализов увеличить время промывки капилляра между анализами;
- проводить промывку в течение 3 мин под напряжением;
- при появлении ступеней заменить свежими порциями ведущий электролит в пробирках.
6.2.2.3 Хранение капилляра
Порядок хранения капилляра при перерывах в работе зависит от интенсивности использования прибора.
При перерывах в работе на 2-3 сут (до недели) капилляр следует промыть дистиллированной водой и оставить заполненным дистиллированной водой.
При перерывах на срок более недели капилляр необходимо после тщательной промывки дистиллированной водой высушить и оставить в сухом состоянии. В этом случае для восстановления работоспособности капилляра его нужно подготовить к работе, как новый капилляр.
6.2.3 Приготовление градуировочных растворов
6.2.3.1 Приготовление запасных растворов витаминов B (тиаминхлорида), B
(пантотеновой кислоты), B
(никотиновой кислоты), B
(никотинамида), B
(пиридоксина) номинальных значений массовых концентраций 1 мг/см
Навески витаминов в соответствии с таблицей 2 вносят в отдельные емкости из темного стекла и растворяют в 5 см дистиллированной воды. Растворы хранят в герметично закрытых емкостях в холодильнике. Срок хранения - 3 месяца.
Таблица 2 - Рекомендуемые навески с учетом форм витаминов, необходимых для приготовления запасных растворов, и коэффициенты пересчета навески на массу соответствующего витамина
Витамин в форме взвешивания | Масса навески | Коэффициент пересчета |
| 0,0056 | 0,893 |
| 0,0050 | 1,000 |
| 0,0054 | 0,916 |
| 0,0050 | 1,000 |
| 0,0050 | 1,000 |
| 0,0061 | 0,823 |
| 0,0050 | 1,000 |
С (аскорбиновая кислота) | 0,0100 | 1,000 |
Массовые концентрации витаминов в каждом растворе , мг/см
, вычисляют по формуле
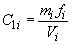 , (1)
, (1)
где - масса навески соответствующего витамина в форме взвешивания, мг;
- коэффициент пересчета массы навески на массу соответствующего витамина;
- объем запасного раствора соответствующего витамина, см
.
6.2.3.2 Приготовление запасного раствора витамина B (фолиевой кислоты) номинального значения массовой концентрации 0,5 мг/см
Навеску фолиевой кислоты массой в соответствии с таблицей 2 вносят в емкость из темного стекла вместимостью 10-15 см, добавляют 10 см
раствора тетраборнокислого натрия (см. 6.2.1.8) и тщательно перемешивают до полного растворения навески. Массовую концентрацию витамина B
(фолиевой кислоты) в полученном растворе вычисляют по формуле (1). Раствор хранят в герметично закрытой емкости в холодильнике. Срок хранения - 1 мес.
6.2.3.3 Приготовление запасного раствора витамина С (аскорбиновой кислоты) номинального значения массовой концентрации 2 мг/см
Навеску аскорбиновой кислоты массой в соответствии с таблицей 2 вносят в емкость из темного стекла вместимостью 10-15 см, добавляют 1 см
раствора соляной кислоты (см. 6.2.1.5), 4 см
раствора щавелевой кислоты (см. 6.2.1.6) и перемешивают до полного растворения навески. Массовую концентрацию витамина С (аскорбиновой кислоты) в полученном растворе вычисляют по формуле (1). Раствор хранят в герметично закрытой емкости в холодильнике. Срок хранения - одна неделя.
6.2.3.4 Приготовление запасного раствора витамина B (рибофлавина) номинального значения массовой концентрации 0,5 мг/см
Навеску рибофлавина массой в соответствии с таблицей 2 вносят в емкость из темного стекла вместимостью 10-15 см, добавляют 0,2 см
раствора соляной кислоты (см. 6.2.1.1), перемешивают до полного растворения навески, добавляют 8 см
раствора щавелевой кислоты (см. 6.2.1.6), 1,8 см
дистиллированной воды и тщательно перемешивают. В случае неполного растворения навески следует нагреть раствор в закрытом сосуде на водяной бане при температуре не выше 80 °С. Массовую концентрацию витамина B
(рибофлавина) в полученном растворе вычисляют по формуле (1). Раствор хранят в герметично закрытой емкости в холодильнике. Срок хранения - 1 мес.
6.2.3.5 Приготовление градуировочных растворов витаминов
Запасные растворы витаминов помещают в стеклянную емкость в объемах, указанных в таблице 3. Добавляют 1065 мм раствора тетраборнокислого натрия (см. 6.2.1.8), 240 мм
раствора щавелевой кислоты (см. 6.2.1.6), 60 мм
раствора соляной кислоты (см. 6.2.1.5) и тщательно перемешивают. Массовые концентрации витаминов в градуировочном растворе
, мг/дм
, вычисляют по формуле
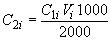 , (2)
, (2)
где - массовая концентрация соответствующего витамина в запасном растворе, мг/см
;
- объем запасного раствора соответствующего витамина, мм
;
1000 - коэффициент пересчета см в дм
;
2000 - общий объем градуировочного раствора, мм.
Примечание - Градуировочный раствор используют в течение 2 ч с момента приготовления.
Таблица 3 - Объемы запасных растворов витаминов, используемые для приготовления градуировочных растворов
Витамин | Объем запасного раствора, мм |
| 100 |
| 90 |
| 70 |
| 80 |
| 25 |
| 15 |
| 205 |
С (аскорбиновая кислота) | 50 |
Итого | 635 |
6.2.3.6 Приготовление рабочего контрольного раствора витаминов
В пробирку типа Эппендорфа помещают 20 мм запасного раствора пиридоксина и 40 мм
запасного раствора рибофлавина, специально приготовленных для этой цели по 6.2.3.1 и 6.2.3.4 соответственно. Добавляют 940 мм
раствора тетраборнокислого натрия (см. 6.2.1.8) и перемешивают. Массовые концентрации витаминов в рабочем контрольном растворе вычисляют по формуле (2). Раствор следует использовать в течение 2 ч с момента приготовления.
Рабочий контрольный раствор витаминов используют для проверки работоспособности прибора и для контроля стабильности градуировочной характеристики (см. 6.2.5).
6.2.4 Градуировка системы
6.2.4.1 Градуировка системы методом капиллярного зонного электрофореза
Рекомендуемые параметры ввода и условия анализа представлены в таблице 4. Непосредственно перед анализом растворы центрифугируют в течение 5 мин при 5000-6000 об/мин.
Таблица 4 - Условия анализа градуировочного раствора методом КЗЭ
Определяемые витамины в порядке выхода | Тиамин ( |
Ввод градуировочного раствора (пробы) | 30 мбар, 20 с |
Условия анализа | |
Длина волны, нм | 200 |
Напряжение, кВ | +25 |
Давление, мбар | В начале анализа - 0 мбар, после появления пика пиридоксина прикладывают давление 30 мбар до конца анализа |
Температура, °С | 30 |
Время, мин | 16-18 |
Ведущий электролит | N 1 (см. 6.2.1.9) |
При выполнении анализа необходимо изменение условий регистрации электрофореграммы, а именно приложения давления после появления пика пиридоксина.
Для определения момента времени, по истечении которого необходимо приложить давление, готовят пробный раствор витаминов в соответствии с 6.2.3.5 и снимают пробную электрофореграмму. В этом случае после регистрации пиридоксина (3-го компонента анализируемого раствора) в ручном режиме задают давление 30 мбар и ведут анализ до появления пика последнего компонента (фолиевой кислоты) пробы. Для этого без остановки анализа необходимо нажать клавишу "5" на клавиатуре прибора и внести новые условия, перелистывая появляющиеся окна клавишей "ENT". Пробную электрофореграмму не используют для построения градуировочной зависимости. Операцию нахождения времени включения давления, описанную выше, можно выполнить один раз и использовать полученный параметр до тех пор, пока время выхода пиридоксина будет меньше задаваемого.
Установленный промежуток времени вносят в программу поэтапного анализа системы капиллярного электрофореза "Капель-105" (пример составления программы представлен в приложении А, таблица А.2) и используют ее для записи электрофореграммы градуировочного раствора и анализа растворов, полученных из испытуемых проб.
Для проведения градуировки системы последовательно, не менее трех раз готовят и сразу же анализируют градуировочный раствор (см. 6.2.3.5). На полученных электрофореграммах проверяют правильность автоматической разметки пиков, при необходимости корректируют разметку, удаляют лишние пики и далее обрабатывают электрофореграммы согласно процедуре градуировки, описанной в руководстве пользователя программы "МультиХром". В таблице компонентов должно быть столько строк, сколько витаминов анализируют. В таблице концентраций создают столько градуировочных уровней, сколько получено электрофореграмм, при этом концентрации компонентов в каждом уровне будут одинаковые.
После выполнения процедуры градуировки программа автоматически рассчитывает градуировочный коэффициент и среднеквадратичное отклонение (СКО) имеющейся выборки. Градуировку следует считать успешной, если величина СКО не превышает 5% для тиамина (), пиридоксина (
), пантотеновой (
), никотиновой (
), фолиевой (
) кислот и 10% - в случае рибофлавина (
) и аскорбиновой кислоты (С), а также если отклонения времени выхода пиков компонентов не превышают 5% среднеарифметических значений. Если градуировку признают неудовлетворительной, продолжают готовить и анализировать градуировочный раствор, создавая дополнительные градуировочные уровни до тех пор, пока указанные условия не будут выполнены. При этом допускается отбраковывать неудовлетворительные данные, однако число принятых к градуировке точек должно быть не меньше трех.
6.2.4.2 Градуировка системы методом мицеллярной электрокинетической хроматографии
Рекомендуемые параметры ввода и условия анализа представлены в таблице 5. Непосредственно перед анализом растворы центрифугируют в течение 5 мин при 5000-6000 об/мин.
Таблица 5 - Условия анализа градуировочного раствора методом МЭКХ
Определяемые витамины в порядке выхода | Никотинамид ( |
Ввод градуировочного раствора (пробы) | 30 мбар, 20 с |
Условия анализа | |
Длина волны, нм | 200 (в начале анализа), 240 (после пика пантотеновой кислоты) |
Напряжение, кВ | +25 |
Давление, мбар | В начале анализа - 0, после появления пика пантотеновой кислоты ( |
Температура, °С | 40 |
Время, мин | 17-20 |
Ведущий электролит | N 2 (см. 6.2.1.10) |
При выполнении анализа необходимо изменение условий регистрации электрофореграммы, а именно приложение давления и изменение рабочей длины волны после появления пика пантотеновой кислоты.
Для определения момента времени, по истечении которого необходимо приложить давление и изменить длину волны, готовят пробный раствор витаминов в соответствии с 6.2.3.5 и регистрируют пробную электрофореграмму при длине волны 200 нм. В этом случае после регистрации пантотеновой кислоты (пятого компонента анализируемого раствора) в ручном режиме задают давление 50 мбар и ведут анализ до появления пика последнего компонента (тиаминхлорида) пробы. Не останавливая анализ, необходимо нажать клавишу "5" на клавиатуре прибора и внести новые условия, перелистывая появляющиеся окна клавишей "ENT". В ручном режиме длина волны без остановки анализа не может быть установлена, поэтому заканчивают пробную электрофореграмму при измерении на длине волны 200 нм. Пробную электрофореграмму не используют для построения градуировочной зависимости. Операцию нахождения времени включения давления и изменения длины волны регистрации, описанную выше, можно выполнить один раз и использовать полученный параметр до тех пор, пока время выхода пантотеновой кислоты будет меньше задаваемого.
Установленный промежуток времени вносят в программу поэтапного анализа системы "Капель-105" вместе с изменением длины волны регистрации (пример составления программы представлен в приложении А, таблица А.3) и используют ее для записи электрофореграмм градуировочных растворов и анализа растворов, полученных из испытуемых проб.
Для проведения градуировки системы последовательно, не менее трех раз готовят и сразу же анализируют градуировочные растворы (см. 6.2.3.5). На полученных электрофореграммах проверяют правильность автоматической разметки пиков, при необходимости корректируют разметку, удаляют лишние пики и далее обрабатывают злектрофореграммы согласно процедуре градуировки, описанной в руководстве пользователя программы "МультиХром". В таблице компонентов должно быть столько строк, сколько витаминов анализируют. В таблице концентраций создают столько градуировочных уровней, сколько получено электрофореграмм, при этом концентрации компонентов в каждом уровне будут одинаковые.
После выполнения процедуры градуировки программа автоматически рассчитывает градуировочный коэффициент и СКО имеющейся выборки. Градуировку следует считать успешной, если величина СКО не превышает 5% для никотинамида (), пиридоксина (
), пантотеновой (
), никотиновой (
), фолиевой (
) кислот и 10% - в случае рибофлавина (
), аскорбиновой кислоты (С) и тиамина (
), а также если отклонения времени выхода пиков компонентов не превышают 5% среднеарифметических значений. Если градуировка признается неудовлетворительной, продолжают готовить и анализировать градуировочные растворы, создавая дополнительные градуировочные уровни до тех пор, пока указанные условия не будут выполнены. При этом допускается отбраковывать неудовлетворительные данные, однако число принятых к градуировке точек должно быть не меньше трех.
6.2.5 Контроль стабильности градуировочной характеристики
Контроль стабильности градуировочной характеристики проводят в начале рабочего дня перед измерениями анализируемых проб. Не допускается использовать для контроля стабильности градуировочной характеристики растворы, применявшиеся при построении градуировочных зависимостей.
Для проверки работоспособности системы и контроля стабильности градуировочной характеристики используют свежеприготовленный рабочий контрольный раствор (см. 6.2.3.6), который анализируют в условиях, соответствующих анализу градуировочных растворов (таблицы 4, 5). Программное обеспечение "МультиХром" определяет время выхода компонентов и вычисляет массовую концентрацию каждого витамина в контрольном растворе, используя действующую на данный момент градуировочную зависимость, построенную в соответствии с 6.2.4.
Градуировка признается стабильной, если выполняется неравенство
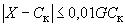 , (3)
, (3)
где - измеренное значение массовой концентрации соответствующего витамина в контрольном растворе, мг/дм
;
- массовая концентрация соответствующего витамина в контрольном растворе, мг/дм
;
- норма контроля стабильности градуировочной характеристики, %.
На стадии освоения методики в качестве значения принимают равным 10% для пиридоксина и 16% для рибофлавина.
При накоплении статистических данных лаборатория вправе устанавливать собственные нормы контроля стабильности градуировочной характеристики при условии, что они не превышают значений, приведенных выше, а также использовать другие соединения (из числа анализируемых) в качестве компонентов образца для контроля.
При невыполнении условия (3) заново анализируют контрольный раствор еще два раза. При повторных отклонениях, превышающих указанные нормы хотя бы один раз, градуировку системы проводят заново, начиная с приготовления новых запасных растворов.
Также необходимо обращать внимание на время выхода пиков компонентов, отклонения которых не должны превышать 5% средних значений.
6.3 Проведение измерений
Рекомендуется начинать работу с пробами только после проведения градуировки системы или после проверки стабильности градуировочной характеристики, что связано с необходимостью анализа получаемых растворов в течение первых 1,5-2 ч после их приготовления.
6.3.1 Получение вытяжки витаминов из испытуемой пробы
Навеску премикса массой 1,000 г помещают в плоскодонную колбу вместимостью 50 см, добавляют 25 см
экстрагирующего раствора, приготовленного по 6.2.1.13, и ставят в перемешивающее устройство при комнатной температуре на 15 мин.
Часть полученной вытяжки переносят в центрифужную пробирку или пробирку типа Эппендорфа и центрифугируют в течение 5 мин при 5000-6000 об/мин. Раствор над осадком отбирают в чистую пробирку типа Эппендорфа.
Примечание - Вытяжку из навески исследуемой пробы необходимо анализировать в течение первых 1,5-2 ч после ее получения, что связано с низкой стабильностью витамина С (аскорбиновой кислоты).
6.3.2 Анализ полученных водных вытяжек
6.3.2.1 Анализ полученных вытяжек витаминов методом КЗЭ
Метод КЗЭ основан на миграции и разделении ионных форм анализируемых компонентов под действием электрического поля вследствие их различной электрофоретической подвижности.
Промывают капилляр ведущим электролитом N 1 в течение 10-15 мин. Далее устанавливают на выходе в рабочее положение пробирку с этим же электролитом, а на входе - пробирку с пробой и проводят ее ввод.
Для каждого раствора полученной вытяжки регистрируют не менее двух электрофореграмм в тех же условиях анализа, при которых была проведена градуировка (таблица 4). На полученных электрофореграммах необходимо проверить правильность автоматической разметки пиков, удалить лишние пики и настроить отчет так, чтобы маркировка пиков включала наименование компонента и его массовую концентрацию.
Для каждого витамина расхождение значений массовой концентрации, полученных при двух последовательных вводах одного и того же раствора, не должно превышать значений, приведенных в таблице 6, т.е. должно выполняться условие
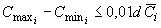 , (4)
, (4)
где 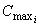 - больший результат измерения массовой концентрации соответствующего витамина в анализируемом растворе, мг/дм
- больший результат измерения массовой концентрации соответствующего витамина в анализируемом растворе, мг/дм;
- меньший результат измерения массовой концентрации соответствующего витамина в анализируемом растворе, мг/дм
;
- норматив контроля приемлемости расхождения результатов для двух последовательных вводов анализируемого экстракта (таблица 6), %;
- среднеарифметическое значение массовой концентрации соответствующего витамина, полученное по зарегистрированным электрофореграммам, мг/дм
.
Если условие (4) выполняется, то за результат анализа принимают среднеарифметическое значение двух параллельных определений.
Если условие (4) не выполняется, то выясняют и устраняют причины нестабильности, после чего ввод пробы повторяют.
В том случае, если измеренные массовые концентрации одного или нескольких витаминов в анализируемом растворе пробы превышают значения верхних границ диапазона линейности градуировочной характеристики (таблица 6), то необходимо разбавить раствор дистиллированной водой так, чтобы массовая концентрация в полученном растворе находилась в середине диапазона измеряемых значений, и повторить ввод.
Таблица 6 - Нормы контроля приемлемости расхождения результатов для двух последовательных вводов анализируемого экстракта
Витамин | Метод | Диапазон линейности градуировочной зависимости |
|
КЗЭ | 4,0-200 | 25 | |
МЭКХ | 4,0-200 | 18 | |
КЗЭ | 4,0-200 | 12 | |
МЭКХ | 4,0-200 | 12 | |
КЗЭ, МЭКХ | 4,0-200 | 14 | |
| КЗЭ, МЭКХ | 2,0-200 | 16 |
КЗЭ, МЭКХ | 1,0-100 | 16 | |
КЗЭ, МЭКХ | 2,5-100 | 16 | |
С | КЗЭ, МЭКХ | 8,0-200 | 14 |
| МЭКХ | 4,0-200 | 22 |
6.3.2.2 Анализ полученных водных вытяжек методом МЭКХ
МЭКХ основана на миграции нейтральных и ионных форм анализируемых компонентов под действием электрического поля вследствие их различной электрокинетической подвижности и распределении между фазой раствора и мицеллярной псевдофазой.
Рекомендуется приступать к работе в мицеллярном варианте после проведения всех необходимых измерений в капиллярном зонном варианте, что связано с нежелательным частым кондиционированием капилляра при переходе с одного ведущего электролита на другой. Смена ведущего электролита чаще одного раза в течение рабочего дня может привести к загрязнению капилляра, которое потребует длительной промывки.
Промывают капилляр ведущим электролитом N 2 в течение 10-15 мин. Далее устанавливают на выходе в рабочее положение пробирку с этим же ведущим электролитом и проверяют стабильность градуировочной характеристики по 6.2.5. Если стабильность удовлетворительная, проводят ввод пробы и анализ. Если стабильность градуировочной характеристики признают неудовлетворительной, то для сохранения приготовленного раствора сначала проводят анализ подготовленных проб, затем градуировку системы повторяют, создают на этой основе новый метод и обрабатывают полученные электрофореграммы в новом методе.
Для каждого раствора полученной вытяжки регистрируют не менее двух электрофореграмм в тех же условиях анализа, при которых была проведена градуировка (см. таблицу 5). Пример электрофореграммы реальной пробы представлен в приложении Б (рисунок Б.3). На полученных электрофореграммах необходимо проверить правильность автоматической разметки пиков, удалить лишние пики и настроить их так, чтобы маркировка пиков включала наименование компонента и его количество.
Проверяют приемлемость расхождений значений массовой концентрации витаминов с использованием неравенства (4).
Если условие (4) выполняется, то за результат принимают среднеарифметическое значение двух параллельных определений.
Если измеренные значения массовой концентрации одного или нескольких витаминов в анализируемом растворе пробы превышают значения верхних границ диапазона линейности градуировочной характеристики (см. таблицу 6), то необходимо разбавить раствор дистиллированной водой так, чтобы массовая концентрация в полученном растворе находилась в середине диапазона измеряемых значений, и повторить ввод.
6.4 Обработка результатов измерения
Содержание соответствующего витамина в пробе , г/кг, вычисляют по формуле
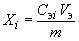 , (5)
, (5)
где - массовая концентрация соответствующего витамина в экстракте, указанная на электрофореграмме или прочитанная в отчете, мг/дм
;
- объем полученного экстракта, дм
(0,025);
- масса навески пробы, г.
6.5 Оформление результатов измерений
Результат измерения представляют в виде 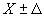 , г/кг,
, г/кг, 0,95.
По полученному результату анализа и значению относительной погрешности
(см. таблицу 1) рассчитывают абсолютную погрешность по формуле
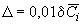 , (6)
, (6)
где - среднеарифметическое значение результатов двух параллельных определений, мг/дм
.
Допускается результат измерения в документах, выдаваемых лабораторией, представлять в виде 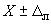 , г/кг,
, г/кг, 0,95, при условии
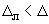 , где
, где - значение характеристики погрешности результатов измерений, установленное при реализации методики в конкретной лаборатории и обеспечиваемое контролем стабильности результатов измерений.
7 Контроль качества результатов измерений
7.1 Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
- оперативный контроль процедуры измерений на основе оценки погрешности при реализации отдельно взятой контрольной процедуры;
- контроль стабильности результатов измерений на основе контроля стабильности СКО повторяемости, СКО промежуточной (внутрилабораторной) прецизионности и погрешности.
Периодичность контроля исполнителем процедуры выполнения измерений на основе оценки погрешности измерений при реализации отдельной контрольной процедуры, а также реализуемые процедуры контроля стабильности результатов измерений регламентируются в Руководстве по качеству лаборатории*.
________________
* Документ в информационных продуктах не содержится. За информацией о документе Вы можете обратиться в Службу поддержки пользователей. - .
7.2 Контроль исполнителем процедуры выполнения измерений
Контроль исполнителем процедуры выполнения измерений проводится с использованием образцов для контроля. В качестве таких образцов применяют образцы, для которых содержание анализируемых витаминов установлено на основании межлабораторного сличительного эксперимента, или образцы, для которых содержание витаминов установлено в данной лаборатории стандартизованными методами.
Сравнивают результат контрольной процедуры с нормой контроля
. Результат контрольной процедуры вычисляют по формуле
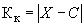 , (7)
, (7)
где - результат измерения содержания витамина в образце для контроля, г/кг;
- опорное (аттестованное) значение, г/кг.
В качестве нормы контроля принимают значение характеристики погрешности измерений, установленное в лаборатории при реализации методики (
, г/кг); если эти значения еще не установлены (например, при освоении методики), то вместо
используют значение
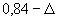 [где
[где - границы абсолютной погрешности измерений для доверительной вероятности
0,95, вычисляемые по формуле (5)]. Качество контрольной процедуры признают удовлетворительным, если
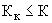 . При невыполнении равенства (7) процедуру контроля повторяют. При повторном неудовлетворительном результате находят и устраняют причины, приводящие к неудовлетворительным результатам.
. При невыполнении равенства (7) процедуру контроля повторяют. При повторном неудовлетворительном результате находят и устраняют причины, приводящие к неудовлетворительным результатам.
7.3 Оценка приемлемости результатов, получаемых в условиях воспроизводимости
Расхождение между результатами, полученными в двух лабораториях, не должно превышать предела воспроизводимости (таблица 7), т.е. должно выполняться условие
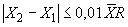 , (8)
, (8)
где и
- результаты измерений, полученные в условиях воспроизводимости (в разных лабораториях), г/кг;
- среднеарифметическое значений
и
, г/кг;
- значение предела воспроизводимости (см. таблицу 7), %.
Таблица 7 - Пределы воспроизводимости
Витамин | Метод | Предел воспроизводимости |
КЗЭ | 28 | |
МЭКХ | 48 | |
КЗЭ | 59 | |
МЭКХ | 39 | |
КЗЭ, МЭКХ | 28 | |
| КЗЭ, МЭКХ | 25 |
| МЭКХ | 39 |
КЗЭ, МЭКХ | 28 | |
КЗЭ, МЭКХ | 28 | |
С | КЗЭ, МЭКХ | 48 |
При выполнении этого условия приемлемы оба результата измерений, и в качестве окончательного может быть использовано их среднеарифметическое значение.
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений в соответствии с [2] (раздел 5).
Приложение А (рекомендуемое). Составление программы для проведения поэтапного анализа
Приложение А
(рекомендуемое)
Перед составлением программы в первую очередь необходимо присвоить каждому используемому раствору номер (от 1 до 10), который будет совпадать с номером пробирки в карусели (пример - таблица А.1).
Таблица А.1 - Пример обозначения растворов
Номер пробирки | Входная карусель | Выходная карусель |
1 | Проба а | |
2 | Проба б | |
3 | Проба в | |
4 | Проба г | |
5 | Проба д | |
6 | Раствор соляной кислоты 0,5 моль/дм | |
7 | Вода | |
8 | Раствор гидроокиси натрия 0,5 моль/дм | |
9 | Ведущий электролит для промывки капилляра | Сливная пробирка |
10 | Ведущий электролит для анализа | Ведущий электролит для анализа |
В начале рабочего дня необходимо установить рабочую температуру анализа: 30 °С - при определении витаминов методом КЗЭ и 40 °С - в случае выполнения анализа методом МЭКХ.
В таблице А.2 приведен пример программы анализа для метода КЗЭ, а в таблице А.3 - для МЭКХ.
Таблица А.2 - Программа анализа методом КЗЭ
Номер шага | Код операции | Условия | Содержание шага |
1 | 11 | 200 нм | Установка рабочей длины волны |
2 | 5 | N 10 | Установка на выходе в рабочую позицию пробирки N 10 с ведущим электролитом |
3 | 4 | N 1 | Установка на входе в рабочую позицию пробирки N 1 с анализируемым раствором |
4 | 2 | 30 мбар, 20 с | Ввод пробы |
5 | 4 | N 10 | Установка на входе в рабочую позицию пробирки N 10 с ведущим электролитом |
6 | 3 | 0 мбар, 25 кВ, 10 мин 50 с | Установка параметров и времени окончания первого этапа анализа |
7 | 3 | 30 мбар, 25 кВ, 16 мин | Установка параметров и времени окончания второго этапа анализа |
8 | 4 | N 9 | Установка на входе пробирки с ведущим электролитом для промывки |
9 | 7 | N 4 | Установка на выходе пробирки для слива в опущенном состоянии |
10 | 1 | 0 кВ, 180 с | Промывка капилляра ведущим электролитом после анализа |
11 | 5 | N 10 | Установка пробирки с ведущим электролитом на выходном конце капилляра в поднятом положении |
Примечание - Моменты времени, указанные в программе поэтапного анализа, устанавливаются на основе пробной электрофореграммы, полученной при изменении давления от 0 до 30 мбар в ручном режиме (см. 6.2.4.1). |
Таблица А.3 - Программа анализа методом МЭКХ
Номер шага | Код операции | Условия | Содержание шага |
1 | 11 | 200 нм | Установка рабочей длины волны первого этапа |
2 | 5 | N 10 | Установка на выходе в рабочую позицию пробирки N 10 с ведущим электролитом |
3 | 4 | N 1 | Установка на входе в рабочую позицию пробирки N 1 с анализируемым раствором |
4 | 2 | 30 мбар, 20 с | Ввод пробы |
5 | 4 | N 10 | Установка на входе в рабочую позицию пробирки N 10 с ведущим электролитом |
6 | 3 | 0 мбар, 25 кВ, 12 мин 30 с | Установка параметров и времени окончания первого этапа анализа |
7 | 11 | 240 нм | Установка рабочей длины волны второго этапа |
8 | 3 | 50 мбар, 25 кВ, 18 мин | Установка параметров и времени окончания второго этапа анализа |
9 | 4 | N 9 | Установка на входе пробирки с ведущим электролитом для промывки |
10 | 7 | N 4 | Установка на выходе пробирки для слива в опущенном состоянии |
11 | 1 | 0 кВ, 180 с | Промывка капилляра ведущим электролитом после анализа |
12 | 5 | N 10 | Установка пробирки с ведущим электролитом на выходном конце капилляра в поднятом положении |
Примечание - Моменты времени, указанные в программе поэтапного анализа, устанавливают на основе первой электрофореграммы, полученной при изменении давления от 0 до 50 мбар в ручном режиме (см. 6.2.4.2). |
Приложение Б (рекомендуемое). Пример электрофореграмм
Приложение Б
(рекомендуемое)
Б.1 Метод КЗЭ
Рисунок Б.1 - Метод КЗЭ. Электрофореграмма градуировочного раствора
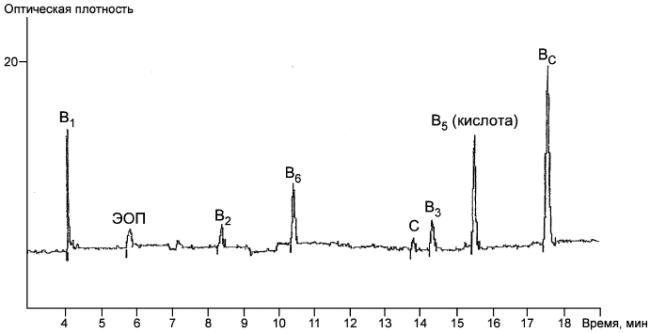
Рисунок Б.1 - Электрофореграмма градуировочного раствора
Б.2 Метод МЭКХ
Рисунок Б.2 - Метод МЭКХ. Электрофореграмма градуировочного раствора
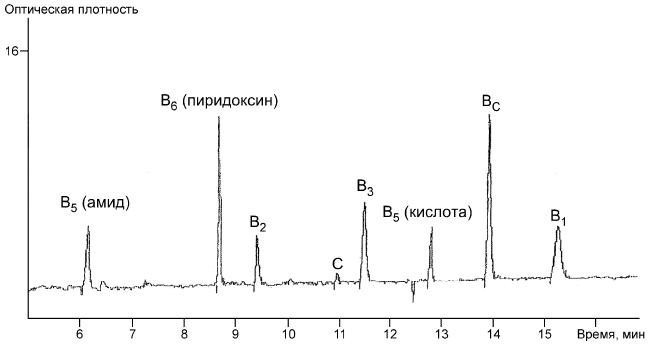
Рисунок Б.2 - Электрофореграмма градуировочного раствора
Рисунок Б.3 - Электрофореграмма экстракта премикса
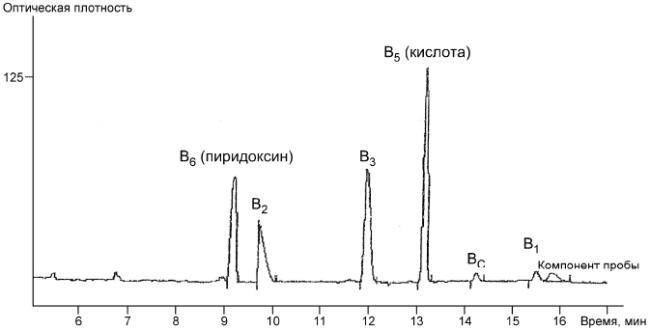
Рисунок Б.3 - Электрофореграмма экстракта премикса
После пика пантотеновой кислоты () может наблюдаться обратный пик, связанный с изменением условий анализа: подача давления 50 мбар и изменение длины волны с 200 на 240 нм.
На рисунке Б.4 показан увеличенный фрагмент электрофореграммы пробы в области выхода пика витамина . Разметку пика
необходимо проводить способом, указанным на рисунке Б.4.
Рисунок Б.4 - Фрагмент электрофореграммы премикса
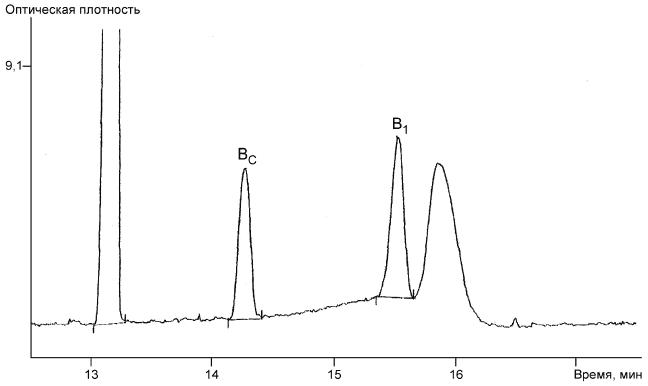
Рисунок Б.4 - Фрагмент электрофореграммы премикса
Библиография
[1] ИСО 6498:1998* | Корма для животных. Приготовление проб для испытания |
[2] ИСО 5725-6:1994* | Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике |
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
Редакция документа с учетом
изменений и дополнений подготовлена

