ГОСТ 33645-2015
Группа Т58
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬ ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ
Оценка метаморфоза земноводных
Testing of chemicals of environmental hazard. The Amphibian Metamorphosis Assay
МКС 13.020.01
Дата введения 2016-09-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием "Всероссийский научно-исследовательский институт стандартизации материалов и технологий" (ФГУП "ВНИИ СМТ") на основе аутентичного перевода на русский язык документа, указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии (Росстандарт)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 27 октября 2015 г. N 81-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по МК (ИСО 3166) 004-97 | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
Таджикистан | TJ | Таджикстандарт |
4 Настоящий стандарт модифицирован по отношению к международному документу OECD, Test No. 231:2009* The Amphibian Metamorphosis Assay (ОЭСР, Тест N 231:2009 Оценка метаморфоза земноводных) путем изменения структуры. Сравнение структуры международного документа со структурой настоящего стандарта приведено в приложении ДА.
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
Перевод с английского языка (en).
Степень соответствия - модифицированная (MOD)
5 Приказом Федерального агентства по техническому регулированию и метрологии от 18 ноября 2015 г. N 1866-ст межгосударственный стандарт ГОСТ 33645-2015 введен в действие в качестве национального стандарта Российской Федерации с 1 сентября 2016 г.
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
Введение
Необходимость разработки и утверждения метода, с помощью которого можно было бы обнаруживать активные вещества для щитовидной железы позвоночных животных, возникла в результате опасений, что воздействие химических веществ в окружающей среде может иметь неблагоприятные последствия для людей и животных. В 1998 г. ОЭСР активно инициировала пересмотр существующих руководств и разработку новых руководств для скрининга и тестирования химических веществ, оказывающих потенциальное отрицательное воздействие на эндокринную систему. Одним из элементов этой деятельности была разработка теста для скрининга веществ, проявляющих активность в системе щитовидной железы позвоночных. Было предложено два теста с введением повторных доз грызунам в течение 28 сут (Руководство по испытанию 407) и оценкой метаморфоза земноводных (ОМЗ). Усовершенствованное руководство TG 407 прошло валидацию, и пересмотренный метод был издан. Тест по оценке метаморфоза земноводных (ОМЗ) подвергся широкой программе валидации, которая включала внутри- и межлабораторные исследования, показывающие актуальность и надежность оценки [1], [2]. Затем валидированный тест прошел экспертную оценку группой независимых экспертов [3]. Данное Руководство по испытанию является результатом опыта, накопленного в ходе исследований по валидации, и оно касается обнаружения веществ, активных в отношении щитовидной железы, и работ, проводимых в других странах - членах ОЭСР.
1 Область применения
Настоящий стандарт устанавливает процедуру оценки метаморфоза земноводных (ОМЗ).
2 Принцип метода
2.1 Оценка метаморфоза земноводных (ОМЗ) является скрининговым методом, предназначенным для эмпирического установления веществ, которые могут нарушать нормальную функцию гипоталамо-гипофизарно-тиреоидной (ТВД) оси. ОМЗ представляет собой обобщенную модель на позвоночных, основанную на консервативных структурах и функции ТВД оси. Данный тест важен, поскольку метаморфоз земноводных обеспечивает хорошо изученный, зависимый от щитовидной железы процесс, который реагирует на вещества, активные для оси ТВД, и это единственный существующий тест, с помощью которого обнаруживается активность в отношении щитовидной железы у животных, подвергающихся морфологическому развитию.
2.2 Общий дизайн опыта включает воздействие на стадию 51 головастика Xenopus Laevis минимум трех различных концентраций испытуемого вещества и воды для разведения, используемой в качестве контроля, в течение 21 сут. Для каждой обработки в испытании должно быть четыре повторности. В начале испытания количество личинок составляет 20 головастиков на испытуемый резервуар для всех обрабатываемых групп. Конечными точками наблюдений являются длина задних конечностей, длина от кончика морды до клоаки (SVL), стадия развития, сырая масса, гистология щитовидной железы и ежедневные наблюдения по гибели.
3 Описание метода
3.1 Тестовые виды
Xenopus laevis обычно культивируют в лабораториях по всему миру, и их легко получить от коммерческих поставщиков. Размножение этого вида легко индуцируется в течение всего года инъекцией человеческого хорионического гонадотропина (ХГЧ), и полученные личинки можно легко культивировать до требуемой стадии развития в больших количествах, позволяющих проводить испытания конкретно на определенной стадии развития. Предпочтительно, чтобы личинки, используемые в тесте, были получены из взрослых особей, культивированных внутри лаборатории. В качестве альтернативы, хотя это не является предпочтительной процедурой, яйца или эмбрионы можно транспортировать в лабораторию, в которой проводится испытание, и организмам дается возможность акклиматизации; доставка на личиночной стадии для использования в испытании недопустима.
3.2 Оборудование и материалы
Для проведения настоящего испытания используют следующее оборудование и материалы:
а) система воздействия (см. описание ниже);
б) стеклянные или из нержавеющей стали аквариумы (см. ниже);
в) резервуары для культивирования;
г) устройство регуляции температуры (например, нагреватели или охладители, регулируемые до температуры (22±1)°C);
д) термометр;
е) препаровальная лупа;
ж) цифровая камера с разрешением не менее 4 мегапикселей и микрофункцией;
и) визуализирующее цифровое программное обеспечение;
к) чашка Петри (например, 100х15 мм) или камера из прозрачного пластика аналогичного размера;
л) аналитические весы с точностью взвешивания до третьего десятичного знака;
м) прибор для измерения растворенного кислорода;
н) рН-метр;
о) прибор для измерения интенсивности света, способный измерять в единицах люкс;
п) необходимая лабораторная посуда и инструменты;
р) регулируемые пипетки (от 10 до 5000 мкл) или подходящие пипетки эквивалентных объемов;
с) испытуемое химическое вещество в количествах, достаточных для проведения испытания, предпочтительно одной партии;
т) аналитические приборы, подходящие для химического анализа испытуемого вещества, или контракт на аналитическое обслуживание.
3.3 Химическая контролируемость
ОМЗ основана на дизайне с воздействием через воду, в котором испытуемое химическое вещество вносится в испытуемые камеры через проточную систему. Однако для проточных методов имеются ограничения в отношении типов химических веществ, которые могут быть испытаны, что определяется их физико-химическими свойствами. Следовательно, прежде чем использовать данный протокол, должна быть получена исходная информация о химическом веществе, т.е. о возможности использовать настоящий протокол для этого вещества, дополнительная информация приведена в [4]. Параметры, указывающие на то, что химическое вещество трудно тестировать в водных системах, включают: высокий коэффициент распределения в системе октанол/вода (log Kow), высокая летучесть, склонность к гидролизу и склонность к фотолизу в лабораторных условиях освещенности. Другие факторы также могут иметь отношение к определению возможности проведения испытания, и их определяют в каждом конкретном случае. Если полноценное испытание химического вещества при использовании проточной испытуемой системы провести невозможно, то может быть использована статическая восстанавливаемая система. Если ни одну из систем не удается приспособить к испытуемому химическому веществу, данный протокол не используют.
3.4 Система воздействия
3.4.1 Проточная система разведения является предпочтительной, когда это возможно, по сравнению со статической восстанавливаемой системой. Если физические и/или химические свойства любого испытуемого вещества не подходят для проточной системы разведения, то используют альтернативную систему воздействия (например, статистическую восстанавливаемую систему). Элементы системы, которые контактируют с водой, должны быть сделаны из материалов, включающих стекло, нержавеющую сталь и/или тефлон. Однако могут использоваться подходящие пластики, если не оказывают отрицательного влияния на испытание. Резервуары, в которых воспроизводится воздействие испытуемого химического вещества, должны представлять собой стеклянные аквариумы или аквариумы из нержавеющей стали, оснащенные водозаборными колонками, что создает приблизительный объем резервуара от 4,0 до 10,0 л и минимальную глубину воды от 10 до 15 см. Система должна включать все концентрации испытуемого вещества и контроль в четырех повторностях для каждой обработки. Скорость потока в каждом резервуаре должна быть постоянной с учетом поддержания биологических условий и воздействия испытуемого химического вещества (например, 25 мл/мин). Резервуары для обработки устанавливают произвольно в системе экспозиции таким образом, чтобы снизить возможные позиционные эффекты, включая незначительные отклонения в температуре, интенсивности света и т.д. Обрабатываемые резервуары должны быть случайным образом распределены на позиции в системе экспозиции с целью снижения потенциальных позиционных эффектов, включая незначительные отклонения в температуре, интенсивности света (освещенности) и т.д. Используют люминесцентное освещение для обеспечения светового цикла 12 ч свет:12 ч темнота при интенсивности в диапазоне от 600 до 2000 люкс (люмен/м
) на поверхности воды. Температура воды поддерживается на уровне (22±1)°C, значение рН находится в диапазоне от 6,5 до 8,5, и концентрации растворенного кислорода (РК) составляют более 3,5 мг/л (более 40% насыщения воздухом) в каждом испытуемом резервуаре. Температуру воды, рН и концентрацию растворенного кислорода измеряют минимум один раз в неделю; температуру предпочтительно измерять постоянно, по меньшей мере в одном испытуемом сосуде. В приложении А приведены экспериментальные условия, в которых выполняется протокол. Для получения дополнительной информации по установке проточной и/или статистической восстанавливаемой системы воздействия можно обратиться к стандарту ASTM по проведению испытаний по острой токсичности химических веществ на рыбах, макробеспозвоночных и земноводных [5] и общим принципам проведения токсикологических испытаний в водной среде.
3.4.2 Качество воды
Используется любая доступная местная вода (например, родниковая или водопроводная, профильтрованная через древесный уголь), обеспечивающая нормальный рост и развитие головастиков X. laevis. Поскольку качество местной воды может существенно различаться от одного района к другому, то проводят анализ качества воды, в частности, если отсутствуют архивные данные о пригодности воды для культивирования Xenopus. Особое внимание обращают на то, чтобы вода не содержала меди, хлора и хлорамина, которые являются токсичными для лягушек и головастиков. Кроме того, рекомендуется анализировать воду на фоновое содержание фторида, перхлората и хлората (побочный продукт дезинфекции питьевой воды), поскольку все эти анионы являются субстратами для транспортера йода в щитовидной железе, и повышенный уровень каждого из этих анионов может оказать влияние на результаты испытаний. Анализ выполняют до начала испытания, и испытуемая вода не должна содержать указанных анионов.
3.4.3 Концентрация йодида в испытуемой воде
Для того чтобы щитовидная железа могла синтезировать ТН, личинки должны быть обеспечены достаточным количеством йодида через воду и источники питательных веществ. В настоящее время отсутствуют эмпирически принятые нормы минимальных концентраций йодида. Однако присутствие йодида может повлиять на реакцию системы щитовидной железы на активные вещества щитовидной железы и, как известно, модулировать исходную активность щитовидной железы, вопрос, который заслуживает внимания при интерпретации результатов гистопатологического исследования щитовидной железы. Таким образом, необходимо представить измеренные концентрации йодида в испытуемой воде. На основе имеющихся результатов валидированных исследований протокол хорошо "работает" при концентрации йодида (I) в испытуемой воде в диапазоне от 0,5 до 10 мкг/л. В идеальных условиях минимальная концентрация йодида в испытуемой воде должна составлять 0,5 мкг/л. Если воду, используемую в испытании, разводят деионизированной водой, то добавляют йод в минимальной концентрации 0,5 мкг/л. В отчете указывают любое дополнительное внесение йода или других солей в испытуемую воду.
3.5 Содержание организмов
3.5.1 Уход и культивирование взрослых особей
Уход и культивирование взрослых особей проводится в соответствии со стандартными руководствами [5], и для получения более подробной информации можно обратиться к руководству для постановки FETAX. В таких стандартных руководствах приводятся инструкции для надлежащего ухода и методов культивирования, но строгого их соблюдения не требуется. Для стимуляции размножения взрослым самкам и самцам (3-5 пар) вводят хорионический гонадотропин (ХГЧ). Самкам и самцам вводят соответственно примерно 800-1000 ЕД и 600-800 ЕД ХГЧ, растворенного в 0,6-0,9% физиологическом растворе. Разведение самцов и самок проводится в большом резервуаре, в покое и статических условиях для обеспечения амлексуса. Каждый резервуар для культивирования имеет двойное дно из нержавеющей стали или пластиковой сетки, что позволяет яичным кладкам опускаться на дно резервуара. Лягушки, которым ХГЧ был введен в конце дня, как правило, откладывают большую часть яиц к середине утра следующего дня. После получения достаточного количества выделенных и оплодотворенных яиц, взрослых особей удаляют из резервуаров для разведения.
3.5.2 Уход и отбор личинок
3.5.2.1 После извлечения взрослых особей из резервуаров для разведения яйца собирают и оценивают их жизнеспособность с использованием репрезентативного количества эмбрионов из всех резервуаров для разведения. Отдельные икринки с наилучшим внешним видом (2-3 рекомендуется оценить на качество нереста) следует сохранить, основываясь на жизнеспособности эмбриона и наличии достаточного количества (не менее 1500) эмбрионов. Все организмы, используемые в испытании, должны исходить от одного нереста (т.е. нересты не должны смешиваться). Эмбрионы переносят в большой плоский лоток или чашку, и все видимые мертвые или аномальные яйца (см. [6]) удаляют с помощью лабораторной пипетки или глазной пипетки. Жизнеспособные эмбрионы из каждого из трех нерестов переносят в три отдельных инкубационных резервуара. Через 4 сут после помещения в инкубационные резервуары выбирают лучшую икру, основываясь на жизнеспособности и результатах инкубации, и имеющееся количество личинок переносят в резервуар для культивирования при температуре (22±1)°C. Кроме того, помещают некоторое количество дополнительных личинок в дополнительные резервуары для возможной замены в случае, если в резервуаре для культивирования имеет место гибель в течение первой недели. Использование такой процедуры обеспечивает равномерную плотность организмов и тем самым снижает вариабельность в развитии потомства одной икры. Все резервуары для культивирования ежедневно очищают перекачиванием. В качестве меры предосторожности: виниловые или нитриловые перчатки являются более предпочтительными по сравнению с латексными перчатками. Погибших личинок ежедневно удаляют и их замещают добавлением новых личинок для поддержания их плотности в течение первой недели. Кормление проводят не менее двух раз в сутки.
3.5.2.2 Перед воздействием испытуемого вещества головастиков адаптируют к условиям реальной экспозиции, в том числе типу корма, температуре, циклу свет-темнота и культуральной среде. Таким образом, рекомендуется использовать одну и ту же воду для культивирования/разведения перед воздействием и во время воздействия. Если для поддержания головастиков перед воздействием испытуемого вещества используется статическая система культивирования, то культуральную среду полностью заменяют не менее двух раз в неделю. Следует избегать скученности, вызванной высокой плотностью личинок перед воздействием, поскольку это может заметно повлиять на развитие головастиков в последующем испытании. Таким образом, плотность при культивировании не должна превышать примерно четыре головастика на 1 литр культуральной среды (статическая система воздействия) или 10 головастиков на 1 литр культуральной среды (например, при скорости потока 50 мл/мин в системе перед воздействием или культивированием). В этих условиях головастики развиваются от стадии 45/46 до стадии 51 в течение 12 сут. Репрезентативное количество головастиков из этой исходной популяции ежедневно осматривают для определения стадии развития с целью установления подходящей временной точки для начала воздействия. Следует соблюдать осторожность, чтобы минимизировать стресс и травмирование головастиков, особенно во время переноса, очистки аквариумов и манипуляций с личинками. Следует избегать стрессовых условий/действий, например громких и/или сохраняющихся длительно звуков, постукивания по аквариуму, вибрации в аквариуме, повышенной активности в лаборатории и резких изменений в окружающей среде (доступности света, температуры, рН, концентрации растворенного кислорода, скорости протекания воды и т.д.) Если головастики не развиваются до стадии 51 в течение 17 сут после оплодотворения, то возможной причиной этого является повышенный стресс.
3.5.3 Культивирование и кормление личинок
Головастикам скармливают, например, Sera Micron (Sera GmbH, Heinsberg, Германия) на протяжении всего периода перед воздействием (после Nieuwkoop и Faber (NF) стадия 45/46) и в течение всего периода испытания, составляющего 21 сут, или другой корм с такой же характеристикой в Оценке трансформации земноводных. Режим кормления в период перед воздействием тщательно корректируют с учетом потребностей развивающихся головастиков. То есть небольшие порции корма дают только что вылупившимся головастикам несколько раз в день (не менее двух раз). Следует избегать избыточного добавления корма для сохранения качества воды и предупреждения засорения жаберных фильтров частицами корма и отложений. По мере роста головастиков ежедневные порции Sera Micron
увеличивают примерно до 30 миллиграмм на особь в сутки незадолго до проведения испытания. При валидации метода было показано, что промышленно доступный корм для головастиков Sera Micron
, который поддерживает нормальный рост и развитие X. laevis, представляет собой мелкие твердые частицы, остающиеся во взвешенном состоянии в толще воды в течение длительного периода времени и подлежащие промывке потоком. Таким образом, общее суточное количество корма разделяют на небольшие порции и скармливают не менее двух раз в день. Режим кормления с использованием Sera Micron
описан в таблице 1. Нормы кормления регистрируют. Sera Micron
можно скармливать сухим или в виде стокового раствора, приготовленного на воде, предназначенной для разведения. Этот стоковый раствор готовят каждый день и хранят при температуре 4°C, когда не используется.
Таблица 1 - Режим кормления головастиков X. laevis на прижизненной стадии ОМЗ в проточных условиях
Сутки испытания | Корм для кормления (мг Sera Micron |
0-4 | 30 |
5-7 | 40 |
8-10 | 50 |
11-14 | 70 |
15-21 | 80 |
3.6 Химический анализ
Перед проведением испытания определяют стабильность испытуемого вещества, используя имеющуюся информацию о его растворимости, разложении и летучести. Для химического анализа отбирают испытуемые растворы из каждого параллельного резервуара для каждой концентрации в начале испытания (сутки 0) и еженедельно во время испытания не менее четырех образцов. Кроме того, рекомендуется определять каждую испытуемую концентрацию в ходе подготовки системы, до начала испытания, чтобы проверить функционирование системы. Кроме того, рекомендуется анализировать стоковые растворы для того, чтобы исключить их изменение, особенно если объем стокового раствора не обеспечивает достаточное количество химических веществ, чтобы охватить продолжительность планового периода отбора проб. В том случае, если химические вещества невозможно определить в некоторых или во всех концентрациях, используемых в испытании, измеряют концентрацию в стоковых растворах и регистрируют скорость потока системы для последующего расчета номинальной концентрации.
3.7 Внесение испытуемых веществ в систему
Метод, используемый для внесения испытуемого вещества в систему, различается в зависимости от его физико-химических свойств. Водорастворимые соединения растворяют в аликвотных порциях воды, используемой в испытании, в концентрации, позволяющей вносить испытуемые вещества в требуемой испытуемой концентрации в проточную систему. Химические вещества, которые являются жидкими при комнатной температуре и плохо растворяются в воде, вносят в смеси жидкость:жидкий растворитель. Химические вещества, твердые при комнатной температуре и слаборастворимые в воде, вносят с помощью колоночного сатуратора со стекловатой [7]. Предпочтительно использовать испытуемую систему без носителей, однако различные испытуемые химические вещества будут обладать различающимися физико-химическими свойствами, что, скорее всего, потребует различных подходов к подготовке воды для воздействия испытуемого вещества. Предпочтительно избегать использование растворителей или носителей по следующим причинам:
а) некоторые растворители сами по себе могут привести к проявлению токсичности и/или нежелательных или неожиданных эндокринологических реакций;
б) испытуемые химические вещества в концентрациях, превышающих их растворимость в воде (что часто возникает за счет использования растворителей), могут привести к неточному определению эффективных концентраций;
в) использование растворителей в долгосрочных испытаниях может привести к образованию "биологической пленки", связанной с микробной активностью.
В качестве последнего средства для трудных для испытания веществ используют растворитель (см. [4]), чтобы выбрать наилучший метод. Выбор растворителя определяется химическими свойствами вещества. Растворители, которые считаются эффективными для испытания на токсичность в водной среде, включают ацетон, этанол, метанол, диметилформамид и триэтиленгликоль. В случае если используется растворитель-носитель, концентрации растворителей должны быть ниже недействующей концентрации при повторных воздействиях (NOEC); в стандарте ОЭСР рекомендуется не более 100 мкл/л; в недавно опубликованном обзоре рекомендуется использовать такие низкие концентрации растворителей, как 20 мкл/л воды для разведения [8]. Если используются носители-растворители, то ставят соответствующие контроли на растворитель (чистая вода) дополнительно к контролю без растворителя. Если невозможно внести испытуемое вещество с водой за счет его физико-химических свойств (низкой растворимости) или ограниченной химической доступности, то его вносят с кормом. Была проведена предварительная работа по отработке воздействия через корм, однако этот путь обработки обычно не используется. Выбор метода регистрируют и аналитически подтверждают.
3.8 Выбор испытуемых концентраций
3.8.1 Установление высокой испытуемой концентрации
3.8.1.1 Для целей данного теста высокую испытуемую концентрацию устанавливают на основе предела растворимости испытуемого вещества; максимально переносимой концентрации (МТС) для высокотоксичных химических веществ; или 100 мг/л, которая является самой низкой.
3.8.1.2 МТС определяется как самая высокая испытуемая концентрация химического вещества, которая приводит не менее чем к 10% гибели в остром опыте. Использование такого подхода предполагает, что существуют эмпирические данные о гибели в остром опыте, на основе которых может быть установлена МТС. Установление МТС может быть неточным, и, как правило, требуется определенное профессиональное заключение. Несмотря на то что использование регрессионной модели может быть наиболее технически правильным подходом для установления МТС, приблизительное значение МТС может быть получено по имеющимся данным острого опыта с использованием значения, составляющего 1/3 от значения LC в остром опыте. Однако могут отсутствовать данные по острой токсичности для конкретного тестового вида, используемого в испытании. Если данные по острой токсичности для этого вида отсутствуют, то можно провести определение LC
за 96 ч на головастиках, которые используются в испытании на ОМЗ (т.е. находятся на одной стадии). При необходимости, если имеются данные по другим водным организмам (например, значения LC
для рыб или других земноводных), эксперт может использовать эти данные для определения вероятного значения МТС с применением межвидовой экстраполяции.
3.8.1.3 В качестве альтернативы, если это химическое вещество не является высокотоксичным в остром опыте и его растворимость составляет более 100 мг/л, то тогда значение 100 мг/л следует рассматривать в качестве самой высокой испытуемой концентрации (НТС), поскольку эта концентрация, как правило, считается практически "нетоксичной".
3.8.1.4 Несмотря на отсутствие рекомендованного протокола, могут быть использованы статические восстановительные методы в тех случаях, когда проточные методы являются недостаточными для достижения МТС. Если используются статические восстанавливаемые методы, то должна быть документирована и оставаться в пределах критериев эффективности стабильность химического вещества в испытуемой концентрации. Рекомендуется 24-часовой период восстановления. Период восстановления более 72 ч, неприемлем. Кроме того, параметры качества воды (например, содержание растворенного кислорода (DO), температура, рН и т.д.) должны измеряться в конце каждого периода восстановления и непосредственно перед восстановлением.
3.8.2 Диапазон испытуемых концентраций
Существует необходимый минимум, включающий три концентрации испытуемого вещества и чистую воду в качестве контроля (и контроль на растворитель при необходимости). Самая высокая и самая низкая концентрации должны различаться минимум примерно на один порядок. Максимальная разница между концентрациями составляет 0,1, а минимальная - 0,33.
4 Проведение испытания
4.1 Начало и проведение испытания
0-е сутки испытания
4.1.1 Воздействие начинают, когда к моменту его начала достаточное количество головастиков в стоковой популяции достигло стадии развития 51 согласно Nieuwkoop и Faber [9] и которые имеют возраст 17 сут или менее после оплодотворения. Для отбора тестовых организмов отбирают здоровых и нормальных головастиков из стоковой популяции и объединяют их в одном сосуде, содержащем соответствующий объем воды для разведения. Для определения стадии развития головастиков по отдельности извлекают из резервуара с объединенными головастиками с помощью небольшой сетки или сетчатого фильтра и помещают в прозрачную измерительную камеру (например, чашки Петри с диаметром 100 мм), содержащую воду для разведения. Для определения стадии развития предпочтительно не использовать анестезию, однако в противном случае можно провести индивидуальное обезболивание головастиков с использованием 100 мг/л трикаина метансульфоната (например, MS-222), соответствующим образом забуференного бикарбонатом натрия (рН 7,0) перед обработкой. Если применяется анестезия с использованием, например, MS-222, то необходимо проконсультироваться в соответствующих испытательных лабораториях по поводу применяемого метода и информировать об этом в отчете по результатам испытания. С головастиками следует обращаться осторожно во время перемещения для сведения к минимуму стресса и их травмирования.
4.1.2 Стадия развития головастиков определяется с помощью бинокулярного микроскопа. Для уменьшения вариабельности в определении конечной стадии развития, важно, чтобы определение возраста проводилось с максимально возможной точностью. Согласно [9], основным признаком развития организма для отбора головастиков со стадией развития 51 является морфология задних конечностей. Морфологию задних конечностей следует исследовать под микроскопом. Несмотря на то что указания в [9] по определению стадии развития должны быть приняты во внимание при определении стадии головастиков, можно надежно определить стадию с использованием известных морфологических признаков. Следующая таблица может быть использована для упрощения и стандартизации определения стадии развития в течение всего испытания с использованием известных морфологических признаков, связанных с различными стадиями развития, полагая, что развитие происходит нормально.
Таблица 2 - Известные морфологические признаки для определения стадий развития согласно Nieuwkoop и Faber
Известные морфологические признаки | Стадия развития | |||||||||||||||
51 | 52 | 53 | 54 | 55 | 56 | 57 | 58 | 59 | 60 | 61 | 62 | 63 | 64 | 65 | 66 | |
Задние конечности | X | X | X | X | X | X | X | |||||||||
Передние конечности | X | X | X | X | X | |||||||||||
Черепно-лицевая структура | X | X | X | X | ||||||||||||
Морфология обонятельного нерва | X | X | X | |||||||||||||
Длина хвоста | X | X | X | X | ||||||||||||
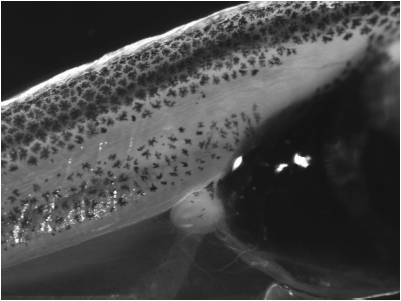
4.1.3 Для начала испытания все головастики должны быть на стадии 51. Наиболее ярким морфологическим признаком этой стадии является морфология задних конечностей, показанная на рисунке 1.
Рисунок 1 - Морфология задних конечностей X. Laevis головастика на стадии 51
4.1.4 Помимо отбора головастиков по стадии развития можно дополнительно использовать отбор тестовых организмов по размеру. С этой целью на сутки 0 измеряют полную длину тела (не SVL) для подгруппы в выборке примерно 20 NF стадии 51 головастиков. После расчета средней полной длины тела для этой группы организмов могут быть установлены минимальный и максимальный пределы для полной длины тела тестовых организмов, с допуском диапазона среднего значения ±3 мм (средние значения диапазона полной длины тела от 24,0 до 28,1 мм для стадии 51 головастиков). Тем не менее определение стадии развития является основным параметром в определении пригодности каждого тестового организма к испытанию. Головастиков с макроскопически видимыми пороками развития или травмами из испытания исключают.
4.1.5 Головастиков, которые отвечают критериям для требуемой в испытании стадии развития, описанным выше, содержат в резервуаре с чистой культуральной водой, пока не завершается процесс определения стадии развития других особей. После завершения определения стадии развития личинок произвольно распределяют в испытуемые резервуары для воздействия, пока каждый резервуар не будет содержать 20 личинок. Затем каждый испытуемый резервуар проверяют на наличие головастиков с аномальным внешним видом (например, травмы, аномальное плавательное поведение и т.д.). Головастиков с подобными и другими отклонениями удаляют из испытуемых резервуаров и заменяют вновь выбранными личинками из резервуара, в котором были объединены личинки.
4.2 Наблюдения
4.2.1 Для получения более подробной информации о процедурах по завершению испытания и обработке головастиков следует обратиться к Руководству ОЭСР по гистологии щитовидной железы земноводных [10].
7-е сутки испытания
4.2.2 На 7-е сутки из каждого испытуемого резервуара извлекают пять произвольно выбранных головастиков из каждой повторности. Произвольный характер процедуры обеспечивает возможность выбора любого организма в испытании с одинаковой вероятностью. Это достигается использованием любого метода рандомизации, но требуется, чтобы каждый головастик был учтен. Неотобранных головастиков возвращают в исходный резервуар и гуманно усыпляют с использованием 150-200 мг/л, например, MS-222, соответствующим образом забуференного бикарбонатом натрия до достижения рН 7,0. Подвергнутых эвтаназии головастиков промывают водой и высушивают с последующим определением массы тела с округлением до ближайшего целого числа в миллиграммах. Длину задних конечностей, длину от кончика морды до клоаки и стадию развития (с помощью бинокулярного микроскопа) определяют для каждого головастика.
21-е сутки испытания (окончание испытания)
4.2.3 По окончании испытания (21 сут) оставшихся головастиков удаляют из испытуемых резервуаров и гуманно усыпляют, например, 150-200 мг/л MS-222, соответствующим образом забуференным бикарбонатом натрия, как описано выше. Головастиков промывают водой и высушивают с последующим определением массы тела с округлением до ближайшего целого значения в миллиграммах. Определяют стадию развития, SVL и длину задних конечностей у каждого головастика.
4.2.4 Всех личинок помещают в фиксатор Дэвидсона на 48-72 ч, в виде цельных образцов или образцов с усеченными тканями головы, содержащими нижнюю челюсть для гистологической оценки. Для гистопатологических исследований в общей сложности отбирают пять головастиков из каждого параллельного резервуара. Поскольку высота фолликулярных клеток зависит от стадии развития [11], то наиболее подходящим методом отбора проб для гистологического анализа является использование особей соответствующей стадии развития, когда это возможно. Для того чтобы выбрать особей соответствующей стадии, у всех личинок вначале, еще до отбора и последующей обработки для сбора и хранения данных определяют стадию развития. Это необходимо, поскольку нормальные колебания в развитии могут привести в результате к различному распределению по стадии развития в каждом параллельном резервуаре.
4.2.5 Головастики, отобранные для гистопатологических исследований (n=5 из каждой повторности), должны соответствовать средней стадии развития в контроле (объединенные повторности), когда это возможно. Если имеются параллельные резервуары с более чем пятью личинками на соответствующей стадии, то произвольно выбирают пять личинок.
4.2.6 Если имеются параллельные резервуары с менее чем пятью личинками на соответствующей стадии развития, то произвольно отбирают особей со следующей более низкой или более высокой стадией развития для достижения общего размера выборки из пяти личинок на повторность. Решение отбирать дополнительных личинок со следующей более низкой или более высокой стадии развития предпочтительно принимать, основываясь на общей оценке распределения по стадиям контрольных и обработанных химическим веществом головастиков. То есть, если обработка химическим веществом является причиной задержки развития, тогда отбирают дополнительных личинок со следующей более низкой стадии. В свою очередь, если обработка химическим веществом связана с ускорением развития, дополнительные личинки отбираются со следующей более высокой стадии.
4.2.7 В случаях существенных изменений в развитии головастиков в результате воздействия испытуемого химического вещества не может быть никакого совмещения стадии в группах с обработкой химическим веществом с расчетной контрольной средней стадией развития. Только в этих случаях процесс отбора должен быть изменен согласно стадии, отличающейся от контрольной средней стадии для достижения выборки личинок соответствующей стадии для гистопатологического анализа щитовидной железы. Кроме того, если стадии не поддаются точному определению (т.е. имеется асинхронность в развитии), то произвольно отбирают по пять головастиков из каждой повторности для гистологического анализа. Следует указать логическое обоснование отбора любых личинок, которые находятся на стадии, не совпадающей со средней стадией развития в контроле.
4.3 Определение биологических конечных точек
Во время 21-суточного периода воздействия проводят измерение основных конечных точек на 7-е и 21-е сутки, однако необходимо проводить ежедневное наблюдение за испытуемыми организмами. В таблице 3 приведен обзор конечных точек измерений и соответствующих временных точек наблюдений. Более подробная информация по техническим процедурам измерения основных конечных точек и гистологических исследований представлена в [10].
Таблица 3 - Временные точки наблюдений для основных конечных точек в ОМЗ
Основные конечные точки | Ежедневно | 7-е сутки | 21-е сутки |
Гибель | - | ||
Стадия развития | - | - | |
Длина задних конечностей | - | - | |
Длина от кончика морды до клоаки | - | - | |
Сырая масса тела | - | - | |
Гистология щитовидной железы | - |
4.4 Основные конечные точки
4.4.1 Стадия развития, длина задних конечностей, SVL и сырая масса тела являются основными конечными точками ОМЗ, и каждая из них кратко описана ниже. Дополнительная техническая информация для сбора этих данных имеется в рекомендуемых для использования приложенных руководствах, включая процедуры компьютерного анализа.
4.4.2 Стадия развития
Стадия развития X. Laevis головастиков определяется с использованием критериев определения стадии по Nieuwkoop и Faber [9]. Результаты определения стадии развития используются для определения того, происходит развитие с ускорением, асинхронно, с задержкой или без изменений. Ускорение или задержка развития определяется сравнением средней стадии развития в контроле и в группах головастиков с обработкой испытуемым веществом. Развитие определяется как асинхронное, когда испытанные ткани не имеют уродств или аномалий, но относительное распределение во времени морфогенеза или развития различных тканей нарушается у одного головастика.
4.4.3 Длина задних конечностей
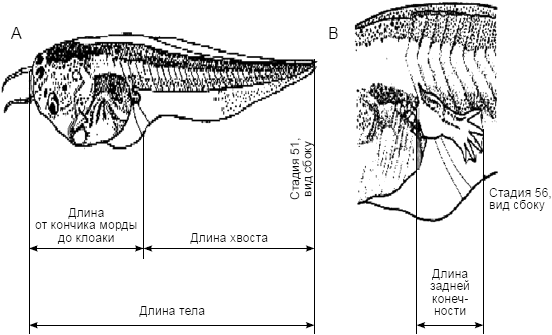
Дифференцировка и рост задних конечностей находятся под контролем гормонов щитовидной железы и являются основными показателями развития, которые ранее использовались для определения стадии развития. Развитие задних конечностей используется в определении стадии развития в виде качественного показателя, но в данном стандарте оно принимается в виде количественной конечной точки. Таким образом, длина задних конечностей измеряется в качестве конечной точки для выявления влияния испытуемого вещества на ось щитовидной железы (рисунок 2). Для единообразия длина задних конечностей измеряется на левой задней конечности. Длина задних конечностей оценивается на 7-е и 21-е сутки испытаний. На 7-е сутки измерение длины задней конечности осуществляется просто, как показано на рисунке 2. Однако измерение длины задних конечностей на 21-е сутки осложняется из-за появления изгибов в конечности. Таким образом, измерение длины задних конечностей на 21-е сутки начинают от стенки тела и продолжают по средней линии конечности через любые угловые изгибы. Изменения в длине задних конечностей на 7-е сутки, даже если они не обнаруживаются на 21-е сутки, по-прежнему считаются значимыми для потенциальной способности испытуемого вещества оказывать влияние на щитовидную железу. Измерение длины проводят по цифровым фотографиям с использованием программного обеспечения для анализа изображений, как описано в [10].
4.4.4 Длина тела и сырая масса тела
4.4.4.1 Определение длины тела от кончика морды до клоаки (SVL) (рисунок 2) и сырой массы включено в протокол испытания для оценки возможных последствий влияния испытуемых веществ на скорость роста головастиков в сравнении с контрольной группой, и они могут быть использованы в выявлении общей токсичности испытуемого вещества. Поскольку удаление прилипшей воды при определении массы тела может вызвать у головастиков стресс и может привести к повреждению кожи, то эти измерения выполняют на 7-е сутки в другой подгруппе в общей выборке головастиков, а для всех остальных головастиков при завершении испытания (21-е сутки). Для единообразия используют вид черепа в качестве каудального ограничения при измерении.
Рисунок 2 - (А) Типы измерения длины тела и (В) измерения длины задней конечности для головастиков X. Laevis [1]
4.4.4.2 Длина от кончика морды до клоаки (SVL) используется для оценки роста головастика, как показано на рисунке 2.
4.4.5 Гистология щитовидной железы
Несмотря на то что стадия развития и длина задней конечности являются важными конечными точками для оценки изменений в метаморфозе, связанных с воздействием испытуемого вещества, задержка развития сама по себе не может считаться диагностическим показателем отрицательного воздействия испытуемого химического вещества на щитовидную железу. Некоторые изменения могут быть обнаружены только с помощью обычного гистологического анализа. Диагностические критерии включают гипертрофию/атрофию щитовидной железы, гипертрофию фолликулярных клеток, гиперплазию фолликулярных клеток и в качестве дополнительных качественных критериев фолликулярную полость, коллоидное состояние и высоту/форму фолликулярных клеток. Следует представить классификацию тяжести изменений (4 класса). Информация о получении и обработке образцов для гистологического анализа и для выполнения гистологических анализов образцов ткани приведена в [10]. Лабораториям, выполняющим анализ впервые, необходимо проконсультироваться с опытными патологоанатомами с целью обучения до проведения гистологического анализа и оценки щитовидной железы. Явные и значительные изменения основных конечных точек, указывающие на ускорение или асинхронность развития, могут исключить необходимость в выполнении гистопатологического анализа щитовидной железы. Тем не менее отсутствие выраженных морфологических изменений или признаков задержки развития служит основанием для проведения гистологических анализов.
4.4.6 Гибель
Все испытуемые резервуары ежедневно осматривают на наличие мертвых головастиков и регистрируют номер каждого резервуара. Регистрируют дату, концентрацию и номер резервуара, где имела место гибель головастиков. При обнаружении мертвых особей их удаляют из испытуемого резервуара. Гибель, превышающая 10%, может указывать на неподходящие условия испытаний и токсические эффекты испытуемого химического вещества.
4.4.7 Дополнительные наблюдения
Регистрируют случаи аномального поведения и хорошо видимых уродств развития и повреждений у головастиков. Регистрируют дату, концентрацию и номер резервуара, где отмечено аномальное поведение, видимые уродства развития или повреждения. Нормальное поведение характеризуется нахождением головастиков во взвешенном состоянии в толще воды с хвостом, поднятым над головной частью, регулярным ритмичным биением хвостового плавника, периодическим всплытием, шевелением жаберной крышки и наличием реакции на раздражители. Аномальное поведение будет включать такие признаки, как плавание по поверхности, нахождение на дне резервуара, плавание в перевернутом или необычном положении, отсутствие всплытия и реакции на раздражители. Кроме того, следует регистрировать большую разницу в потреблении корма у головастиков, относящихся к различным обработкам. Видимые уродства и патологические повреждения могут включать морфологические аномалии (например, деформацию конечностей), геморрагические очаги, бактериальные или грибковые инфекции, это если назвать только некоторые из них. Такие показатели являются качественными, и наблюдаемые признаки следует сопоставить с похожими клиническими признаками, свидетельствующими о заболевании/стрессе, и сравнить с контрольными животными. Если возникновение или частота появления патологических признаков выше в обработанных резервуарах, чем в контрольных, то их следует расценивать как выраженные признаки проявления токсичности испытуемого вещества.
5 Данные и отчет о проведении испытания
5.1 Сбор данных
5.1.1 Все данные собирают с использованием электронных или ручных систем, которые соответствуют надлежащей лабораторной практике (GLP). Результаты исследования должны включать:
5.1.1.1 Испытуемое вещество:
- Характеристика испытуемого вещества: физико-химические свойства, информация о стабильности и способности к биологическому разложению.
- Химическая информация и данные: метод и частота приготовления разведений. Информация об испытуемом химическом веществе включает фактические и номинальные концентрации испытуемого вещества, а в некоторых случаях - продуктов разложения испытуемого вещества, как это соответствует ситуации. Могут потребоваться результаты химических измерений для стоковых растворов, а также для испытуемых растворов.
- Растворитель (если это не вода): обоснование выбора растворителя и характеристика растворителя (свойства, используемая концентрация).
5.1.1.2 Условия испытания:
- Рабочие записи: они состоят из описания наблюдений, касающихся функционирования системы испытания и поддерживающей среды и инфраструктуры. Стандартные записи включают: температуру окружающей среды, температуру, при которой проводилось испытание, световой период, состояние критических компонентов системы воздействия (например, насосы, счетчики циклов, давление), скорость потока, уровень воды, изменение бутылей со стоковыми растворами и записи по графику кормления. Общие показатели качества воды включают в себя: рН, содержание растворенного кислорода (DO), проводимость, общий йод, щелочность и жесткость.
- Отклонения от используемого метода испытания: эта информация должна включать любые сведения или хронологическое описание отклонений от протокола испытания.
5.1.1.3 Результаты
- Биологические наблюдения и данные: к ним относятся ежедневные наблюдения по гибели, потреблению корма, аномальному плавательному поведению, адинамии, потере равновесия, уродствам развития, патологическим повреждениям и т.д. Наблюдения и данные, собранные через определенные интервалы включают: стадии развития, длину задних конечностей, длину от ноздрей до клоаки и сырую массу.
- Статистические методы анализа и обоснование используемых методов; результаты статистического анализа предпочтительно приводятся в табличной форме.
- Результаты гистологических исследований: к ним относятся изложенные в хронологическом порядке описания морфологии, а также выводы по классификации степени тяжести и частоте патологических изменений, как указано в руководящем документе по гистопатологии.
- Особые замечания: эти наблюдения должны включать изложенные в хронологическом порядке описания исследования, не попадающие в вышеописанные категории.
5.1.1.4 Представление результатов испытаний
В приложении Б приводятся электронные таблицы для ежедневного сбора данных, которые могут использоваться в качестве руководства для ввода необработанных данных и для расчета сводных статистических данных. Кроме того, приводятся таблицы для регистрации получаемых данных, удобные для обобщения сводных данных по конечным точкам. Отчетные таблицы для гистологических оценок приведены в приложении Б.
5.2 Критерии качества и приемлемости/достоверности испытания
Как правило, грубые отклонения от протокола испытаний приводят к получению данных, непригодных для интерпретации или отчетности. Таким образом, в качестве руководства были разработаны приведенные в таблице 4 критерии для определения качества испытания, общей характеристики контрольных организмов.
Таблица 4 - Критерии качества для ОМЗ
Критерий | Допустимые пределы |
Испытуемая концентрация | Поддерживается не более 20% CV (вариабельность измеряемой испытуемой концентрации) на 21 сут испытаний |
Гибель в контрольных группах | Не более 10% - гибель в любой из повторностей в контрольной группе не должна превышать 2 головастиков |
Минимальная средняя стадия развития в контроле в конце испытания | 57 |
Размах данных по определению стадии развития в контрольной группе | 10 и 90-й процентильный размах данных по определению стадии развития не должен отличаться более чем на 4 стадии |
Растворенный кислород | Не менее 40% насыщения воздухом* |
рн | Значение рН должно поддерживаться в пределах 6,5-8,5. Разница между повторностями/между обработками не должна превышать 0,5 |
Температура воды | Температура (22±1)°C - разница между повторностями/между обработками не должна превышать 0,5°C |
Испытуемая концентрация без проявления явной токсичности | Не менее 2 |
Повторности | Не более 2 повторностей в испытании может быть нарушено |
Особые условия использования растворителя | Если применяется растворитель-носитель, то должны быть использованы контроль на растворитель и чистый контроль с водой и результаты представлены |
Особые условия использования растворителя | Статистически значимые различия между контролем на растворитель и водой, используемой в качестве контроля, рассматриваются особо. |
Специальные условия для статистической восстанавливаемой системы | Репрезентативный химический анализ следует представлять до и после восстановления |
Уровни аммиака следует измерять непосредственно перед восстановлением | |
Все показатели качества воды, приведенные в таблице А.1 приложения А, следует измерять непосредственно перед восстановлением | |
Период восстановления не должен превышать 72 ч | |
Соответствующий график кормления (50% суточного пищевого рациона Sera Micron ®) | |
* Аэрация воды может поддерживаться с помощью барботеров. Рекомендуется установить барботеры на уровнях, не создающих избыточный стресс для головастиков | |
5.3 Достоверность испытания
Следующие требования должны быть выполнены, чтобы считать испытание приемлемым/достоверным.
Достоверный результат эксперимента в испытании, определяемый как отрицательный результат в отношении активности щитовидной железы:
1) для любой определенной обработки, включая контроль, гибель должна быть не более 10%. Для любой определенной повторности гибель не должна превышать гибель трех головастиков, в противном случае повторности нарушаются;
2) для анализа представляют не менее двух уровней обработок со всеми четырьмя ненарушенными повторностями;
3) для анализа представляют не менее двух уровней обработок без проявления общей токсичности.
Достоверный результат эксперимента в испытании, определяемый как положительный результат в отношении активности щитовидной железы:
может иметь место гибель не более двух головастиков/повторность в контрольной группе.
5.4 Схема обоснования порядка проведения ОМЗ
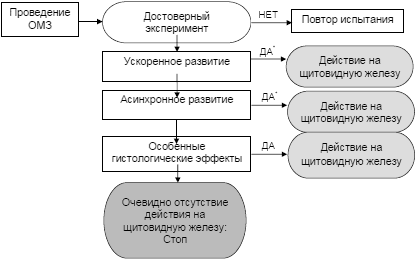
5.4.1 Разработана схема обоснования порядка проведения ОМЗ, чтобы помочь в постановке и интерпретации результатов биологического анализа (см. рисунок 3). В данной схеме в основном оцениваются конечные точки, среди которых особое значение уделяется таким показателям, как ускоренное развитие, асинхронное развитие и результаты гистологии щитовидной, в то время как задержка развития, длина от кончика морды до клоаки и сырая масса тела представляют параметры, которые потенциально могут находиться под влиянием общей токсичности, и их оценка имеет меньшее значение.
5.4.2 Ускоренное развитие (определяется по стадии развития, SVL и HLL).
5.4.2.1 Известно, что ускоренное развитие опосредовано эффектами, связанными с гормонами щитовидной железы. Это могут быть эффекты периферических тканей, такие как прямое взаимодействие с рецептором гормона щитовидной железы (например, с Т4), или эффекты, которые изменяют уровни циркулирующего гормона щитовидной железы. В любом случае это считается достаточным доказательством, чтобы показать, что химическое вещество оказывает активное влияние на щитовидную железу. Ускоренное развитие оценивается одним из двух следующих методов. В первом определяется общая стадия развития с помощью стандартизированного подхода, описанного Nieuwkoop и Faber [9]. Во втором количественно определяют специфические морфологические признаки, например, длину задних конечностей на 7-е и 21-е сутки, которые непосредственно связаны с агонистическим воздействием на рецептор гормона щитовидной железы. Если происходят статистически значимые изменения в развитии или длине задних конечностей, то испытание показывает, что химическое вещество оказывает активное влияние на щитовидную железу.
Рисунок 3 - Схема обоснования порядка проведения ОМЗ
* Примечание - Проведение гистологических исследования может быть требованием некоторых регулирующих органов, несмотря на имеющиеся существенные различия, проявляющиеся в ускоренном и асинхронном развитии. Экспериментатору, выполняющему данное испытание, рекомендуется проконсультироваться в соответствующих органах до проведения испытания, чтобы определить требуемые конечные точки.
5.4.2.2 Оценка тестовых организмов на наличие ускоренного развития в сравнении с контрольной популяцией основывается на результатах статистического анализа, выполненного для следующих четырех конечных точек:
- длина задней конечности (нормированная SVL) на 7-е сутки испытания;
- длина задней конечности (нормированная SVL) на 21-е сутки испытания;
- стадия развития на 7-е сутки испытания;
- стадия развития на 21-е сутки испытания.
5.4.2.3 Статистический анализ по длине задней конечности выполняют на основе данных измерения длины левой задней конечности. Длина задней конечности нормализуется как отношение длины задней конечности к длине от кончика морды до клоаки у отдельной особи. Затем сравниваются средние нормализованные значения для каждой концентрации. На ускоренное развитие будет указывать статистически значимое увеличение средней длины задней конечности (нормализованной к длине от кончика морды до клоаки) в группе, обработанной испытуемым веществом, по сравнению с контрольной группой на 7-е и/или 21-е сутки испытания (см. приложение В).
5.4.2.4 Статистический анализ данных по стадии развития выполняют, основываясь на определении стадии развития в соответствии с морфологическими критериями, описанными Nieuwkoop и Faber [9]. Ускоренное развитие идентифицируется, когда результаты многофакторного анализа свидетельствуют о достоверном наличии более высокой стадии развития в группе, обработанной химическим веществом, по сравнению с контрольной группой на 7-е и/или 21-е сутки испытания.
5.4.2.5 В методе испытаний ОМЗ достоверное изменение любой из четырех конечных точек, указанных выше, считается достаточным, чтобы сделать положительное заключение об ускоренном развитии. То есть для статистически значимого влияния на длину задней конечности в определенной временной точке не требуется наличия доказательств достоверного влияния на длину задней конечности в другой временной точке или достоверного влияния на стадию развития на эту временную точку. В свою очередь, для статистически значимого влияния на стадию развития в определенной временной точке не требуется доказательств достоверного влияния на стадию развития в другой временной точке или достоверного влияния на длину задней конечности на эту временную точку. Однако значимость доказательств для ускоренного развития повышается, если достоверный эффект обнаруживается для более чем одной конечной точки.
5.4.3 Асинхронное развитие (определяется с помощью критериев определения стадии развития).
5.4.3.1 Асинхронное развитие характеризуется нарушением относительного времени морфогенеза или развития различных тканей у одного головастика. Неспособность четко определить стадию развития организма с помощью набора морфологических конечных точек, которые рассматриваются в качестве стандартных для определенной стадии, показывает, что ткани развиваются асинхронно через метаморфоз. Асинхронное развитие является показателем активности испытуемого вещества в отношении щитовидной железы. Единственный известный к настоящему времени механизм, вызывающий асинхронное развитие, опосредуется через воздействие химических веществ на периферическое действие гормонов щитовидной железы и/или метаболизм гормонов щитовидной железы в развивающихся тканях, как это наблюдается с ингибиторами дейодиназы.
5.4.3.2 Оценка тестовых организмов на наличие асинхронного развития по сравнению с контрольной популяцией основывается на общей морфологической оценке тестовых организмов на 7-е и/или 21-е сутки испытания.
5.4.3.3 Описание нормального развития Xenopus Laevis согласно критериям Nieuwkoop и Faber [9] дает основу идентифицировать последовательный порядок нормального ремоделирования ткани. Термин "асинхронное развитие" специфически относится к отклонениям в общей морфологии развития у головастиков, затрудняющим проведение окончательного определения стадии развития в соответствии с критериями Nieuwkoop и Faber [9], потому что основные используемые морфологические признаки характерны для разных стадий развития.
5.4.3.4 К термину "асинхронное развитие" относятся только случаи, которые свидетельствуют об отклонениях в ремоделировании определенных тканей относительно ремоделирования других тканей. Некоторые классические фенотипы включают задержку или отсутствие появления передней конечности, несмотря на нормальное или ускоренное развитие задних конечностей и тканей хвоста, или преждевременную резорбцию жабр относительно стадии морфогенеза задних конечностей и резорбции хвоста. Конкретного головастика относят к особи с асинхронным развитием, если его невозможно отнести к определенной стадии, поскольку его развитие не соответствует большинству из основных критериев, используемых для определения стадии развития по Niewkoop и Faber [9], или если есть чрезмерная задержка или ускорение одной или нескольких основных особенностей (например, хвост полностью резорбируется, но передние конечности не появились). Такая оценка носит качественный характер, и следует изучить полный набор ориентировочных критериев, перечисленных Nieuwkoop и Faber [9]. Однако необязательно регистрировать статус развития по различным ориентировочным признакам у обследуемых особей. Особи, определенные как особи с асинхронным развитием, не подлежат определению стадии развития по Nieuwkoop и Faber [9].
5.4.3.5 Таким образом, главным критерием для установления аномального морфологического развития в виде "асинхронного развития", является то, что нарушается относительное время ремоделирования и морфогенеза тканей, тогда как морфология затронутых тканей является нормальной. Одним из примеров толкования выраженных морфологических аномалий является замедленный морфогенез задних конечностей относительно развития других тканей, соответствующий критерию "асинхронного развития", тогда как случаи, показывающие отсутствие задних конечностей, наличие аномальных пальцев (например эктродактилия, полидактилия) или других выраженных уродств конечностей не следует рассматривать в качестве "асинхронного развития".
5.4.3.6 В данном контексте основные морфологические признаки, которые должны быть оценены для характеристики протекания метаморфоза, должны включать морфогенез задних конечностей, морфогенез передних конечностей, появление передних конечностей, стадию резорбции хвоста (особенно резорбцию хвостового плавника) и морфологию головного участка (например, размер жабр и стадию резорбции жабр, морфологию нижней челюсти, мекелев дивертикул).
5.4.3.7 В зависимости от способа воздействия испытуемого вещества могут возникнуть широко различающиеся морфологические фенотипы. Некоторые классические фенотипы включают в себя задержку появления или отсутствие передней конечности, несмотря на нормальное или ускоренное развитие задних конечностей и ткани хвоста, преждевременную резорбцию жабр относительно ремоделирования задней конечности и хвоста.
5.4.4 Гистопатология
5.4.4.1 Если химическое вещество не вызывает высокой общей токсичности, не ускоряет развития или не приводит к асинхронному развитию, то исследуется гистопатология щитовидной железы с помощью [10]. Отставание в развитии, при отсутствии токсичности, является веским доказательством антитиреоидной активности испытуемого вещества, но определение стадии развития является менее чувствительным и менее ценным в диагностическом отношении, чем гистопатологический анализ щитовидной железы. С учетом этого обстоятельства проведение гистопатологического исследования щитовидной железы в данном случае необходимо. Воздействие на гистологию щитовидной железы демонстрируется в отсутствие влияния на развитие. Если изменения в гистопатологии щитовидной железы имеют место, то химическое вещество считается активным для щитовидной железы. Если задержка в развитии отсутствует или не наблюдаются патологические изменения в микроструктуре щитовидной железы, то химическое вещество считается неактивным для щитовидной железы. Основанием для этого решения является то, что щитовидная железа находится под влиянием ТТГ и любое химическое вещество, изменяющее циркуляцию гормона щитовидной железы, достаточно для изменения секреции ТТГ, что в конечном итоге будет приводить к гистопатологическим изменениям в щитовидной железе. Различные способы и механизмы действия могут изменить циркуляцию гормона щитовидной железы. Таким образом, несмотря на то, что уровень гормона щитовидной железы свидетельствует об эффекте, связанном с щитовидной железой, этого недостаточно, чтобы определить, какой способ или механизм действия непосредственно ответственен за ответную реакцию.
5.4.4.2 Поскольку эта конечная точка не подлежит анализу с использованием основных статистических подходов, то определение эффекта, связанного с воздействием химического вещества, должно осуществляться на основе экспертного заключения патологоанатома.
5.4.5 Задержка развития (определяется по стадии развития, HLL, BW, SVL)
5.4.5.1 Задержка развития может иметь место в результате антитиреоидного действия и опосредованной токсичности испытуемого вещества. Незначительная задержка развития в сочетании с явными признаками общей токсичности, вероятнее всего, указывает на неспецифический токсический эффект на щитовидную железу. Оценка токсичности, не связанной с щитовидной железой, является важным элементом испытания для снижения вероятности получения ложноположительных результатов. Очень высокая гибель является очевидным свидетельством того, что имеют место другие механизмы токсичности, а не антитиреоидное действие. Аналогичным образом незначительное снижение роста, что определяется сырой массой и/или длиной SVL, также предполагает проявление токсичности, не связанной с щитовидной железой. Кажущееся увеличение роста, как правило, наблюдается для веществ, которые негативно влияют на нормальное развитие. Следовательно, появление крупных особей не обязательно указывает на токсичность, которая не связана с щитовидной железой. Тем не менее никогда не используют только один такой критерий, как рост, для определения токсичности для щитовидной железы. Напротив, рост в сочетании с данными по стадии развития и гистопатологии щитовидной железы должен использоваться для определения активности испытуемого вещества для щитовидной железы. Также следует учитывать другие параметры при определении общей токсичности, которые включают отек, геморрагии, адинамию, снижение потребления корма, неустойчивое/измененное плавательного поведения и т.д. Если все испытуемые концентрации демонстрируют признаки общей токсичности, то испытуемое вещество должно быть повторно испытано в более низких испытуемых концентрациях, прежде чем определить, является ли вещество потенциально активным или неактивным для щитовидной железы.
5.4.5.2 Статистически значимая задержка развития в отсутствие других признаков общей токсичности показывает, что испытуемое химическое вещество является активным (обладает антагонистическим действием) для щитовидной железы. При отсутствии статистически значимых отклонений этот результат может быть дополнен результатами гистопатологии щитовидной железы.
5.5 Статистические анализы
5.5.1 Статистический анализ данных должен выполняться в соответствии с процедурами, описанными в [12]. Для всех непрерывных количественных конечных точек (HHL, SVL, сырая масса) в соответствии с монотонной зависимостью "доза-ответ" для установления значимого эффекта воздействия следует использовать тест Джонкхиера-Терпстра с пошаговым понижением.
5.5.2 Для непрерывных конечных точек, которые не соответствуют монотонной зависимости "доза-ответ", данные должны быть оценены на нормальность (например, с помощью тестов Шапиро-Уилка или Андерсон-Дарлинга) и однородность дисперсии (с помощью теста Левена). В обоих исследованиях проводится анализ остатков ANOVA. Вместо формальных тестов для оценки нормальности и однородности дисперсии может применяться и экспертное заключение, хотя формальные тесты являются предпочтительными. В тех случаях, когда выявлено отсутствие нормальности или неоднородности дисперсии, данные подвергают преобразованию. Если данные после преобразования являются нормально распределенными с однородной дисперсией, то значимый эффект воздействия определяется тестом Дунетта. Если данные после преобразования становятся нормально распределенными с неоднородной дисперсией, то значимый эффект воздействия определяется тестом Тамхане-Дунетта (Т3 тест) или U-тестом Манна-Уитни-Вилкоксона. В случае если после преобразования данные не распределяются нормально, то значимые отличия могут быть установлены с применением критерия Манна-Уитни-Вилкоксона (U-тест) с помощью поправки Бонферони-Холма к р-значениям. Тест Дунетта применяется независимо от F-теста ANOVA, тестов Манна-Уитни, Крускалла-Уоллиса.
5.5.3 Статистически значимой гибели не ожидается, но когда данные характеризуются монотонностью "доза-эффект", то она должна быть оценена критерием Кохрана-Армитажа, в противном случае - точным критерием Фишера с поправкой Бонферрони-Холма.
5.5.4 Статистически значимое влияние на стадию развития можно оценить с использованием критерия Джонкхиера-Терпстра, который применяется к медианам реплик. Кроме того, для определения влияния предпочтительно использовать тест Джонкхиера для нескольких выборок, в диапазоне от 20 до 80 процентилей, так как в нем учитываются изменения в профиле распределения.
5.5.5 Подходящая единица для анализа - это повторности (реплики). Если используется тест Джонкхиера-Терпстра или U-тест Манна-Уитни, тогда данные представляются медианами повторных данных, либо, если используется тест Дунетта, - средних от повторов. Монотонность кривых "доза-ответ" может быть оценена визуально из повторов средних, или медиан, либо от формальных тестов, таких, как описано в [12]. По возможности тесты Джонкхиера-Терпстра и Манна-Уитни используют не менее чем на пяти повторностях в опытных и контрольных группах. Статистическая значимость всех тестов оценивается на уровне значимости 0.05.
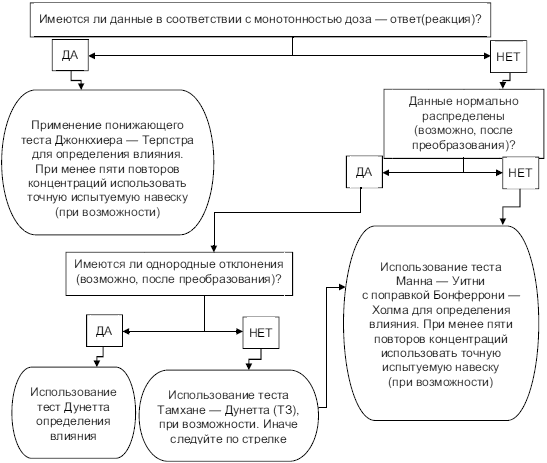
5.5.6 Рисунок 4 представляет собой блок-схему для выполнения статистических тестов непрерывных данных.
Рисунок 4 - Блок-схема для статистических методов для непрерывных (постоянных) данных ответа (реакции)
5.6 Обсуждение данных специфических анализов
5.6.1 Использование нарушенных уровней обработки
Несколько факторов учитываются при определении общей токсичности для повторностей и всего воздействия, и их следует исключить из анализа. Общая токсичность определяется как гибель >2 особей в каждой повторности, которую можно объяснить только токсичностью, а не техническими ошибками. Другие признаки общей токсичности включают геморрагии, аномальное поведение, аномальный характер плавания, отсутствие потребления корма, а также любые другие признаки, представляющие собой клинические признаки патологического состояния. Для сублетальных признаков токсичности могут потребоваться качественные оценки, и всегда они должны проводиться по сравнению с чистой контрольной группой, получавшей воду.
5.6.2 Контроль на растворитель
Использование растворителя следует рассматривать только в качестве последнего средства, когда все другие варианты доставки испытуемого химического вещества проверены. Если используют растворитель, то в испытание также должен быть включен чистый контроль, т.е. вода. По завершении испытания должна быть выполнена оценка возможных последствий воздействия растворителя. Это делается с помощью статистического сравнения контрольной группы с растворителем и группы чистого контроля, т.е. с водой. На наиболее важные конечные точки при учете результатов в данном испытании, стадию развития, SVL и сырую массу также могут оказать влияние эффекты, не связанные с щитовидной железой. Если статистически значимые различия обнаружены в этих конечных точках между чистым контролем с водой и контролем на растворитель, то определяют конечные точки для ответных реакций с использованием чистого контроля, представляющего воду. Если статистически значимые различия между чистым контролем с водой и контролем на растворитель отсутствуют для всех измеряемых показателей, то определяют конечные точки испытания для ответных реакций с использованием чистого контроля, представляющего воду, и контроля на растворитель.
5.6.3 Обработанные группы, достигающие стадии развития 60 и выше
5.6.3.1 После стадии 60 у головастиков происходит снижение размера и массы за счет резорбции тканей и уменьшения абсолютного содержания воды. Таким образом, измерение сырой массы и SVL для особей со стадией развития >NF60 не может использоваться для статистического анализа за счет различий в показателях прироста. Поэтому сырая масса и данные по длине тела головастиков со стадией развития >NF60 не могут использоваться в анализе повторов или медиан повторов. Два разных подхода могут быть использованы для анализа параметров, связанных с ростом.
5.6.3.2 Один подход заключается в проведении измерений только с головастиками, находящимися на стадии развития ниже или равной стадии 60, для статистического анализа сырой массы и/или SVL. Этот подход, как полагается, обеспечивает достаточно надежную информацию об уровне выраженности возможных эффектов в отношении роста, если только небольшая часть тестовых организмов удаляется из анализа (20%). Если у большого количества головастиков (
20%) имеет место более высокая стадия развития, чем стадия 60 при одной или нескольких номинальных концентрациях, то проводят двухфакторный иерархический анализ ANOVA для всех головастиков в целях оценки влияния испытуемого вещества на рост, принимая во внимание влияние конечной стадии развития на рост. В приложении В приведены рекомендации по двухфакторному ANOVA для массы и длины головастиков.
Приложение А
(рекомендуемое)
Экспериментальные условия оценки метаморфоза земноводных в течение 21 сут
Таблица А.1 - Экспериментальные условия оценки метаморфоза земноводных в течение 21 сут
Тестовые организмы | Личинки Xenopus Laevis | ||
Начальная личиночная стадия | Nieuwkoop и Faber стадия 51 | ||
Период воздействия | 21-е сут | ||
Критерии отбора личинок | Стадия развития и общая длина (необязательно) | ||
Испытуемые концентрации | Минимум три концентрации, охватывающие примерно один порядок величины | ||
Режим воздействия | Проточный (предпочтительно) и/или статистического восстановления | ||
Скорость потока в испытуемой системе | 25 мл/мин (полностью замененный объем приблизительно каждые 2,7 ч) | ||
Основные конечные точки/сутки определения | Гибель | Ежедневно | |
Стадия развития | 7 и 21 сут | ||
Длина задних конечностей | 7 и 21 сут | ||
Длина от кончика морды до клоаки | 7 и 21 сут | ||
Сырая масса тела | 7 и 21 сут | ||
Гистология щитовидной железы | 21 сут | ||
Разведенная вода/лабораторный контроль | Дехлорированная водопроводная вода (активированным углем) или эквивалентный лабораторный источник | ||
Плотность личинок | 20 личинок/испытуемый сосуд (5 л) | ||
Испытуемый раствор/испытуемый сосуд | 4-10 л (воды минимум 10-15 см)/испытуемый сосуд из стекла или нержавеющей стали (например, 22,5х14х16,5 см) | ||
Повторности | 4 повторности испытуемых сосудов/испытуемые концентрации и контроль | ||
Допустимый уровень гибели в контролях | 10% в повторности испытательного сосуда | ||
Фиксация образцов щитовидной железы | Фиксируемое количество | Все головастики (первоначально оцениваются 5 головастиков на повторность) | |
Область | Голова или все тело | ||
Фиксирующая жидкость | Фиксатор Дэвидсона | ||
Кормление | Питание | Сыворотка Микрон | |
Количество/периодичность | Смотри таблицу 1 по режиму кормления с использованием Сыворотки Микрон | ||
Освещение | Световый день | 12 ч света; 12 ч темноты | |
Интенсивность | От 600 до 2000 люкс (измеряется на поверхности воды) | ||
Температура воды | (22±1)°С | ||
рН | 6,5-8,5 | ||
Концентрация растворенного кислорода (DO) | Более 3,5 мг/л (более 40% насыщенного воздуха) | ||
Примерное расписание аналитической химии | Один раз/неделя (4 примерных события/испытание) | ||
Приложение Б
(рекомендуемое)
Отчетные таблицы для первичных и итоговых данных
Химическая информация:
Введение испытуемого вещества, концентрация единиц измерения и обработки.
Таблица Б.1 - Общий анализ информации о химическом веществе
Испытуемое вещество: | ||
Концентрация (единицы измерения): | ||
Обработка 1: | ||
Обработка 2: | ||
Обработка 3: | ||
Обработка 4: | ||
Дата (0-е сутки): | 00/00/00 | Дата ввода (мм/дд/гг) |
Дата (7-е сутки): | 00/00/00 | Дата ввода (мм/дд/гг) |
Дата (21-е сутки): | 00/00/00 | Дата ввода (мм/дд/гг) |
Таблица Б.2 - Сбор первичных данных листы для 7-х и 21-х суток
Х день
Дата 00/00/00
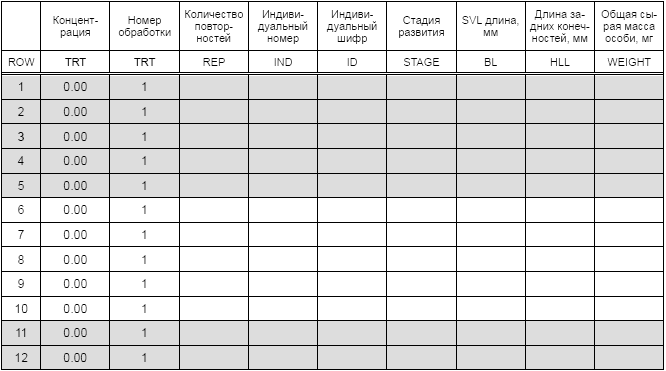
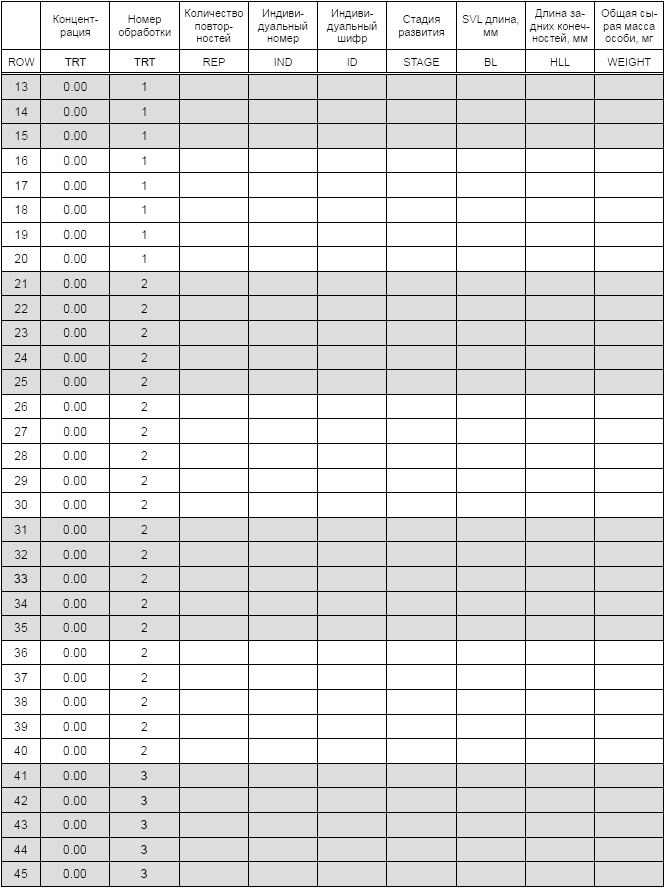
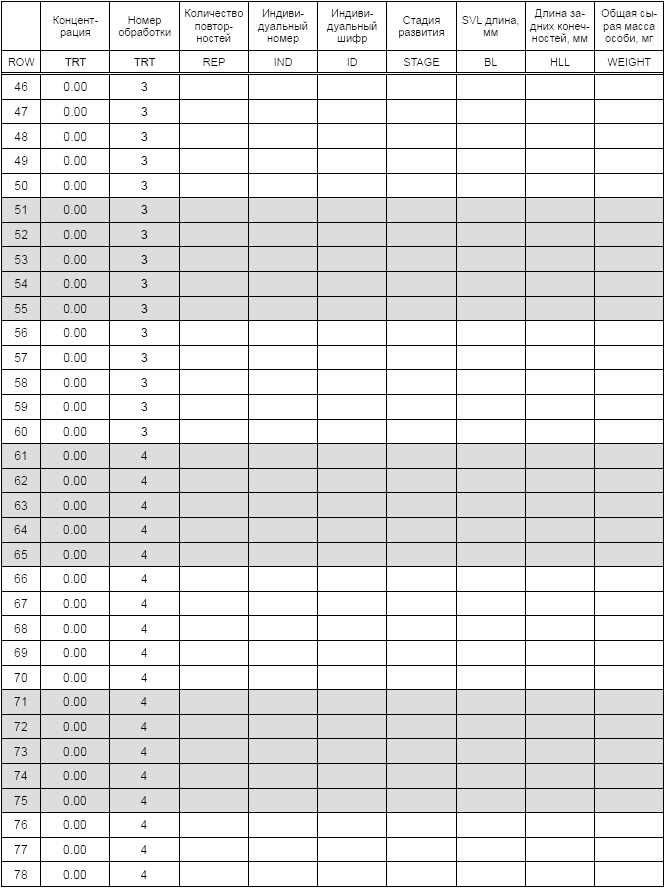
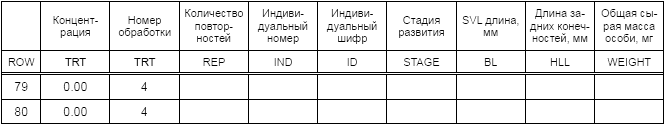
Таблица Б.3 - Обобщение данных по конечным точкам на 7-е и 21-е сутки
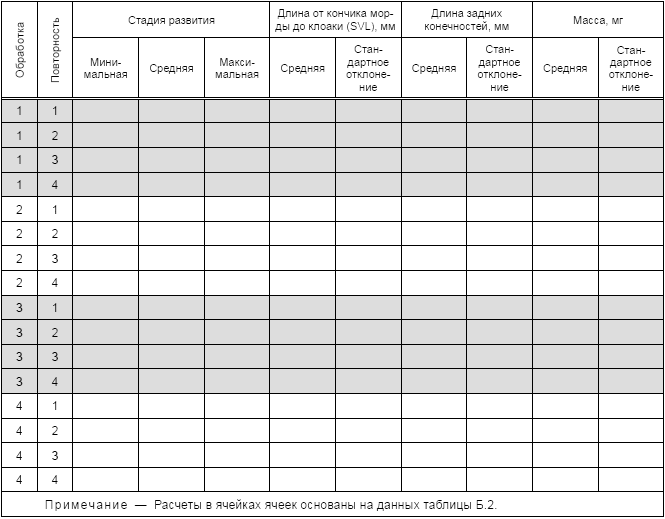
Таблица Б.4 - Ежедневные данные по гибели
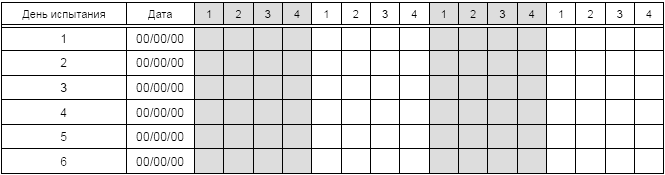
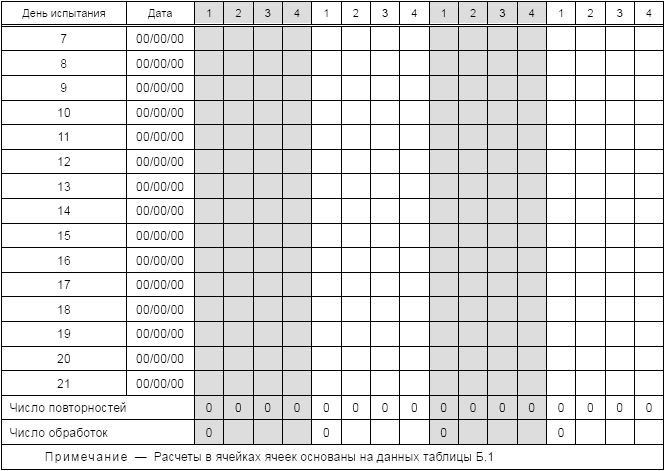
Таблица Б.5 - Критерии качества воды
Система воздействия (проточная/статистического восстановления): | |
Температура: | |
Интенсивность света: | |
Цикл свет-темнота | |
Кормление: | |
Норма кормления: | |
рН воды: | |
Концентрация йода в воде, используемой в испытании |
Таблица Б.6 - Сводные данные по химическому анализу
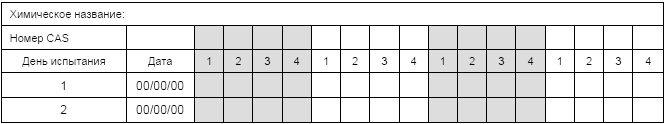
Таблица Б.7 - Таблицы по регистрации данных по гистопатологии по основным критериям
Дата: | Химическое вещество: | Патологоанатом: | ||||||||||
Гипер- | Атрофия щито- | Фолли- | Фолли- | Гипер- | Атрофия щито- | Фолли- | Фолли- | |||||
Контроль- | _____ доза особь N - повтор- | |||||||||||
Контроль- | _____ доза особь N - повтор- | |||||||||||
Всего: | Всего: | |||||||||||
Гипер- | Атрофия щито- | Фолли- | Фолли- | Гипер- | Атрофия щито- | Фолли- | Фолли- | |||||
_____ доза особь N - повтор- | _____ доза особь N - повтор- | |||||||||||
_____ доза особь N - повтор- | _____ доза особь N - повтор- | |||||||||||
Всего: | Всего: | |||||||||||
Таблица Б.8 - Дополнительные критерии для гистопатологии
Дата: | Химическое вещество: | Патологоанатом: | ||||||
Увеличение области фолли- | Уменьшение области фолли- | Увеличение области фолли- | Уменьшение области фолли- | |||||
Контрольная особь N - повторность 1 | _____ доза особь N - повторность 1 | |||||||
Контрольная особь N - повторность 2 | _____ доза особь N - повторность 2 | |||||||
Всего: | Всего: | |||||||
Увеличение области фолли- | Уменьшение области фолли- | Увеличение области фолли- | Уменьшение области фолли- | |||||
_____ доза особь N - повторность 1 | _____ доза особь N - повторность 1 | |||||||
_____ доза особь N - повторность 2 | _____ доза особь N - повторность 2 | |||||||
Всего: | Всего: | |||||||
Таблица Б.9 - Описание результатов гистопатологических исследований
Дата: Химическое вещество: Патологоанатом: | ||
Описание результатов | ||
Контрольная особь N - повторность 1 | ||
Контрольная особь N - повторность 2 | ||
________ доза особь N - повторность 1 | ||
________ доза особь N - повторность 2 | ||
________ доза особь N - повторность 1 | ||
________ доза особь N - повторность 2 | ||
________ доза особь N - повторность 1 | ||
________ доза особь N - повторность 2 | ||
Таблица Б.10 - Форма итоговой таблицы для х (7 или 21) суток ОМЗ
Контроль | Доза 1 | Доза 2 | Доза 3 | |||||||||||||||||
Конечная точка | Повтор- | Сред- | SD | CV | N | Сред- | SD | CV | N | р-значение | Сред- | SD | CV | N | р-значение | Сред- | SD | CV | N | р-значение |
Длина задних конечностей, мм | 1 | |||||||||||||||||||
2 | ||||||||||||||||||||
3 | ||||||||||||||||||||
4 | ||||||||||||||||||||
Среднее значение | ||||||||||||||||||||
SVL, мм | ||||||||||||||||||||
1 | ||||||||||||||||||||
2 | ||||||||||||||||||||
3 | ||||||||||||||||||||
4 | ||||||||||||||||||||
Среднее значение | ||||||||||||||||||||
Вес с влагой, мг | ||||||||||||||||||||
1 | ||||||||||||||||||||
2 | ||||||||||||||||||||
3 | ||||||||||||||||||||
4 | ||||||||||||||||||||
Среднее значение | ||||||||||||||||||||
Таблица Б.11 - Итоговый отчетный табличный шаблон для х (7 или 21) суток данных стадий развития для ОМЗ
Контроль | Доза 1 | Доза 2 | Доза 3 | |||||||||||||||||
Повтор- | Сред- | SD | CV | N | Сред- | SD | CV | N | р- | Сред- | SD | CV | N | р- | Сред- | SD | CV | N | р- | |
Стадия развития | ||||||||||||||||||||
1 | ||||||||||||||||||||
2 | ||||||||||||||||||||
3 | ||||||||||||||||||||
4 | ||||||||||||||||||||
Среднее значение | ||||||||||||||||||||
Приложение В
(рекомендуемое)
Альтернативный анализ массы и длины в случае наличия поздней стадии развития у более чем 20% головастиков при одной или более концентрациях испытуемого вещества
Если у большого числа головастиков не менее 20% имеется стадия развития 60 при одной или более номинальных концентрациях испытуемого вещества, то проводят двухфакторный иерархический анализ ANOVA для всех головастиков в целях оценки влияния испытуемого вещества на рост с учетом поздней стадии развития.
Рекомендуется использовать все данные, но необходимо учитывать влияние поздней стадии развития. Это может быть сделано с помощью двухфакторного иерархического анализа ANOVA. Наличие поздней стадии, т.е. результат "Да", определяют для головастика, если имеется стадия развития 61 или выше. В противном случае устанавливают отсутствие поздней стадии, т.е. результат "Нет". Тогда проводят двухфакторный анализ ANOVA относительно концентрации, и взаимосвязь поздней стадии и концентрации осуществляется с Rер(Конц) в качестве случайного фактора и Головастик(Rер) с другим случайным воздействием. Это также относится к повтору в качестве единицы анализа и дает, по существу, те же результаты как взвешенный анализ с rep* поздняя стадия, взвешенных по количеству животных в среднем. Если данные не соответствуют требованиям нормальности или дисперсии однородности для анализа ANOVA, то для элиминации этого недостатка проводится нормализация.
В дополнение стандартные F-тесты ANOVA для оценки влияния Конц, Поздней стадии и их взаимосвязи, взаимосвязи F-тестов можно "слайсировать" на два дополнительных F-теста ANOVA, на средних откликах по всей концентрации для "Поздняя стадия" = "Нет", а другой - на средних откликах по всей концентрации для "Поздняя стадия" = "Да". Дальнейшие сравнения средних обработок против контроля выполняются в пределах каждого уровня "Поздняя стадия". Анализ тенденций может осуществляться с использованием соответствующих контрастов или простых попарных сравнений, если есть доказательства немонотонности зависимости доза-отклик в пределах уровня переменной "Поздняя стадия". Поправка Бонферони-Холма для р-значений проводится только тогда, когда соответствующий F-слайс не имеет существенного значения. Это может быть сделано в SAS и, вероятно, в других пакетах статистического программного обеспечения. Осложнения могут возникнуть, когда отсутствуют поздние стадии у животных при некоторых концентрациях, но эти ситуации могут обрабатываться прямым способом.
Приложение ДА
(справочное)
Сравнение структуры международного документа со структурой настоящего стандарта
Таблица ДА.1
Структура настоящего стандарта | Структура международного документа | |||
Разделы | Подразделы | Перечисления | Разделы | Перечисления |
Введение | 1 | - | ||
1 | - | - | - | - |
2 | 2.1 | - | 2 | - |
2.2 | - | 3 | - | |
3 | 3.1 | - | 4 | - |
3.2 | а | 5 | а | |
б | b | |||
в | с | |||
г | d | |||
д | е | |||
е | f | |||
ж | g | |||
з | h | |||
и | i | |||
к | j | |||
л | k | |||
м | I | |||
н | m | |||
о | n | |||
п | о | |||
р | р | |||
с | q | |||
3.3 | - | 6 | - | |
3.4 | - | - | - | |
3.4.1 | - | 7 | - | |
3.4.2 | - | 8 | - | |
3.4.3 | - | 9 | - | |
3.5 | - | - | - | |
3.5.1 | - | 10 | - | |
3.5.2 | - | - | - | |
3.5.2.1 | - | 11 | - | |
3.5.2.2 | - | 12 | - | |
3.5.3 | - | 13 | - | |
3.6 | - | 14 | - | |
3.7 | - | 15 | - | |
3.8 | - | - | - | |
3.8.1 | - | - | - | |
3.8.1.1 | - | 16 | - | |
3.8.1.2 | - | 17 | - | |
3.8.1.3 | - | 18 | - | |
3.8.1.4 | - | 19 | - | |
3.8.2 | - | 20 | - | |
4 | 4.1 | - | - | - |
4.1.1 | - | 21 | - | |
4.1.2 | - | 22 | - | |
4.1.3 | - | 23 | - | |
4.1.4 | - | 24 | - | |
4.1.5 | - | 25 | - | |
4.2 | - | - | - | |
4.2.1 | - | 26 | - | |
4.2.2 | - | 27 | - | |
4.2.3 | - | 28 | - | |
4.2.4 | - | 29 | - | |
4.2.5 | - | 30 | - | |
4.2.6 | - | 31 | - | |
4.2.7 | - | 32 | - | |
4.3 | - | 33 | - | |
4.4 | - | - | - | |
4.4.1 | - | 34 | - | |
4.4.2 | - | 35 | - | |
4.4.3 | - | 36 | - | |
4.4.4 | - | - | - | |
4.4.4.1 | - | 37 | - | |
4.4.4.2 | - | 38 | - | |
4.4.5 | - | 39 | - | |
4.4.6 | - | 40 | - | |
4.4.7 | - | 41 | - | |
5 | 5.1 | - | - | - |
5.1.1 | - | 42 | - | |
5.1.1.1 | - | 42 | - | |
5.1.1.2 | - | 42 | - | |
5.1.1.3 | - | 42 | - | |
5.1.1.4 | - | 43 | - | |
5.2 | - | 44 | - | |
5.3 | - | 45 | - | |
5.4 | - | - | - | |
5.4.1 | - | 46 | - | |
5.4.2 | - | - | - | |
5.4.2.1 | - | 47 | - | |
5.4.2.2 | - | 48 | - | |
5.4.2.3 | - | 49 | - | |
5.4.2.4 | - | 50 | - | |
5.4.2.5 | - | 51 | - | |
5.4.3 | - | - | - | |
5.4.3.1 | - | 52 | - | |
5.4.3.2 | - | 53 | - | |
5.4.3.3 | - | 54 | - | |
5.4.3.4 | - | 55 | - | |
5.4.3.5 | - | 56 | - | |
5.4.3.6 | - | 57 | - | |
5.4.3.7 | - | 58 | - | |
5.4.4 | - | - | - | |
5.4.4.1 | - | 59 | - | |
5.4.4.2 | - | 60 | - | |
5.4.5 | - | - | - | |
5.4.5.1 | - | 61 | - | |
5.4.5.2 | - | 62 | - | |
5.5 | - | - | - | |
5.5.1 | - | 63 | - | |
5.5.2 | - | 64 | - | |
5.5.3 | - | 65 | - | |
5.5.4 | - | 66 | - | |
5.5.5 | - | 67 | - | |
5.5.6 | - | 68 | - | |
5.6 | - | - | - | |
5.6.1 | - | 69 | - | |
5.6.2 | - | 70 | - | |
5.6.3 | - | - | - | |
5.6.3.1 | - | 71 | - | |
5.6.3.2 | - | 72 | - | |
Приложение А | Приложение 1 | |||
Приложение Б | Приложение 2 | |||
Приложение В | Приложение 3 | |||
Библиография | Литература | |||
Библиография
[1] | OECD (2004) Report of the Validation of the Amphibian Metamorphosis Assay for the detection of thyroid active substances: Phase 1 - Optimisation of the Test Protocol. Environmental Health and Safety Publications. Series on Testing and Assessment. No. 77, Paris |
[2] | OECD (2007) Final Report of the Validation of the Amphibian Metamorphosis Assay: Phase 2 - Multi-chemical Interlaboratory Study. Environmental Health and Safety Publications. Series on Testing and Assessment. No. 76. Paris |
[3] | OECD (2008) Report of the Validation Peer Review for the Amphibian Metamorphosis Assay and Agreement of the Working Group of the National Coordinators of the Test Guidelines Programme on the Follow-up of this Report. Environmental Health and Safety Publications. Series on Testing and Assessment. No. 92. Paris |
[4] | OECD (2000) Guidance Document on Aquatic Toxicity Testing of Difficult Substances and Mixtures. Environmental Health and Safety Publications. Series on Testing and Assessment. No. 23. Paris |
[5] | ASTM (2004) Standard Guide for Conducting the Frog Embryo Teratogenesis Assay - Xenopus (FETAX). E 1439-98 |
[6] | ASTM (2002) Standard Guide for Conducting Acute Toxicity Tests on Test Materials with Fishes, Macroinvertebrates, and Amphibians. American Society for Testing and Materials, ASTM E729-96(2002), Philadelpia, PA |
[7] | Kahl, M.D., Russom, C.L., DeFoe, D.L. & Hammermeister, D.E. (1999) Saturation units for use in aquatic bioassays. Chemosphere 39, pp.539-551 |
[8] | Hutchinson Т.Н., Shillabeer N., Winter M.J., Pickford DB, 2006. Acute and chronic effects of carrier solvents in aquatic organisms: A critical review. Review. Aquatic Toxicology, 76; pp.69-92 |
[9] | Nieuwkoop, P.D. & Faber, J. (1994) Normal Table of Xenopus laevis. Garland Publishing, New York |
[10] | OECD (2007) Guidance Document on Amphibian Thyroid Histology. Environmental Health and Safety Publications. Series on Testing and Assessment. No. 82. Paris |
[11] | Dodd, M.H.I. & Dodd, J.M. (1976) Physiology of Amphibia. Lofts, B. (ed.), Academic Press, New York, pp.467-599 |
[12] | OECD (2006) Current Approaches in the Statistical Analysis of Ecotoxicity Data: A Guidance to Application. Environmental Health and Safety Publications. Series on Testing and Assessment, No. 54. Paris |
УДК 658.382.3:006.354 | МКС 13.020.01 | Т58 |
Ключевые слова: химическая продукция, окружающая среда, метаморфоз, земноводные, токсичность | ||
Электронный текст документа
и сверен по:
, 2016