ГОСТ Р ИСО 7405-2011
Группа Р22
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
СТОМАТОЛОГИЯ
Оценка биологической совместимости медицинских изделий, применяемых в стоматологии
Dentistry. Evaluation of biocompatibility of medical devices used in dentistry
ОКС 11.060.10
11.100.99
ОКП 93 9000
Дата введения 2012-03-01
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. N 184-ФЗ "О техническом регулировании", а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 ПОДГОТОВЛЕН Автономной некоммерческой организацией "Институт медико-биологических исследований и технологий" (АНО "ИМБИИТ") на основе собственного аутентичного перевода на русский язык текста стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 422 "Оценка биологического действия медицинских изделий"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 22 сентября 2011 г. N 333-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 7405:2008* "Стоматология. Оценка биологической совместимости стоматологических инструментов" (ISO 7405:2008 "Dentistry - Evaluation of biocompatibility of medical devices used in dentistry").
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячно издаваемых информационных указателях "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
Введение
ИСО (Международная организация стандартизации) является всемирной федерацией органов национальных стандартов (организации - члены ИСО). Работа по подготовке международных стандартов обычно осуществляется Техническими комитетами ИСО. Каждая организация-член, заинтересованная в предмете, для которого создавался Технический комитет, имеет право быть представленной в этом комитете. Международные правительственные и неправительственные организации также принимают участие в работе во взаимодействии с ИСО. ИСО тесно сотрудничает с Международной электротехнической комиссией (МЭК) по всем вопросам электротехнической стандартизации.
Международные стандарты разрабатываются в соответствии с правилами, приведенными в Директивах ИСО/МЭК, часть 2.
Основной задачей Технических комитетов является подготовка международных стандартов. Проекты международных стандартов, принятые Техническими комитетами, распространяются организациям-членам для голосования. Публикация в качестве международного стандарта требует одобрения, по меньшей мере, 75% организаций-членов с правом голоса.
Необходимо обратить внимание на возможность того, что некоторые элементы данного документа могут подвергаться патентным правам. ИСО не несет ответственности за обозначение каких-либо таковых патентных прав.
ИСО 7405 был подготовлен Техническим комитетом ИСО/ТК 194 "Стоматология".
Настоящее второе издание отменяет и заменяет первое издание (ИСО 7405:1997), которое было пересмотрено в техническом отношении. Были сделаны следующие изменения:
a) добавление испытаний цитотоксичности дентинного барьера к приложению В;
b) улучшенное описание методов испытаний;
c) обновленные ссылки на серию ИСО 10993.
1 Область применения
Настоящий стандарт устанавливает методы исследования для оценки биологического эффекта медицинских изделий, применяемых в стоматологии. Он включает испытание фармакологических агентов, являющихся неотъемлемой частью испытуемого устройства.
Настоящий стандарт не распространяется на испытания материалов и устройств, которые не контактируют прямо или косвенно с организмом пациента.
2 Нормативные ссылки
Следующие справочные документы* являются необходимыми для применения данного документа. При датированной ссылке применимо только указанное издание. При ссылке без даты применимо последнее издание указанного документа (включая любые поправки).
_______________
* Таблицу соответствия национальных стандартов международным см. по ссылке. - .
ИСО 1942 Стоматология. Словарь. Часть 1. Общие и клинические термины. Изменение 2
ИСО 6344-1 Шлифовальный материал с покрытием. Гранулометрический анализ. Часть 1. Определение гранулометрического состава
ИСО 10993-1 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования
ИСО 10993-2 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 2. Требования к обращению с животными
ИСО 10993-3 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 3. Исследование генотоксичности, канцерогенности и токсического действия на репродуктивную функцию
ИСО 10993-5 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 5. Исследования на цитотоксичность: методы in vitro
ИСО 10993-6 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследование местного действия после имплантации
ИСО 10993-10 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 10. Исследование раздражающего и сенсибилизирующего действия
ИСО 10993-11 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 11. Исследование общетоксического действия
ИСО 10993-12:2007 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и стандартные образцы
ИСО 14971 Изделия медицинские. Применение менеджмента рисков к медицинским изделиям
3 Термины и определения
В настоящем стандарте применены термины по ИСО 1942, ИСО 10993-1, ИСО 10993-12, а также следующие термины с соответствующими определениями:
3.1 медицинское изделие: Любой прибор, аппарат, приспособление, материал или другое изделие, включая программное обеспечение, используемое либо изолированно, либо в комбинации, которое предназначено изготовителем для применения, главным образом, в следующих целях:
- диагностика, профилактика, наблюдение, лечение или облегчение болезни;
- диагностика, наблюдение, лечение, облегчение или компенсация повреждения органов или физического недостатка;
- исследование, замена или изменение анатомии или физиологического процесса;
- контрацепция
и которое не является фармакологическим, иммунологическим или метаболическим средством, но может быть дополнено такими средствами.
3.2 стоматологический материал: Материал и/или вещество или сочетание материалов и/или веществ, специально разработанный и приготовленный для применения в стоматологической практике и/или сопряженных процедурах.
3.3 конечный продукт: Медицинское изделие в том состоянии, в котором его применяют в медицинской практике.
Примечание - Многие стоматологические материалы применяются в свежесмешанном виде, и необходимо рассмотреть оценку материалов как в свежесмешанном, так и в застывшем состоянии.
3.4 положительный контрольный образец: Любой достаточно охарактеризованный образец материала или вещества, который, подвергаясь исследованию по описанной методике, показывает пригодность этой методики для получения воспроизводимого, соответствующего положительного или реактивного ответа в тест-системе.
3.5 отрицательный контрольный образец: Любой достаточно охарактеризованный образец материала или вещества, который, подвергаясь исследованию по описанной методике, показывает пригодность этой методики для получения воспроизводимого, соответствующего отрицательного, нереактивного или минимального ответа в тест-системе.
Примечание - На практике отрицательные контрольные образцы включают в себя бланковые пробы, основы/растворители и эталонные материалы.
3.6 стандартный образец: Образец вещества (материала) с установленными по результатам испытаний значениями одной или более величин, характеризующих состав или свойство этого вещества (материала) и дающих возможность точного определения количественных характеристик с отклонениями на установленном доверительном уровне.
Примечание - В настоящем стандарте под эталонным материалом подразумевается любой хорошо изученный материал и/или вещество, который при испытании описанным методом демонстрирует пригодность процедуры давать воспроизводимый предсказуемый ответ. Ответ может быть отрицательным или положительным.
4 Классификация медицинских изделий
4.1 Классификация по виду контакта с организмом человека
4.1.1 Общая часть
В настоящем стандарте классификация медицинских изделий, применяемых в стоматологии, взята из ИСО 10993-1. Если изделие или материал может быть отнесено более чем к одной категории, будут применимы более жесткие требования испытаний. При многократном воздействии изделия решение об отнесении изделия к какой-либо категории должно учитывать потенциальный совокупный эффект, принимая во внимание период времени, в течение которого происходит это воздействие.
Примечание - В данном контексте термин стоматология включает оральную и челюстно-лицевую области.
4.1.2 Изделия, не контактирующие с поверхностностью тела человека
Эти устройства не контактируют с организмом пациента прямо или косвенно и не включены в ИСО 10993-1.
4.1.3 Изделия, контактирующие с поверхностностью тела человека
Эта группа включает в себя изделия, входящие в контакт с поверхностью неповрежденной или вскрытой, или как-либо еще нарушенной кожей, с поверхностью неповрежденной или вскрытой, или как-либо еще нарушенной слизистой полости рта и контактирующие с внешними поверхностями зубных твердых тканей, включая эмаль, дентин и цемент.
Примечание - При некоторых обстоятельствах дентин и цемент рассматривают как поверхности, например после рецессии десны.
4.1.4 Изделия, присоединяемые извне
Эти изделия включают в себя стоматологические изделия, которые проникают в слизистую поверхность и контактируют со слизистой полости рта, зубными твердыми тканями, зубной пульпарной тканью или костью, либо их сочетанием и открыты для пероральной среды.
Примечание - Эта группа изделий также включает любой вид прослойки или основного материала, используемых для восстановления.
4.1.5 Имплантируемые изделия, применяемые в стоматологии
Эти изделия включают в себя зубные имплантаты и другие стоматологические изделия, которые частично или полностью внедрены в одном или более из следующих случаев:
a) мягкая ткань, например субпериостальные и подкожные имплантаты;
b) кость, например внутрикостные имплантаты и заменители кости;
c) пульподентинная система зуба, например эндодонтические материалы;
d) любое сочетание таковых, например трансостеальные имплантаты.
4.2 Классификация изделий по длительности контакта
4.2.1 Общая часть
В настоящем стандарте медицинские изделия, применяемые в стоматологии, классифицируют по длительности контакта, как описано в ИСО 10993-1 и приведено в 4.2.2-4.2.4.
4.2.2 Изделия кратковременного контакта
Изделия однократного, многократного или непрерывного использования, контакт которых в общей сложности составляет менее 24 ч.
4.2.3 Изделия длительного контакта
Изделия, однократное, многократное или долгосрочное использование или контакт которых вероятно превысит 24 ч, но не более 30 сут.
4.2.4 Изделия постоянного контакта
Изделия, однократное, многократное или долгосрочное использование или контакт которых превышает 30 сут.
Примечания
1 Определение термина "постоянный" предназначено для применения исключительно при использовании настоящего стандарта. Оно совпадает с определением, приведенным в ИСО 10993-1.
2 При многократном воздействии изделия решение об отнесении изделия к какой-либо категории должно учитывать потенциальный совокупный эффект, принимая во внимание каждый период времени, в течение которого происходит это воздействие.
5 Процесс биологической оценки
5.1 Общая часть
Каждое медицинское изделие, применяемое в стоматологии, должно быть подвергнуто структурированной программе биологической оценки в рамках процесса контроля риска (см. ИСО 10993-1). Руководство по внедрению этой программы приведено в ИСО 14971 и ИСО 10993-1. Программа биологической оценки должна включать в себя обзор комплектов данных, касающихся биологических свойств каждого медицинского изделия, используемого в стоматологии. В случае, если эта часть программы биологической оценки обозначает, что один или более комплект данных является неполным и необходимы дальнейшие испытания, таковые должны быть выбраны из методов, описанных в серии стандартов ИСО 10993 или в настоящем стандарте, или в обоих. Если выбраны испытания, не включенные в настоящий стандарт, необходимо сделать обоснование выбора других испытаний.
Для комбинированных продуктов конечный продукт должен быть оценен в соответствии с настоящим стандартом в сочетании с любыми применимыми стандартами.
Примечания
1 В данном контексте комбинированными продуктами являются стоматологические устройства любого типа, которые включают в себя или имеют предназначением включить в качестве неотъемлемой части вещество, которое:
a) при отдельном использовании служит лекарством или биологическим продуктом;
b) способно повлиять на организм пациента сопутствующим действием.
Примером может служить изделие для наполнения/наращивания кости, содержащее фактор роста (т.е. биологический продукт).
2 Для комбинированных продуктов, когда изделие и фармакологические компоненты укомплектованы раздельно, может быть достаточным испытать только компоненты изделия.
5.2 Выбор испытаний и общая оценка
Выбор испытаний и общая оценка результатов должны быть проведены специалистом, обладающим соответствующими химическими, физическими и биологическими данными, касающимися изделия, и который осведомлен о предполагаемых условиях использования.
5.3 Выбор методов испытаний
Выбор методов испытаний должен быть основан на рассмотрении:
a) предназначенного применения медицинского изделия;
b) тканей, с которыми медицинское изделие может контактировать;
c) длительности контакта.
Если избранное испытание не включено в международные стандарты, необходимо включить обоснование выбора методов в отчет об испытании для каждого изделия. Если стандарты рекомендуют более чем один метод испытания в той же категории, выбор одного испытания из нескольких должен быть обоснован.
5.4 Типы испытаний
Согласно классификации изделия, испытания должны быть рассмотрены для использования, как суммировано в таблице А.1 приложения А. Эта таблица обозначает, какие типы методов исследования должны быть приняты во внимание, но не то, что их проведение является обязательным. Решение не проводить тип испытания, обозначенный в таблице А.1, должно быть обосновано в отчете об испытании для каждого изделия. Приведенные типы испытаний рассматривают как основу для оценки биосовместимости медицинских изделий, применяемых в стоматологии. Для большинства типов испытаний определены конкретные методы, но признается, что для некоторых изделий альтернативные методы, не включенные в международные стандарты, могут быть более подходящими.
Для удобства типы испытаний разбиты на три группы.
a) Группа I
Данная группа включает в себя испытания на цитотоксичность in vitro. Общие рекомендации по испытаниям цитотоксичности in vitro приведены в ИСО 10993-5 и должны соблюдаться. Подробные протоколы испытаний для методов диффузии в агаре или агарозе и фильтрующей диффузии, подходящие для стоматологических материалов, включены в настоящий стандарт. Методы цитотоксичности in vitro включают:
1) испытание диффузией в агар (см. 6.2);
2) испытание диффузией через фильтр (см. 6.3);
3) испытания прямого контакта или экстракции в соответствии с ИСО 10993-5;
4) испытание цитотоксичности дентинного барьера (см. приложение В);
5) модель среза зуба.
Примечания
1 Последовательность списка не означает какого-либо предпочтения одному методу по сравнению с другими.
2 Данный список не означает, что все упомянутые испытания на цитотоксичность следует проводить для каждого рассматриваемого медицинского изделия.
3 Использование испытания на цитотоксичность дентинного барьера поощряется, и описание испытания приведено в приложении В. Другим подходом является модель зубного среза. Ссылки на это испытание приведены в библиографии.
b) Группа II
Данная группа включает в себя испытания в соответствии с серией стандартов ИСО 10993, и конкретные испытания идентифицированы, где это уместно:
1) острая системная токсичность - пероральное применение - в соответствии с ИСО 10993-11;
2) острая системная токсичность - применение ингаляцией - в соответствии с ИСО 10993-11;
3) подострая и субхроническая системная токсичность - пероральное применение - в соответствии с ИСО 10993-11;
4) кожное раздражение и внутрикожная реактивность в соответствии с ИСО 10993-10;
5) гиперчувствительность замедленного типа в соответствии с ИСО 10993-10;
6) генотоксичность в соответствии с ИСО 10993-3;
7) местное действие после имплантации в соответствии с ИСО 10993-6.
Примечания
1 Для осуществимости использования только самого последнего издания справочного документа возможна перекрестная ссылка без даты. Обозначение соответствующей статьи и раздела возможно только для датированных ссылок. Таким образом, пользователю настоящего стандарта предлагается обратиться к справочным материалам для соответствующего номера статьи.
2 Информация по испытаниям острой токсичности приведена в приложении С.
3 При оценке материалов после местной имплантации, включающей минерализованные ткани, в соответствии с ИСО 10993-6, рекомендуется осмотр недеминерализованных секций в дополнение к регулярному осмотру деминерализованных секций.
с) Группа III
Данная группа включает в себя испытания, специфичные для медицинских изделий, применяемых в стоматологии, не упомянутые в серии стандартов ИСО 10993:
1) испытание пульпарного и дентинного использования (см. 6.4);
2) испытание пульпарной прокладки (см. 6.5);
3) испытание эндодонтического использования (см. 6.6).
Примечание - Испытание использования системы зубного имплантата в соответствии с ИСО/ТС 22911 также может быть рассмотрено по применимости.
5.5 Переоценка биосовместимости
В соответствии с ИСО 10993-1 изделие должно быть рассмотрено для переоценки его биосовместимости согласно описанию в 5.4, если были сделаны поправки или модификации формулы, качества и/или эксплуатационных характеристик.
6 Процедуры испытаний, специфичные для стоматологических материалов
6.1 Рекомендации по приготовлению проб
6.1.1 Общая часть
Эти рекомендации предназначены для испытаний in vitro, но также могут быть использованы для других целей в случае применимости.
6.1.2 Общие рекомендации по приготовлению проб
При приготовлении испытуемых проб следует обратиться к стандартам на соответствующий продукт и/или к инструкциям изготовителя и следовать этим описаниям в максимально возможной степени. Любое отклонение от инструкции изготовителя должно быть обосновано.
Подробное описание приготовления пробы должно быть включено в отчет об исследовании. Принимают во внимание следующие факторы (например, окружающей среды), учитывая конечное использование изделия:
a) температура;
b) влажность;
c) воздействие света: пробы светочувствительных материалов следует проводить при условии, что их не активирует естественный свет;
d) материал опытной формы: следует убедиться, что материал опытной формы и возможная применяемая смазка не препятствуют процессу застывания материала.
Примечание - Приемлемыми материалами могут быть полупрозрачные или белые пластиковые материалы, такие как полиэтилен или политетрафторэтилен (PTFE);
e) воздействие кислорода: для материалов, производящих ингибированный кислородом слой во время затвердевания, следует убедиться, что опытная форма надлежащим образом закупорена в течение затвердевания;
f) стерилизация: пробы либо должны быть произведены в стерильных условиях, либо простерилизованы методом, пригодным для материала, если необходимо и возможно; следует убедиться, что стерилизация не влияет на материал (например, стерилизация не должна извлекать вещества из материала);
g) соотношение площади поверхности пробы и поверхности клеточного слоя или клеточной культуральной среды: следует отразить документально соотношение площади поверхности пробы и поверхности клеточного слоя или клеточной культуральной среды; обосновать выбор формы и площади поверхности пробы, а также использованного соотношения площади поверхности пробы и поверхности клеточного слоя или клеточной культуральной среды;
h) экстракты: если экстракты требуются для процедуры испытания, пробы экстракта приготовляют в соответствии с ИСО 10993-12, раздел 10.
6.1.3 Специальные рекомендации для светоотверждающихся материалов
Учитывают следующие факторы, принимая во внимание конечное использование светоотверждающегося материала:
a) материал опытной формы: коэффициент отражения материалов, использованных для опытных форм, должен быть максимально приближен к коэффициенту отражения дентина для имитации клинической ситуации.
Примечание - Приемлемыми материалами могут быть полупрозрачные или белые пластиковые материалы, такие как полиэтилен или политетрафторэтилен (PTFE);
b) воздействие света: светоотверждение должно быть проведено для наиболее близкой имитации клинического применения. Необходимо следовать инструкциям изготовителя по применению для обеспечения того же уровня отверждения, как и при настоящем использовании. Это часто требует отверждения только с одной стороны, но иногда включает и двустороннее отверждение. Метод отверждения зависит от материала и/или процесса. В случаях, когда для исследования требуются полностью отвержденные пробы, важно убедиться, что испытуемые пробы являются однородными после удаления формы. В случае однокомпонентных материалов не должно быть каких-либо пустот, трещин или воздушных пузырей при осмотре без увеличения. Необходимо отметить используемый источник света (интенсивность, время отверждения, спектральное распределение отверждающего света и тип отверждающего света должны быть зарегистрированы). Необходимо убедиться, что источник света рекомендован для испытуемых материалов и находится в удовлетворительном рабочем состоянии;
c) воздействие кислорода: для материалов, производящих ингибированный кислородом слой во время светоотверждения, оба конца формы должны быть накрыты прозрачными материалами противокислородной защиты (например, полиэфирной пленкой) в течение светоотверждения. Если изготовитель рекомендует обработку поверхности материала после отверждения, поверхности пробы должны быть отшлифованы и отполированы с использованием рекомендуемых клинических процедур. Если таковых инструкций нет и если требуется для испытания, пробы следует отшлифовать с обоих концов бумагой Р2 000 в соответствии с ИСО 6344-1, предварительно поместив их на прозрачный материал противокислородной защиты.
6.1.4 Особые рекомендации для материалов, застывающих с химической добавкой
Принимают во внимание следующие факторы, учитывая конечное использование материалов, застывающих с помощью химической добавки:
a) смешивание: смешивают достаточное количество материала, чтобы обеспечить, что приготовление каждой исследуемой пробы выполняется из одного замеса. Готовят свежую смесь для каждой исследуемой пробы. Смешивание следует проводить согласно соответствующим стандартам на продукт, если применимо;
b) воздействие кислорода: для материалов, производящих ингибированный кислородом слой во время химического отверждения, оба конца формы должны быть накрыты материалами противокислородной защиты (например, полиэфирной пленкой) в течение отверждения. Если изготовитель рекомендует обработку поверхности материала после отверждения, поверхности пробы должны быть отшлифованы и отполированы с использованием рекомендуемых клинических процедур. Если таковых инструкций нет и если требуется для испытания, пробы следует отшлифовать с обоих концов бумагой Р2 000 в соответствии с ИСО 6344-1, предварительно поместив их на материал противокислородной защиты.
6.2 Испытание диффузией в агар
6.2.1 Цель
Данное испытание предназначено для демонстрации неспецифичной цитотоксичности испытуемых материалов после диффузии через агар или агарозу. Данный метод испытания не применим для вымываемых веществ, которые не диффундируют через агар или агарозу.
6.2.2 Клеточная линия
Используют установившуюся клеточную линию фибробластов или эпителия, являющуюся общедоступной [например, из Американской Коллекции Типовых Культур (АТСС), см. http://www.atcc.org]. Обозначают в отчете идентификационный номер клеточной линии, если применимо, описание и назначение использованной клеточной линии и обоснование ее выбора.
_______________
Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
6.2.3 Культуральная среда, реагенты и оборудование
Используют культуральную среду, указанную для выбранной клеточной линии. Стерилизуют фильтрацией. Для приготовления агара готовят двойную концентрацию культуральной среды. Стерилизуют фильтрацией. Готовят либо 3%-ный агар, либо 3%-ную агарозу. Стерилизуют автоклавированием.
Готовят витальный краситель разведением основного раствора 1%-ного водного раствора нейтрального красного (регистрируют источник) 1:100 посредством 0,01 моль/л 100 мл фосфатно-буферных физрастворов [например, фосфатно-буферного физраствора Dulbecco] немедленно перед использованием. Хранят растворы нейтрального красного в темном месте. Используют 6-луночные планшетки для культуры тканей (диаметром 35 мм) или чашки Петри номинальным диаметром от 50 до 100 мм, пригодные для культуры тканей.
_______________
Dulbecco является торговым наименованием. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
6.2.4 Приготовление проб
Готовят пробы в соответствии с 6.1. Исследование проводят на экстракте материала и/или самом материале, согласно руководству в ИСО 10993-5.
a) Для твердых материалов готовят круглые испытуемые пробы диаметром примерно 5 мм с плоской поверхностью для обеспечения адекватного контакта с верхним слоем агара.
b) Для застывающих материалов вводят свежесмешанный материал в кольца внутренним диаметром 5 мм и высотой 2 мм. Материал кольца должен быть указан в отчете об исследовании. При испытании материалов в свежесмешанном состоянии помещают кольца на агар до введения материала. При испытании после различных периодов застывания наполняют кольца так, чтобы материал находился вровень с кромкой, и дают ему застыть при температуре (37±2) °С и относительной влажности (90±10)% до готовности для испытания.
c) Для жидких используемых проб или экстрактов впитывают 0,01 мл жидкости в боросиликатный тонкостекольный фильтровый диск диаметром 5 мм, помещенный на агар.
Примечания
1 Подходящими инертными материалами являются стекло или PTFE.
2 Подходящие диски могут быть приготовлены из предфильтров.
6.2.5 Контрольные образцы
Используют положительные контрольные образцы, отрицательные контрольные образцы и эталонные материалы.
6.2.6 Процедура испытания
Культивируют клетки, пока они не достигнут конца фазы логарифмического роста. Пипетируют надлежащий объем (например, 10 мл для 100-миллиметровой чашки Петри) клеточной суспензии (2,5x10 клетки/мл) в достаточное число чашек Петри и инкубируют при температуре (37±2) °С в водонасыщенной атмосфере с 5% (объемная доля) углекислого газа в течение 24 ч. Если используют другие условия культивирования клеток, необходимо предоставить обоснование.
Нагревают стерильный агар или агарозу до температуры 100 °С на водяной бане и дают остыть до температуры 48 °С.
Смешивают одну часть агара или агарозы с одной частью свежеприготовленной культуральной среды двойной концентрации и нагревают до температуры 48 °С. Аспирируют жидкую культуральную среду из каждой чашки Петри и заменяют 10 мл свежеприготовленной смесью агара или агарозы и культуральной среды.
Дают смеси агара или агарозы и культуральной среды затвердеть при комнатной температуре (примерно 30 мин). Добавляют 10 мл раствора нейтрального красного и держат в темноте от 15 до 20 мин. Аспирируют избыточный раствор нейтрального красного. Защищают культуру от света в присутствии нейтрального красного, так как клетки могут быть повреждены.
Вносят в каждую чашку необходимое число проб испытуемого материала и контрольных образцов с адекватным расстоянием (больше 20 мм) между соседними пробами, если применимо. Инкубируют при температуре (37±2) °С в водонасыщенной атмосфере с 5% (объемная доля) углекислого газа в течение 24 ч. Осматривают каждый испытуемый материал, по меньшей мере, четыре раза (т.е., две чашки на испытуемый материал).
6.2.7 Параметры оценки
Оценивают зону обесцвечивания вокруг испытуемых материалов и контрольных образцов, используя инвертированный микроскоп с калиброванным экраном, и определяют индекс обесцвечивания и индекс лизиса для каждой испытуемой пробы в соответствии с критериями, приведенными в таблицах 1 и 2.
Таблица 1 - Индекс обесцвечивания
Индекс обесцвечивания | Описание |
0 | Без обнаруживаемой зоны обесцвечивания вокруг и под препаратом |
1 | Зона обесцвечивания ограничена областью вокруг препарата |
2 | Зона обесцвечивания выходит менее чем на 0,5 см за пределы препарата |
3 | Зона обесцвечивания занимает от 0,5 до 1,0 см за пределами препарата |
4 | Зона обесцвечивания занимает более чем 1,0 см за пределами препарата, но не включает всю чашку |
5 | Зона обесцвечивания включает всю чашку |
Таблица 2 - Индекс лизиса
Индекс лизиса | Описание обесцвеченной зоны |
0 | Без наблюдаемой цитотоксичности |
1 | Затронуто <20% обесцвеченной зоны |
2 | Затронуто 20% до <40% обесцвеченной зоны |
3 | Затронуто 40% до <60% обесцвеченной зоны |
4 | Затронуто 60% до 80% обесцвеченной зоны |
5 | Затронуто <80% обесцвеченной зоны |
Вычисляют средний индекс обесцвечивания и индекс лизиса отдельно для каждого испытуемого материала. Если значения индекса для четырех репликатов испытуемого вещества различаются более чем на 2 единицы в диапазоне 0 до 3, повторяют испытание. При индексах 4 и 5 повторения не требуется. При испытании экстрактов следует вычесть средний индекс одной экстракционной среды из среднего индекса экстракционной среды, содержащей испытуемое вещество, для получения индекса только испытуемого вещества. Если средний индекс экстракционной среды, служащей контрольным образцом, больше 1, повторяют испытание, используя другую экстракционную среду.
Примечание - Для достоверного испытания под негативным контрольным образцом должен быть расположен неповрежденный клеточный слой.
6.2.8 Оценка результатов
При оценке результатов испытания необходимо учитывать всю информацию, полученную в течение испытания, особенно какие-либо различия в результатах опытной и контрольной групп. Клеточный ответ должен быть основан на среднем индексе обесцвечивания и индексе лизиса по меньшей мере четырех дублирующих испытаний. Клеточный ответ должен быть оценен отдельно по каждому параметру в соответствии с таблицей 3.
Таблица 3 - Клеточный ответ (оценен отдельно для индекса обесцвечивания и индекса лизиса) и интерпретация цитотоксичности
Шкала | Клеточный ответ | Интерпретация |
0 | 0 | Не цитотоксичный |
1 | 1 | Легкая цитотоксичность |
2 | 2-3 | Средняя цитотоксичность |
3 | 4-5 | Значительная цитотоксичность |
Включают результаты оценки в отчет об испытании.
Примечание - Необходимо учитывать, что интерпретация данных испытаний клеточной культуры должна принимать во внимание ограничения этой испытательной системы, т.е., цитотоксичныи материал не является непригодным как таковой, но данные должны быть интерпретированы для каждого конкретного применения.
6.2.9 Отчет об испытании
Представляют результаты в отчете об испытании, который включает полное отражение всех проведенных процедур, полученных результатов и любых других данных, необходимых для оценки результатов. Включают детали приготовления и методов применения испытуемого материала вместе с номером партии материала, где применимо.
6.3 Испытание диффузией через фильтр
6.3.1 Цель
Данное испытание предназначено для демонстрации неспецифичной цитотоксичности испытуемых материалов после диффузии через целлюлозоацетатный фильтр.
6.3.2 Клеточная линия
Используют установившуюся клеточную линию фибробластов или эпителия, являющуюся общедоступной [например, из Американской Коллекции Типовых Культур (АТСС), см. http://www.atcc.org]. Обозначают в отчете идентификационный номер клеточной линии, если применимо, описание и назначение использованной клеточной линии и обоснование ее выбора.
6.3.3 Культуральная среда, реагенты и оборудование
Готовят культуральную среду и агар или агарозу для использования в качестве верхнего слоя, как описано в 6.2.3. Готовят растворы либо для окрашивания сукцинатдегидрогеназой, либо для окрашивания неспецифичной гидролазой.
Для окрашивания сукцинатдегидрогеназой готовят следующие основные растворы:
a) раствор сукцината, 13,6 г сукцината натрия в 100 мл 0,2 моль/л фосфатного буфера, рН 7,6;
b) раствор хлорида нитросинего тетразолия, 100 мг хлорида нитросинего тетразолия на 100 мл 0,2 моль/л фосфатного буфера, рН 7,6;
c) раствор феназинметосульфата, 4 мг феназинметосульфата на 10 мл свежей дистиллированной воды.
Готовят окрашивающий раствор 1 мл раствора сукцината, 9 мл раствора хлорида нитросинего тетразолия и 1 мл раствора феназинметосульфата.
Для окрашивания неспецифичной гидролазой готовят основной раствор диацетата флуоресцина, состоящий из 5 мг диацетата флуоресцина в 1 мл ацетона. Для использования добавляют 20 мкл основного раствора к 100 мл фосфатно-буферного физраствора (например, фосфатно-буферного физраствора Dulbecco). Используют чашки Петри диаметром 60 мм, пригодные для культуры тканей.
Используют фильтры, состоящие из смеси ацетатцеллюлозы и нитроцеллюлозы, диаметром 47 мм, размер пор 0,45 мкм.
_______________
Millipore HATF 04700 является примером пригодного, коммерчески доступного продукта. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
6.3.4 Приготовление проб
Готовят пробы в соответствии с 6.1. Исследование должно быть проведено на экстракте материала и/или самом материале согласно руководству в ИСО 10993-5.
a) Для твердых материалов готовят круглые испытуемые пробы диаметром примерно 5 мм с плоской поверхностью для обеспечения адекватного контакта с фильтром. Масса испытуемых проб не должна превышать 3,5 г.
b) Для застывающих материалов вводят свежесмешанный материал в кольца внутренним диаметром 5 мм и высотой 2 мм. При испытании материалов в свежесмешанном состоянии помещают кольца на фильтр до введения материала. При испытании после различных периодов застывания наполняют кольца так, чтобы материал находился вровень с кромкой, и дают ему застыть при температуре (37±2) °С и относительной влажности (90±10)% до готовности для испытания. Масса испытуемых проб не должна превышать 3,5 г.
Примечание - Подходящими инертными материалами являются стекло или PTFE.
c) Для жидких испытуемых проб или экстрактов впитывают 0,01 мл жидкости в боросиликатный тонкостекольный фильтровый диск диаметром 5 мм, помещенный на агар.
Примечание - Подходящие диски могут быть приготовлены из предфильтров.
6.3.5 Контроли
Используют положительные контрольные образцы, отрицательные контрольные образцы и эталонные материалы.
6.3.6 Процедура испытания
Культивируют клетки, пока они не достигнут конца фазы логарифмического роста. Помещают целлюлозоацетатные фильтры на дно достаточного числа чашек Петри и пипетируют 6 мл клеточной суспензии (2,5х10 клетки/мл) в каждую. Инкубируют при температуре (37±2) °С в водонасыщенной атмосфере с 5% (объемная доля) углекислого газа в течение 24 ч. Если используют другие условия культивирования клеток, необходимо предоставить обоснование. Пипетируют 5 мл свежеприготовленного агара или смеси агарозы и культуральной среды (см. 6.2.6), содержащейся при температуре 48 °С, в достаточное число чашек Петри и дают затвердеть при комнатной температуре. Аспирируют избыточную культуральную среду из чашек, содержащих целлюлозоацетатные фильтры, промывают фильтры фосфатно-буферным физраствором (например, фосфатно-буферным физраствором Dulbecco) при температуре (37±2) °С и помещают их поверх агара или агарозы клеточной стороной вниз. Наносят от трех до пяти испытуемых проб поверх фильтра в каждую чашку и инкубируют еще 2 ч и 24 ч при температуре (37±2) °С в водонасыщенной атмосфере с 5% (объемная доля) углекислого газа. Следует убедиться, что испытуемые пробы находятся в тесном контакте с поверхностью фильтра. Признаки цитотоксичности должны быть оценены после периодов воздействия в 2 ч и 24 ч. В каждую чашку помещают один положительный контрольный образец и один отрицательный контрольный образец. Дополнительно используют добавочные контрольные образцы фильтра с клеточным монослоем, но без испытуемых проб, и фильтра без клеток, но с испытуемыми пробами. При испытании экстрактов необходимо также применить контрольный образец, используя только экстракционную среду. Осматривают каждую испытуемую пробу по меньшей мере четыре раза.
После инкубации удаляют испытуемые пробы и осторожно высвобождают фильтр из агара или агарозы. Оценивают с цитохимической точки зрения область пониженной активности клеточных ферментов методом А или методом В.
а) Метод А
Проявляют сукцинатдегидрогеназу согласно методу Барка и Андерсона [14]. Инкубационный период 3 ч при температуре (37±2) °С. Промывают фильтр в дистиллированной воде и высушивают на воздухе до измерения.
Примечание - Удерживанию клеток может способствовать их фиксация с помощью 10%-ного нейтрального формалина на 15 мин до промывания в дистиллированной воде.
b) Метод В
Проявляют неспецифичную гидролазу инкубацией с раствором диацетата флуоресцина в течение 30 мин при температуре 4 °С. Осматривают фильтр под ультрафиолетовым светом.
6.3.7 Оценка клеточного повреждения
Оценивают клеточное повреждение путем:
a) измерения зоны обесцвечивания (например, используя систему анализа изображений) или
b) использования шкалы, приведенной в таблице 4.
Таблица 4 - Оценка клеточного повреждения
Шкала | Определение оценки | Зона обесцвечивания |
0 | Разница в интенсивности окрашивания по всему фильтру отсутствует | Нет |
1 | Зона сниженной интенсивности окрашивания или неокрашенная зона диаметром менее диаметра (5 мм) испытуемой пробы | <20 мм |
2 | Неокрашенная зона диаметром от 5 до 7 мм | От 20 до 40 мм |
3 | Неокрашенная зона диаметром более чем 7 мм | >40 мм |
Примечание - Фильтры под отрицательными контрольными образцами и контрольные фильтры должны быть равномерно окрашены в темно-синий цвет (при использовании сукцинатдегидрогеназы) или светло-синий (при использовании неспецифичной гидролазы).
Контрольные фильтры без клеток позволяют определить возможный эффект испытуемой пробы на фильтр.
6.3.8 Оценка результатов
При оценке результатов испытания необходимо учитывать всю информацию, полученную в течение испытания, особенно какие-либо различия в результатах опытной и контрольной групп. Удобный способ оценки испытуемых материалов приведен в таблице 5.
Таблица 5 - Оценка испытуемого материала
Индекс клеточного повреждения | Описание обесцвеченной зоны по ИСО 10993-5 |
0 | Не цитотоксичность |
1 | Легкая цитотоксичность |
2 | Средняя цитотоксичность |
3 | Значительная цитотоксичность |
Результаты оценки включают в отчет об испытании.
Примечание - Необходимо учитывать, что интерпретация данных испытаний клеточной культуры должна принимать во внимание ограниченность этой испытательной системы, т.е., цитотоксичный материал не является непригодным как таковой, но данные должны быть интерпретированы для каждого конкретного применения.
6.3.9 Отчет об испытании
Представляют результаты в отчете об испытании, который включает в себя полное отражение всех проведенных процедур, полученных результатов и любых других данных, необходимых для оценки результатов. Включают детали приготовления и методов применения испытуемого материала вместе с номером партии материала, где применимо.
6.4 Испытание пульпарного и дентинного использования
6.4.1 Цель
Данное испытание предназначено для оценки биосовместимости стоматологических материалов с дентином и зубной пульпой. В оценку должны быть включены методологические процедуры, необходимые для предполагаемого клинического использования материала.
6.4.2 Животные и гуманное обращение с животными
Для гуманного обращения с животными следуют
a) ИСО 10993-2 или
b) национальным нормативным требованиям для лабораторных животных.
Примечания
1 Животные должны быть размещены согласно ИСО 10993-2 со свободным доступом к пище и воде. Используют млекопитающих одного вида, не являющихся грызунами, такого возраста, что их зубной ряд содержит неповрежденные постоянные зубы с закрытыми зрелыми верхушками. Обезьяны, собаки, хорьки или миниатюрные свиньи являются подходящими видами. Для особых целей могут быть выбраны другие виды. Выбранные виды должны быть наиболее низкими в биологической цепи из требуемых для удовлетворения научных целей при наименьшем ущербе для животных. Выбор вида должен быть обоснован и отражен документально.
2 Подходящими обезьянами, собаками и миниатюрными свиньями являются такие, у которых прорезались все постоянные зубы, кроме молярных зубов. Подходящими хорьками являются такие, у которых прорезались четыре постоянных клыка, так как только эти зубы являются применимыми.
6.4.3 Процедура испытания
6.4.3.1 Подготовка животных
Выбирают достаточное число животных для предоставления по меньшей мере семи зубов, содержащих испытуемый материал, на каждый период времени. Анестезируют животных и проводят процедуру, описанную в 6.4.3.2.
6.4.3.2 Обработка зубов
6.4.3.2.1 Удаляют налет и какие-либо инородные вещества с поверхностей зубов. Очищают и дезинфицируют поверхности используемых зубов тампоном с нанесенной 3%-ной (объемная доля) перекисью водорода, затем дезинфектантом, состоящим из повидон-йода или хлоргексидина. Готовят требуемое число буккальных или лабиальных полостей класса V, используя острые боры при адекватном водовоздушном распылении. Глубина полостей должна быть таковой, чтобы толщина остающегося дентина была менее 1,0 мм и предпочтительно менее чем 0,5 мм, но без обнажения пульпы.
Промывают полости водой и высушивают их ватными шариками, кроме случаев, когда метод введения испытуемого материала требует другой процедуры.
Примечания
1 При выраженном гингивальном воспалении у животных может быть необходимым провести удаление налета и инородных веществ за несколько дней до подготовки полости, возможно, повторно, пока гингивальное воспаление не будет под контролем.
2 Измерительные инструменты электрического сопротивления, такие как определители верхушки корня зуба, могут быть откалиброваны предварительно и использованы для оценки толщины остающегося дентина при подготовке полостей.
6.4.3.2.2 При приготовлении испытуемых материалов следуют инструкциям изготовителя. Если изготовитель испытуемого материала рекомендует его использование с материалом покрытия или агентом обработки полостей (например, дентинный адгезионный агент), используют эти дополнительные процедуры согласно рекомендациям изготовителя.
6.4.3.2.3 На каждый период времени восстанавливают по меньшей мере семь полостей испытуемым материалом и четыре полости отрицательным контрольным образцом путем произвольного распределения. Если необходимо (см. примечание 1), на каждый период времени восстанавливают до четырех полостей положительным контрольным образцом.
Примечание 1 - Для лабораторий, обладающих банком данных предыдущих материалов положительных контрольных образцов, дальнейшие исследования необязательны, кроме периодического подтверждения положительной реакции.
Выбранные виды должны быть наиболее низкими в биологической цепи из требуемых для удовлетворения научных целей при наименьшем ущербе для животных. Выбор вида должен быть обоснован и отражен документально. При использовании обезьян, собак или миниатюрных свиней необходимо использовать одно животное на каждый период времени. При использовании хорьков необходимо использовать по меньшей мере трех животных на каждый период времени.
Примечания
1 Быстросхватывающий цинк-оксид-эвгеноловый цемент (ZOE) является подходящим материалом отрицательного контрольного образца. Для долгосрочных исследований целесообразно защитить ZOE от гидролиза. Это можно сделать нанесением тонкого слоя либо поликарбоксилатного цемента, либо обычного (самоотверждающегося) стеклоиономерного цемента поверх ZOE, за которым следует композит на основе смол с сохраненной протравленностью. Следует учесть, что помещение композита на основе смол в прямом контакте с цементом ZOE может привести к подавлению полимеризации композита на основе смол. Обычный стеклоиономерный цемент может быть рассмотрен как альтернативный отрицательный контрольный образец.
2 Восстанавливающий материал или метод, не включающий обнажения пульпы, последовательно приводящий к пульпарному ответу от умеренного до резкого является подходящим положительным контролем.
6.4.3.2.4 Состояние животных следует проверять и регистрировать по меньшей мере раз в день после операции. Должны быть внедрены меры для сведения к минимуму каких-либо болей или страданий, вызванных изменениями в режиме питания, воспалением или инфекцией. Анальгетики следует применять согласно послеоперационным требованиям.
6.4.3.3 Приготовление препаратов
6.4.3.3.1 После (7±2) сут, (28±3) сути (70±5) сут проводят эвтаназию передозировкой анестетика или применением других общепринятых веществ достаточного числа животных для предоставления, по меньшей мере семи зубов, содержащих испытуемый материал. Осматривают восстановления, зубы и их опорные ткани и регистрируют подробности каких-либо аномалий. Удаляют каждый обработанный зуб вместе с окружающими его твердыми и мягкими тканями и фиксируют в подходящем растворе (формалин).
Примечание - Сосудистая перфузия тканей с фиксатором во время умерщвления до их удаления предоставляет лучшую фиксацию.
6.4.3.3.2 После фиксации деминерализуют зубы в подходящем реагенте (например, 10% муравьиной кислоты или 0,5 моль/л этилендиаминтетрауксусной кислоты при рН 7,4) и готовят серийные секции толщиной 5 до 7 мкм сквозь каждую полость по продольной оси зуба. Окрашивают препараты, чередуя гематоксилин и эозин. Окрашивают промежуточные препараты соответствующим бактериальным красителем (например, Браун-Бренн) или другими красителями, необходимыми для обнаружения бактерий.
6.4.3.4 Оценка дентина и зубной пульпы
Осматривают секции без предварительного знания, является ли испытуемая проба опытной или контрольной. Для каждой серии секций регистрируют полное описание всех гистологических признаков в дентине, пульпе и прикорневых тканях, включая те, которые могли образоваться в результате методики подготовки полостей. Из серийных секций выбирают по меньшей мере пять равноотстоящих в полости для последующего анализа воспаления. Оценивают отдельно воспалительный инфильтрат в поверхностных тканях (слой одонтобластов, бесклеточная зона и зона с высокой плотностью клеток) и в остатке (более глубокие ткани) пульпы по шкале, обозначенной в таблице 6.
Таблица 6 - Оценочная шкала для испытания пульпарного и дентинного использования
Балл воспаления | Описание воспалительных изменений |
0 | Воспаление отсутствует: пульпарная ткань с нормальной структурой, прилегающая к дентину в канальцевом контакте с полостным дном |
1 | Легкое воспаление: рассеянные воспалительные клетки в пульпарной ткани с нормальной в других отношениях структурой, прилегающей к дентину в канальцевом контакте с полостным дном |
2 | Умеренное воспаление: воспалительные клетки с небольшими фокальными скоплениями в пульпарной ткани, все еще включающей структурно нормальные области, прилегающей к дентину в канальцевом контакте с полостным дном |
3 | Значительное воспаление: обширное проникновение воспалительных клеток с потерей нормальной структуры в пульпарной ткани, прилегающей к дентину в канальцевом контакте с полостным дном |
4 | Абсцедирование или расширенное проникновение воспалительных клеток, не ограничивающееся только пульпарной тканью, прилегающей к дентину в канальцевом контакте с полостным дном |
Для каждой оцененной секции регистрируют минимальную толщину остающегося дентина, измеряя как под прямыми углами от полостного дна к поверхности соприкосновения пульпы-предентина, так и по направлению дентинных канальцев. В последнем случае, когда плоскость секций не совсем совпадает с плоскостью дентинных канальцев, так что каждый каналец в интересующей области не простирается на все расстояние от дна полости до поверхности соприкосновения пульпы-предентина, проводят измерение вдоль линии общего направления дентинных канальцев. Вычисляют показатель воспалительного ответа на обоих участках для каждого интервала времени путем суммирования отдельных оценок, разделенных на общее число наблюдений.
Представляют данные отдельно для полостей, заполненных испытуемым материалом, включая материал покрытия или агент обработки полостей, если рекомендовано изготовителем, с отрицательным и положительным контрольными образцами. Для полостей, заполненных положительным контрольным образцом, данные могут быть получены из предыдущих исследований с идентичными условиями испытания. Дополнительно регистрируют число полостей, содержащих бактерии на дне или стенке полости для каждого временного интервала испытуемого материала и контрольных образцов. Индекс воспалительного ответа для каждого периода времени соответственно предоставляют для каждого материала, основываясь на вышеуказанной шкале, дополняя предоставлением диапазона измеренной минимальной остающейся толщины дентина и наблюдаемым количеством бактериальной микротечи.
6.4.3.5 Анализ выживания одонтобластов (по выбору)
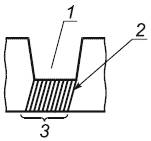
Для гистоморфометрического анализа выживания одонтобластов выбирают по меньшей мере пять секций, расположенных с равными интервалами на дне полости и окрашенных гематоксилином и эозином, и осматривают их с увеличением, позволяющим идентификацию отдельных клеток и предоставляющим поле обзора, включающее всю поверхность соприкосновения пульпы-предентина под полостью. Используя окулярную шкалу (масштабную сетку), подсчитывают число морфологически цельных одонтобластов на единицу длины предентинной поверхности по всей длине поверхности соприкосновения пульпы-предентина под полостью. Поверхность соприкосновения определяют как такую, в которой дентинные канальцы сообщаются с полостным дном, как показано на рисунке 1.
1 - полость; 2 - дентинные канальцы; 3 - поверхность соприкосновения пульпы-предентина для подсчета одонтобластов
Рисунок 1 - Поверхность соприкосновения пульпы-предентина для подсчета одонтобластов
Проводят подсчет одонтобластов на единицу длины области поверхности соприкосновения пульпы-предентина под полостью для каждой из пяти секций от каждой испытуемой пробы и выводят среднее количество клеток для этой полости. Затем выводят средние значения количества клеток для всех испытуемых полостей и полостей отрицательного контрольного образца
. Гибель клеток, в %, выводят из уравнения (1)
![]() , (1)
, (1)
где - гибель клеток в процентном соотношении;
- число клеток в полости отрицательного контроля;
- число клеток в полости с испытуемым материалом.
Оценивают гибель одонтобластов по шкале, приведенной в таблице 7.
Таблица 7 - Оценка гибели одонтобластов
Шкала | Гибель одонтобластов |
0 | Нет |
1 | <25% клеточной гибели |
2 | От 25% до 50% клеточной гибели |
3 | >50% до 75% клеточной гибели |
4 | >75% клеточной гибели |
Для каждой оцененной секции регистрируют минимальную остающуюся толщину дентина, как описано выше. Таким образом, показатель выживаемости одонтобластов предоставляют для каждого материала, основываясь на вышеуказанной шкале, и дополняя предоставлением диапазона минимальной остающейся толщины дентина, измеренной для полостей в данной группе материалов. Представляют данные отдельно для полостей, заполненных испытуемым материалом, включая материал покрытия или агент обработки полостей, если рекомендовано изготовителем, и для полостей, используемых в качестве положительного контрольного образца. Выражают данные положительных контрольных образцов в виде процента отрицательного контрольного образца, как указано выше для опытных полостей. Где применимо, данные для положительного контрольного образца могут быть получены из предыдущих исследований с идентичными условиями испытания.
6.4.4 Оценка результатов
При оценке результатов испытания необходимо учитывать всю информацию, полученную в течение испытания, особенно какие-либо различия в результатах опытной и контрольной групп.
Регистрируют результаты оценки в отчете об испытании.
6.4.5 Отчет об испытании
Представляют результаты в отчете об испытании, который включает полное отражение всех проведенных процедур, полученных результатов и любых других данных, необходимых для оценки результатов. Включают детали приготовления и методов применения испытуемого материала вместе с номером партии материала.
6.5 Испытание пульпарной прокладки
6.5.1 Цель
Испытание предназначено для оценки биосовместимости материалов пульпарной прокладки с зубной пульпой. В оценку должны быть включены методологические процедуры, необходимые для предполагаемого клинического использования материала.
Примечания
1 С отдельными модификациями это испытание может быть использовано для испытания пульпотомии.
2 Испытание пульпарного и дентинного использования и испытание пульпарной прокладки могут быть проведены одновременно на одних и тех же животных с использованием разных зубов.
6.5.2 Животные и гуманное обращение с животными
Соблюдают требования по обращению с животными в соответствии с 6.4.2. Используют как минимум двух млекопитающих одного вида, не являющихся грызунами, как описано в 6.4.2.
6.5.3 Процедура испытания
6.5.3.1 Подготовка животных
Выбирают достаточное число животных для предоставления по меньшей мере 10 зубов, содержащих испытуемый материал, на каждый период времени. Анестезируют животных и проводят процедуру, описанную в 6.5.3.2.
6.5.3.2 Обработка зубов
6.5.3.2.1 Удаляют налет и какие-либо инородные вещества с поверхностей зубов. Размещают резиновую прокладку для изоляции используемых зубов. Очищают поверхность зуба и операционное поле и высушивают. Дезинфицируют тампоном с нанесенной 3%-ной (объемная доля) перекисью водорода, затем - дезинфектантом, состоящим из повидон-йода или хлоргексидина. Подготавливают требуемое число буккальных или лабиальных полостей класса V, используя острые боры при адекватном водовоздушном распылении. Препараты должны быть окаймлены эмалью, внедряться в мезиальные и дистальные поверхности зуба и в одну внутреннюю треть дентина. В центре полости аккуратно делают пульпарное отверстие диаметром примерно от 0,5 до 1,0 мм под распылением стерильного физраствора [0,9%-ным (массовая доля)] без погружения бора в пульпарную ткань. Диаметр отверстия должен соответствовать десятым долям миллиметра. Диаметр отверстия может быть рассчитан с использованием известного диаметра бора. Тщательно промывают место отверстия стерильным физраствором до достижения гемостаза. Высушивают стерильными ватными шариками.
Примечание - При выраженном гингивальном воспалении у животных может быть необходимым провести удаление налета и инородных веществ за несколько дней до подготовки полости, возможно повторно, пока гингивальное воспаление не будет под контролем.
6.5.3.2.2 При приготовлении испытуемых материалов следуют инструкциям изготовителя. Если изготовитель рекомендует другие промывающие растворы или реагенты для прекращения кровотечения либо особую предварительную обработку пульпарной раны, следуют инструкциям изготовителя.
6.5.3.2.3 На каждый период времени заполняют по меньшей мере 10 полостей испытуемым материалом и пять полостей подходящим эталонным материалом путем произвольного распределения. Смешивают прокладочные и контрольные материалы на пластине (подкладке), избегая микробной контаминации. Наносят материалы на пульпарную рану без давления. Восстанавливают полость либо композитом на основе смол, модифицированным поликислотой, либо стеклоиономерным цементом, модифицированным смолами. За этим должно следовать восстановление адгезивно связанным композитом на основе смол.
Выбранные виды должны быть наиболее низкими в биологической цепи из требуемых для удовлетворения научных целей при наименьшем ущербе благосостоянию животных. Выбор вида должен быть обоснован и отражен документально. При использовании обезьян, собак или миниатюрных свиней необходимо использовать по меньшей мере одно животное на каждый период времени. При использовании хорьков необходимо использовать не менее четырех животных на каждый период времени, так как применимы только клыки.
Примечания
1 Гидроокись кальция, свежесмешанная со стерильным 0,9%-ным (массовая доля) физраствором до консистенции замазки, является приемлемым эталонным контролем.
2 Если цинк-оксид-эвгеноловый (ZOE) цемент используют для долгосрочных исследований, целесообразно защитить его от гидролиза. Это можно сделать, нанеся тонкий слой либо поликарбоксилатного цемента, либо обычного (самоотверждающегося) стеклоиономерного цемента поверх ZOE, за которым следует композит на основе смол с сохраненной протравленностью. Учитывают, что помещение композита на основе смол в прямом контакте с цементом ZOE может привести к подавлению полимеризации композита на основе смол.
6.5.3.2.4 Наблюдают за животными и обращаются с ними, как описано в 6.4.3.2.4.
6.5.3.3 Приготовление препаратов
6.5.3.3.1 После (7±2) сут и (70±5) сут проводят эвтаназию передозировкой анестетика или применением других общепринятых веществ достаточного числа животных для предоставления по меньшей мере 10 зубов, содержащих испытуемый материал. Осматривают восстановленные зубы и их опорные ткани и регистрируют подробности каких-либо аномалий. Удаляют каждый обработанный зуб вместе с окружающими его твердыми и мягкими тканями единым блоком и закрепляют в подходящем фиксирующем агенте.
Примечание - Сосудистая перфузия тканей с фиксатором во время умерщвления до их удаления предоставляет лучшую фиксацию.
6.5.3.3.2 После фиксации делают рентгенограмму каждого блока ткани для определения каких-либо рентгенографических изменений. Готовят секции для осмотра, как указано в 6.4.3.3.2.
6.5.3.4 Оценка зубной пульпы
Осматривают секции, описывают гистологические признаки, оценивают воспалительный инфильтрат и вычисляют индекс воспалительного ответа согласно протоколу, описанному в 6.4.3.4. Так как поверхностная пульпарная ткань будет разрушена в результате создания пульпарного отверстия, готовят отдельную оценку воспалительного инфильтрата, используя шкалу, приведенную в таблице 8.
Таблица 8 - Оценочная шкала испытания пульпарной прокладки
Балл воспаления | Описание воспалительных изменений |
0 | Нет воспаления |
1 | Легкое воспаление: рассеянные воспалительные клетки в пульпарной ткани, прилегающей к пульпарному отверстию |
2 | Умеренное воспаление: воспалительные клетки с небольшими фокальными скоплениями в пульпарной ткани, прилегающей к пульпарному отверстию |
3 | Значительное воспаление: обширное проникновение воспалительных клеток в пульпарную ткань, прилегающую к пульпарному отверстию |
4 | Абсцедирование или расширенное проникновение воспалительных клеток, не ограничивающееся только пульпарной тканью, прилегающей к пульпарному отверстию |
Дополнительно необходимо предоставить полное описание степени, распределения и характера какой-либо дентинной перемычки, обращая особое внимание на наличие тоннельных дефектов и клеточных включений, каковые могут препятствовать эффективности перемычки в качестве барьера. Оценивают степень образования перемычки отверстия третичным дентином (частичная или полная). Рекомендации по интерпретации гистологических признаков образования дентинной перемычки приведены в примечании ниже.
Примечание - Степень и распределение какой-либо дентинной перемычки должны быть рассмотрены исходя из того, покрывает ли перемычка полностью участок пульпарного отверстия, или учитывая ее глубины и толщины, а также ее распределения относительно участка отверстия. Неполная перемычка не предоставляет эффективной защиты открытой пульпы. Хотя адекватная глубина перемычки требуется для эффективной пульпарной защиты, неконтролируемый восстановительный дентиногенез для образования перемычки может вызвать окклюзию пульповой камеры и подвергнуть риску жизнеспособность пульпы. Широко распространенный восстановительный дентиногенез за местными пределами дентинной перемычки и ее канальцевого сообщения с материалом может предполагать клеточный ответ на травму (например, хирургическую травму), выходящий за границы прямого ответа на материал. Регулярность структуры канальцев в дентинной перемычке может свидетельствовать о степени дисплазии во время ее формирования с отсутствием или наличием нескольких канальцев, предполагающих дальнейшее формирование диспластическои ткани. Наличие тоннельных дефектов и клеточных включений в дентинной перемычке также указывает на формирование диспластической ткани и может повлиять на проницаемость и степень закупоривания, предоставляемые перемычкой.
6.5.4 Оценка результатов
Оценивают результаты, как указано в 6.4.4.
6.5.5 Отчет об испытании
Представляют результаты в отчете об испытании, как указано в 6.4.5.
6.6 Испытание эндодонтического использования
6.6.1 Цель
Испытание предназначено для оценки биосовместимости эндодонтических материалов с остающимися верхушечными пульпарными тканями (остатками) и прикорневыми тканями. В оценку должны быть включены процедуры, необходимые для предполагаемого клинического использования материала.
Примечание - Испытание эндодонтического использования должно применяться для биоактивных эндодонтических материалов, например, материалов, заявленных как стимулирующие формирование верхушечных твердых тканей, предназначенных для ортоградного или ретроградного применения.
6.6.2 Животные и гуманное обращение с животными
Благосостояние животных должно соответствовать положениям 6.4.2.
Используют как минимум четырех млекопитающих одного вида, не являющихся грызунами, как описано в 6.4.2, такого возраста, что их зубной ряд содержит неповрежденные постоянные зубы с закрытыми (зрелыми) верхушками; использование резцов, клыков и премоляров предпочтительно. Использование премоляров допустимо, если в наличии два корня.
6.6.3 Процедура исследования
6.6.3.1 Подготовка животных
Выбирают достаточное число животных для предоставления по меньшей мере 10 зубов, содержащих испытуемый материал, на каждый период времени.
Примечание - У собак некоторых пород морфология верхушечной части корневого канала может затруднить подготовку корня.
Анестезируют животных и проводят процедуру, описанную в 6.6.3.2.
6.6.3.2 Обработка зубов
6.6.3.2.1 Делают рентгенограммы, показывающие прикорневую область всех пломбируемых зубов. Очищают и изолируют зубы, как описано в 6.4.3.2.1.
Примечание - При выраженном гингивальном воспалении у животных может быть необходимым провести удаление налета и инородных веществ за несколько дней до подготовки полости, возможно повторно, пока гингивальное воспаление не будет под контролем.
Подготавливают требуемое число зубов для размещения пломб корневого канала. Просверливают соответствующее отверстие в пульповой камере, используя острые боры при стерильных условиях. Очищают открытую пульпу физраствором [0,9%-ным (массовая доля)] и высушивают стерильными ватными шариками. Используют новый стерильный пульпэкстрактор или зазубренный зонд для корневого канала для отрезания пульпы (1,0±0,5) мм от верхушечного отверстия, используют рентгенограммы в качестве руководства при использовании инструментов. Повторно промывают корневой канал раствором гипохлорита натрия [рекомендуемые концентрации колеблются от 1,0% до 5,25% (массовая доля)], затем стерильным 0,9%-ным (массовая доля) физраствором.
Увеличивают корневой канал, используя все более длинные стерильные пульпэкстракторы, калиброванные по длине до уровня, на котором была отрезана пульпа, пока его длина не стала приемлемой для пломбирования. Прилагают особые усилия для исключения дентинных осколков из корневого канала, которые могут заблокировать верхушку зуба и препятствовать контакту эндодонтического материала с верхушечной тканью. По завершении применения инструментов промывают корневой канал раствором гипохлорита натрия [рекомендуемые концентрации колеблются от 1,0% до 5,25% (массовая доля)], затем стерильным 0,9%-ным (массовая доля) физраствором и высушивают стерильными ватными шариками и большими притупленными стерильными бумажными штифтами, не затрагивая верхушечный пульпарный остаток.
6.6.3.2.2 При приготовлении испытуемых материалов следуют инструкциям изготовителя. Если изготовитель рекомендует процедуры подготовки зубов, отличающиеся от описанных выше, следуют инструкциям изготовителя.
6.6.3.2.3 На каждый период времени заполняют по меньшей мере 10 зубов испытуемым материалом и по меньшей мере пять подходящим эталонным материалом путем произвольного распределения. Смешивают эндодонтические и эталонные материалы на пластине (подкладке), избегая микробной контаминации. Заполняют корневой канал испытуемым или эталонным материалом, используя гуттаперчу у места разрыва пульпы. Заделывают полость доступа усиленным цинк-оксид-эвгеноловым (ZOE) цементом, покрытым либо поликарбоксилатным цементом, либо обычным (самоотверждающимся) стеклоиономерным цементом, либо композитом на основе смол с сохраненной протравленностью. Делают рентгенограммы, показывающие прикорневую область всех заполненных зубов.
При использовании обезьян, собак или миниатюрных свиней необходимо использовать не менее двух животных на каждый период времени. При использовании хорьков необходимо использовать не менее четырех животных на каждый период времени, так как применимы только клыки.
При использовании композита на основе смол необходимо предварительно нанести на ZOE тонкий слой либо обычного (самоотверждающегося) стеклоиономерного цемента, либо поликарбоксилатного цемента. Помещение композита на основе смол в прямом контакте с цементом ZOE может привести к подавлению полимеризации композита на основе смол.
Примечание - Цемент ZOE, отдельно или с другими добавками, такими как герметик Гроссмана, является подходящим эталонным материалом.
6.6.3.2.4 Наблюдают за животными и обращаются с ними, как описано в 6.4.3.2.4.
6.6.3.3 Приготовление препаратов
6.6.3.3.1 После (28±3) сут и (90±5) сут проводят эвтаназию передозировкой анестетика или применением других общепринятых веществ достаточного числа животных для предоставления по меньшей мере 10 зубов, содержащих испытуемый материал. Осматривают восстановленные зубы и их опорные ткани и регистрируют подробности каких-либо аномалий. Удаляют каждый обработанный зуб вместе с окружающими его твердыми и мягкими тканями единым блоком и закрепляют в подходящем фиксирующем агенте.
Примечание - Сосудистая перфузия тканей с фиксатором во время умерщвления до их удаления предоставляет лучшую фиксацию.
6.6.3.3.2 После фиксации делают рентгенограмму каждого блока ткани для определения каких-либо рентгенографических изменений. Готовят секции для осмотра, как указано в 6.4.3.3.2, параллельно длинной оси зуба сквозь корневой канал и его ответвления, показывая поверхность контакта материал/пульпарная ткань и прилегающие прикорневые ткани.
6.6.3.4 Оценка тканей
Осматривают секции слепым методом, не удостоверясь, является ли испытуемая проба опытной или контрольной. Для каждой серии секций регистрируют полное описание всех гистологических признаков в пульпе, прикорневых тканях, дентине и цементе в верхушечной части зуба. Для каждой испытуемой пробы оценивают изменения ткани по шкале, обозначенной в таблице 9. Примеры гистологических признаков для рассмотрения приведены в примечании ниже.
Таблица 9 - Оценочная шкала испытания эндодонтического использования
Шкала | Наблюдение |
0 | Нет воспаления |
1 | Легкое воспаление: испытуемые пробы показывают рассеянные воспалительные клетки с преобладанием хронических, а структурные характеристики остаточной пульпы еще определяемы |
2 | Умеренное воспаление: испытуемые пробы показывают фокальные скопления воспалительных клеток, но без некроза тканей, и некоторое нарушение структурных характеристик остаточной пульпы и прикорневых тканей |
3 | Значительное воспаление: обширное замещение остаточной пульпы или прикорневых тканей воспалительным инфильтратом |
4 | Абсцедирование |
Примечание - Примеры гистологических признаков для регистрации включают следующие:
a) оценку для определения, является ли наполнение корневого канала коротким, вровень или экструдированным: соотносят это наблюдение с наличием воспаления, резорбцией корня и костной реакцией;
b) экструдирование уплотнителя (цемента) корневого канала: определяют, экструдирован ли уплотнитель сквозь верхушку в окружающее периодонтальное пространство и костные ткани. Хотя вероятнее всего наблюдается при интервале в 28 сут, долгосрочный период не должен быть исключен из этой оценки;
c) наличие некротической верхушечной ткани;
d) качество адаптации материала, заполняющего корневой канал, оцениваемое как хорошее, среднее или плохое: хорошая адаптация означает, что пломбирующий материал хорошо адаптируется к стенкам корня не только на одной, но и на сериях секций, без видимых пустот. Среднюю оценку ставят, когда некоторые секции обнаруживают пустоты или области, где пломбирующий материал плохо адаптируется к корню. Плохая адаптация отмечается, когда пломбирующий материал не прилегает плотно к стенкам корня или когда наблюдаются многочисленные пустоты;
e) дальнейшее уточнение воспаления, очерченного выше (и оцененного по шкале от 0 до 4) по типу присутствующих воспалительных клеток: регистрируют преобладающий тип клетки и учитывают, что острые клетки (лейкоциты) появляются раньше, в то время как одноядерные клетки (лимфоциты, моноциты, макрофаги и многоядерные гигантские клетки) появляются позже. Классифицируют воспалительную реакцию как острую (О), хроническую (X) или смешанную (С);
f) резорбцию корня (наличие или отсутствие);
g) реакцию верхушечной кости, оцениваемую как нормальная, воспаленная (оценивают воспаление) и определение, присутствует ли гранулема и показывает ли кость признаки резорбции;
h) оценку гиперемии по шкале от 0 до 3.
6.6.4 Оценка результатов
Оценивают результаты, как указано в 6.4.4.
6.6.5 Отчет об испытании
Представляют результаты в отчете об испытании, как указано в 6.4.5.
Приложение А
(справочное)
Типы испытаний, рассматриваемых для оценки биосовместимости медицинских изделий, применяемых в стоматологии
Таблица А.1 - Типы испытаний, рассматриваемых для оценки биосовместимости медицинских изделий, применяемых в стоматологии
| Длительность контакта | Группа I | Группа II | Группа III | |||||||||
Характер контакта с организ- | А - Кратковре | Испы- | Испы- | Испы- | Гипер- | Раздра- | Острая сис- | Субхро- | Гено- | Имплан- | Испы- | Испы- | Испы- |
ИСО 7405, подраздел 6.2 и 6.3 | ИСО 10993-5 | ИСО 7405, прило- жение В | ИСО 10993-10 | ИСО 10993-10 | ИСО 10993-11 | ИСО 10993-11 | ИСО 10993-3 | ИСО 10993-6 | ИСО 7405, подраз- дел 6.4 | ИСО 7405, подраз- дел 6.5 | ИСО 7405, подраз- дел 6.6 | ||
Изделия, контакти- рующие с поверх- ностью тела человека | А | X | X | X | X | ||||||||
В | X | X | X | X | |||||||||
С | X | X | X | X | X | X | |||||||
Изделия, присое- диняемые извне | А | X | X | X | X | X | X | ||||||
В | X | X | X | X | X | X | X | X | X | X | |||
С | X | X | X | X | X | X | X | X | X | X | |||
Имплан- тируемые изделия | А | X | X | X | X | X | X | ||||||
В | X | X | X | X | X | X | X | X | X | X | |||
С | X | X | X | X | X | X | X | X | X | X | |||
Примечание 1 - X - обозначает, что испытание должно быть рассмотрено для применения. Примечание 2 - Эта таблица является основой для развития программы оценки, а не контрольным списком. | |||||||||||||
Приложение В
(справочное)
Испытание цитотоксичности дентинного барьера
B.1 Цель
Испытание предназначено для оценки цитотоксичности стоматологических пломбирующих материалов методом культуры клеток, при котором клетки и материал разделены дентинным барьером, таким образом моделируя клиническую ситуацию зубной полости, наполненной восстанавливающим материалом.
B.2 Приборы и материалы
B.2.1 Клетки
Установившаяся клеточная линия, являющаяся общедоступной, например из Американской Коллекции Типовых Культур (АТСС). В качестве варианта могут быть использованы клональные клетки, трансфицированные большим Т-антигеном SV40, например выведенные из зубного сосочка теленка. Их поддерживают в питательной среде в увлажненной атмосфере при температуре (37±2) °С и 5% СО. Также возможно использовать другие установившиеся клеточные линии со свойствами, подобными одонтобластам, или другими свойствами, имеющими отношение к физиологии зубных пульпарных тканей.
B.2.2 Культуральная среда
Среда, указанная для выбранной клеточной линии, как приведено в Американской Коллекции Типовых Культур (АТСС) или эквивалент.
Примечание - Для рекомендаций см. http://www.atcc.org]. Питательная среда для клеток, трансфицированных большим Т-антигеном SV40, состоит из ![]() с добавленными 20%-ной сывороткой зародыша теленка (FBS), 150 ME пенициллина, 150 мкг/мл стрептомицина, 0,125 мкг/мл амфотерицина Б и 0,1 мг/мл генетицина.
с добавленными 20%-ной сывороткой зародыша теленка (FBS), 150 ME пенициллина, 150 мкг/мл стрептомицина, 0,125 мкг/мл амфотерицина Б и 0,1 мг/мл генетицина.
B.2.3 Реагенты
B.2.3.1 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолий бромид (МТТ).
B.2.3.2 Антибиотики/фунгициды, пенициллин, стрептомицин, амфотерицин Б и генетицин только для клональных клеток, трансфицированных SV40.
B.2.4 Оборудование
B.2.4.1 Вкладыши для планшета для культуры клеток, например Millicell.
_______________
Millicell является торговым наименованием изделия, поставляемого Millipore, Билрике, США. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
B.2.4.2 6-луночные и 24-луночные культуральные планшетки.
B.2.4.3 Полиамидные сетки диаметром 8 мм, например Sefar, ширина ячейки 150 мкм.
_______________
Sefar является торговым наименованием изделия, поставляемого Sefar, Вассербург-на-Инне, Германия. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
B.2.4.4 Двухкамерное перфузионное устройство.
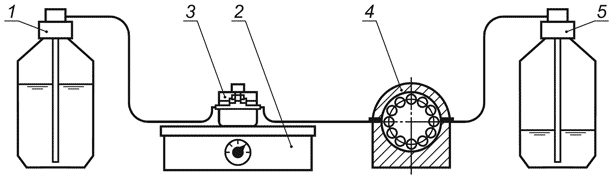
Первое двухкамерное перфузионное устройство, Minucells, (см. рисунок В.1) состоит из перфузионной камеры, изготовленной из поликарбоната с основой 40х40 мм и высотой 35 мм. Пульповая часть устройства соединена с одной стороны с емкостью с запасом культуральной среды и с другой стороны с перистальтическим насосом и сосудом для отработанной среды. Внутри опытного прибора две камеры разделены срезом дентина, закрепленным в стальном штативе (см. рисунок В.2).
_______________
Minucells является торговым наименованием изделия, поставляемого Minucells & Minutissue GmbH, Бад-Аббах, Германия. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
1 - подача культуральной среды; 2 - нагреватель; 3 - перфузионная камера; 4 - насос; 5 - сливной сосуд
Рисунок В.1 - Опытная установка для испытания цитотоксичности дентинного барьера
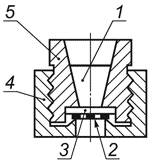
1 - испытуемый материал; 2 - сетка с клетками; 3 - срез дентина; 4 - стальное кольцо; 5 - стальная вставка
Рисунок В.2 - Штатив из нержавеющей стали для закрепления среза дентина и клеточной культуры в опытном приборе
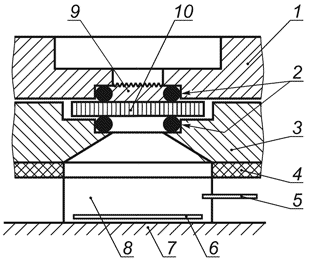
Второе двухкамерное устройство, перфузионная камера Американской Ассоциации Стоматологов (ADA) (см. рисунок В.З), состоит из полупрозрачных стен, изготовленных либо из Delrin
, либо из Lexan
, оба нетоксичные. Входные и выходные клапаны являются нетоксичными игловыми отверстиями из нержавеющей стали. Маленькие уплотнительные кольца изготовлены из красного силикона (внешний диаметр 15,9 мм, внутренний диаметр 12,42 мм). Внутренний 6-миллиметровый диаметр меньшего уплотнительного кольца создает область поверхностной диффузии в 28 мм
. Камерный отдел вмещает 0,5 мл жидкости. Этот отдел может быть сокращен наполнением камеры снизу нетоксичным поливинилсилоксановым слепочным материалом (например, Reprosil)
, так, чтобы внутри камеры находилось материала менее чем 100 мкл.
_______________
Перфузионная камера ADA является торговым наименованием изделия, поставляемого Biomedical Engineering, Медицинский Колледж Джорджии, Огаста, Джорджия 30912, США, #NT-8214A. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
Delrin является торговым наименованием изделия из класса материалов полиацеталь, поставляемого DuPont. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
Lexan является торговым наименованием изделия из класса материалов поликарбонат, поставляемого General Electric Plastics. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
Reprosil является торговым наименованием изделия из класса материалов гидрофобный нетоксичный поливинилсилоксановый слепочный материал, поставляемого Dentsply International, Йорк, Пенсильвания, США. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
1 - верхняя часть; 2 - резиновое уплотнительное кольцо; 3 - средняя часть; 4 - эластомерный лист; 5 - вход-выход; 6 - покровное стекло; 7- низ; 8 - культуральная среда; 9 - испытуемый материал; 10 - срез дентина, удерживаемый резиновыми уплотнительными кольцами
Рисунок В.3 - Перфузионная камера ADA
B.2.4.5 Планшет-ридер, 96-луночные планшеты, длина волны 540 нм, или любой аналогичный фотометр, с требуемыми параметрами.
B.2.4.6 Срезы дентина, из дентина человека или рогатого скота.
Примечание - При применении дентина происхождением не от человека, определяют проницаемость срезов до использования для подтверждения, что он схож с дентином человека на сопоставимом уровне пульпарно-дентинного соприкосновения. Для этих целей применяют капиллярную систему [например, Flowdec].
_______________
Flowdec является торговым наименованием изделия, поставляемого DeMarco Engineering, Женева, Швейцария. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО. Возможно использование эквивалентных продуктов, если доказано, что они приведут к тем же результатам.
В.3 Процедура испытания
B.3.1 Приготовление клеточной культуры
B.3.1.1 Трехмерные клеточные культуры
Трехмерные клеточные культуры рекомендуется использовать вместе с перфузионной камерой Minucells. Инкубируют полиамидные сетки в 0,1 моль/л уксусной кислоты в течение 30 мин, промывают три раза деминерализованной водой, высушивают на воздухе, покрывают фибронектином (0,03 мг/мл) и высушивают на воздухе в стерильных условиях. Помещают вкладыш клеточной культуры в каждую лунку 6-луночной планшетки вместе с 1,25 мл культуральной среды. Помещают сетки на вкладыши и засевают 20 мкл клеточной суспензии при 4х10 клеток/мл. После 48 ч инкубации при температуре (37±2) °С и под 5% СО
при относительной влажности (90±10)% переносят сетки в 24-луночные планшетки и инкубируют (14±2) сут. Меняют культуральную среду три раза в неделю и переносят сетки в новую 24-луночную планшетку в конце первой недели.
B.3.1.2 Мономерные культуры
Мономерные клеточные культуры рекомендуется использовать вместе с перфузионной камерой ADA. Применяют методы, описанные в ИСО 10993-5, используя установившуюся клеточную линию, являющуюся общедоступной, например из Американской Коллекции Типовых Культур (АТСС).
B.3.2 Приготовление срезов дентина
B.3.2.1 Дентин человека
Выбирают некариозные свежеизвлеченные молярные зубы, удаляют инородные частицы и присоединенные мягкие ткани ручными инструментами и погружают в 70%-ный этанол по меньшей мере на 15 мин. Готовят срезы дентина путем секционирования зубов под прямым углом к их длинным осям через самую широкую часть их головок, под окклюзионной эмалью и над окклюзионными пределами пульповых камер.
B.3.2.2 Дентин животного происхождения (быка)
Выбирают целые зубы, без видимых признаков стираемости, из числа четырех средних нижних резцов убойных животных возрастом от 3 до 7 лет. Удаляют зубы, очищают от инородных частиц и присоединенных мягких тканей ручными инструментами и хранят в 0,5%-ном хлорамине или других схожих агентах до использования. Секционируют зубы вдоль их длинных осей как можно ближе к пульповой камере. Для испытания используют срезы околошеечной части зуба.
B.3.2.3 Обработка срезов дентина
Протравливают предполагаемый "пульпарный" фрагмент среза дентина 50%-ной лимонной кислоты в течение 30 с, тщательно промывают и стерилизуют либо автоклавированием (121 °С; 9,6 мПа; 25 мин) в 0,9%-ном хлориде натрия, либо погружением в 70%-ный этанол на 15 мин, затем тщательным промыванием деминерализованной водой. Дентинные срезы могут храниться в 0,9%-ном растворе хлорида натрия при температуре (4±2) °С до трех недель. Следует убедиться в стерильности дентинных срезов с помощью микробиологической культуры испытуемой пробы из каждой партии перед использованием.
Примечание - Толщина среза дентина может различаться в зависимости от глубины клинической полости, которую испытание должно смоделировать. Срез дентина толщиной (500±50) мкм представляет количество дентина, остающееся под клинической полостью средней глубины. Более тонкие срезы могут быть использованы для изображения ситуации в более глубоких клинических полостях.
Срезы дентина могут храниться в 0,9%-ном хлориде натрия до использования.
B.3.2.4 Сборка перфузии
B.3.2.4.1 Устройство Minucells
Помещают сетку с клетками в опытный прибор и вставляют срез дентина, закрепленный в штативе из нержавеющей стали.
Примечание - Подходящий штатив показан на рисунке В.2.
Опрыскивают камеры 0,3 мл среды для количественного определения (питательная среда с 6 г/л буфера HEPES) каждый час в течение 24 ч. Останавливают перфузию и помещают испытуемый материал в верхнее отделение в прямом контакте с "полостной" стороной среза дентина.
После приемлемого периода времени (например, 24 ч или 3 сут) удаляют сетку с клетками из пульповой части камеры и помещают в 48-луночные планшетки, содержащие 0,5 мл предварительно нагретого раствора МТТ (0,5 мл в питательной среде), инкубируют 2 ч при температуре (37±2) °С с фосфатно-буферным физраствором. Экстрагируют осадок синего формазана, используя 0,25 мл диметилсульфоксида, встряхивая планшетки при комнатной температуре 30 мин. Переносят 200 мкл этого раствора на 96-луночную планшетку и определяют абсорбцию спектрофотометрическим путем при 540 нм. Выражают результаты как процент контрольных образцов или как фотометрические показания.
Используют от пяти до 10 камер для каждого материала и контрольного образца в одном испытании и проводят каждое испытание по меньшей мере дважды.
B.3.2.4.2 Сборка перфузионной камеры ADA
Устанавливают срез дентина в устройстве перфузионной камеры. Наполняют нижнее отделение приемлемой клеточной культуральной средой (или другим экстракционным средством) и соединяют его с сосудами подачи и слива, если необходимо. Затем наполняют испытуемыми материалами. После определенного времени воздействия удаляют клеточную культуральную среду и используют ее для испытания цитотоксичности в обычных монослойных культурах, например используя синтез ДНК, митохондральную активность (анализ МТТ) или стимуляцию функций, таких как регуляция генов, в качестве биологических конечных точек.
В.4 Контрольные образцы
Используют положительный и отрицательный контрольные образцы для каждого испытуемого вещества. Положительный контрольный образец должен сократить жизнеспособность клеток примерно на 50% после воздействия в 24 ч; отрицательный контрольный образец не должен иметь никакого воздействия на жизнеспособность клеток. Примеры материалов положительного контроля приведены в таблице В.1.
_______________
Следующие сырьевые материалы являются примерами пригодных коммерчески доступных продуктов. Эта информация приведена для удобства пользователей настоящего стандарта и не является рекламой означенного изделия со стороны ИСО.
Стеклянный порошок с размером частицы (30±10) мкм: Schott, номер для заказа GM35429.
Полиакриловая кислота: Sigma-Aldrich, номер для заказа 323667.
Хлорид дифенилиодония: Sigma, номер для заказа D209082.
Камфорохинон: Sigma, номер для заказа 124893.
Этил-4-диметиламинобензоат: Merck, номер для заказа 841086.
НЕМА (2-гидроксиэтил-метакрилат): Merck, номер для заказа 800588.
Примечание - В качестве отрицательного контрольного образца приемлем гидрофобный нетоксичный поливинилсилоксановый слепочный материал. В качестве положительного контрольного образца можно использовать материалы с составами, перечисленными в таблице В.1, или эквивалентные.
Таблица В.1 - Пример материала положительного контроля
Материал | Взвешенная выборка, мг | Взвешенная выборка, % | Конечная масса, |
Порошок | |||
Стеклянный порошок | 829,000 | 82,90 | 66,30 |
Полиакриловая кислота | 146,000 | 14,60 | 11,70 |
Хлорид дифенилиодония | 25,000 | 2,50 | 2,00 |
Всего | 1000,00 | 100,00 | 80,00 |
Жидкость | |||
Камфорохинон | 0,625 | 0,25 | 0,05 |
Этил-4-диметиламинобензоат | 0,625 | 0,25 | 0,05 |
НЕМА | 187,500 | 75,00 | 15,00 |
Дистиллированная вода | 61,250 | 24,50 | 4,90 |
Всего | 250,000 | 100,00 | 20,00 |
Смешивают компоненты порошка и жидкости отдельно и затем немедленно смешивают оба компонента в пропорции 1000 мг порошка и 250 мг жидкости. Отверждают стандартным агрегатом отверждения в течении 40 с при 700-800 мВт/см.
В.5 Оценка результатов
Не учитывают опыт, если между отрицательным и положительным контрольными образцами нет статистически значимой разницы.
В дополнение к описанной оценке следует обратиться к ИСО 10993-5 для дальнейшей информации. Оценка данных, полученных от устройства Minucells, основана на статистическом сравнении (непараметрические методы) данных испытуемого материала с данными контрольных материалов, предполагая от пяти до 10 независимых культур для каждого материала. Определяют клеточные повреждения согласно таблице В.2 и оценивают результаты согласно таблице В.3.
Таблица В.2 - Оценка клеточного повреждения
Шкала | Определение оценки |
0 | Не отличается статистически от отрицательного контрольного образца, но отличается от положительного контрольного образца или вызывает еще меньшее клеточное повреждение, чем отрицательный контрольный образец |
1 | Отличается статистически как от отрицательного, так и от положительного контрольных образцов |
2 | Не отличается статистически от положительного контрольного образца, но отличается от отрицательного контрольного образца или вызывает еще более сильное клеточное повреждение по сравнению с положительным контрольным образцом |
Таблица В.3 - Оценка испытуемого материала
Шкала | Описание |
0 | Не цитотоксичный |
1 | Умеренно цитотоксичный |
2 | Значительно цитотоксичный |
Включают результаты оценки в отчет об испытании.
В.6 Отчет об испытании
Отчет об испытании должен включать следующую информацию:
a) использованную клеточную линию;
b) использованную культуральную среду;
c) подробности испытуемого материала;
d) подробности приготовления испытуемого материала;
e) подробности положительного и отрицательного контрольных образцов;
f) процент жизнеспособности клеток по сравнению с отрицательным контрольным образцом;
g) результаты оценки.
Приложение С
(справочное)
Испытание острой токсичности
Классический метод LD был признан нецелесообразным и неприемлемым с точки зрения благосостояния животных. Процедура фиксированной дозы (Руководство ОЭСР 420[11]), Ступенчатая процедура (Руководство ОЭСР 423[12]) и "Скачкообразная" процедура (Руководство ОЭСР 425[13]) были утверждены для использования как нормативные испытания острой токсичности.
Приложение ДА
(справочное)
Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации
Таблица ДА.1
Обозначение ссылочного международного стандарта | Степень соответствия | Обозначение и наименование соответствующего национального стандарта |
ИСО 1942 | - | * |
ИСО 6344-1 | - | * |
ИСО 10993-1 | IDT | ГОСТ Р ИСО 10993-1-2009 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования" |
ИСО 10993-2 | IDT | ГОСТ Р ИСО 10993-2-2009 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 2. Требования к обращению с животными" |
ИСО 10993-3 | IDT | ГОСТ Р ИСО 10993-3-2009 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 3. Исследование генотоксичности, канцерогенности и токсического действия на репродуктивную функцию" |
ИСО 10993-5 | IDT | ГОСТ Р ИСО 10993-5-2009 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 5. Исследования на цитотоксичность: методы in vitro" |
ИСО 10993-6 | IDT | ГОСТ Р ИСО 10993-6-2009 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследование местного действия после имплантации" |
ИСО 10993-10 | IDT | ГОСТ Р ИСО 10993-10-2009 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 10. Исследование раздражающего и сенсибилизирующего действия" |
ИСО 10993-11 | IDT | ГОСТ Р ИСО 10993-11-2009 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 11. Исследование общетоксического действия" |
ИСО 10993-12 | IDT | ГОСТ Р ИСО 10993-12-2009 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и стандартные образцы" |
ИСО 14971 | - | ГОСТ Р ИСО 14971-2009 "Изделия медицинские. Применение менеджмента риска к медицинским изделиям" |
* Соответствующий национальный стандарт отсутствует. До его утверждения рекомендуется использовать перевод на русский язык данного международного стандарта. Перевод данного международного стандарта находится в Федеральном информационном фонде технических регламентов и стандартов. Примечание - В настоящей таблице использовано следующее условное обозначение степени соответствия стандартов: - IDT - идентичные стандарты. | ||
Библиография
[1] | ИСО 10993-7 Оценка биологическая медицинских изделий. Часть 7. Остаточное содержание этиленоксида после стерилизации |
[2] | ИСО 10993-9 Оценка биологическая медицинских изделий. Часть 9. Структура идентификации и квантификации потенциальных продуктов разложения |
[3] | ИСО 10993-13 Оценка биологическая медицинских изделий. Часть 13. Идентификация и количественная оценка продуктов разложения в полимерных медицинских устройствах |
[4] | ИСО 10993-14 Оценка биологическая медицинских изделий. Часть 14. Идентификация и количественная оценка продуктов разложения керамики |
[5] | ИСО 10993-15 Оценка биологическая медицинских изделий. Часть 15. Идентификация и количественная оценка продуктов разложения металлов и сплавов |
[6] | ИСО 10993-16 Оценка биологическая медицинских изделий. Часть 16. Концепция токсикокинетических исследований продуктов разложения и выщелачиваемых веществ |
[7] | ИСО 10993-17 Оценка биологическая медицинских изделий. Часть 17. Установление допустимых пределов вымываемых веществ |
[8] | ИСО 10993-18 Оценка биологическая медицинских изделий. Часть 18. Определение химических характеристик материалов |
[9] | ИСО/ТС 22911 Стоматология. Доклиническая оценка систем зубных имплантатов. Методы испытаний на животных |
[10] | ANSI/ADA Specification N 41, Recommended Standard Practices for Biological Evaluation of Dental Materials |
[11] | OECD 420: OECD Guidelines for Testing Chemicals - Acute Oral Toxicity. Fixed Dose Procedure, Organisation for Economic Co-operation and Development, 75775 Paris Cedex 16, France |
[12] | OECD 423: OECD Guidelines for Testing Chemicals - Acute Oral Toxicity. Acute Toxic Class Method, Organisation for Economic Co-operation and Development, 75775 Paris Cedex 16, France |
[13] | OECD 425: OECD Guidelines for Testing Chemicals - Acute Oral Toxicity. Up-and-Down Procedure, Organisation for Economic Co-operation and Development, 75775 Paris Cedex 16, France |
[14] | Barka, T. and Anderson, P.J., Histochemistry. Theory, practice and bibliography, Chapter XIII, Hoeber Medical Division, Harper & Row Publishers, New York, 1963 |
[15] | Berbert, F.L., Leonardo, M.R., Silva, L.A., Tanomaru Filho, M. and Bramante, С.М., Influence of root canal dressings and sealers on repair of apical periodontitis after endodontic treatment, Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod., 93, pp. 184-189, 2002 |
[16] | Browne, R.M., Animal tests for biocompatibility of dental materials: relevance, advantages and limitations, J. Dent., 22, pp. 21-24, 1994 |
[17] | Franz, A., |
[18] | Hanks, С.Т., Diehl, M.L., Craig, R.G., Makinen, P.L. and Pashley, D.A., Characterization of the "in vitro pulp chamber" using the cytotoxicity of phenol, J. Oral Path., 18, pp. 97-107, 1989 |
[19] | Magloire, H., Joffre, A. and Bleicher, F., An in vitro model of human dental pulp repair. J. Dent. Res., 75, pp. 1971-1978,1996 |
[20] | Meryn, S.D., The model cavity method incorporating dentine, Int. Endod. J., B, pp. 79-84, 1988 |
[21] | Murray, P., Hafez, A.A., Smith, A.J., Windsor, L.J. and Cox, C.F., Histomorphometric analysis of odontoblast-like cell numbers and dentine bridge secretory activity following pulp exposure, Int. Endod. J., 36, pp. 106-116, 2003 |
[22] | Murray, P.E., Lumley, P.J., Ross, H.F. and Smith, A.J., Tooth slice organ culture for cytotoxicity assessment of dental materials, Biomaterials, 21, pp. 1711-1721, 2000 |
[23] | Pameijer, C.H. and Stanley, H.R., Pulp reaction to a dentin bonding agent, Am. J. Dent., 8, pp. 140-114, 1995 |
[24] | Pascon, E.A., Leonardo, M.R., Safavi, K. and Langeland, K., Tissue reaction to endodontic materials: methods, criteria, assessment, and observations, Oral Surg. Oral Med. Oral Pathol., 72, pp. 222-237,1991. Erratum in: Oral Surg. Oral Med., 73, p. 347, 1992 |
[25] | Schmalz, G., Agar overlay method, Int. Endod. J., 21, pp. 59-66, 1988 |
[26] | Schmalz, G., Garhammer, P. and Schweikl, H., A commercially available cell culture device for dentin barrier tests, J. Endod., 22, pp. 249-252, 1996 |
[27] | Schmalz, G., Hillerl, K.-A. and |
[28] | Schmalz, G. and Schweikl, H., Characterization of an in vitro barrier test using a standard toxicant, J. Endod., 20, pp. 592-594, 1994 |
[29] | Schuster, U., Schmalz, G., Thonemann, В., Mendell, N. and Metzl, C, Cytotoxicity testing with three-dimensional cultures of transfected pulp-derived cells, J. Endod., 27, pp. 259-265, 2001 |
[30] | Wennberg, A., Hasselgreen, G. and Tronstad, L., A method for toxicity screening of biomaterials using cells cultured on millipore filters, J. Biomed. Mater. Res., 13, pp. 109-120, 1979 |
Электронный текст документа
и сверен по:
, 2011