ГОСТ Р ЕН 12296-2009
Группа Р26
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Биотехнология
ОБОРУДОВАНИЕ
Методы контроля эффективности очистки
Biotechnology. Equipment. Guidance on testing procedures for cleanability
ОКС 11.120.10
ОКП 94 5120
Дата введения 2010-07-01
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. N 184-ФЗ "О техническом регулировании", а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 ПОДГОТОВЛЕН Общероссийской общественной организацией "Ассоциация инженеров по контролю микрозагрязнений" (АСИНКОМ) на основе собственного аутентичного перевода стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 458 "Производство и контроль качества лекарственных средств"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 3 сентября 2009 г. N 317-ст
4 Настоящий стандарт идентичен европейскому стандарту ЕН 12296:1998 "Биотехнология. Оборудование. Методы контроля эффективности очистки" (EN 12296:1998 "Biotechnology - Equipment - Guidance on testing procedures for cleanability")
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячно издаваемых информационных указателях "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
Введение
Очистка оборудования является важным процессом в биотехнологическом производстве и предназначена для предотвращения загрязнения продукции, окружающей среды и отрицательного воздействия на персонал.
Следует разработать и документально оформить методики контроля эффективности процессов очистки.
Стандарты (например, комплекс стандартов ИСО 9000 [9]) и правила производства лекарственных средств (GMP) [10] устанавливают основные требования, выполнение которых обеспечивает высокое качество производства продукции.
Данный стандарт позволяет оценить эффективность процессов очистки оборудования, используемого в биотехнологии, где имеются дополнительные специфические требования, связанные с безопасностью и особыми свойствами биотехнологических процессов. Его следует рассматривать совместно со стандартами, указанными выше. В частности, настоящий стандарт устанавливает принципы, на которых базируются методы испытаний. Руководство по выбору методов испытаний приведено в приложении А.
Необходимая степень очистки оборудования существенно зависит от типа процесса. В некоторых случаях значительное остаточное загрязнение после очистки не наносит вреда людям и окружающей среде и не создает трудностей для процесса производства. В других случаях может быть существенным даже очень незначительное остаточное загрязнение. Невозможно добиться полного удаления загрязнений с поверхности (оборудования), так как все поверхности в той или иной степени обладают абсорбционными свойствами.
Стандарт ЕН 12296 подготовлен Техническим комитетом ЕКС/ТК 233 "Биотехнология".
Ссылка в тексте стандарта приведена для пояснения смысла и выделена курсивом.
1 Область применения
Настоящий стандарт устанавливает методы оценки эффективности очистки оборудования (элементов и узлов), используемых в биотехнологических процессах.
Требования настоящего стандарта применяют, прежде всего, для оборудования, используемого для работы с потенциально опасными микроорганизмами. Требования стандарта также применяют к процессам с использованием безопасных микроорганизмов и/или в случае, когда остаточные загрязнения могут отрицательно влиять на процессы стерилизации, либо вызывать перекрестное загрязнение продукции и процессов.
Требования стандарта распространяются на оборудование или его части, например такие, как вентили, емкости, насосы, трубопроводы, установки для сепарации и наполнения, а также на контрольно-измерительные приборы, контактирующие с жидкостями, используемыми в технологическом процессе.
2 Термины и определения
В настоящем стандарте применяются следующие термины с соответствующими определениями:
2.1 чистый (clean): Состояние продукта, поверхности, устройства, газов и/или жидкостей с остаточным загрязнением ниже установленного порогового уровня.
2.2 эффективность очистки (cleanability): Свойство объекта, характеризующее возможность проведения его эффективной очистки.
2.3 очистка (cleaning): Удаление загрязнения с оборудования.
2.4 очистка на месте (Cleaning-In Place): Очистка оборудования без демонтажа его деталей и узлов.
2.5 узлы оборудования (components of equipment): Конструктивные элементы, являющиеся составными частями оборудования.
Примечание - Примерами узлов оборудования являются сосуды, вентили и датчики.
2.6 контаминация (contamination): Наличие загрязнений на оборудовании*.
________________
* Контаминация также может включать в себя наличие посторонних веществ.
2.7 остаточное загрязнение (residual soil): Загрязнение, оставшееся после очистки.
2.8 загрязнение (soil): Материал, включая микроорганизмы, метаболиты и компоненты технологических сред, находящиеся на поверхности.
2.9 блок оборудования (unit of equipment): Совокупность узлов, оборудования, используемых для проведения одной или нескольких операций.
3 Испытания
3.1 Общие положения
Требования к эффективности очистки оборудования зависят от типа применяемого технологического процесса, особенно с точки зрения оценки риска. Поэтому классификация эффективности очистки по признаку биологической опасности установлена в стандартах на конкретное оборудование. Это позволяет изготовителям оборудования определить его характеристики с использованием методов тестирования, включая визуальный осмотр, процедура которого разработана в соответствии с принципами, описанными в подразделе 3.2, а потребителям оборудования изложить свои требования, используя простую терминологию. Эти классы определяют характеристики только по отношению к определенному веществу - индикатору и одному (или нескольким) выбранному протоколу очистки и соответствуют указанному способу использования оборудования. Классы эффективности очистки, указанные для оборудования, изменяются в зависимости от применяемого индикатора и протокола очистки.
Загрязнение, скопившееся на поверхности оборудования по окончании биотехнологического процесса, может содержать множество компонентов. Индикатор, выбранный для демонстрации эффективности очистки, должен определить те компоненты, которые отрицательно влияют на безопасность людей, окружающей среды или на характеристики самого процесса. Краткое описание индикаторов и методов испытаний приведено в приложении В.
3.2 Методы испытаний
Для определения эффективности очистки оборудования следует выбрать метод испытания или комбинацию методов (см. приложения А, В), включая:
a) выбор индикатора, соответствующего назначению оборудования;
b) выбор методов отбора проб и анализа, которые должны использоваться для определения количества этого индикатора, находящегося на соответствующих поверхностях оборудования;
c) разработку методики очистки, содержащей, как минимум, состав средства очистки, порядок его применения и режим работы.
Примечания
1 Необходимо определить потенциальную опасность, которой может подвергаться персонал при проведении очистки.
2 В методике должны быть указаны такие параметры, как продолжительность очистки, температура и скорость потока жидкости, используемой для очистки.
3 Методика очистки может содержать ряд последовательно выполняемых операций.
3.3 Проведение испытаний
Порядок проведения испытаний:
a) поместить в оборудование загрузку, содержащую индикатор, при нормальных условиях эксплуатации или условиях, имитирующих нормальную эксплуатацию;
b) включить оборудование при указанных в перечислении а) условиях и не прекращать его работу до удаления (расхода) загрузки и готовности оборудования к проведению очистки;
c) перед началом очистки, используя аналитический метод, выбранный согласно подразделу 3.2, определить количество индикаторного вещества, оставшегося после удаления загрузки;
d) провести очистку в соответствии с методикой, описанной в подразделе 3.2;
e) используя аналитический метод, описанный в подразделе 3.2, определить количество индикаторного вещества, находящегося на испытуемых поверхностях оборудования после проведения очистки;
f) используя полученные данные, определить эффективность очистки оборудования;
g) определить приспособленность испытуемого оборудования к очистке (класс оборудования) по соответствующему стандарту на оборудование с учетом данного индикаторного вещества и метода очистки.
Примечание - Метод, предложенный Европейской группой разработки гигиенических критериев (EHEDG) [2], может рассматриваться как пример испытаний с применением способа, описанного в подразделе 3.2, когда индикаторным веществом являются споры специфических бактерий, а аналитическим методом - метод культивирования. Определяют число специфических бактерий до и после очистки и оформляют протокол очистки [3].
В качестве индикатора могут использоваться и другие микроорганизмы, специальные группы химических соединений, таких как определенные протеины, углеводы или липиды, а также соединения, для которых известна способность оказывать отрицательное влияние на людей, окружающую среду или последующий технологический процесс (см. приложение С). Метод очистки может быть простым, например, путем промывки поверхности оборудования водой через шланг, или сложным, таким как очистка оборудования на месте (CIP), включающая в себя использование опасных химических соединений при высокой температуре.
Допускается применять различные методы испытаний: биологические индикаторы, химический количественный анализ, иммунологические методы, флуоресцентные и другие физические методы анализа, включая микроскопию (см. приложение В).
4 Документация
Изготовитель и/или пользователь оборудования должны разработать и документально оформить методики оценки эффективности очистки оборудования. Эти методики должны содержать данные об испытаниях (методы испытаний, аналитические методики и инструкции по очистке) и результаты испытаний.
Приложение А
(справочное)
Выбор методов контроля чистоты
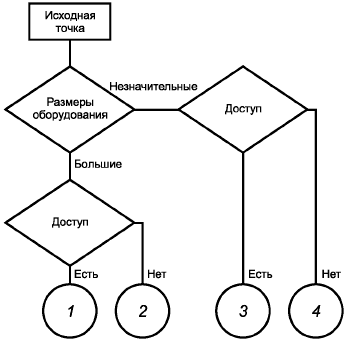
На рисунке А.1 приведена схема выбора метода испытаний по определению эффективности очистки оборудования.
1 - промывка (см. приложение В, раздел В.4), визуальный осмотр (см. приложение В, раздел В.2), мазки тампоном (см. приложение В, раздел В.3) - дополнительный метод;
2 - промывка, контроль загрязнений в последующей загрузке или серии продукции (см. приложение В, раздел В.5);
3 - промывка*, визуальный осмотр, мазки тампоном*;
________________
* Следует сравнить результат с данными после промывки.
4 - промывка, контроль загрязнений в последующей загрузке или серии продукции - дополнительный метод.
Рисунок А.1 - Схема выбора метода испытаний по определению эффективности очистки оборудования
Приложение В
(справочное)
Сведения о методах контроля чистоты
В.1 Общие положения
Существуют четыре метода контроля чистоты оборудования [3]: визуальный осмотр, мазки тампоном с внутренних поверхностей, отбор проб моющей жидкости после последней промывки и контроль загрязнений в последующей загрузке (серии продукции).
В.2 Визуальный осмотр
Остаточное загрязнение, адсорбированные микробные популяции или следы индикаторов могут быть обнаружены при визуальном осмотре оборудования или с использованием методов микроскопии таких, как световая микроскопия, сканирующая или просвечивающая электронная микроскопия [4]. При применении этих методов, как правило, необходим доступ к контролируемым поверхностям.
В.3 Мазки с внутренних поверхностей
Количественную оценку индикаторов (химического или биологического происхождения) можно провести путем взятия мазков с определенных участков оборудования, которые вступают в контакт с продуктом. Мазки с легко доступных плоских поверхностей оборудования могут дать сверхоптимистические результаты в отношении чистоты. Мазки с малодоступных мест могут дать сверхпессимистические результаты. Для получения статистически значимых результатов важно правильно определить места и площади для взятия мазков с оборудования. Мазки могут быть взяты непосредственно, например, с помощью агаровых пластинок, или косвенно, например, с использованием таких материалов, как хлопок, шерсть, альгинатных наконечников или пластин Petrifilm. При применении этого метода испытания необходим доступ к контролируемым поверхностям.
В качестве примера ниже приведен очень чувствительный, простой и недорогой метод для определения аминокислот и протеинов, остающихся на поверхности оборудования. Данный нингидриновый метод основан на реакции аминокислот, пептидов и протеинов с трикетогидринденгидратом. Эта известная реакция широко используется при тонкослойной хроматографии. Преимуществом данного метода для биотехнологических процессов по сравнению с методом остаточных загрязнений является возможность обнаружить широкий спектр веществ из культуральной среды и микроорганизмов таких, как аминокислоты, пептиды и протеины. Таким образом, один и тот же метод позволяет определять разнообразные среды, клеточные культуры, белковые жидкости и суспензии. Благодаря простоте и легкости выполнения данный метод используют в сложных и спорных случаях, а также для доказательства эффективности методов очистки, особенно для оборудования производителей или пользователей, которые не имеют лабораторий.
Порядок работы: отбирают пробу методом мазка с определенной площади с помощью ролика из влажного хлопка или шерсти. Для определения аминокислот, пептидов и протеинов непосредственно на поверхность хлопкового ролика наносят несколько капель нингидринового реагента, а затем выдерживают при температуре от 110 °С до 120 °С в течение времени от 20 до 30 мин. В случае наличия остатков на поверхности ролика появится фиолетовая окраска. Для доказательства эффективности очистки оборудования оно может быть загружено веществом, окрашиваемым нингидрином (например, аминокислотой типа аргинина), затем очищено, после чего проводят анализ на наличие остатков данного вещества. Чувствительность этого метода к аргинину составляет приблизительно 1 мг/м.
Для приготовления нингидринового реагента к смеси 100 мл n-бутанола и 3 мл ледяной уксусной кислоты добавляют 0,30 г нингидрина.
В.4 Отбор проб моющей жидкости после последней промывки
Моющая жидкость после последней промывки может быть проверена на наличие индикатора, продукта или технологических сред.
Примерами загрязнений являются:
- жизнеспособные микроорганизмы [2];
- общее содержание протеинов;
- липополисахариды;
- соли, сахара [7];
- общий органический углерод (ООУ).
Следует обратить внимание на то, чтобы загрязняющие вещества были растворены или суспендированы в моющей жидкости, которая должна иметь хороший контакт со всеми частями оборудования.
В.5 Контроль загрязнений в следующей серии
Контроль загрязнений в следующей серии продукции (например, индикаторы, используемые в соответствии с методом контроля, указанным в подразделе В.3) не является лучшим методом контроля эффективности очистки оборудования, но он может быть использован, если по каким-либо причинам приведенные выше методы неприменимы или дают противоречивые результаты. Следующую серию следует контролировать в случае, если были использованы патогенные микроорганизмы, отличающиеся от микроорганизмов предыдущей серии.
В.6 Методы непосредственного контроля для определения остаточного загрязнения
Примерами методов непосредственного контроля являются:
- ультразвук [5];
- лазерная сканирующая микроскопия;
- поляриметрические методы;
- методы, основанные на теплопередаче [6].
Приложение С
(справочное)
Библиография
[1] | Hygienic Equipment Design Criteria. EHEDA Update. Trends in Food Science & Technology. Vol.4, July 1993 |
[2] | A method for assessing the in-place cleanability of food-processing equipment. EHEDA Update. Trends in Food Science & Technology. Vol.3, December 1992 |
[3] | Cleaning Validation and Residue Limits: a contribution to current discussions. A.O. Zeller. Phar. Techn. Eur. P.18-27. November 1993 |
[4] | Some techniques involved in study of adsorption of micro-organisms to surfaces. J.W. Costerton. In: Attachment of micro-organisms to living and detrital surfaces (p.403-423). John Wiley & Sons, Inc. USA |
[5] | Ultrasound as a means of detaching biofilms. Zips, A et al. Biofouling, p.323-333, Vol.2, 1990 |
[6] | Continuous on-line monitoring of microbial deposition on surfaces. Characklis W.G. et al. In: Biodeterioration 6 Papers presented at the 6th International Biodeterioration Symposium, Washington DC, August 1984 |
[7] | New developments in aseptic design relating to CIP and SIP. M. |
[8] | ISO 4288. Geometrical Product Specifications (GPS) - Surface texture: Profile method - Rules and procedures for the assessment of surface texture |
[9] | EN ISO 9000-1. Quality management and quality assurance standards - Part 1: Guidelines for selection and use (ISO 9000-1:1994) |
[10] | The rules governing medicinal products in the EC. Volume IV: Guide to good manufacturing practice for medical products, 1989 |
[11] | EH-626-1. Safety of machinery - Reduction of risks to health from hazardous substances emitted by machinery - Part 1: Principles and specifications for machinery manufacturers |
[12] | ЕН-626-2. Safety of machinery - Reduction of risk to health from hazardous substances emitted by machinery - Part 2: Methodology leading to verification procedures |
[13] | Guide to inspection of bulk pharmaceutical chemicals (reference materials and training aid for investigators), 1991 |
[14] | Guide to inspection of validation of cleaning processes. FDA, July 1993 |
Электронный текст документа
и сверен по:
, 2009