ГОСТ Р 55298-2012
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕРМЕНТНЫЕ ПРЕПАРАТЫ ДЛЯ ПИЩЕВОЙ ПРОМЫШЛЕННОСТИ
Методы определения пектолитической активности
Enzyme preparations for food industry. Methods for determination of pectolytic activity*
________________
* Поправка. ИУС N 9-2015.
ОКС 07.100.30
ОКСТУ 9291
Дата введения 2014-01-01
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. N 184-ФЗ "О техническом регулировании", а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 РАЗРАБОТАН Государственным научным учреждением Всероссийским научно-исследовательским институтом пищевой биотехнологии Российской академии сельскохозяйственных наук (ГНУ ВНИИПБТ Россельхозакадемии)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 176 "Спиртовая, дрожжевая и ликероводочная продукция"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 29 ноября 2012 г. N 1503-ст
4 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.-2012* (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе "Национальные стандарты", а официальный текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети интернет (gost.ru)
________________
* Вероятно, ошибка оригинала. Следует читать: ГОСТ Р 1.0-2012. - .
ВНЕСЕНА поправка*, опубликованная в ИУС N 9, 2015 год
_________________________
* См. ярлык "Примечания".
Поправка внесена изготовителем базы данных
1 Область применения
Настоящий стандарт распространяется на ферментные препараты и ферментсодержащие смеси - источники ферментов пектолитического комплекса, применяемые в пищевой промышленности, и устанавливает методы определения пектолитической активности.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ Р ИСО 5725-1-2002 Точность (повторяемость и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения
ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть I. Метрологические технические требования. Испытания
ГОСТ 12.0.004-90 Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.2.007.0-75 Система стандартов безопасности труда. Изделия электротехнические. Общие требования безопасности
ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
ГОСТ 12.4.021-75 Система стандартов безопасности труда. Системы вентиляционные. Общие требования
ГОСТ 12.4.103-83 Система стандартов безопасности труда. Одежда специальная защитная, средства индивидуальной защиты ног и рук. Классификация
ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
ГОСТ 83-79 Реактивы. Натрий углекислый. Технические условия
ГОСТ 199-78 Реактивы. Натрий уксуснокислый 3-водный. Технические условия
ГОСТ 1277-75 Реактивы. Серебро азотнокислое. Технические условия
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ 3760-79 Реактивы. Аммиак водный. Технические условия
ГОСТ 4159-79 Реактивы. Йод. Технические условия
ГОСТ 4161-77 Реактивы. Кальций хлористый. Технические условия
ГОСТ 4174-77 Реактивы. Цинк сернокислый 7-водный. Технические условия
ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
ГОСТ 4220-75 Реактивы. Калий двухромовокислый. Технические условия
ГОСТ 4232-76* Реактивы. Калий йодистый. Технические условия
________________
* Вероятно, ошибка оригинала. Следует читать: ГОСТ 4232-74, здесь и далее по тексту. - .
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ 5556-81 Вата медицинская гигроскопическая. Технические условия
ГОСТ 5850-72 Реактивы. Фенолфталеин. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 9412-93 Марля медицинская. Общие технические условия
ГОСТ 10163-76 Реактивы. Крахмал растворимый. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 13867-68 Продукты химические. Обозначения чистоты
ГОСТ 15615-79 Иониты. Метод определения содержания ионов хлора
ГОСТ 18300-87 Реактивы. Спирт этиловый ректификованный технический. Технические условия
ГОСТ 18481-81 Ареометры и цилиндры стеклянные. Общие технические условия
ГОСТ 20264.0-74 Препараты ферментные. Правила приемки и методы отбора проб
ГОСТ 22180-76 Реактивы. Кислота щавелевая. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 27068-86 Реактивы. Натрий серноватистокислый (натрия тиосульфат) 5-водный. Технические условия
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
ГОСТ 29027-91 Влагомеры твердых и сыпучих веществ. Общие технические требования и методы испытаний
ГОСТ 29186-91 Пектин. Технические условия
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 29251-91 Посуда лабораторная стеклянная. Бюретки. Часть 1. Общие требования
ГОСТ 29298-2005 Ткани хлопчатобумажные и смешанные бытовые. Общие технические условия.
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если заменен ссылочный стандарт, на который дана недатированная ссылка, то рекомендуется использовать действующую версию этого стандарта с учетом всех внесенных в данную версию изменений. Если заменен ссылочный стандарт, на который дана датированная ссылка, то рекомендуется использовать версию этого стандарта с указанным выше годом утверждения (принятия). Если после утверждения настоящего стандарта в ссылочный стандарт, на который дана датированная ссылка, внесено изменение, затрагивающее положение, на которое дана ссылка, то это положение рекомендуется применять без учета данного изменения. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, рекомендуется применять в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 гидролиз: Расщепление исходного соединения на более простые в присутствии молекул воды.
3.2 ферментативный гидролиз: Расщепление высокомолекулярных соединений при участии катализаторов белковой природы - гидролитических ферментов.
3.3 субстрат: Соединение или вещество, на которое воздействует соответствующий фермент.
3.4 пектин: Высокомолекулярный полисахарид, состоящий из водорастворимых полигалактуроновых кислот, карбоксильные группы которых в различной степени этерифицированы метанолом.
3.5 пектиновая кислота: Полигалактуроновая кислота, состоящая из остатков -галактуроновой кислоты соединенных
-1,4 связями, в малой степени этерифицированная остатками метанола.
3.6 пектовая кислота: Кислота, представляющая собой линейный полимер, состоящий из остатков -
-галактуроновой кислоты, связанных 1,4-гликозидными связями, выделенная из пектиновой кислоты гидролизом сложноэфирных групп.
3.7 системные названия ферментов: Названия, указывающие природу химической реакции, катализируемой данным ферментом, в соответствии с современной классификацией ферментов (КФ), принятой Международной комиссией по ферментам.
Примечания
Системные названия ферментов.
Пектолитические ферменты подразделяют на две основные группы: полигалактуроназа (КФ 3.2.1.15) и пектинэстераза (КФ 3.1.1.11) [1].
1 Полигалактуронид-гликаногидролаза (КФ 3.2.1.15) - полигалактуроназа - осуществляет гидролитическое расщепление -1,4-
-гликозидных связей в цепи пектиновых веществ. По субстратной специфичности к пектиновым веществам полигалактуроназы разделяют на два типа:
- эндополигалактуроназа - разжижающий фермент эндодействия, катализирующий гидролиз пектовой кислоты;
- экзополигалактуроназа - осахаривающий фермент экзодействия, катализирующий отщепление одного остатка галактуроновой кислоты по концевой гликозидной связи в молекуле пектовой кислоты.
2 Пектингидролаза пектинов (КФ 3.1.1.11) - пектинэстераза - фермент, действующий на сложноэфирные связи карбоновых кислот, катализирующий гидролиз пектина с образованием метанола и полигалактуроновой кислоты.
3.8 пектолитический комплекс: Пектиназы микробного происхождения, катализирующие гидролиз пектина и пектовой кислоты.
3.9 ферментативная активность: Количество фермента, катализирующее гидролиз 1 мкмоля субстрата в определенных условиях.
4 Метод определения пектолитической активности ферментных препаратов - источников пектиназ (ПкС)
4.1 Сущность метода
4.1.1 Метод позволяет оценить результаты совместного действия ферментов пектолитического комплекса, катализирующих гидролиз пектина. Метод основан на количественном определении продуктов гидролиза пектина, не осаждаемых сернокислым цинком, под действием ферментов пектолитического комплекса в стандартных условиях (температура 30 °С, значение рН реакционной среды 5,0 ед. рН, продолжительность гидролиза 1 ч).
4.1.2 За единицу пектолитической активности ПкС принято такое количество фермента, которое при значении 5,0 ед. рН, и температуре 30 °С за 1 мин катализирует гидролиз 1 г пектина до продуктов, не осаждаемых сернокислым цинком, что составляет 30% пектина, введенного в реакцию. Активность выражается в ед. ПкС/г (для порошкообразного) или в ед. ПкС/см (для жидкого) анализируемого ферментного препарата.
4.1.3 Количество продуктов прогидролизованного пектина, не осаждаемых сернокислым цинком, определяется интерферометрическим методом.
4.2 Средства измерений, вспомогательное оборудование, посуда, реактивы, материалы
4.2.1 Весы неавтоматического действия по ГОСТ 53228*, обеспечивающие точность взвешивания с пределами допускаемой абсолютной погрешности ±0,003 г.
________________
* Вероятно, ошибка оригинала. Следует читать: ГОСТ Р 53228-2008. - .
4.2.2 Интерферометр типа ИТР-2 или ЛИР-2 со шкалой компенсации 3000 дел и пределом допускаемого значения погрешности установки ширины полосы 2 дел.
4.2.3 рН-метр любого типа для измерения в диапазоне от 0 до 14 ед. рН с пределом допускаемой погрешности в эксплуатации ±0,1 ед. рН.
4.2.4 Влагомер твердых и сыпучих веществ по ГОСТ 29027.
4.2.5 Холодильник бытовой.
4.2.6 Мешалка магнитная любой марки, которая обеспечивает скорость вращения до 800 мин.
4.2.7 Ультратермостат или водяной термостат с точностью регулирования температуры ±1 °С.
4.2.8 Баня водяная любого типа, которая обеспечивает поддержание температуры (100±1) °С с точностью регулирования температуры ±1 °С.
4.2.9 Секундомер с емкостью шкалы счетчика 1 мин, ценой деления 1 с и погрешностью ±1,5 с.
4.2.10 Пипетки автоматические вместимостью от 0,1 до 1,0 см, 1,0 см
и от 0,2 до 10 см
с наконечниками.
4.2.11 Встряхиватель V-3 типа Вортекс или аналогичный для перемешивания жидкости со скоростью вращения от 50 до 3400 об./мин.
4.2.12 Термометры ртутные стеклянные лабораторные от 0 °С до 50 °С и от 0 °С до 100 °С с ценой деления шкалы 0,5 °С по ГОСТ 28498.
4.2.13 Стаканы и колбы стеклянные лабораторные В-1-150 ТС, В-1-800 ТС, В-1-50 ТС, Кн-1-100-14/23 ТС по ГОСТ 25336.
4.2.14 Стаканчики для взвешивания (бюксы) СВ-19/9 по ГОСТ 25336.
4.2.15 Воронки В-75-140 ХС по ГОСТ 25336.
4.2.16 Пробирки П1-14-120 ХС или П1-16-150 ХС или П1-18-200 по ГОСТ 25336.
4.2.17 Колбы мерные 1-25-2, 1-50-2, 1-100-2, 1-200-2, 1-250-2, 1-500-2, 2-1000-2 по ГОСТ 1770.
4.2.18 Цилиндры 1-25-2, 1-50-2, 1-100-2, 1-250-2 по ГОСТ 1770.
4.2.19 Пипетки стеклянные 1-2-2-1, 1-2-2-2, 1-2-2-5, 1-2-2-10 по ГОСТ 29227.
4.2.20 Бумага фильтровальная лабораторная по ГОСТ 12026.
4.2.21 Марля медицинская по ГОСТ 9412.
4.2.22 Пектин свекловичный со степенью метоксилирования не менее 35% и массовой долей основного вещества не менее 70% по ГОСТ 29186.
4.2.23 Натрий уксуснокислый по ГОСТ 199.
4.2.24 Кислота уксусная по ГОСТ 61.
4.2.25 Цинк сернокислый по ГОСТ 4174.
4.2.26 Вода дистиллированная по ГОСТ 6709.
Примечание - Для приготовления растворов (см. 4.3) используют дистиллированную воду температурой 20 °С.
4.2.27 Все реактивы должны относиться к подгруппе чистоты 2 (х.ч.) или 3 (ч.д.а.).
4.2.28 Допускается применение средств измерений, вспомогательного оборудования с аналогичными метрологическими и техническими характеристиками, а также реактивов по качеству не хуже вышеуказанных.
4.3 Подготовка к анализу
4.3.1 Приготовление ацетатного буферного раствора молярной концентрации 0,1 моль/дм с 5,0 ед. рН из растворов уксуснокислого натрия и уксусной кислоты (ледяной)
4.3.1.1 Приготовление раствора уксуснокислого натрия молярной концентрации ![]() 0,1 моль/дм
0,1 моль/дм (раствор А)
В мерную колбу вместимостью 1 дм помещают (8,20±0,01) г безводного уксуснокислого натрия или (13,60±0,01) г
![]() и растворяют приблизительно в 300 см
и растворяют приблизительно в 300 см дистиллированной воды. Затем доводят до метки дистиллированной водой и перемешивают.
4.3.1.2 Приготовление раствора ледяной уксусной кислоты молярной концентрации ![]() 0,1 моль/дм
0,1 моль/дм (раствор Б)
В мерную колбу вместимостью 1 дм вносят 5,72 см
ледяной уксусной кислоты, приливают около 300 см
дистиллированной воды, доводят до метки дистиллированной водой и перемешивают.
4.3.1.3 Для приготовления ацетатного буферного раствора в колбе смешивают растворы уксуснокислого натрия (раствор А) и уксусной кислоты (раствор Б) в соотношении 2:1 для получения кислотности буферного раствора, равной 5,0 ед. рН. При необходимости кислотность раствора доводят до 5,0 ед. рН одним из исходных растворов.
Срок хранения буферного раствора в закрытой стеклянной посуде при температуре 4 °С - не более 1 мес.
4.3.2 Приготовление раствора сернокислого цинка массовой концентрации 15%
21,43 г сернокислого цинка растворяют в стаканчике в небольшом количестве дистиллированной воды.
Растворенную соль переносят количественно в мерную колбу вместимостью 100 см и объем доводят до метки дистиллированной водой.
Срок хранения раствора сернокислого цинка при температуре 20 °С - не более 1 мес.
4.3.3 Приготовление раствора пектина с массовой долей 1,0% (субстрат)
Пектин, взятый с расчетом, чтобы 100 см раствора содержало 1,00 г чистого пектина (в соответствии с приложением А) всыпают тонкой струей при непрерывном перемешивании в мерную колбу вместимостью 100 см
, в которую предварительно наливают 25 см
ацетатного буфера кислотностью 5,0 ед. рН. Раствор непрерывно перемешивают на магнитной мешалке в течение 30 мин до полного растворения пектина. По истечении этого времени объем раствора доводят до 100 см
ацетатным буфером кислотностью 5,0 ед. рН, тщательно перемешивают и фильтруют через два слоя марли.
Срок хранения раствора пектина в холодильнике при температуре 4 °С - не более двух суток.
4.4 Подготовка пробы
4.4.1 Отбор проб - по ГОСТ 20264.0.
Анализируемые пробы ферментных препаратов в порошкообразном или жидком виде используют без предварительной подготовки.
4.4.2 Приготовление основного раствора анализируемой пробы ферментного препарата
В стаканчик для взвешивания шпателем помещают порошкообразный ферментный препарат для получения анализируемой пробы массой (0,1000±0,0002) г. Жидкий ферментный препарат (1,00±0,02) см вносят в стаканчик пипеткой. Полученную анализируемую пробу ферментного препарата суспендируют в небольшом количестве дистиллированной воды и количественно переносят в мерную колбу вместимостью 100 см
, доводят объем до метки дистиллированной водой при температуре 20 °С и тщательно перемешивают. Приготовленный раствор ферментного препарата является основным раствором анализируемой пробы.
Срок хранения основного раствора ферментного препарата при температуре 20 °С - не более 1 ч.
4.4.3 Приготовление рабочего раствора анализируемой пробы ферментного препарата
Рабочий раствор анализируемой пробы ферментного препарата готовят из основного раствора по 4.4.2 путем дальнейшего разведения его дистиллированной водой в зависимости от предполагаемой активности таким образом, чтобы при ее определении показания интерферометра соответствовали пределу измерений от 400 до 1250 дел (по 4.2.2).
С учетом разведения рассчитывают количество препарата, взятого на анализ.
Каждую пробу анализируют два раза в условиях повторяемости в соответствии в требованиями ГОСТ Р ИСО 5725-1.
Раствор готовят в день определения. Длительность использования рабочего раствора ферментного препарата не должна превышать 1 ч с момента приготовления во избежание потерь его ферментативной активности.
4.5 Проведение анализа
Для анализа берут несколько пробирок размером 18х200 мм по количеству анализируемых проб.
4.5.1 В каждую пробирку размером 18х200 мм вносят по 10 см субстрата 1%-ного раствора пектина (см. 4.3.3). Содержимое пробирок прогревают в ультратермостате при температуре (30,0±1,0) °С в течение 5 мин.
4.5.2 В пробирки с субстратом добавляют по 5,0 см рабочего раствора анализируемой пробы ферментного препарата по 4.4.3, предварительно прогретого при температуре 30 °С, тщательно перемешивают и включают секундомер, отмечая начало ферментативной реакции. Реакционную смесь инкубируют при температуре (30,0±1,0) °С в течение 1 ч (с точностью, определяемой по секундомеру от начала ферментативной реакции).
4.5.3 По окончании реакции в пробирки с реакционной смесью добавляют 1,0 см сернокислого цинка для инактивации фермента и осаждения продуктов гидролиза, вынимают из термостата, тщательно перемешивают и фильтруют через бумажный фильтр. Полученный фильтрат должен быть прозрачным.
4.5.4 Одновременно готовят контрольный раствор. Для этого в пробирки наливают 1,0 см сернокислого цинка, добавляют 5,0 см
анализируемого ферментного раствора и 10 см
субстрата, интенсивно перемешивают и фильтруют через бумажный фильтр. Раствор должен быть прозрачным.
4.5.5 Полученные анализируемый и контрольный растворы используют для измерения разности показателей преломления на интерферометре (см. 4.2.2). Полученные показатели преломления используют для расчета пектолитической активности.
4.6 Обработка результатов
4.6.1 Расчет пектолитической активности в анализируемой пробе
Пектолитическую активность в анализируемой пробе ферментного препарата вычисляют по формулам
- для порошкообразного препарата в ед. ПкС/г
![]() , (1)
, (1)
- для жидкого препарата в ед.ПкС/см
![]() , (2)
, (2)
где 0,06425; 19,62; 1000 - коэффициенты расчетного уравнения, полученные при математической обработке экспериментальных данных зависимости количества образующихся продуктов гидролиза пектина и количеством единиц активности фермента, взятого для анализа;
- показания прибора с учетом разведения по 4.4.3;
- масса ферментного препарата с учетом разведения по 4.4.3, взятая для анализа, г;
- плотность для концентрированных жидких ферментных препаратов по ГОСТ 18481, г/см
.
При значении пектолитической активности выше 100 ед. ПкС/г (см), допускается разведение анализируемой пробы дистиллированной водой при температуре 20 °С до значений, находящихся в пределах допустимых показаний прибора.
4.6.2 Оформление результатов измерений
За окончательный результат определения принимают среднеарифметическое значение результатов двух параллельных определений, выполненных в условиях повторяемости, если выполняется условие приемлемости (3).
Результат анализа при доверительной вероятности 0,95 представляют в виде
![]() ,
,
где - среднеарифметическое значение результатов двух параллельных определений, признанных приемлемыми (см. 4.7.1), ед.ПкС/г(для порошкообразного препарата) или ед. ПкС/см
(для жидкого препарата);
- значение границ абсолютной погрешности измерений (расширенная неопределенность
с коэффициентом охвата
2, ед. ПкС/г (для порошкообразного препарата) или ед. ПкС/см
(для жидкого препарата), определяемое по формуле
![]() , (3)
, (3)
где - границы относительной погрешности результата анализа пектолитической активности в анализируемой пробе при
0,95 составляют ±7%.
Результаты анализа выражают с точностью до первого десятичного знака ед. ПкС/г (для порошкообразного препарата) или ед. ПкС/см (для жидкого препарата).
4.7 Сходимость и воспроизводимость результатов
4.7.1 Результаты определений, полученные в условиях повторяемости (сходимости), признаются удовлетворительными, если выполняется условие приемлемости
![]() , (4)
, (4)
где и
- результаты двух параллельных определений, полученные в условиях повторяемости при
0,95, ед. ПкС/г (для порошкообразного препарата) или ед. ПкС/см
(для жидкого препарата);
- среднеарифметическое значение результатов двух параллельных определений, ед. ПкС/г (для порошкообразного препарата) или ед. ПкС/см
(для жидкого препарата);
- предел повторяемости (сходимости) при
0,95, равный 5%.
4.7.2 Результаты определений, полученные в условиях воспроизводимости по ГОСТ Р ИСО 5725-1, признаются удовлетворительными, если выполняется условие приемлемости
![]() , (5)
, (5)
где и
- окончательные результаты определений, полученные в двух лабораториях в условиях воспроизводимости в точном соответствии с методом, ед. ПкС/г (для порошкообразного препарата) или ед. ПкС/см
(для жидкого препарата);
- среднеарифметическое значение двух окончательных результатов определений, полученных в условиях воспроизводимости, ед. ПкС/г (для порошкообразного препарата) или ед. ПкС/см
( )(для жидкого препарата);
![]() - критическая разность, равная 10% при доверительной вероятности
- критическая разность, равная 10% при доверительной вероятности 0,95.
5 Метод определения эндополигалактуроназной активности ферментных препаратов (Эндо-ПгС)
5.1 Сущность метода
5.1.1 Метод основан на гидролизе пектовой кислоты анализируемым ферментным препаратом с контролем степени расщепления и снижения вязкости субстрата.
5.1.2 Эндополигалактуроназная активность (Эндо-ПгС) характеризует способность ферментного препарата снижать вязкость 1,0%-ного раствора пектовой кислоты.
5.1.3 За единицу эндополигалактуроназной активности принято такое количество фермента, которое способно катализировать гидролиз 1,0 г пектовой кислоты при температуре 30 °С и кислотности 5,0 ед. рН, снижая за 1 мин вязкость раствора на 30%. Эндополигалактуроназную активность выражают в ед. Эндо-ПгС/г (для порошкообразного) или ед. Эндо-ПгС/см (для жидкого) анализируемого ферментного препарата.
5.2 Средства измерений, вспомогательное оборудование, посуда и реактивы
5.2.1 Для определения эндополигалактуроназной активности применяют средства измерений, аппаратуру, лабораторную посуду, материалы, реактивы, указанные в 4.2, со следующими дополнениями:
5.2.1.1 Вискозиметр Оствальда с размером диаметра капилляра 0,99 мм.
5.2.1.2 Кислота пектовая.
5.2.1.3 Кислота серная по ГОСТ 4204 (плотность 1,850 г/см
).
5.2.1.4 Натрия гидроокись по ГОСТ 4328.
5.2.1.5 Воронка Бюхнера по ГОСТ 9147.
5.2.1.6 Спирт этиловый ректификованный технический по ГОСТ 18300.
5.2.1.7 Кислота соляная по ГОСТ 3118 (плотность 1,15-1,19 г/см
).
5.2.1.8 Бязь по ГОСТ 29298.
5.2.1.9 Вата медицинская гигроскопическая по ГОСТ 5556.
5.2.2 Все реактивы должны относиться к подгруппе чистоты 2 (х.ч.) или 3 (ч.д.а.).
5.2.3 Допускается применение средств измерений, вспомогательного оборудования с аналогичными метрологическими и техническими характеристиками, а также реактивов по качеству не хуже вышеуказанных.
5.3 Подготовка к анализу
5.3.1 Приготовление ацетат-HCI буферного раствора молярной концентрации 0,2 моль/дм с кислотностью 5,0 ед. рН из растворов уксуснокислого натрия и соляной кислоты
5.3.1.1 Приготовление раствора уксуснокислого натрия молярной концентрации ![]() 0,2 моль/дм
0,2 моль/дм (раствор А)
В мерную колбу вместимостью 1 дм помещают (16,4±0,01) г безводного уксуснокислого натрия или (27,2±0,01) г
![]() и растворяют приблизительно в 300 см
и растворяют приблизительно в 300 см дистиллированной воды. Затем доводят до метки дистиллированной водой при температуре 20 °С и перемешивают.
5.3.1.2 Приготовление раствора соляной кислоты молярной концентрации ![]() 0,2 моль/дм
0,2 моль/дм (раствор Б)
В мерную колбу вместимостью 1 дм приливают около 300 см
дистиллированной воды и медленно вносят 7,2 см
концентрированной соляной кислоты, доводят до метки дистиллированной водой при температуре 20 °С и перемешивают.
5.3.1.3 Для приготовления ацетат- буферного раствора в колбе смешивают растворы уксуснокислого натрия (раствор А) и соляной кислоты (раствор Б) в соотношении 2:0,5, создавая кислотность смеси, равную 5,0 ед. рН. При необходимости доводят кислотность раствора до 5,0 ед. рН одним из исходных растворов.
Срок хранения буферного раствора в закрытой стеклянной посуде при температуре 4 °С - не более 1 мес.
5.3.2 Приготовление пектовой кислоты (субстрат)
30,0 г свекловичного пектина заливают 600 см дистиллированной воды и оставляют на ночь в холодильнике при температуре 4 °С для набухания и растворения. Затем при температуре 20 °С добавляют 300 см
0,5 н раствора гидроокиси натрия для полного растворения пектина и снижения вязкости раствора. Фильтруют на воронке Бюхнера через два слоя марли с проложенной ватой. Далее добавляют к фильтрату еще 300 см
0,5 н раствора гидроокиси натрия и оставляют для омыления на 1 ч в холодильнике при температуре 4 °С. Через 1 ч осаждают пектовую кислоту 900 см
0,5 н раствора соляной кислоты. Выпавшую кислоту сразу отжимают через бязь, помещают в стакан и добавляют 70%-ный этиловый спирт, тщательно перемешивают до растворения комков и снова фильтруют на воронке Бюхнера через бязь. Далее продолжают промывать 50 см
70%-ного этилового спирта, а затем 50 см
96%-ного этилового спирта. Полученную промытую пектовую кислоту сушат на воздухе при температуре 20 °С. Высушенную кислоту снимают с бязи и растирают в ступке до получения мелкодисперсного порошка.
5.3.3 Приготовление раствора пектовой кислоты с массовой долей 1,0% (субстрат)
1,0 г пектовой кислоты в пересчете на абсолютно сухое вещество (см. 4.2.4) всыпают тонкой струей при непрерывном перемешивании в мерную колбу вместимостью 100 см, куда предварительно наливают 25 см
ацетат-
буфера кислотностью 5,0 ед. рН. Раствор непрерывно перемешивают на магнитной мешалке в течение 30 мин до полного растворения. По истечении этого времени объем раствора доводят до 100 см
ацетат-HCI буфером кислотностью 5,0 ед. рН, тщательно перемешивают и фильтруют через два слоя марли.
Раствор пектовой кислоты готовят в день проведения анализа.
5.4 Подготовка пробы
5.4.1 Отбор проб - по ГОСТ 20264.0.
Анализируемые пробы порошкообразных или жидких ферментных препаратов допускается использовать без предварительной подготовки.
5.5 Приготовление основного раствора анализируемой пробы ферментного препарата
В стаканчик для взвешивания шпателем помещают порошкообразный ферментный препарат для получения анализируемой пробы массой (0,1000±0,0002) г. Жидкий ферментный препарат (1,00±0,02) см вносят в стаканчик пипеткой. Полученную анализируемую пробу ферментного препарата суспендируют в небольшом количестве дистиллированной воды и количественно переносят в мерную колбу вместимостью 100 см
, доводят объем до метки дистиллированной водой при температуре 20 °С и тщательно перемешивают. Приготовленный раствор ферментного препарата является основным раствором анализируемой пробы.
Срок хранения основного раствора ферментного препарата при температуре 20 °С - не более 1 ч.
5.5.1 Приготовление рабочего раствора анализируемой пробы ферментного препарата
Рабочий раствор анализируемой пробы ферментного препарата готовят из основного раствора по 5.5 путем дальнейшего разведения его дистиллированной водой в зависимости от предполагаемой активности таким образом, чтобы при ее определении процент гидролиза пектина был в пределах от 10% до 15%.
С учетом разведения рассчитывают количество препарата, взятого на анализ.
Каждую пробу анализируют два раза в условиях повторяемости в соответствии в требованиями ГОСТ Р ИСО 5725-1.
Раствор готовят в день определения. Длительность использования рабочего раствора ферментного препарата не должна превышать 1 ч с момента приготовления во избежание потерь его ферментативной активности.
5.6 Проведение анализа
5.6.1 В сухой вискозиметр Оствальда с размером диаметра капилляра 0,99 мм, погруженный в термостат с температурой 50 °С, автоматической пипеткой вносят 10 см 1,0%-ного раствора пектовой кислоты, прогревают в течение 5 мин. Через 5 мин автоматической пипеткой вводят предварительно прогретый раствор фермента (от 1,0 до 5,0 см
) в зависимости от активности ферментного препарата. Общий объем реакционной смеси всегда должен быть 15,0 см
, поэтому при добавлении меньшего количества раствора фермента вносят соответственное количество прогретой дистиллированной воды. Дистиллированную воду обязательно вносят непосредственно перед внесением раствора фермента.
5.6.2 После введения раствора фермента сразу по секундомеру отмечают время начала гидролиза и одновременно перемешивают содержимое вискозиметра при помощи груши, надетой на узкое колено вискозиметра.
5.6.3 Через 3 мин после введения раствора фермента измеряют вязкость по времени истечения реакционной смеси. Время истечения реакционной смеси отмечают вторым секундомером через каждые 2 мин, пока вязкость не снизится на 30% от исходной. При отклонении от этой величины необходимо увеличить или уменьшить количество ферментного препарата. Время гидролиза не должно превышать 15 мин.
5.6.4 Контрольное определение вязкости раствора субстрата (контрольный раствор) проводят аналогично опытному, но вместо раствора фермента вводят 5,0 см воды.
5.7 Обработка результатов
5.7.1 Снижение вязкости 1%-ного раствора пектовой кислоты , %, рассчитывают по формуле
![]() , (6)
, (6)
где - время истечения контрольного раствора, с;
- время истечения дистиллированной воды, с;
- время истечения анализируемого раствора, с.
Снижение вязкости пектина вычисляют для всех произведенных замеров. Для построения градуировочного графика используются данные снижения вязкости анализируемого раствора после 3-5 мин гидролиза в пределах от 10% до 15%, при условии двукратной повторяемости результата.
По полученным данным строят градуировочный график, где на оси абсцисс () откладывают время гидролиза (
) в мин; на оси ординат (
) - соответствующее этому времени снижение вязкости (см. рисунок 1).
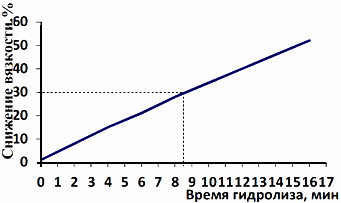
Рисунок 1
Градуировочный график строят каждый раз при приготовлении нового раствора пектовой кислоты.
Найденное интерполированием время, за которое взятое на анализ количество ферментного препарата снизило вязкость пектовой кислоты на 30% (), используют для расчета эндополигалактуроназной активности (см. рисунок 1).
5.7.2 Эндополигалактуроназную активность в анализируемой пробе, ед. Эндо-ПгС/г (для порошкообразного препарата) или ед. Эндо-ПгС/см (для жидкого препарата) рассчитывают по формулам
- для порошкообразного препарата в ед.Эндо-ПгС/г
![]() , (7)
, (7)
- для жидкого препарата в ед.Эндо-ПгС/см
![]() , (8)
, (8)
где 0,1 - количество пектовой кислоты, взятой на определение в 10 см 1,0%-ного раствора субстрата, г;
- количество ферментного препарата, введенного в реакционную смесь, г (см
);
- найденное интерполированием время гидролиза, снижающее вязкость раствора пектовой кислоты на 30%, мин;
- плотность для жидких концентрированных ферментных препаратов по ГОСТ 18481, г/см
.
При значении эндополигалактуроназной активности выше 100 ед. Эндо-ПгС/г(см), допускается разведение анализируемой пробы дистиллированной водой при температуре 20 °С, до значений, находящихся в пределах допустимых показателей (%) гидролиза пектовой кислоты (3-5 мин, от 10% до 15%).
5.8 Оформление результатов измерений
5.8.1 За окончательный результат определения принимают среднеарифметическое результатов двух параллельных определений, выполненных в условиях повторяемости, если выполняется условие приемлемости (9).
Результат анализа при доверительной вероятности 0,95 представляют в виде
![]() ,
,
где - среднеарифметическое значение результатов двух параллельных определений, признанных приемлемыми (см. 5.7.1), ед. Эндо-ПгС/г (для порошкообразного препарата) или ед. Эндо-ПгС/см
(для жидкого препарата);
- значение границ абсолютной погрешности измерений (расширенная неопределенность
с коэффициентом охвата
2), ед. Эндо-ПгС/г (для порошкообразного препарата) или ед. Эндо-ПгС/см
(для жидкого препарата), вычисляемое по формуле
![]() , (9)
, (9)
где - границы относительной погрешности результата анализа эндополигалактуроназной активности в анализируемой пробе при
0,95 составляют ±7%.
Результаты анализа выражают с точностью до первого десятичного знака ед. Эндо-ПгС/г (для порошкообразного препарата) или ед. Эндо-ПгС/см (для жидкого препарата).
5.8.2 Результаты определения, полученные в условиях воспроизводи-мости по ГОСТ Р ИСО 5725-1, признаются удовлетворительными, если выполняется условие приемлемости препарата или ед. Эндо-ПгС/см (для жидкого препарата).
5.9 Сходимость и воспроизводимость результатов
5.9.1 Результаты определения, полученные в условиях повторяемости (сходимости), признаются удовлетворительными, если выполняется условие приемлемости
![]() , (10)
, (10)
где и
- результаты двух параллельных определений, полученные в условиях повторяемости при
0,95, ед. Эндо-ПгС/г (для порошкообразного препарата) или ед. Эндо-ПгС/см
(для жидкого препарата);
- среднеарифметическое значение результатов двух параллельных определений, ед. Эндо-ПгС/г (для порошкообразного препарата) или ед. Эндо-ПгС/см
(для жидкого препарата);
- предел повторяемости (сходимости), равный 5%.
5.9.2 Результаты определений, полученные в условиях воспроизводимости по ГОСТ Р ИСО 5725-1, признаются удовлетворительными, если выполняется условие приемлемости
![]() , (11)
, (11)
где и
- окончательные результаты определений, полученные в двух лабораториях в точном соответствии с методом, ед. Эндо-ПгС/г (для порошкообразного препарата) или ед. Эндо-ПгС/см
(для жидкого препарата);
- среднеарифметическое значение двух окончательных результатов определений, полученных в условиях воспроизводимости, ед. Эндо-ПгС/г (для порошкообразного препарата) или ед. Эндо-ПгС/см
(для жидкого препарата);
![]() - критическая разность, равная 10% при доверительной вероятности
- критическая разность, равная 10% при доверительной вероятности 0,95.
6 Метод определения экзополигалактуроназной активности ферментных препаратов (Экзо-ПгС)
6.1 Сущность метода
6.1.1 Метод основан на учете количества прогидролизованных связей в пектовой кислоте, рассчитываемых по увеличению конечных альдегидных групп.
6.1.2 За единицу экзополигалактуроназной активности принято такое количество фермента, которое способно катализировать гидролиз 1,0 мкмоль эквивалента гликозидных связей в молекуле пектовой кислоты за 1 мин при температуре 30 °С и значении рН 4,0.
Экзополигалактуроназную активность выражают в ед. Экзо-ПгС/г (для порошкообразного) или ед. Экзо-ПгС/см (для жидкого) анализируемого ферментного препарата.
6.2 Средства измерений, вспомогательное оборудование, посуда и реактивы
6.2.1 Для определения экзополигалактуроназной активности применяют средства измерений, аппаратуру, лабораторную посуду, материалы, реактивы, указанные в 4.2, со следующими дополнениями:
6.2.1.1 Натрий углекислый по ГОСТ 83.
6.2.1.2 Калий йодистый по ГОСТ 4232.
6.2.1.3 Калий двухромовокислый по ГОСТ 4220.
6.2.1.4 Натрий тиосульфат по ГОСТ 27068.
6.2.1.5 Крахмал растворимый по ГОСТ 10163.
6.2.1.6 Йод по ГОСТ 4159.
6.2.1.7 Воронка Бюхнера по ГОСТ 9147.
6.2.1.8 Спирт этиловый ректификованный технический по ГОСТ 18300.
6.2.1.9 Кислота серная по ГОСТ 4204 (плотность 1,850 г/см
).
6.2.1.10 Бязь по ГОСТ 29298.
6.2.1.11 Марля медицинская по ГОСТ 9412.
6.2.2 Все реактивы должны относиться к подгруппе чистоты 2 (х.ч.) или 3 (ч.д.а.).
6.2.3 Допускается применение средств измерений, вспомогательного оборудования с аналогичными метрологическими и техническими характеристиками, а также реактивов по качеству не хуже вышеуказанных.
6.3 Подготовка к анализу
6.3.1 Приготовление пектовой кислоты проводят по 5.3.2.
6.3.2 Приготовление раствора пектовой кислоты с массовой долей 1,0% (субстрат) проводят по 5.3.3.
6.3.3 Приготовление раствора углекислого натрия молярной концентрации ![]() 1 моль/дм
1 моль/дм
106,0 г углекислого натрия растворяют в стаканчике в небольшом количестве дистиллированной воды.
Растворенную соль переносят количественно в мерную колбу вместимостью 1000 см и объем доводят до метки дистиллированной водой при температуре 20 °С.
Срок хранения раствора углекислого натрия при температуре 20 °С - не более 10 дней.
6.3.4 Приготовление раствора серной кислоты молярной концентрации ![]() 2 моль/дм
2 моль/дм
В мерную колбу вместимостью 1 дм вносят 108,6 см
концентрированной серной кислоты, приливают около 300 см
дистиллированной воды, доводят до метки дистиллированной водой при температуре 20 °С и перемешивают.
Срок хранения раствора серной кислоты при температуре 20 °С - не более 1 мес.
6.3.5 Приготовление раствора крахмала с массовой долей 1,0%
1,00 г крахмала в пересчете на абсолютно сухое вещество (см. 4.2.4) помещают в мерную колбу вместимостью 100 см, добавляют 25 см
дистиллированной воды и перемешивают. Затем добавляют в колбу еще 25 см
дистиллированной воды, помещают колбу в кипящую водяную баню не менее чем на 15-20 мин, непрерывно перемешивая содержимое до полного растворения крахмала, объем жидкости доводят до метки дистиллированной водой при температуре 20 °С и содержимое колбы перемешивают. Для полученного раствора крахмала характерна легкая опалесценция.
Раствор крахмала готовят в день проведения анализа.
6.3.6 Приготовление раствора йода молярной концентрацией 0,1 моль/дм
25,0 г йодистого калия растворяют в мерной колбе вместимостью 1 дм в 100 см
дистиллированной воды и туда же вносят 12,70 г йода. После полного растворения йода объем раствора доводят до метки дистиллированной водой. Титр не устанавливают, но проверяют по раствору гипосульфита. Молярная концентрация приготовленного раствора йода должна быть от 0,95 до 1,05 моль/дм
.
Срок хранения раствора в склянке из темного стекла с притертой пробкой при температуре 20 °С - не более 1 мес.
6.3.7 Приготовление раствора тиосульфата натрия молярной концентрацией ![]() 0,05 моль/дм
0,05 моль/дм
24,8 г тиосульфата натрия растворяют в мерной колбе вместимостью 1 дм в небольшом количестве дистиллированной воды. Содержимое колбы перемешивают и объем жидкости доводят до метки дистиллированной водой. Титр устанавливают по двухромовокислому калию после выдерживания раствора в течение 15 сут.
Срок хранения раствора в склянке из темного стекла с сифоном и бюреткой с хлоркальциевой трубкой, заполненной натронной известью при температуре 20 °С, - не более 10 дней.
6.4 Подготовка пробы
6.4.1 Отбор проб - по ГОСТ 20264.0.
Анализируемые пробы порошкообразных или жидких ферментных препаратов допускается использовать без предварительной подготовки.
6.5 Приготовление основного раствора анализируемой пробы ферментного препарата
В стаканчик для взвешивания шпателем помещают порошкообразный ферментный препарат для получения анализируемой пробы массой (0,1000±0,0002) г. Жидкий ферментный препарат (1,00±0,02) см вносят в стаканчик пипеткой. Полученную анализируемую пробу ферментного препарата суспендируют в небольшом количестве дистиллированной воды и количественно переносят в мерную колбу вместимостью 100 см
, доводят объем до метки дистиллированной водой при температуре 20 °С и тщательно перемешивают. Приготовленный раствор ферментного препарата является основным раствором анализируемой пробы.
Срок хранения основного раствора ферментного препарата при температуре 20 °С - не более 1 ч.
6.5.1 Приготовление рабочего раствора анализируемой пробы ферментного препарата
Рабочий раствор анализируемой пробы ферментного препарата готовят из основного раствора по 6.5 путем дальнейшего разведения его дистиллированной водой в зависимости от предполагаемой активности таким образом, чтобы при ее определении разность между контрольным и анализируемым раствором при титровании была в пределах от 1,5 до 2,5 см.
С учетом разведения рассчитывают количество препарата, взятого на анализ.
Каждую пробу анализируют два раза в условиях повторяемости в соответствии в требованиями ГОСТ Р ИСО 5725-1.
Раствор готовят в день определения. Длительность использования рабочего раствора ферментного препарата не должна превышать 1 ч с момента приготовления во избежание потерь его ферментативной активности.
6.6 Проведение анализа
6.6.1 В мерную колбу вместимость 100 см вносят 10 см
1,0%-ного раствора пектовой кислоты и помещают в термостат с температурой 30 °С. Через 10 мин приливают в колбу от 1 до 5 см
ферментного раствора в зависимости от ферментативной активности, тщательно перемешивают и отмечают время по секундомеру для проведения гидролиза.
6.6.2 Реакционную смесь инкубируют в термостате с такой продолжительностью, чтобы степень гидролиза пектовой кислоты находилась в пределах 20% и не более (см. формулу 12).
Продолжительность инкубации зависит от ферментативной активности исследуемого препарата и представлена в таблице 1.
Таблица 1
Активность препарата, ед./г или ед./см | Продолжительность инкубации, мин |
100 | 45 |
101-250 | 30 |
251-500 | 20 |
501-750 | 15 |
751-1250 | 10 |
1251-1500 | 7,5 |
По истечении времени инкубации в колбу добавляют 1,8 см раствора углекислого натрия молярной концентрацией 1,0 моль/дм и 10 см
раствора йода молярной концентрации 0,1 моль/дм
.
6.6.3 Растворы тщательно перемешивают, закрывают стеклянными пробками и оставляют в темном месте на 20 мин. Затем к реакционной смеси приливают 2,0 см раствора серной кислоты, молярной концентрации 2 моль/дм
, интенсивно перемешивают и оттитровывают избыток йода раствором тиосульфата натрия молярной концентрации 0,05 моль/дм
с индикатором - 1,0%-ным раствором крахмала.
6.6.4 В качестве контроля используют то же количество реактивов, только раствор ферментного препарата вводят после добавления 1,8 см раствора углекислого натрия, непосредственно перед внесением раствора йода молярной концентрации 0,1 моль/дм
.
6.6.5 При анализе ферментных растворов, величина активности которых неизвестна, берут 50 см1,0%-ного раствора пектовой кислоты (субстрат) и от 1,0 до 25,0 см
раствора фермента. Объем раствора фермента менее 25 см
восполняют дистиллированной водой. Общий объем смеси - 75 см
. Из реакционной смеси отбирают каждые 5-10 мин пробы по 15 см
в колбу, где предварительно налито 1,8 см
раствора углекислого натрия молярной концентрации 1 моль/дм
. Все остальные процедуры проводят как описано выше.
6.7 Обработка результатов
6.7.1 Для обеспечения точности анализа необходимо, чтобы объем раствора йода молярной концентрации 0,1 моль/дм, пошедший на окисление альдегидных групп, образовавшихся при гидролизе субстрата, не превышал 2,0 см
(предельное значение
).
Это предельное значение соответствует 20%-ному гидролизу пектовой кислоты, что видно из следующего расчета
![]() , (12)
, (12)
где 20 - степень гидролиза 1,0%-ного раствора пектовой кислоты, %;
- объем 1,0%-ного раствора пектовой кислоты, введенной в реакционную среду, см
;
100 - коэффициент перевода в проценты;
9,03 - объем 1,0%-ного раствора пектовой кислоты, соответствующий 1,0 см раствора тиосульфата натрия молярной концентрации 0,05 моль/дм
(в 10 см
раствора субстрата находится 100 мг пектовой кислоты), см
.
6.7.2 Экзополигалактуроназную активность (Экзо-ПгС) в анализируемой пробе, ед. Экзо-ПгС/г (для порошкообразного препарата) или ед. Экзо-ПгС/см (для жидкого препарата) вычисляют по формулам
- для порошкообразного препарата в ед. Экзо-ПгС/г
![]() , (13)
, (13)
- для жидкого препарата в ед. Экзо-ПгС/см
![]() , (14)
, (14)
где 51,3 - число микроэквивалентов альдегидных групп, соответствующих 1 см 0,1 н раствора йода (или тиосульфата натрия);
,
- объем 0,05 н раствора тиосульфата натрия, пошедший на титрование контрольного (
) и опытного (
) растворов, см
;
2 - коэффициент пересчета 0,05 н раствора тиосульфата натрия в 0,1 н раствор;
- длительность гидролиза 1,0%-ного раствора пектовой кислоты, мин;
- объем ферментного препарата, введенного в реакционную среду, см
;
- плотность для жидких концентрированных ферментных препаратов по ГОСТ 18481, г/см
.
При значении экзополигалактуроназной активности выше 100 ед. Экзо-ПгС/г(см), допускается разведение анализируемой пробы дистиллированной водой при температуре 20 °С до значений, находящихся в пределах допустимых значений при титровании.
6.8 Оформление результатов определений
6.8.1 За окончательный результат определения принимают среднеарифметическое результатов двух параллельных определений, выполненных в условиях повторяемости, если выполняется условие приемлемости (15).
Результат анализа при доверительной вероятности 0,95 представляют в виде
![]() ,
,
где - среднеарифметическое значение результатов двух параллельных определений, признанных приемлемыми, ед. Экзо-ПгС/г (для порошкообразного препарата) или ед. Экзо-ПгС/см
(для жидкого препарата);
- значение границ абсолютной погрешности результата определений (расширенная неопределенность
с коэффициентом охвата
2), ед. Экзо-ПгС/г (для порошкообразного препарата) или ед. Экзо-ПгС/см
(для жидкого препарата), вычисляемое по формуле
![]() , (15)
, (15)
где - границы относительной погрешности результата анализа экзополигалактуроназной активности в анализируемой пробе при
0,95 составляют ±7%.
Результаты анализа выражают с точностью до первого десятичного знака ед. Экзо-ПгС/г (для порошкообразного препарата) или ед. Экзо-ПгС/см (для жидкого препарата).
6.9 Сходимость и воспроизводимость результатов
6.9.1 Результаты определений, полученные в условиях повторяемости (сходимости), признаются удовлетворительными, если выполняется условие приемлемости
![]() , (16)
, (16)
где и
- результаты двух параллельных определений, полученные в условиях повторяемости при
0,95, ед. Экзо-ПгС/г (для порошкообразного препарата) или ед. Экзо-ПгС/см
(для жидкого препарата);
- среднеарифметическое значение результатов двух параллельных определений, ед. Экзо-ПгС/г (для порошкообразного препарата) или ед. Экзо-ПгС/см
(для жидкого препарата);
- предел повторяемости (сходимости), равный 8%.
6.9.2 Результаты определений, полученные в условиях воспроизводимости по ГОСТ Р ИСО 5725-1, признаются удовлетворительными, если выполняется условие приемлемости
![]() , (17)
, (17)
где и
- окончательные результаты определений, полученные в двух лабораториях в точном соответствии с методом, в условиях повторяемости, ед. Экзо-ПгС/г (для порошкообразного препарата) или ед. Экзо-ПгС/см
(для жидкого препарата);
- среднеарифметическое значение двух окончательных результатов определений, полученных в условиях воспроизводимости, ед. Экзо-ПгС/г (для порошкообразного препарата) или ед. Экзо-ПгС/см
(для жидкого препарата);
![]() - критическая разность, равная 10% при доверительной вероятности
- критическая разность, равная 10% при доверительной вероятности 0,95.
7 Метод определения пектинэстеразной активности ферментных препаратов (ПэС)
7.1 Сущность метода
7.1.1 Метод основан на гидролизе высокометоксилированного пектина анализируемым ферментным препаратом с последующим определением освободившихся в результате гидролиза карбоксильных групп.
7.1.2 Пектинэстеразная активность (ПэС) характеризует способность ферментного препарата катализировать гидролиз сложноэфирных связей в молекуле высокометоксилированного пектина с образованием карбоновых кислот и метилового спирта.
7.1.3 За единицу пектинэстеразной активности принято такое количество фермента, которое способно катализировать гидролиз 1,0 мкмоль сложноэфирных связей в молекуле пектина за 1 мин при температуре 30 °С и значении кислотности 4,0 ед. рН.
Пектинэстеразная активность выражается в ед. ПэС/г (для порошко-образного) или ед. ПэС/см (для жидкого) анализируемого ферментного препарата.
Сравнимые результаты при работе с различными субстратами можно получить только при пересчете полученных данных на субстрат со 100%-ной степенью метоксилирования.
7.2 Средства измерений, вспомогательное оборудование, посуда и реактивы
7.2.1 Для определения пектинэстеразной активности применяют средства измерений, аппаратуру, лабораторную посуду, материалы, реактивы, указанные в 4.2, со следующими дополнениями:
7.2.1.1 Микробюретка вместимостью 1,0 см по ГОСТ 29251.
7.2.1.2 Пектин свекловичный со степенью метоксилирования (этерификации) не менее 80% и массовой долей основного вещества не менее 70% по ГОСТ 29186.
7.2.1.3 Кислота щавелевая по ГОСТ 22180.
7.2.1.4 Фенолфталеин по ГОСТ 5850.
7.2.1.5 Воронка Бюхнера по ГОСТ 9147.
7.2.1.6 Марля медицинская по ГОСТ 9412.
7.2.1.7 Стекло часовое диаметром 80 мм.
7.2.1.8 Натрия гидроокись по ГОСТ 4328.
7.2.2 Все реактивы должны относиться к подгруппе чистоты 2 (х.ч.) или 3 (ч.д.а.).
7.2.3 Допускается применение средств измерений, вспомогательного оборудования с аналогичными метрологическими и техническими характеристиками, а также реактивов по качеству не хуже вышеуказанных.
7.3 Подготовка к анализу
7.3.1 Приготовление раствора пектина массовой долей 1,0% (субстрат)
Пектин, взятый с расчетом, чтобы 100 см раствора содержало 1,00 г чистого пектина (в соответствии с приложением А), всыпают тонкой струей при непрерывном перемешивании в стаканчик вместимостью 100 см
, куда предварительно наливают 70 см
дистиллированной воды и оставляют на 2 ч при температуре 20 °С для набухания и растворения, после чего помещают на ночь в холодильник.
На следующий день раствор нагревают до температуры 20 °С, количественно переносят в мерную колбу вместимостью 100 см, доводят до метки дистиллированной водой, тщательно перемешивают и фильтруют на воронке Бюхнера через два слоя марли с ватой.
Срок хранения раствора пектина в холодильнике при температуре 4 °С - не более двух суток.
7.3.2 Приготовление раствора гидроокиси натрия молярной концентрации ![]() 0,1 моль/дм
0,1 моль/дм
4,0 г гидроокиси натрия растворяют в стаканчике в небольшом количестве дистиллированной воды.
Раствор после растворения переносят количественно в мерную колбу вместимостью 1 дм и объем доводят до метки дистиллированной водой при температуре 20 °С.
Срок хранения раствора гидроокиси натрия при температуре 20 °С - не более 10 дней.
7.3.3 Приготовление основного раствора анализируемой пробы ферментного препарата
В стаканчик для взвешивания шпателем помещают порошкообразный ферментный препарат для получения анализируемой пробы массой (0,1000±0,0002) г. Жидкий ферментный препарат (1,00±0,02) см вносят в стаканчик пипеткой. Полученную анализируемую пробу ферментного препарата суспендируют в небольшом количестве дистиллированной воды и количественно переносят в мерную колбу вместимостью 100 см
, доводят объем до метки дистиллированной водой при температуре 20 °С и тщательно перемешивают. Приготовленный раствор ферментного препарата является основным раствором анализируемой пробы.
Срок хранения основного раствора ферментного препарата при температуре 20 °С - не более 1 ч.
7.3.4 Приготовление рабочего раствора анализируемой пробы ферментного препарата
Рабочий раствор анализируемого ферментного препарата готовят из основного раствора по 7.3.3 путем дальнейшего разведения его дистиллированной водой в зависимости от предполагаемой активности таким образом, чтобы при ее определении разность между контрольной пробой и анализируемой пробой при титровании была в пределах от 0,5 до 1,5 см.
С учетом разведения рассчитывают количество препарата взятого на анализ.
Каждую пробу анализируют два раза в условиях повторяемости в соответствии в требованиями ГОСТ Р ИСО 5725-1.
Раствор готовят в день определения. Длительность использования рабочего раствора ферментного препарата не должна превышать 1 ч с момента приготовления во избежание потерь его ферментативной активности.
7.3.5 Приготовление инактивированного раствора анализируемой пробы ферментного препарата
Для приготовления инактивированного ферментного раствора 25 см основного ферментного раствора помещают в мерную колбу вместимостью 50 см
, закрывают пробкой с воздушным холодильником и кипятят на водяной бане в течение 1 ч.
7.4 Проведение анализа
В четыре стакана вместимостью 50 см помещают по 20 см
1,0%-ного раствора пектина, накрывают часовым стеклом и ставят в термостат при температуре 30 °С с промежутками в 15 мин. Далее в два стакана прибавляют по 10 см
ферментного раствора, а в другие два - по 10 см
инактивированного ферментного раствора и выдерживают 1 ч для проведения гидролиза пектина. Общий объем реакционной смеси должен быть всегда 30 см
. Если для анализа берут меньше 10 см
ферментного раствора, то недостающий объем дополняют дистиллированной водой, которую вводят непосредственно перед добавлением фермента.
Через 1 ч пробу вынимают из термостата и сразу титруют, используя микробюретку, раствором гидроокиси натрия молярной концентрации 0,1 моль/дм до рН 7,5, используя для этой цели рН-метр. Сначала титруют контрольный раствор, а затем - анализируемый. Разность между контрольной пробой и анализируемой пробой при титровании должна быть в пределах от 0,5 до 1,5 см
.
7.5 Обработка результатов
7.5.1 Пектинэстеразную активность (ПэС) в анализируемой пробе, ед. ПэС/г (для порошкообразного препарата) или ед. ПэС/см (для жидкого препарата), вычисляют по формулам
- для порошкообразного препарата в ед. ПэС/г
![]() , (18)
, (18)
- для жидкого препарата в ед.ПэС/см
![]() , (19)
, (19)
где 100 - число микроэквивалентов прогидролизованных сложноэфирных связей, соответствующее 1 см раствора гидроокиси натрия молярной концентрации 0,1 моль/дм
;
- объем раствора гидроокиси натрия молярной концентрации 0,1 моль/дм
, необходимое для титрования освободившихся в результате гидролиза карбоксильных групп (находят по разности между количеством раствора гидроокиси натрия, израсходованным на титрование анализируемой пробы и контрольной пробы) см
;
100 - степень этерификации пектина, на который ведется расчет, %; (см. 7.1.3);
- время гидролиза, мин;
- количество ферментного препарата, взятое для анализа, г;
- степень этерификации пектина, используемого в качестве субстрата, %, по ГОСТ 29186;
- плотность для жидких концентрированных ферментных препаратов по ГОСТ 18148*, г/см
.
________________
* Вероятно, ошибка оригинала. Следует читать: ГОСТ 18481-81. - .
При значении пектинэстеразной активности выше 100 ед. ПэС/г(см), допускается разведение дистиллированной водой при температуре 20 °С до значений, находящихся в пределах допустимых значений при титровании.
7.5.2 Оформление результатов определений
За окончательный результат определения принимают среднеарифметическое результатов двух параллельных определений, выполненных в условиях повторяемости, если выполняется условие приемлемости (19).
Результат анализа при доверительной вероятности 0,95 представляют в виде
![]() ,
,
где - среднеарифметическое значение результатов двух параллельных определений, признанных приемлемыми (см. 5.7.1), ед. ПэС/г (для порошкообразного препарата) или ед. ПэС/см
(для жидкого препарата);
- значение границ абсолютной погрешности измерений (расширенная неопределенность
с коэффициентом охвата
2), ед. ПэС/г (для порошкообразного препарата) или ед. ПэС/см
(для жидкого препарата), вычисляемое по формуле
![]() , (20)
, (20)
где - границы относительной погрешности результата анализа пектинэстеразной активности в анализируемой пробе при
0,95 составляют ±7%.
Результаты анализа выражают с точностью до первого десятичного знака ед. Экзо-ПгС/г (для порошкообразного препарата) или ед. Экзо-ПгС/см (для жидкого препарата).
7.6 Сходимость и воспроизводимость результатов
7.6.1 Результаты определений, полученные в условиях повторяемости (сходимости), признаются удовлетворительными, если выполняется условие приемлемости
![]() , (21)
, (21)
где и
- результаты двух параллельных определений, полученные в условиях повторяемости при
0,95, ед. ПэС/г (для порошкообразного препарата) или ед. ПэС/см
(для жидкого препарата);
- среднеарифметическое значение результатов двух параллельных определений, ед. ПэС/г (для порошкообразного препарата) или ед. ПэС/см
(для жидкого препарата);
- предел повторяемости (сходимости), равный 5%.
7.6.2 Результаты определений, полученные в условиях воспроизводимости по ГОСТ Р ИСО 5725-1, признаются удовлетворительными, если выполняется условие приемлемости
![]() , (22)
, (22)
где и
- окончательные результаты определений, полученные в двух лабораториях в точном соответствии с методикой, ед. ПэС/г (для порошкообразного препарата) или ед. ПэС/см
(для жидкого препарата);
- среднеарифметическое значение двух окончательных результатов определений, полученных в условиях воспроизводимости, ед. ПэС/г (для порошкообразного препарата) или ед. ПэС/см
(для жидкого препарата);
![]() - критическая разность, равная 10% при доверительной вероятности
- критическая разность, равная 10% при доверительной вероятности 0,95.
8 Требования к условиям измерений
При выполнении измерений в лаборатории должны соблюдаться следующие условия:
температура окружающего воздуха | (20±1) °С; |
относительная влажность воздуха | (60±20)%; |
атмосферное давление | 84,0-106,7 кПа; |
напряжение в сети | (220±10) В. |
9 Требования безопасности
9.1 Условия безопасности проведения работ
При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007 и ГОСТ 12.4.103.
Помещение, где проводят работы с реактивами, должно быть оснащено приточно-вытяжной вентиляцией по ГОСТ 12.4.021.
Электробезопасность при работе с электроустановками - по ГОСТ 12.2.007.0 и по ГОСТ Р 12.1.019.
Организация обучения работающих безопасности труда - по ГОСТ 12.0.004.
Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
Содержание вредных веществ в воздухе рабочей зоны не должно превышать норм, установленных ГОСТ 12.1.005.
9.2 Требования к квалификации операторов
К проведению анализов допускаются лица, имеющие квалификацию не ниже среднего технического образования, владеющие навыками работы в лаборатории, проведения анализов и изучившие инструкции по эксплуатации используемой аппаратуры.
Приложение А
(обязательное)
Метод определения чистого пектина (кальцийпектатный метод)
А.1 Характеристика метода
Метод основан на получении соли пектата кальция в виде осадка.
А.2 Средства измерений, вспомогательное оборудование, посуда и реактивы
А.2.1 Для определения чистого пектина используют аппаратуру, лабораторную посуду, материалы, реактивы, указанные в 4.2 настоящего стандарта, со следующими дополнениями:
- пектин свекловичный со степенью метоксилирования не менее 30% и содержанием основного вещества не менее 70% по ГОСТ 29186;
- натрия гидроокись по ГОСТ 4328;
- шкаф сушильный электрический;
- эксикатор по ГОСТ 25336;
- кальций хлористый по ГОСТ 4161;
- серебро азотнокислое по ГОСТ 1277.
А.2.2 Все реактивы должны относиться к подгруппе чистоты 2 (х.ч.) или 3 (ч.д.а.).
А.3 Подготовка к анализу
А.3.1 Отбор проб - по ГОСТ 20264.0.
А.З.2 Приготовление раствора хлористого кальция молярной концентрации ![]() 2,0 моль/дм
2,0 моль/дм
222,0 г хлористого кальция растворяют в стаканчике в небольшом количестве дистиллированной воды. Раствор переносят количественно в мерную колбу вместимостью 1 дм и объем доводят до метки дистиллированной водой при температуре 20 °С.
Срок хранения раствора хлористого кальция при температуре 20 °С - не более 10 дней.
А.3.3 Приготовление раствора уксусной кислоты молярной концентрации ![]() 1,0 моль/дм
1,0 моль/дм
В мерную колбу вместимостью 1 дм вносят 57,2 см
ледяной уксусной кислоты, приливают около 300 см
дистиллированной воды, доводят до метки дистиллированной водой при температуре 20 °С и перемешивают.
Срок хранения раствора уксусной кислоты в закрытой стеклянной посуде при температуре 4 °С - не более 1 мес.
А.3.4 Приготовление раствора азотнокислого серебра массовой долей 1,0%
1,0 г азотнокислого серебра растворяют в стаканчике в небольшом количестве дистиллированной воды. Растворенную соль переносят количественно в мерную колбу вместимостью 100 см и объем доводят до метки дистиллированной водой при температуре 20 °С.
Срок хранения раствора азотнокислого серебра при температуре 20 °С - не более 10 дней.
А.3.5 Приготовление раствора гидроокиси натрия молярной концентрации 0,1 моль/дм проводят по 7.3.2.
А.3.6 Проведение анализа
0,15 г анализируемого свекловичного пектина, взвешенного на аналитических весах с погрешностью не более 0,002 г, растворяют в небольшом количестве дистиллированной воды при температуре 20 °С, при постоянном перемешивании на магнитной мешалке в течение 15-20 мин. Затем количественно переносят в мерную колбу вместимостью 100 см, доводят дистиллированной водой до метки и оставляют на 20 мин для получения однородного раствора.
Далее отбирают 20 см раствора пектина в колбу вместимостью 500 см
, приливают 100 см
раствора гидроокиси натрия молярной концентрации 0,1 моль/дм
и оставляют на ночь для полного омыления пектина. На следующий день в колбу приливают 50 см
раствора уксусной кислоты молярной концентрации 1,0 моль/см
, а через 5 мин добавляют 50 см
раствора хлористого кальция молярной концентрации 2,0 моль/дм
и оставляют еще на 1 ч.
После этого раствор кипятят 5 мин на водяной бане и фильтруют через обеззоленный фильтр, высушенный до постоянной массы (в эксикаторе). Осадок пектата кальция промывают горячей дистиллированной водой (температура 80 °С - 90 °С) до исчезновения ионов хлора (реакция с 1,0%-ным раствором азотнокислого серебра по ГОСТ 15615).
После промывки осадок с фильтра помещают в бюксу и высушивают до постоянной массы при температуре 105 °С в сушильном шкафу.
А.3.7 Обработка результатов
Количество пектина , г, взятое на омыление, вычисляют по формуле
![]() , (23)
, (23)
где - масса пектина, взятая для приготовления раствора, г;
- объем пектина, взятый на омыление, см
;
- объем исходного раствора пектина, см
.
По разности масс между фильтром и осадком с фильтром без осадка находят содержание пектата кальция ().
Массовую долю пектина , %, вычисляют по формуле
![]() , (24)
, (24)
где - масса осадка пектата кальция, г;
0,92 - постоянный коэффициент, учитывающий содержание кальция в осадке;
100 - переводной коэффициент в проценты;
- количество пектина, взятое на омыление, г.
А.3.8 Оформление результатов определений
За окончательный результат определения принимают среднеарифметическое результатов двух параллельных определений, выполненных в условиях повторяемости, если выполняется условие приемлемости (22).
Результат анализа при доверительной вероятности 0,95 представляют в виде
![]() ,
,
где - среднеарифметическое значение результатов двух параллельных определений, признанных приемлемыми;
- значение границ абсолютной погрешности измерений для двух определений;
![]() , (25)
, (25)
где - границы относительной погрешности результата анализа определения пектина в анализируемой пробе при
0,95 составляют ±7%.
А.3.9 Сходимость и воспроизводимость результатов
А.3.9.1 Результаты определений, полученные в условиях повторяемости (сходимости), признаются удовлетворительными, если выполняется условие приемлемости
![]() , (26)
, (26)
где и
- результаты двух параллельных определений, полученные в условиях повторяемости при
0,95,
- среднеарифметическое значение результатов двух параллельных определений;
- предел повторяемости (сходимости), равный 5%.
А.3.9.2 Результаты определений, полученные в условиях воспроизводимости по ГОСТ Р ИСО 5725-1, признаются удовлетворительными, если выполняется условие приемлемости
![]() , (27)
, (27)
где и
- окончательные результаты определений, полученные в двух лабораториях в точном соответствии с методикой;
- среднеарифметическое значение двух окончательных результатов определений, полученных в условиях воспроизводимости;
![]() - критическая разность, равная 10% при доверительной вероятности
- критическая разность, равная 10% при доверительной вероятности 0,95.
Библиография
[1] | Enzyme Nomenclature, recommendations of the nomenclature Committee of the IUB* // N.Y., Academic Press - 1984 |
________________ * Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - . | |
[2] | Полыгалина Г.В., Чередниченко B.C., Римарева Л.В. Определение активности ферментов: справочник. - М.: ДеЛи принт, 2003 |
__________________________________________________________________________
УДК 577.15:543.06:006.354 ОКС 07.100.30 ОКСТУ 9291
Ключевые слова: препараты ферментные, активность пектиназы, эндополигалактуроназы, экзополигалактуроназы, пектинэстеразы, методы определения с использованием субстрата пектина различной степени метоксилирования и пектовой кислоты, гидролиза их при 30 °С
__________________________________________________________________________
Электронный текст документа
и сверен по:
, 2014

