ГОСТ 30087-93
Группа С19
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ДРОЖЖИ КОРМОВЫЕ - ПАПРИН
Методы определения 3,4-бензпирена
Fodder yeast - paprine. Methods for determination of 3,4-benzopyrene
МКС 07.100.30
65.120
ОКСТУ 9209
Дата введения 1997-01-01
Предисловие
1 РАЗРАБОТАН МТК 326, институтом питания Российской АМН, ВНИИканцерогенеза ВОНЦ Российской АМН
ВНЕСЕН Госстандартом Российской Федерации
2 ПРИНЯТ Межгосударственным Советом по стандартизации, метрологии и сертификации 15.04.94 (отчет Технического секретариата N 2)
За принятие проголосовали:
Наименование государства | Наименование национального органа по стандартизации |
Республика Армения | Армгосстандарт |
Республика Беларусь | Госстандарт Беларуси |
Республика Казахстан | Госстандарт Республики Казахстан |
Киргизская Республика | Киргизстандарт |
Республика Молдова | Молдовастандарт |
Российская Федерация | Госстандарт России |
Туркменистан | Главная государственная инспекция Туркменистана |
Украина | Госстандарт Украины |
3 Постановлением Комитета Российской Федерации по стандартизации, метрологии и сертификации 29 февраля 1996 г. N 147 межгосударственный стандарт ГОСТ 30087-93 введен в действие непосредственно в качестве государственного стандарта Российской Федерации с 1 января 1997 г.
4 ВВЕДЕН ВПЕРВЫЕ
5 ПЕРЕИЗДАНИЕ
ИНФОРМАЦИОННЫЕ ДАННЫЕ
ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Обозначение НТД, на который дана ссылка | Номер пункта, раздела |
ГОСТ 1770-74 | 2.1 |
ГОСТ 2603-79 | 3.1 |
ГОСТ 4204-77 | 3.1 |
ГОСТ 5789-78 | 3.1 |
ГОСТ 5815-77 | 3.1 |
ГОСТ 5955-75 | 3.1 |
ГОСТ 5962-67 | 2.1; 3.1 |
ГОСТ 9147-80 | 3.1 |
ГОСТ 9293-74 | 2.1 |
ГОСТ 12026-76 | 3.1 |
ГОСТ 17299-78 | 2.1; 3.1 |
ГОСТ 18300-87 | 2.1; 3.1 |
ГОСТ 20015-88 | 2.1 |
ГОСТ 20289-74 | 3.1 |
ГОСТ 24104-88 | 2.1; 3.1 |
ГОСТ 24363-80 | 2.1; 3.1 |
ГОСТ 25336-82 | 2.1; 3.1 |
ГОСТ 28178-89 | 1 |
ГОСТ 29228-91 | 2.1; 3; 1 |
ГОСТ 29229-91 | 2.1; 3.1 |
Настоящий стандарт распространяется на кормовые дрожжи-паприн и устанавливает методы определения в них 3,4-бензпирена.
1 Методы отбора проб
Отбор проб - по ГОСТ 28178.
2 Метод низкотемпературной спектрофлуориметрии
(метод Шпольского)
Сущность метода заключается в экстракции углеводородов, в том числе 3,4-бензпирена, гексаном из продукта, предварительно обработанного спиртовым раствором едкого калия, выделении фракции полициклических ароматических углеводородов тонкослойной хроматографией на окиси алюминия и количественном определении в полученной фракции 3,4-бензпирена низкотемпературной спектрофлуориметрией (метод Шпольского).
2.1 Аппаратура и реактивы
Спектрофотометр флуоресцентный с криогенной приставкой для измерений при температуре жидкого азота (-196) °С (типов Хитачи-850, MPF-43A, MPF-44B или других типов).
Хроматоскоп или облучатель ультрафиолетовый типа ОЛД.
Шкаф сушильный лабораторный типа СНОЛ, обеспечивающий температуру 250-300 °С.
Весы лабораторные 2-го класса точности с наибольшим пределом взвешивания - 200 г по ГОСТ 24104*.
_____________________
* С 1 июля 2002 г. вводится в действие ГОСТ 24104-2001 (здесь и далее).
Весы лабораторные технические любого типа.
Испаритель ротационный типа ИР-IМ.
Баня водяная.
Сосуд Дьюара для жидкого азота любой вместимости.
Ванны для хроматографирования (фотокюветы эмалированные).
Пластины стеклянные размером 15х30 и 15х40 см.
Экстрактор (рисунок 1).
Экстрактор
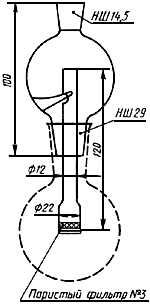
Рисунок 1
Насадка Дина и Старка по нормативному документу.
Колбы К-1-250-29/32 ТХС, К-1-500-29/32 ТХС или П-1-500-29/32 ТХС по ГОСТ 25336.
Холодильник ХПТ-2-400-29/32 ХС и ХШ-1-300-29/32 или ХШ1-1-400-29/32 ХС по ГОСТ 25336.
Холодильник ХПТ-1-300-14/23 ХС или ХПТ-1-400-14/23 ХС по ГОСТ 25336.
Дефлегматор 250-19/26-29/32 ТС или дефлегматор 300-19/26-29/32 ТС по ГОСТ 25336.
Пробирки стеклянные П2-10-180 ХС по ГОСТ 25336.
Алонж АИО-14/23-50 ТС по ГОСТ 25336.
Насадка Н-1-19/26-14/23-14/23 ТС или Н2-19/26-14/23 по ГОСТ 25336.
Пипетки вместимостью 1, 2, 5, 10 см по ГОСТ 29228 и ГОСТ 29229.
Пробирки мерные П-2-15-14/23 ХС по ГОСТ 1770.
Электроплитка бытовая с закрытой спиралью.
Воронка делительная ВД-1-500 или ВД-3-500 по ГОСТ 25336.
Цилиндры мерные 1-100, 1-250 или 3-100, 3-250 по ГОСТ 25336.
Стаканчики для взвешивания (бюксы) СВ-14/8 или СВ-19/9, или СВ-24/10, или СВ-34/12 по ГОСТ 25336.
Колбы мерные 2-100-2 по ГОСТ 25336.
Капилляры стеклянные.
-октан, ч.
Гексан, ч.
Спирт этиловый ректификованный технический по ГОСТ 18300 или спирт этиловый технический по ГОСТ 17299, или спирт этиловый ректификованный по ГОСТ 5962*.
_____________________
* В Российской Федерации действует ГОСТ Р 51652-2000 (здесь и далее).
Эфир петролейный (фракция 40-70 °С).
Хлороформ по ГОСТ 20015, х.ч.
Алюминия окись для хроматографии 2-й степени активности.
Калия гидроокись по ГОСТ 24363.
Вода дистиллированная.
3,4-бензпирен.
1,12-бензперилен.
Азот жидкий по ГОСТ 9293.
2.2 Подготовка к испытанию
2.2.1 Очистка растворителей
Растворители (-октан, этиловый спирт, петролейный эфир, хлороформ и гексан) перегоняют общепринятым способом с елочным дефлегматором.
2.2.2 Подготовка окиси алюминия
Окись алюминия высушивают в сушильном шкафу при температуре 250 °С в течение 4 ч и хранят в сосуде с пришлифованной пробкой.
2.2.3 Приготовление раствора 3,4-бензпирена для хроматографии в тонком слое концентрации 100 мкг/см (раствор-свидетель)
Раствор 3,4-бензпирена готовят в петролейном эфире. Для этого в бюксу отвешивают около 10 мг 3,4-бензпирена, приливают несколько миллилитров петролейного эфира до полного растворения взятой навески. Полученный раствор количественно переносят в мерную колбу вместимостью 100 см и доводят объем раствора до метки петролейным эфиром.
2.2.4 Приготовление стандартного раствора 3,4-бензпирена для спектрофлуориметрического определения его по методу Шпольского
Стандартный раствор 3,4-бензпирена готовят в -октане с исходной концентрацией 100 мкг/см
. Для этого в бюксу отвешивают 10 мг 3,4-бензпирена, приливают несколько миллилитров
-октана до полного растворения взятой навески. Полученный раствор количественно переносят в мерную колбу вместимостью 100 см
и доводят до метки
-октаном.
2.2.5 Приготовление рабочих растворов 3,4-бензпирена для спектрофлуориметрического определения его по методу Шпольского
Рабочие растворы 3,4-бензпирена концентрации 0,1; 0,04 и 0,02 мкг/см в
-октане готовят последовательным разведением исходного стандартного раствора 3,4-бензпирена в мерных колбах вместимостью 100 см
.
2.2.6 Приготовление внутреннего стандарта для спектрофлуориметрического определения содержания 3,4-бензпирена
В качестве внутреннего стандарта используют раствор 1,12-бензперилена в -октане рабочей концентрации 0,01-0,001 мкг/см
, который готовят путем последовательных разведений исходного стандартного раствора 1,12-бензперилена концентрации 100 мкг/см
. Для приготовления исходного раствора 1,12-бензперилена в бюксу отвешивают 10 мг 1,12-бензперилена, приливают несколько миллилитров
-октана до полного растворения взятой навески. Полученный раствор количественно переносят в мерную колбу вместимостью 100 см
и доводят до метки
-октаном.
2.3 Проведение испытания
В две круглодонные колбы вместимостью 500 см помещают по 25 г продукта, добавляют в каждую 20 см
дистиллированной воды, 200 см
этилового спирта и 20 г гидроокиси калия. Содержимое колб перемешивают встряхиванием. Колбы соединяют с обратным холодильником и нагревают на водяной бане при кипении реакционной смеси в течение 3 ч. Затем в колбы через холодильник добавляют по 150 см
дистиллированной воды, колбы с бани снимают и охлаждают до комнатной температуры.
После охлаждения жидкую фазу реакционной смеси декантацией переносят в делительную воронку, оставляя остаток продукта в колбе. В колбу с остатком добавляют 150 см гексана, содержимое колбы энергично перемешивают и гексан декантируют в делительную воронку.
Воронку закрывают пробкой и энергично встряхивают, затем закрепляют в штативе и оставляют для расслаивания жидкостей. Для разделения образовавшейся устойчивой эмульсии к смеси в делительной воронке добавляют 20 см этилового спирта. После расслаивания нижнюю вводно-спиртовую фазу сливают обратно в колбу с осадком, в гексановый экстракт переливают в колбу вместимостью 500 см
.
Такую обработку реакционной смеси повторяют еще два раза, используя для экстракции гексан по 100 см и этиловый спирт для расслаивания эмульсии, порциями по 20 см
.
По окончании экстракции остаток в колбе и гидролизат отбрасывают, а экстракт из двух параллельных проб объединяют, промывают в делительной воронке дистиллированной водой три раза по 50 см и упаривают порциями в предварительно взвешенной с точностью до второго знака после запятой круглодонной колбе вместимостью 250 см
на ротационном испарителе при остаточном давлении не ниже 50 мм рт.ст. и температуре водяной бани не более 60 °С. Колбу с экстрактом оставляют в вытяжном шкафу для удаления следов растворителя, после чего взвешивают с точностью до второго знака после запятой.
От взвешенного экстракта отбирают 1/5 часть в бюксу, не взвешивая. Колбу с остатком экстракта взвешивают с указанной выше точностью. В бюксу с частью экстракта добавляют 0,1-0,2 см раствора-свидетеля 3,4-бензпирена, приготовленного, как указано в п.2.2.3. Содержимое бюксы растворяют в петролейном эфире. Полученный раствор служит "свидетелем" при проведении тонкослойной хроматографии. Остаток в колбе также растворяют в небольшом объеме петролейного эфира. Полученный раствор является рабочей (анализируемой) пробой.
Для хроматографического разделения экстракта на стеклянную пластину размером 20х40 см равномерно насыпают окись алюминия. Затем с помощью стеклянной палочки, разделенной на три части (14, 1 и 3 см) резиновыми колечками толщиной 1 мм и шириной 3 мм, тщательно разравнивают окись алюминия.
Полученные растворы количественно наносят на подготовленную пластину стеклянными капиллярами на узкую часть - раствор из бюксы (свидетель), на широкую часть - раствор из колбы (рабочая проба). Растворы наносят равномерно сплошной полосой, отступив от нижнего края пластины 7-8 см.
После нанесения пробы и "свидетеля" пластину помещают в ванну под углом 10-15°, наливают петролейный эфир так, чтобы он не доходил до линии нанесения пробы. Ванну накрывают стеклом и проводят хроматографию, доводя фронт растворителя почти до верхнего края пластины.
Не высушивая пластину, облучают ее ультрафиолетовым светом и по светящейся полосе "свидетеля" определяют место нахождения 3,4-бензпирена в исследуемой пробе. Отмечают границы полосы 3,4-бензпирена на хроматограмме исследуемой пробы. Пластину высушивают в вытяжном шкафу.
При анализе некоторых образцов не происходит полного и четкого разделения флуоресцирующих компонентов при первичном хроматографировании в петролейном эфире. В этом случае по "свидетелю" выделяют довольно широкую полосу окиси алюминия с перекрывающимися флуоресцирующими компонентами. Полное разделение достигается при повторном хроматографировании, как указано в п.2.3.1.
Отмеченную на хроматограмме исследуемой пробы полосу с помощью предметного стекла количественно переносят в экстрактор (см. рисунок 1). Экстрактор с пробой подвешивают на крючок специальной насадки, помещают в круглодонную колбу вместимостью 250 см с 10 см
этилового спирта. Закрепляют колбу на штативе над плиткой, соединяют с обратным холодильником и приступают к элюированию пробы. Нагрев колбы регулируют так, чтобы слой растворителя над окисью алюминия был 3-5 мм. Экстракцию проводят в течение 45 мин, начиная с момента слива растворителя из экстрактора. По окончании экстракции отключают нагрев и оставляют до полного слива растворителя из экстрактора.
Так как спектрофлуориметрический анализ по определению содержания 3,4-бензпирена проводят в -октане, необходимо далее перевести выделенный 3,4-бензпирен в
-октан. Для этого в колбу со спиртовым раствором 3,4-бензпирена, охлажденную до комнатной температуры, добавляют 15 см
-октана, соединяют ее с насадкой Дина и Старка, к которой присоединяют обратный холодильник и колбу нагревают. При этом из колбы отгоняют спирт и часть
-октана, 3,4-бензпирен остается в колбе, растворенным в
-октане. Окончание отгонки определяется тем, что положение границы между спиртом и
-октаном в приемнике остается неизменным (см. рисунок 2).
Схема установки для перевода 3,4-бензпирена в  -октан
-октан
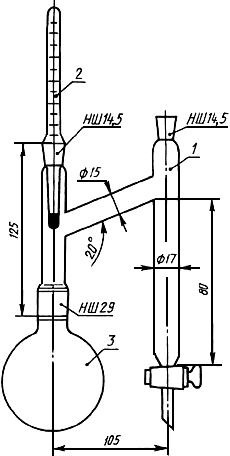
1 - приемник спирта; 2 - термометр со шкалой измерения до 200 °С;
3 - колба круглодонная вместимостью 250 см
Рисунок 2
2.3.1 Более тонкое хроматографическое разделение
При неполном и нечетком разделении анализируемой смеси при первичном хроматографировании в петролейном эфире выделенную по "свидетелю" широкую полосу окиси алюминия, содержащую фракцию 3,4-бензпирена, элюируют вышеуказанным способом, после чего проводят вторичное разделение полученного спиртового экстракта.
Для этого спиртовой экстракт наносят пипеткой на пластину с окисью алюминия размером 15х30 см с толщиной слоя окиси алюминия 0,3 мм.
Пластину помещают в ванну под углом 10-15° и проводят хроматографию в хлороформе, доводя фронт растворителя до верхнего края пластины.
Далее повторяют все операции, как указано выше.
В полученном по пп.2.3 или 2.3.1 экстракте 3,4-бензпирена в -октане проводят спектрофлуориметрическое определение содержания 3,4-бензпирена.
Объем экстракта не должен превышать 4 см при исходной навеске продукта 50 г.
Количественное определение содержания 3,4-бензпирена на спектрофлуориметре можно проводить методом добавок или методом внутреннего стандарта.
2.3.1.1 Количественное определение содержания 3,4-бензпирена методом добавок
В три пробирки наливают пипеткой по 1 см экстракта 3,4-бензпирена в
-октане, приготовленного, как указано в п.2.3 или 2.3.1. В первую пробирку приливают 2 см
-октана. Во вторую пробирку приливают 1,5 см
-октана и 0,5 см
раствора 3,4-бензпирена концентрации 0,1 мкг/см
, приготовленного, как указано в п.2.2.5. В третью пробирку приливают 1 см
-октана и 1 см
того же раствора 3,4-бензпирена, что и во вторую пробирку.
Спектрофлуориметрический анализ начинают с третьей пробирки. Для этого третью пробирку помещают в сосуд Дьюара перед входной щелью спектрофотометра: выводят прибор барабаном длин волн флуоресценции на аналитическую линию флуоресценции 3,4-бензпирена - 403 нм при длине волны возбуждающего света 367 нм. Регулировкой коэффициента усиления и раскрытием щели, а также одновременной юстировкой пробирки в сосуде Дьюара добиваются максимального сигнала по регистрирующему прибору спектрофотометра (до 50-80%), после чего записывают спектрограмму аналитической линии 3,4-бензпирена в области 401-404 нм. При этом обязательно фиксируют, при каком значении регистрирующего прибора спектрофотометра перо самописца находилось при значении длины волны 401 нм.
Это условие необходимо выполнять при сканировании всех проб для компенсации влияния фона, который создают присутствующие в экстракте пробы люминесцирующие примеси, содержащиеся в одинаковых количествах во всех трех пробирках.
Запись спектра повторяют 2-3 раза, добиваясь хорошей сходимости.
Затем последовательно замораживают в жидком азоте вторую и первую пробирки и записывают спектры флуоресценции в области длин волн 401-404 нм, обязательно выставляя перо самописца при длине волны 401 нм в то же положение, что и при сканировании пробы в третьей пробирке, добиваясь этого регулировкой размера щели и коэффициента усиления спектрофотометра.
Концентрацию 3,4-бензпирена в анализируемом экстракте определяют по графику, на котором по оси абсцисс откладывают значение добавки 3,4-бензпирена в микрограммах, а по оси ординат - высоту пика максимума характеристической линии 3,4-бензпирена при 403 нм, измеренную по полученным спектрограммам в миллиметрах.
Если концентрация исследуемого раствора попадает в область, пригодную для измерений, то полученные экспериментальные точки лежат на одной прямой. Экстраполяция этой прямой до пересечения с осью абсцисс дает на ней отрезок, соответствующий содержанию 3,4-бензпирена в растворе с нулевой добавкой, т.е. в 1 см исследуемого экст
ракта.
2.3.1.2 Количественное определение содержания 3,4-бензпирена методом внутреннего стандарта
В качестве внутреннего стандарта используют 1,12-бензперилен. В пробирку наливают 3 см экстракта 3,4-бензпирена в
-октане, приготовленного, как указано в п.2.3 или 2.3.1 и помещают в сосуд Дьюара с жидким азотом перед входной щелью спектрофотометра, юстируют пробирку на линии 403 нм при длине волны возбуждающего света 367 нм, а затем производят запись спектра исходного экстракта в области длин волн 401-409 нм. По интенсивности линии (по высоте пика максимума характеристической линии 3,4-бензпирена при 403 нм), ширине щели и коэффициенту усиления прибора оценивают приблизительное содержание 3,4-бензпирена в пробе. В соответствии с этой оценкой в пробирку с 3 см
экстракта добавляют 1,12-бензперилена в таком количестве, чтобы в спектре пробы интенсивность линии 1,12-бензперилена при 406,3 нм была в 3-5 раз больше интенсивности линии 3,4-бензпирена при 403 нм.
Проводят запись спектра в области длин волн 401-409 нм дважды.
Интенсивности характеристических линий 3,4-бензпирена при 403 нм и 1,12-бензперилена при 406,3 нм ( и
соответственно) определяют по спектрограмме, измеряя в миллиметрах высоты пиков максимумов характеристических линий этих соединений. В расчет принимают среднее значение. Далее рассчитывают коэффициент отношения (
) интенсивности линии 3,4-бензпирена (
) к интенсивности линии 1,12-бензперилена (
),
![]() .
.
Далее определяют этот коэффициент для стандартных растворов 3,4-бензпирена (). Для этого в две пробирки наливают по 3 см
стандартных растворов 3,4-бензпирена концентрацией 0,02 и 0,04 мкг/см
. В каждую из пробирок наливают такое же количество 1,12-бензперилена, что и в пробирку с пробой. Проводят запись спектров дважды для каждого раствора 3,4-бензпирена в области длин волн 401-409 нм.
При этом обязательно следят за тем, чтобы положение пера самописца на длине волны 401 нм во всех случаях фиксировалось на одном уровне.
Далее по спектрограммам определяют интенсивности характеристических линий 3,4-бензпирена при 403 нм и 1,12-бензперилена при 406,3 нм ( и
соответственно). В расчет принимают среднее значение. Рассчитывают
![]() для каждой концентрации 3,4-бензпирена.
для каждой концентрации 3,4-бензпирена.
Концентрацию 3,4-бензпирена () в анализируемом растворе в микрограммах на кубический сантиметр вычисляют по формуле
![]() ,
,
где - концентрация 3,4-бензпирена в стандартном растворе, мкг/см
;
- коэффициент, найденный по спектрограмме анализируемого раствора;
- коэффициент, найденный по спектрограмме стандартного раствора, значение которого ближе по значению к коэффициенту анализируемого раствора.
Проводят два параллельных определения и одновременно контрольный опыт, который проводят через все стадии анализа с использованием всех реактивов согласно прописи методик, но без навески продукта.
2.4 Обработка результатов
Содержание 3,4-бензпирена () в микрограммах на килограмм вычисляют по формуле
![]() ,
,
где - концентрация 3,4-бензпирена в исходном экстракте, мкг/см
;
- концентрация 3,4-бензпирена в контрольном опыте, найденная по п.2.3.1.1 или 2.3.1.2, мкг/см
;
- объем исходного экстракта, см
;
,
- массы экстрактов, нанесенных на широкую (
) и узкую (
) части хроматографической пластинки, г;
- коэффициент пересчета граммов в килограммы;
- масса навески продукта, г.
Результат округляют до второго десятичного знака.
Из результатов двух параллельных определений вычисляют среднее арифметическое значение с тем же числом знаков после запятой и определяют расхождение между каждым результатом и средним арифметическим значением. Допускаемое относительное расхождение не должно превышать 40%, рассчитанных и округленных до целого числа.
За окончательный результат определения принимают среднее арифметическое результатов двух параллельных определений, увеличенное на значение систематической составляющей погрешности измерений, равное 0,3 . Окончательный результат округляют до первого десятичного знака.
Минимальная концентрация 3,4-бензпирена, определяемая этим методом, составляет 0,001 мкг/см.
3 Методы высокоэффективной жидкостной хроматографии
и спектрофлуориметрии при комнатной температуре
Сущность метода заключается в экстракции углеводородов, в том числе 3,4-бензпирена, гексаном из продукта, предварительно обработанного спиртовым раствором едкого калия, выделении фракции полициклических ароматических углеводородов колоночной хроматографией на сефадексе и количественном определении в полученной фракции 3,4-бензпирена высокоэффективной жидкостной хроматографией или спектрофлуориметрией при комнатной температуре.
3.1 Аппаратура, материалы и реактивы
Спектрофлуориметр типа MPF-43A.
Хроматограф высокоэффективный жидкостной с детектором по флуоресценции и колонкой с обращенной фазой типа С.
Весы лабораторные 2-го класса точности с наибольшим пределом взвешивания 200 г по ГОСТ 24104.
Весы лабораторные технические любого типа.
Испаритель ротационный типа ИР-IМ.
Насос водоструйный лабораторный.
Мешалка магнитная.
Облучатель ультрафиолетовый типа ОЛД или хроматоскоп.
Камера хроматографическая стеклянная 40х40х40 см.
Пластинки стеклянные для тонкослойной хроматографии 5х20 и 20х20 см.
Колонка стеклянная хроматографическая длиной 500 мм и диаметром 20 мм с оттянутым внизу концом и резервуаром вместимостью 50-60 см НШ 14/23.
Холодильник ХПТ-2-400-29/32 ХС или ХШ-1-400-29/32 ХС по ГОСТ 25336.
Алонж типа АИО-14/23-50 ТС или АИО-14/23-14/23-65 ТС по ГОСТ 25336.
Дефлегматор 250-19/26-29/32 ТС или 300-19/26-29/32 ТС по ГОСТ 25336.
Насадка Н-1-19/26-14/23-14/23 ТС или Н-2-19/26-14/23 ТС по ГОСТ 25336.
Воронка делительная ВД-1-500 или ВД-3-500 по ГОСТ 25336.
Воронка ВФО-32-ПОР 100-14/23 ХС или ВФО-32-ПОР 160-14/23 ХС по ГОСТ 25336.
Цилиндры мерные 1-100, 1-250 или 3-100, 3-250 по ГОСТ 25336.
Стакан химический В-1-100 или В-1-150 по ГОСТ 25336.
Колба 1-500 по ГОСТ 25336.
Колба Гр 50-14/23 по ГОСТ 25336.
Колбы К-1-100-29/32 TXC, К-1-25P-29/32 ТХС, К-1-500-29/32 ТХС или П-1-500-29/32 ТХС по ГОСТ 25336.
Колбы -1000-29/32 ТХС по ГОСТ 25336,
-250-34 ТХС по ГОСТ 25336.
Колбы мерные 2-100-2 по ГОСТ 25336.
Воронка Бюхнера 1 или 2, или 3 по ГОСТ 9147.
Стаканчики для взвешивания (бюксы) СВ-14/8 или СВ-19/9, или СВ-24/10, или СВ-34/12 по ГОСТ 25336.
Микрошприцы типов МШ-1, МШ-10 или стеклянные капилляры.
Пипетки градуированные вместимостью 0,5; 1; 2,5 см по ГОСТ 29228 и ГОСТ 29229.
Бумага индикаторная универсальная.
Бумага фильтровальная лабораторная по ГОСТ 12026.
Скальпель или тонкий шпатель.
Гексан, ч.
Спирт этиловый ректификованный по ГОСТ 5962 или спирт этиловый ректификованный технический по ГОСТ 18300, или спирт этиловый технический по ГОСТ 17299.
Бензол по ГОСТ 5955 или толуол по ГОСТ 5789.
Кислота серная по ГОСТ 4204.
Ацетон по ГОСТ 2603, ч, или ос.ч.
Ангидрид уксусный по ГОСТ 5815, ч.
Диметилформамид по ГОСТ 20289, ч.д.а.
Ацетонитрил для жидкостной хроматографии ОП-3, ос. ч.
Вода дистиллированная.
Калия гидроокись по ГОСТ 24363.
Целлюлоза микрокристаллическая для хроматографии ЛК.
3,4-бензпирен.
Бенз(в)хризен.
Сефадекс Н-20.
Силикагель марки АСКГ или молекулярные сита типа 5А.
3.2 Подготовка к испытанию
3.2.1 Подготовка растворителей
Растворители (гексан, этиловый спирт, ацетон, бензол) перегоняют общепринятым способом с елочным дефлегматором.
3.2.2 Приготовление ацетилированной целлюлозы
(50±0,2) г микрокристаллической целлюлозы помещают в плоскодонную колбу вместимостью 500 см, добавляют приготовленную в отдельной колбе смесь 150 см
бензола или толуола, 70 см
уксусного ангидрида и 0,3 см
серной кислоты. Реакционную смесь перемешивают на магнитной мешалке в течение 6-8 ч, оставляют еще на 18 ч после чего декантируют жидкую фазу, а осадок заливают 300 см
этилового спирта, перемешивают и оставляют на 24 ч, затем осадок отфильтровывают на воронке Бюхнера, промывают 100 см
этилового спирта и дистиллированной водой до нейтральной реакции промывных вод (по индикаторной бумаге).
Затем проверяют хроматографическую активность ацетилированной целлюлозы. Для этого за 3-4 ч до проведения хроматографии готовят смесь этилового спирта, ацетона и воды, взятых в объемном соотношении 60:25:15, и выливают ее в выстланную полосками фильтровальной бумаги хроматографическую камеру. Высота слоя растворителя должна составлять 1,5-2 см. 1,5 г ацетилированной целлюлозы суспензируют в 7 см этилового спирта и выливают суспензию ровным слоем на стеклянную пластинку 5х20 см, дают растворителю полностью испариться на воздухе и наносят на пластинку микрошприцем или стеклянным капилляром в точку 5 мкдм
раствора 3,4-бензпирена концентрации 1 мкг/см
. Пластинку помещают в хроматографическую камеру и оставляют в камере до тех пор, пока уровень растворителя поднимется не менее чем на 100 мм от линии старта. По окончании хроматографическую пластинку вынимают, высушивают на воздухе и под лампой ультрафиолетового облучателя отмечают флуоресцирующее голубым цветом пятно 3,4-бензпирена. Измеряют расстояние от стартовой линии до фронта растворителя и до середины пятна 3,4-бензпирена. Вычисляют значение, оценивающее скорость перемещения 3,4-бензпирена по пластинке (
), по формуле
![]() ,
,
где - расстояние от стартовой линии до середины пятна 3,4-бензпирена, мм;
- расстояние от стартовой линии до фронта растворителя, мм.
Значение 3,4-бензпирена должно составлять 0,1.
Для приготовления рабочей пластины 5 г ацетилированной целлюлозы суспензируют в 20 см этилового спирта и выливают ровным слоем на пластинку 20х20 см.
3.2.3 Приготовление стандартных растворов 3,4-бензпирена и бенз(в)хризена
3.2.3.1 Приготовление раствора А, содержащего 100 мкг/см 3,4-бензипрена
В стаканчик для взвешивания (бюксу) отвешивают (10±0,2) мг 3,4-бензпирена, навеску количественно переносят бензолом в мерную колбу вместимостью 100 см, объем раствора доводят до метки бензолом.
3.2.3.2 Приготовление рабочих растворов 3,4-бензпирена
При использовании высокоэффективной жидкостной хроматографии из раствора А отбирают пипетками соответствующей вместимости 0,25; 1,0 и 5 см, переносят в мерные колбы вместимостью 100 см
, доводят до метки ацетонитрилом и перемешивают. Полученные растворы содержат соответственно 0,25; 1,0 и 5,0 мкг/см
3,4-бензпирена.
При спектрофлуориметрическом определении 3,4-бензпирена из раствора А отбирают 1 см раствора и переносят в мерную колбу вместимостью 100 см
, добавляют до метки бензол и перемешивают. Полученный раствор содержит 1,0 мкг/см
3,4-бензпирена.
3.2.3.3 Приготовление раствора Б, содержащего 100 мкг/см бенз(в)хризена
В стаканчик для взвешивания (бюксу) отвешивают (10±0,2) мг бенз(в)хризена, количественно ацетонитрилом переносят в мерную колбу вместимостью 100 см, объем раствора доводят до метки ацетонитрилом и перемешивают.
3.2.3.4 Приготовление рабочего раствора бенз(в)хризена
Из раствора Б пипеткой соответствующей вместимости отбирают 0,5 см, переносят в мерную колбу вместимостью 100 см
, добавляют до метки ацетонитрил и перемешивают. Полученный раствор содержит 0,5 мкг/см
бенз(в)хризена.
3.2.4 Условия высокоэффективной жидкостной хроматографии
Рекомендуются следующие условия, которые могут быть уточнены в процессе работы в зависимости от типа хроматографа, устройства детектора и инжектора:
колонка Supercosil LC-PAH 150х4,6 мм, подвижная фаза - смесь ацетонитрила и воды, взятых в объемном соотношении 9:1, скорость потока 1 см/мин. Перед проведением смесь дегазируют под вакуумом, создаваемым водоструйным насосом. Детектор флуориметрический, длина волны возбуждающего света 360 нм, эмиссионный фильтр - 418 нм. Объем вводимой в инжектор пробы 20 мкдм
, из него на колонку - 10 мкдм
. Чувствительность усилителя подбирают таким образом, чтобы интенсивность сигнала 3,4-бензпирена и внутреннего стандарта - бенз(в)хризена не превышала 95% шкалы амперметра, так как при сигнале более 100% нарушается линейность показаний детектора.
Площади пиков 3,4-бензпирена и бенз(в)хризена измеряют с помощью интегратора или вручную по высоте пика и его ширине на половине высоты.
3.2.5 Определение калибровочного коэффициента для расчета по методу внутреннего стандарта
Калибровочный коэффициент рассчитывают по результатам анализа трех растворов, содержащих смесь 3,4-бензпирена и бенз(в)хризена, взятых в соотношении 10:1, 2:1, 1:1. Для приготовления растворов в три стаканчика для взвешивания (бюксы) с точностью до 0,2 мг отвешивают 3,4-бензпирен и бенз(в)хризен в количествах, указанных в таблице 1.
Таблица 1
Номер раствора | 3,4-бензпирен, мг | Бенз(в)хризен, мг | |
Раствор | 1 | 20 | 2 |
" | 2 | 10 | 5 |
" | 3 | 5 | 5 |
Навески количественно переносят бензолом в мерные колбы вместимостью 100 см, доводят объем раствора до метки бензолом и перемешивают.
Из этих исходных растворов в мерных колбах вместимостью 25 см готовят рабочие растворы, для чего в мерные колбы микрошприцем вносят следующие объемы исходных растворов: из раствора 1-50 мкдм
, 2-20 мкдм
, 3-50 мкдм
и доводят растворы в колбах до метки ацетонитрилом, перемешивают и хранят в холодильнике.
Таким образом, концентрация 3,4-бензпирена и бенз(в)хризена в полученных рабочих растворах должна соответствовать указанной в таблице 2.
Таблица 2
Номер раствора | Концентрация 3,4-бензпирена, мкг/ см | Концентрация бенз(в)хризена, | |
Раствор | 1 | 0,4 | 0,04 |
" | 2 | 0,2 | 0,04 |
" | 3 | 0,1 | 0,01 |
Записывают по три хроматограммы из каждого раствора и измеряют площади пиков 3,4-бензпирена и бенз(в)хризена. За окончательный результат испытания принимают среднее арифметическое значение площади пика, рассчитанное из трех хроматограмм.
Калибровочный коэффициент () вычисляют по формуле
![]() ,
,
где ,
- массы введенных на колонку 3,4-бензпирена (
) и бенз(в)хризена (
), мкг;
,
- площади пиков 3,4-бензпирена (
) и бенз(в)хризена (
), см
.
Калибровочный коэффициент () рассчитывают для каждого раствора. Его значения не должны отличаться от среднего арифметического значения из всех результатов более чем на 10%.
При длине волны возбуждающего света 360 нм и эмиссионном фильтре 418 нм значение калибровочного коэффициента составляет
9,5.
3.3 Проведение испытания
3.3.1 Выделение фракции полициклических ароматических углеводородов, содержащей 3,4-бензпирен
В круглодонную колбу вместимостью 500 см помещают 25 г продукта, добавляют раствор, состоящий из 20 г гидроокиси калия в 220 см
смеси этилового спирта и воды, взятых в объемном соотношении 10:1. Содержимое колбы перемешивают встряхиванием. Колбу соединяют с обратным холодильником и нагревают на водяной бане при кипении реакционной смеси в течение 3 ч. Затем в колбу через холодильник добавляют 150 см
дистиллированной воды. Охлаждают реакционную массу до комнатной температуры. После охлаждения жидкую фазу реакционной массы декантацией переносят в делительную воронку, оставляя остаток продукта в колбе. В колбу с остатком добавляют 150 см
гексана, содержимое колбы энергично перемешивают и гексан декантируют в делительную воронку. Воронку энергично встряхивают и оставляют для расслаивания жидкостей. В случае образования устойчивой эмульсии к смеси в делительной воронке добавляют 20 см
этилового спирта. После расслаивания нижнюю водно-спиртовую фазу сливают обратно в колбу с осадком, а гексановый экстракт переливают в другую делительную воронку. Такую обработку реакционной массы проводят еще два раза, используя для экстракции гексан по 100 см
и этиловый спирт для расслаивания эмульсии, порциями по 20 см
.
По окончании экстракции остаток в колбе и гидролизат отбрасывают, а объединенный экстракт промывают в делительной воронке дистиллированной водой три раза по 50 см и упаривают в круглодонной колбе вместимостью 250 см
на ротационном испарителе при остаточном давлении не ниже 50 мм рт.ст и температуре водяной бани не более 60 °С до объема 100 см
.
Экстракт переносят в делительную воронку вместимостью 500 см и добавляют к нему 100 см
смеси диметилформамида и воды, взятых в объемном соотношении 9:1. Интенсивно встряхивают смесь в течение 1 мин, после расслоения фаз нижнюю сливают в плоскодонную колбу вместимостью 200 см
, а из верхнего гексанового слоя снова проводят экстракцию 100 см
смеси диметилформамида и воды. Гексановый слой отбрасывают, объединенный диметилформамидовый экстракт переносят в делительную воронку, добавляют 200 см
дистиллированной воды и проводят экстракцию в водной фазы гексаном трижды по 75 см
. Водную фазу отбрасывают, а гексановый экстракт промывают водой трижды по 30 см
. Гексан упаривают на ротационном испарителе до объема 1,5-2,0 см
, а остаток гексана удаляют током воздуха через вакуумный алонж, соединенный с водоструйным насосом, экстракт растворяют в 0,5 см
этилового спирта.
В стакан вместимостью 100 см отвешивают (10±0,2) г сефадекса
Н-20, добавляют 50 см
этилового спирта и оставляют для набухания на 3-4 ч. Затем гель переносят, смывая небольшим количеством спирта, в стеклянную хроматографическую колонку, дают растворителю стечь. На подготовленную колонку наносят полученный экстракт трижды смывая его из колбы этиловым спиртом порциями по 0,5 см
. Элюирование с колонки полициклических ароматических углеводородов, в том числе 3,4-бензпирена, проводят 160 см
этилового спирта, первую фракцию объемом 60 см
отбрасывают, собирают вторую фракцию объемом 100 см
. Скорость элюирования растворителя 0,5-1,0 см
/мин обеспечивают, создавая небольшое избыточное давление током воздуха или азота через насадку, соединенную с воздуходувкой или газовым баллоном. Газ следует подавать через стеклянную трубку, заполненную силикагелем или молекулярными ситами.
Раствор второй фракции переносят в грушевидную колбу вместимостью 50 см, растворитель упаривают до объема 0,5-1,0 см
, его остаток удаляют в токе воздуха или азота. Полученную фракцию полициклических ароматических углеводородов далее анализируют с помощью высокоэффективной жидкостной хроматографии или подвергают дополнительной очистке в тонком слое ацетилированной целлюлозы для анализа спектрофлу
ориметрическим методом.
3.3.2 Количественное определение 3,4-бензпирена методом высокоэффективной жидкостной хроматографии
Количественное определение 3,4-бензпирена при использовании высокоэффективной жидкостной хроматографии проводят методом внутреннего стандарта или методом добавок.
3.3.2.1 Определение методом внутреннего стандарта
При использовании такого способа количественной оценки одновременно с пробой продукта анализируют пробу контрольного опыта, добавляя в пробу продукта и пробу контрольного опыта по 50 мкдм раствора бенз(в)хризена концентрации 0,5 мкг/см
на стадии подготовки проб к щелочному гидролизу. Обе пробы проводят через все стадии испытания, указанные в п.3.3.1. Сухой остаток растворяют в 200 мкдм
ацетонитрила.
В условиях, указанных в п.3.2.4, записывают хроматограммы раствора 3,4-бензпирена концентрации 250 мкг/см, раствора бенз(в)хризена концентрации 100 мкг/см
, пробы контрольного опыта с добавкой бенз(в)хризена и пробы продукта с такой же добавкой бенз(в)хризена. Измеряют площади пиков 3,4-бензпирена и бенз(в)хризена на хроматограммах пробы продукта и пробы контрольного опыта.
Для каждой пробы записывают по две хроматограммы, отмечают пики, совпадающие по времени с 3,4-бензпиреном и бенз(в)хризеном, определяют их площади. За окончательный результат испытания принимают среднее арифметическое значение площади пика, рассчитанное из двух хроматограмм.
3.3.2.2 Определение методом добавок
Для количественной оценки при использовании метода добавок одновременно с пробой продукта анализируют пробу контрольного опыта (все предусмотренные по методике реактивы проводят через все стадии определения по п.3.3.1). Полученные фракции полициклических ароматических углеводородов, выделенные из проб продукта и контрольного опыта, растворяют в 400 мкдм ацетонитрила (микрошприцем).
Полученные растворы делят на две части, отбирая меньшую часть (40 мкдм) в пробирку или грушевидную колбу.
В условиях, указанных в п.3.2.4, записывают хроматограммы пробы продукта, пробы контрольного опыта и хроматограмму раствора 3,4-бензпирена концентрации 0,25 мкг/см. Отмечают время выхода 3,4-бензпирена.
В оставшиеся части проб продукта и контрольного опыта (360 мкдм) делают добавку 10-20 мкдм
раствора 3,4-бензпирена концентрации 5 мкг/см
. Полученные растворы вновь вводят в хроматограф.
Все хроматограммы записывают дважды. Измеряют площади пиков 3,4-бензпирена. За окончательный результат принимают среднее арифметическое значение площади, рассчитанное из двух хроматограмм.
3.3.3. Количественное определение 3,4-бензпирена методом спектрофлуориметрии при комнатной температуре
Для количественной оценки содержания 3,4-бензпирена при использовании метода спектрофлуориметрии одновременно с пробой продукта анализируют раствор сравнения (50 мкдм раствора 3,4-бензпирена концентрации 1 мкг/см
обрабатывают так, как указано в п.3.3.1).
Полученные по п.3.3.1 фракции полициклических ароматических углеводородов из пробы продукта и пробы раствора сравнения растворяют в 0,5 см бензола и далее подвергают дополнительной очистке в тонком слое ацетилированной целлюлозы.
Для этого пластинку 20х20 см, подготовленную, как указано в п.3.2, делят на два поля: боковое - шириной 1,5-2 см и основное, проводя по слою сорбента скальпелем или тонким шпателем разделяющую полосу. На основное поле сплошной полосой, отступив 2 см от нижнего края пластинки и по 1 см с боковых краев, наносят раствор фракции полициклических ароматических углеводородов. Раствор наносят с помощью тонко оттянутого стеклянного капилляра или микрошприца, размер пятен не должен превышать 5 мм. Для количественного переноса вещества его дважды смывают со стенок колбы небольшим количеством бензола (0,4-0,6 см). На стартовую линию бокового поля наносят в точку 5 мкдм
раствора 3,4-бензпирена концентрации 1 мкг/см
. После полного испарения растворителей со стартовой линии пластинки ее помещают в предварительно насыщенную хроматографическую камеру и проводят элюирование в смеси этилового спирта, ацетона и воды, взятых в объемном соотношении 60:25:15. Когда фронт растворителя достигнет 2 см от верхнего края пластинки, ее вынимают из камеры, высушивают на воздухе и проявляют хроматографическую зону 3,4-бензпирена под лампой ультрафиолетового облучателя. Сорбент из зоны 3,4-бензпирена с основного поля с помощью скальпеля или тонкого шпателя соскабливают с пластинки и переносят на стеклянный фильтр, с которого вещество элюируют в несколько приемов 50 см
бензола в колбу вместимостью 100 см
, далее растворитель упаривают до небольшого объема, его остаток удаляют током воздуха и добавляют в колбу 1 см
бензола.
На спектрофлуориметре при длине волны возбуждающего света 388 нм в диапазоне 395-440 нм при скорости сканирования 60 нм/мин записывают спектры флуоресценции пробы продукта и пробы раствора сравнения (раствор 3,4-бензпирена, проведенный через все стадии анализа). Спектры записывают в одном режиме усиления, регулируя щель и коэффициент усиления по раствору сравнения так, чтобы сигнал составлял в максимуме при 406 нм 0,4-0,6 шкалы. При высоких уровнях 3,4-бензпирена в продукте пробу следует растворить в большом объеме бензола и вновь записать спектр в том же режиме усиления, что и стандарт. Для расчета используют интенсивность флуоресценции раствора в максимуме с длиной волны 406 нм. На полученных спектрограммах измеряют высоту спектральной линии 3,4-бензпирена в максимуме при 406 нм.
Проводят два параллельных определен
ия.
3.3.4 Обработка результатов
3.3.4.1 Обработка результатов по методу внутреннего стандарта
Содержание 3,4-бензпирена () в микрограммах на килограмм вычисляют по формулам:
![]() ,
,
![]() ,
,
![]() ,
,
где - масса продукта, взятая для испытания, г;
- масса 3,4-бензпирена в пробе продукта, мкг;
- масса 3,4-бензпирена в пробе контрольного опыта, мкг;
- масса бенз(в)хризена, введенная в пробу контрольного опыта и пробу продукта, мкг;
,
- площади пиков 3,4-бензпирена на хроматограммах пробы контрольного опыта и пробы продукта, см
;
,
- площади пиков бенз(в)хризена на хроматограммах пробы контрольного опыта и пробы продукта, см
;
- калибровочный коэффициент;
- коэффициент пересчета граммов в килограммы.
Результат округляют до второго десятичного знака.
Из результатов двух параллельных определений вычисляют среднее арифметическое значение с тем же числом знаков после запятой и определяют расхождение между каждым результатом и средним арифметическим значением. Допускаемое относительное расхождение не должно превышать 40%, округленных до целых единиц.
За окончательный результат испытания принимают среднее арифметическое результатов двух параллельных определений, которое округляют до одного знака после запятой.
Минимальная концентрация 3,4-бензпирена, определяемая этим методом, составляет 0,01 м
кг/см.
3.3.4.2 Обработка результатов по методу добавок
Содержание 3,4-бензпирена () в микрограммах на килограмм вычисляют по формулам:
![]() ,
,
где:
![]() ,
,
![]() ,
,
где - масса продукта, взятая для испытания, г;
- масса 3,4-бензпирена в пробе продукта, мкг;
- масса 3,4-бензпирена в пробе контрольного опыта, мкг;
,
- массы 3,4-бензпирена, добавленные к части экстракта из пробы продукта (
) и пробы контрольного опыта (
), мкг;
,
- площади пиков 3,4-бензпирена на хроматограммах пробы продукта (
) и пробы продукта с добавкой 3,4-бензпирена (
), см
;
,
- площади пиков 3,4-бензпирена на хроматограммах пробы контрольного опыта (
) и пробы контрольного опыта с добавкой 3,4-бензпирена (
);
- доля пробы, к которой делают добавку 3,4-бензпирена;
- коэффициент пересчета граммов в килограммы.
Из результатов двух параллельных определений вычисляют среднее арифметическое значение с тем же числом знаков после запятой и определяют расхождение между каждым результатом и средним арифметическим значением. Допускаемое относительное расхождение не должно превышать 40%, округленных до целых единиц.
За окончательный результат испытания принимают среднее арифметическое результатов двух параллельных определений, увеличенное на значение систематической составляющей погрешности измерений, равное 0,30 . Окончательный результат округляют до первого десятичного знака.
Минимальная концентрация 3,4-бензпирена, определяемая этим методом, составляет
0,01 мкг/см.
3.3.4.3 Обработка результатов по методу спектрофлуориметрии
Содержание 3,4-бензпирена () в микрограммах на килограмм вычисляют по формуле
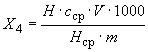 ,
,
где - высота спектральной линии 3,4-бензпирена на спектрограмме продукта, мм;
- концентрация раствора сравнения, мкг/см
;
- объем пробы продукта, см
;
- высота спектральной линии 3,4-бензпирена на спектрограмме раствора сравнения, мм;
- масса продукта, г.
Из результатов двух параллельных определений вычисляют среднее арифметическое значение с тем же числом знаков после запятой и определяют расхождение между каждым результатом и средним арифметическим. Допускаемое относительное расхождение не должно превышать 40%, округленное до целого числа.
За окончательный результат испытания принимают среднее арифметическое результатов двух параллельных определений, которое округляют до первого десятичного знака.
Минимальная концентрация 3,4-бензпирена, определяемая этим методом, составляет 0,001 мкг/см анализируемого раствора.
Текст документа сверен по:
Комбикорма. Часть 6.
Жмыхи, шроты и горчичный порошок.
Дрожжи. Методы анализа: Сб. ГОСТов. -
М.: ИПК Издательство стандартов, 2002

