ГОСТ 34440-2018
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ФЕРМЕНТНЫЕ ПРЕПАРАТЫ ДЛЯ ПИЩЕВОЙ ПРОМЫШЛЕННОСТИ
Методы определения амилолитической активности
Enzyme preparations for food industry. Methods for the determination of amylase activity
МКС 07.100.30
Дата введения 2019-07-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2015 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 РАЗРАБОТАН Всероссийским научно-исследовательским институтом пищевой биотехнологии - филиалом Федерального бюджетного учреждения науки "Федеральный исследовательский центр питания, биотехнологии и безопасности пищи" (ВНИИПБТ - филиал ФГБУН "ФИЦ питания и биотехнологии")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 27 июля 2018 г. N 110-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
Узбекистан | UZ | Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 21 августа 2018 г. N 510-ст межгосударственный стандарт ГОСТ 34440-2018 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2019 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
1 Область применения
Настоящий стандарт распространяется на ферментные препараты (источники -амилазы и глюкоамилазы с применением в качестве субстрата крахмала), используемые в пищевой промышленности, и устанавливает методы определения амилолитической активности.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.018-93 Система стандартов безопасности труда. Пожаровзрывобезопасность статического электричества. Общие требования
ГОСТ 12.2.007.0-75 Система стандартов безопасности труда. Изделия электротехнические. Общие требования безопасности
ГОСТ 12.4.021-75 Система стандартов безопасности труда. Системы вентиляционные. Общие требования
ГОСТ 12.4.103-83 Система стандартов безопасности труда. Одежда специальная защитная, средства индивидуальной защиты ног и рук. Классификация
ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 199-78 Реактивы. Натрий уксуснокислый 3-водный. Технические условия
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ 4159-79 Реактивы. Йод. Технические условия
ГОСТ 4172-76 Реактивы. Натрий фосфорнокислый двузамещенный 12-водный. Технические условия
ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
ГОСТ 4207-75 Реактивы. Калий железистосинеродистый 3-водный. Технические условия
ГОСТ 4232-74 Реактивы. Калий йодистый. Технические условия
ГОСТ ИСО 5725-6-2003* Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
_________________
* В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002.
ГОСТ 6038-79 Реактивы. D-глюкоза. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 10163-76 Реактивы. Крахмал растворимый. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 13586.5-2015 Зерно. Метод определения влажности
ГОСТ 13867-68 Продукты химические. Обозначение чистоты
ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия
ГОСТ 18321-73 Статистический контроль качества. Методы случайного отбора выборок штучной продукции
ГОСТ 18481-81 Ареометры и цилиндры стеклянные. Общие технические условия
ГОСТ 18995.1-73 Продукты химические жидкие. Методы определения плотности
ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 гидролиз: Расщепление исходного соединения на более простые в присутствии молекулы воды.
3.2 ферментный гидролиз: Расщепление высокомолекулярных соединений при участии катализаторов белковой природы - гидролитических ферментов.
3.3 субстрат: Соединение или вещество, на которое воздействует фермент.
3.4 крахмал: Высокомолекулярный полисахарид, в котором остатки глюкозы соединены -гликозидными связями, состоящий из амилозы и амилопектина, являющийся субстратом для амилолитических ферментов.
3.5 прогидролизованный крахмал: Крахмал, подвергнутый действию амилолитических ферментов различной степени деструкции в зависимости от активности фермента.
3.6 системные названия ферментов: Названия, указывающие природу химической реакции, катализируемой ферментом, в соответствии с современной классификацией (КФ), принятой Международной комиссией по ферментам [1] (см. приложение А).
3.7 амилолитические ферменты: -амилазы и глюкоамилаза, катализирующие гидролиз субстрата.
3.8 бактериальные -амилазы: Ферменты бактериального происхождения, которые катализируют гидролиз субстрата до декстринов различной степени полимеризации.
Примечание - Мезофильные -амилазы проявляют максимальный уровень активности при температуре 60-70°С, термостабильные
-амилазы - при температуре 80-95°С.
3.9 грибные -амилазы: Ферменты грибного происхождения, которые катализируют расщепление субстрата с глубокой степенью гидролиза, при этом образуются декстрины, олигосахариды и мальтоза.
3.10 глюкоамилаза: Фермент, который катализирует гидролиз -1,4- и
-1,6-гликозидных связей крахмала, декстринов, олигосахаридов, последовательно отщепляя остатки глюкозы от нередуцирующих концов субстрата.
4 Метод определения амилолитической активности ферментных препаратов - источников  -амилазы (АС)
-амилазы (АС)
4.1 Сущность метода
4.1.1 Метод основан на количественном определении прогидролизованного крахмала в результате его гидролиза ферментами амилолитического комплекса до декстринов различной молекулярной массы при 6,0 ед. рН (для бактериальных -амилаз) и 4,7 ед. рН (для грибных
-амилаз), температуре 30°С. Продолжительность гидролиза - 10 мин.
4.1.2 За единицу амилолитической активности (АС) принимают такое количество фермента, которое в определенных условиях температуры, рН и времени катализирует гидролиз 1 г растворимого крахмала до декстринов различной молекулярной массы, что составляет 30-50% от количества крахмала, введенного в реакцию. Активность выражают в ед. АС/г (для порошкообразного) или в ед. АС/см (для жидкого) ферментного препарата.
4.1.3 Количество прогидролизованного крахмала определяют колориметрическим методом по разнице между интенсивностью окраски с раствором йода исходного и остаточного крахмала.
4.2 Средства измерений, вспомогательное оборудование, посуда, реактивы и материалы
Весы лабораторные по OIML R 76-1* высокого класса точности, с ценой поверочного деления 0,1 мг и пределом допускаемой погрешности в эксплуатации ±0,15 мг.
________________
* Вероятно, ошибка оригинала. Следует читать: ГОСТ OIML R 76-1-2011. - .
Фотоэлектроколориметр или спектрофотометр любого типа, который обеспечивает измерение оптической плотности анализируемых растворов при длине световой волны =670 нм с погрешностью измерения коэффициента пропускания ±1% в кюветах с толщиной поглощающего свет слоя 10 мм. рН-метр любого типа для измерения в диапазоне от 0 до 14 ед. рН с пределом допускаемой погрешности в эксплуатации ±0,1 ед. рН.
Холодильник бытовой по ГОСТ 16317.
Ультратермостат или термостат водяной с точностью регулирования температуры ±1°С.
Баня водяная любого типа, которая обеспечивает поддержание температуры (100±1)°С.
Мешалка магнитная любой марки, которая обеспечивает скорость вращения до 800 мин.
Секундомер с емкостью шкалы счетчика 1 мин, ценой деления 1 с и погрешностью ±1,5 с.
Встряхиватель для перемешивания жидкости со скоростью вращения гнезда от 50 до 3000 об/мин.
Термометры ртутные стеклянные лабораторные от 0 до 50°С и от 0 до 100°С с ценой деления 0,1 или 0,5°С по ГОСТ 28498.
Ареометры общего назначения по ГОСТ 18481.
Стаканы стеклянные В-1-100 ТС, В-1-150 ТС, В-1-800 ТС по ГОСТ 25336.
Колбы стеклянные конические Кн-1-100-14/23 ТС, Кн-1-250-24/29 ТС по ГОСТ 25336.
Стаканчики для взвешивания СВ-19/9 по ГОСТ 25336.
Воронки ВР-56 ХС, ВР-75 ХС по ГОСТ 25336.
Пробирки П1-14-120 ХС, П1-21-200 ХС по ГОСТ 25336.
Колбы мерные 1-50-2, 1-100-2, 1-200-2, 1-250-2, 2-1000-2 по ГОСТ 1770.
Цилиндры 1-25-2, 1-50-2, 1-100-2, 1-250-2 по ГОСТ 1770.
Пипетки стеклянные 1-2-2-1, 1-2-2-2, 1-2-2-5, 1-2-2-10 по ГОСТ 29227 или автоматические с постоянной и переменной вместимостью на 0,5; 1,0 и 5,0 см.
Бумага фильтровальная лабораторная по ГОСТ 12026.
Крахмал растворимый по ГОСТ 10163.
Натрий уксуснокислый 3-водный по ГОСТ 199.
Кислота уксусная по ГОСТ 61.
Натрий фосфорнокислый двузамещенный 12-водный по ГОСТ 4172.
Калий фосфорнокислый однозамещенный по ГОСТ 4198.
Кислота соляная по ГОСТ 3118.
Йод кристаллический по ГОСТ 4159.
Вода дистиллированная по ГОСТ 6709.
Все реактивы должны относиться к подгруппе чистоты 2 (х.ч.) или 3 (ч.д.а.) по ГОСТ 13867.
Допускается применение других средств измерений с метрологическими характеристиками, вспомогательного оборудования, посуды, материалов с техническими характеристиками не ниже вышеуказанных и химических реактивов аналогичной квалификации.
4.3 Отбор и подготовка проб
4.3.1 Отбор проб
4.3.1.1 Ферментные препараты принимают партиями. Партией считают определенное количество продукции одного наименования, одинаково упакованной, изготовленной одним изготовителем по одному документу в определенный промежуток времени, сопровождаемое товаросопроводительной документацией, обеспечивающей прослеживаемость продукции.
4.3.1.2 В сопроводительным документе должны быть указаны:
- наименование предприятия-изготовителя;
- наименование ферментного препарата;
- номер партии;
- количество мест в партии;
- дата выработки;
- дата выдачи документа.
4.3.1.3 Для определения амилолитической активности ферментного препарата выборку упаковочных единиц проводят методом случайного отбора по ГОСТ 18321.
4.3.1.4 Из каждой отобранной упаковочной единицы отбирают точечную пробу:
- для сухих ферментных препаратов при помощи специального мешочного щупа, погружаемого на всю глубину единицы упаковки по вертикальной оси;
- жидких ферментных препаратов после тщательного перемешивания пробоотборником, погружаемым на всю глубину единицы упаковки по вертикальной оси.
4.3.1.5 Отобранные точечные пробы соединяют вместе и получают объединенную пробу:
- для сухих ферментных препаратов массой не менее 150 г;
- жидких ферментных препаратов - не менее 1 дм.
4.3.1.6 Объединенные пробы тщательно перемешивают, делят на две части и помещают в сухие чистые стеклянные банки с притертыми пробками или полиэтиленовые пакеты, которые затем запаивают.
Одну банку или один пакет передают в лабораторию для проведения микробиологических и физико-химических анализов, другую(ой) банку (пакет) хранят в течение одного года - для сухих препаратов; 6 мес - для жидких препаратов.
4.3.1.7 На каждую(ый) банку (пакет) с пробой наклеивают этикетку с указанием:
- наименования препарата;
- даты выработки;
- номера партии;
- даты отбора пробы;
- массы нетто партии;
- должности и подписи лица, отобравшего пробу.
4.3.2 Подготовка пробы
4.3.2.1 Приготовление основного раствора ферментного препарата
В стаканчик для взвешивания помещают анализируемую пробу сухого ферментного препарата массой (0,1000±0,0005) г или жидкого ферментного препарата массой (1,0000±0,0200) г и суспендируют в небольшом количестве дистиллированной воды. Суспензию количественно переносят в мерную колбу вместимостью 100 см, доводят объем до метки дистиллированной водой при температуре 20°С и тщательно перемешивают.
Приготовленный раствор является основным раствором ферментного препарата.
Срок хранения раствора в закрытой стеклянной посуде при температуре 20°С - не более 2 ч.
4.3.2.2 Приготовление рабочего раствора ферментного препарата
Рабочий раствор ферментного препарата готовят из основного раствора, приготовленного по 4.3.2.1, путем разведения его дистиллированной водой в мерных колбах вместимостью 100, 200 или 250 см.
Рабочий раствор ферментного препарата готовят непосредственно перед проведением анализа.
4.4 Подготовка к анализу
4.4.1 Приготовление ацетатного буферного раствора молярной концентрации 1,0 моль/дм со значением 4,7 ед. рН
4.4.1.1 Приготовление раствора уксуснокислого натрия молярной концентрации 1,0 моль/дм (раствор А)
В мерную колбу вместимостью 1000 см помещают (136,0000±0,1000) г уксуснокислого 3-водного натрия и растворяют в 300 см
дистиллированной воды. Затем доводят до метки дистиллированной водой при температуре 20°С и перемешивают.
Срок хранения раствора в закрытой стеклянной посуде при температуре 4°С - не более 1 мес.
4.4.1.2 Приготовление раствора уксусной кислоты молярной концентрации 1,0 моль/дм (раствор Б)
Концентрированную уксусную кислоту объемом 58,0 см разводят в 300 см
дистиллированной воды в мерной колбе вместимостью 1000 см
, доводят до метки дистиллированной водой при температуре 20°С и перемешивают.
Срок хранения раствора в закрытой стеклянной посуде при температуре 4°С - не более 1 мес.
4.4.1.3 Приготовление ацетатного буферного раствора
Для приготовления ацетатного буферного раствора в конической колбе вместимостью 250 см смешивают растворы уксуснокислого натрия (раствор А) и уксусной кислоты (раствор Б) в равных объемах, получая значение рН смеси, равное 4,7 ед. рН. При необходимости доводят рН раствора до значения 4,7 ед. рН одним из исходных растворов.
Срок хранения буферного раствора в закрытой стеклянной посуде при температуре 4°С - не более 1 мес.
4.4.2 Приготовление фосфатного буферного раствора молярной концентрации 1/15 моль/дм со значением 6,0 ед. рН
4.4.2.1 Приготовление раствора фосфорнокислого натрия двузамещенного 12-водного молярной концентрации 1/15 моль/дм (раствор В)
В мерную колбу вместимостью 1000 см помещают (23,8700±0,0100) г фосфорнокислого натрия двузамещенного 12-водного, растворяют в 300 см
дистиллированной воды и доводят объем до метки дистиллированной водой при температуре 20°С.
Срок хранения раствора в закрытой стеклянной посуде при температуре 4°С - не более 1 мес.
4.4.2.2 Приготовление раствора фосфорнокислого калия однозамещенного молярной концентрации 1/15 моль/дм (раствор Г)
В мерную колбу вместимостью 1000 см помещают (9,0870±0,0010) г фосфорнокислого калия однозамещенного, растворяют в 300 см
дистиллированной воды и доводят объем до метки дистиллированной водой при температуре 20°С.
Срок хранения раствора в закрытой стеклянной посуде при температуре 4°С - не более 1 мес.
4.4.2.3 Приготовление фосфатного буферного раствора молярной концентрации 1/15 моль/дм со значением 6,0 ед. рН
Для приготовления фосфатного буферного раствора молярной концентрации 1/15 моль/дм со значением 6,0 ед. рН растворы В и Г смешивают в соотношении 1:9.
Величину рН проверяют на рН-метре. В случае отклонения рН фосфатного буферного раствора от 6,0 ед. рН, его доводят до нужного значения раствором В или Г.
Срок хранения буферного раствора в закрытой стеклянной посуде при температуре 4°С - не более 1 мес.
4.4.3 Приготовление раствора соляной кислоты молярной концентрации 0,5 моль/дм
Концентрированную соляную кислоту объемом 41,0 см разводят в 300 см
дистиллированной воды в мерной колбе вместимостью 1000 см
, доводят до метки дистиллированной водой при температуре 20°С и перемешивают.
Срок хранения раствора соляной кислоты в закрытой стеклянной посуде при температуре 20°С - не более 1 мес.
4.4.4 Приготовление раствора йода
4.4.4.1 Приготовление основного раствора йода
(0,5000±0,0100) г йода и (5,0000±0,0100) г йодистого калия растворяют в стаканчике для взвешивания с притертой крышкой в небольшом количестве воды. Содержимое перемешивают на магнитной мешалке при плотно закрытой крышке бюкса.
Раствор после полного растворения йода переносят количественно в мерную колбу с притертой пробкой вместимостью 200 см и объем доводят до метки дистиллированной водой при температуре 20°С.
Срок хранения основного раствора йода в стеклянной посуде из темного стекла с притертой пробкой - не более 1 мес.
4.4.4.2 Приготовление рабочего раствора йода
20 см основного раствора йода, приготовленного по 4.4.4.1, разводят в мерной колбе вместимостью 1000 см
раствором соляной кислоты молярной концентрации 0,5 моль/дм
, приготовленной по 4.4.3.
Перед использованием рабочего раствора проверяют его оптическую плотность на фотоэлектроколориметре или спектрофотометре при длине световой волны =440 нм в кюветах с толщиной поглощающего свет слоя 10 мм. Оптическая плотность рабочего раствора йода, измеренная в сравнении с дистиллированной водой, должна иметь значение 0,22±0,01. В случае отклонения от этого значения добавляют раствор соляной кислоты молярной концентрации 0,5 моль/дм
или основного раствора йода до достижения нужной величины оптической плотности.
4.4.5 Приготовление раствора крахмала с массовой долей 1,0% (субстрат)
1,0000 г крахмала в пересчете на абсолютно сухое вещество (учитывая влагу, определяемую по ГОСТ 13586.5) помещают в мерную колбу вместимостью 100 см, добавляют 25 см
дистиллированной воды и перемешивают. Затем добавляют в колбу еще 25 см
дистиллированной воды, помещают колбу в кипящую водяную баню на 15-20 мин, непрерывно перемешивая содержимое до полного растворения крахмала. После этого содержимое колбы охлаждают, добавляют 10 см
ацетатного буферного раствора с 4,7 ед. рН (см. 4.4.1) - для препаратов грибного происхождения или фосфатного буферного раствора с 6,0 ед. рН (см. 4.4.2) - для препаратов бактериального происхождения. Объем жидкости доводят до метки дистиллированной водой при температуре 20°С и содержимое колбы перемешивают. Для полученного раствора крахмала характерна легкая опалесценция.
Раствор крахмала готовят в день проведения анализа и хранят в закрытой стеклянной посуде не более 6 ч.
4.5 Условия проведения анализа
Анализ проводят в следующих лабораторных условиях:
- температура | (20±5)°С; |
- относительная влажность воздуха | от 45 до 80%; |
- атмосферное давление | от 630 до 800 мм рт.ст. |
4.6 Проведение анализа
4.6.1 Каждое разведение рабочего раствора ферментного препарата анализируют в двух повторностях. Для анализа берут две параллельные навески препарата.
4.6.2 В две пробирки размером 21200 мм вносят по 10 см
1%-ного раствора субстрата, приготовленного по 4.4.5. Содержимое пробирок выдерживают в ультратермостате или водяном термостате при температуре (30,0±1,0)°С в течение 5 мин.
4.6.3 В пробирки с субстратом добавляют по 5,0 см рабочего раствора ферментного препарата, приготовленного по 4.3.2.2, предварительно прогретого в течение трех-четырех минут при температуре (30,0±1,0)°С. Пробирки встряхивают и оставляют в ультратермостате или водяном термостате для проведения ферментативной реакции на 10 мин при температуре (30,0±1,0)°С (с точностью, определяемой по секундомеру от начала ферментативной реакции).
4.6.4 По окончании ферментативной реакции отбирают 0,5 см смеси и вносят в коническую колбу вместимостью 100 см
с 50 см
рабочего раствора йода, приготовленного по 4.4.4.2. Содержимое колбы перемешивают и выдерживают в течение 5 мин, при этом раствор приобретает фиолетовую окраску различной интенсивности в зависимости от количества непрогидролизованного крахмала. Интенсивность окраски раствора измеряют на фотоэлектроколориметре или спектрофотометре при длине световой волны
=670 нм в кюветах при толщине поглощающего свет слоя 10 мм в сравнении с дистиллированной водой, получая значение оптической плотности анализируемого раствора
.
4.6.5 В качестве контроля используют 1%-ный раствор субстрата (см. 4.4.5) объемом 10 см, в который вместо рабочего раствора ферментного препарата добавляют 5,0 см
дистиллированной воды. Полученную смесь выдерживают в ультратермостате при температуре 30°С в течение 10 мин. Затем все дальнейшие действия проводят аналогично 4.6.3, получая значение оптической плотности контрольного раствора
. Цвет контрольного раствора - синий.
4.7 Оформление результатов
4.7.1 Вычисление степени гидролиза крахмала
Степень гидролиза крахмала вычисляют по соотношению прогидролизованного крахмала (разница между оптической плотностью контрольного раствора и анализируемого раствора) к исходному крахмалу (оптическая плотность контрольного раствора) по формуле
![]() , (1)
, (1)
где - оптическая плотность контрольного раствора (см. 4.6.5);
- оптическая плотность анализируемого раствора (см. 4.6.4);
0,1 - коэффициент, учитывающий степень разведения крахмала, взятого на анализ.
Если степень гидролиза крахмала менее 0,02 или более 0,07, то анализ повторяют с меньшим или большим количеством основного раствора ферментного препарата (см. 4.3.2.1), используемого для приготовления рабочего раствора (см. 4.3.2.2).
4.7.2 Вычисление амилолитической активности
4.7.2.1 Вычисление амилолитической активности для препаратов бактериального происхождения
а) Амилолитическую активность для препаратов бактериальной мезофильной -амилазы
![]() , ед. АС/г или ед. АС/см
, ед. АС/г или ед. АС/см, вычисляют по формуле
![]() , (2)
, (2)
где 5,885; 0,0017 - коэффициенты, полученные при математической обработке зависимости массы прогидролизованного крахмала от массы фермента, взятого на анализ, в пересчете на 1 ч действия фермента;
- степень гидролиза крахмала (см. 4.7.1);
- масса ферментного препарата с учетом разведения, взятая на анализ, г;
- плотность ферментного препарата, определенная по ГОСТ 18995.1 (для жидкого препарата), г/см
.
б) Амилолитическую активность для препаратов термостабильной -амилазы
![]() , ед. АС/г или ед. АС/см
, ед. АС/г или ед. АС/см, вычисляют по формуле
![]() , (3)
, (3)
где 6,6138; 0,0192 - коэффициенты, полученные при математической обработке зависимости массы прогидролизованного крахмала от массы фермента, взятого на анализ, в пересчете на 1 ч действия фермента.
4.7.2.2 Вычисление амилолитической активности для препаратов грибной -амилазы
Амилолитическую активность для препаратов грибной -амилазы
, ед. АС/г или ед. АС/см
, вычисляют по формуле
![]() , (4)
, (4)
где 7,264; 0,0377 - коэффициенты, полученные при математической обработке зависимости массы прогидролизованного крахмала от массы фермента, взятого на анализ, в пересчете на 1 ч действия фермента.
4.7.2.3 Вычисления проводят до второго десятичного знака с последующим округлением до первого десятичного знака, если полученное значение амилолитической активности 100 ед. АС/г (ед. АС/см) и менее. Вычисления проводят до первого десятичного знака с последующим округлением до целого числа, если полученное значение амилолитической активности более 100 ед. АС/г (ед. АС/см
).
4.7.2.4 За окончательный результат принимают среднеарифметическое значение двух параллельных измерений, выполненных в условиях повторяемости, если выполняется условие приемлемости (7).
Границы относительной погрешности =±7% (соответствуют значению относительной расширенной неопределенности
при коэффициенте охвата
=2).
Результат анализа представляют в виде
![]() при Р=0,95, (5)
при Р=0,95, (5)
где - среднеарифметическое значение двух параллельных измерений, признанных приемлемыми, ед. АС/г (ед. АС/см
);
- границы абсолютной погрешности измерений, ед. АС/г (ед. АС/см
), вычисляют по формуле
![]() или
или ![]() . (6)
. (6)
Наименьшие разряды численных значений результата измерения и показателей точности должны быть одинаковы.
Значащих цифр численных показателей точности измерений должно быть не более двух.
4.8 Сходимость и воспроизводимость результатов
4.8.1 Результаты измерений, полученные в условиях повторяемости (сходимости), признаются удовлетворительными, если выполняется условие приемлемости
![]() , (7)
, (7)
где и
- результаты двух параллельных измерений амилолитической активности ферментного препарата, полученные в условиях повторяемости, ед. АС/г или ед. АС/см
;
0,01 - коэффициент для пересчета процентов в абсолютные значения;
- предел повторяемости (сходимости), равный 8%;
- среднеарифметическое значение двух параллельных измерений амилолитической активности, ед. АС/г или ед. АС/см
.
4.8.2 Результаты измерений, полученные в условиях воспроизводимости по ГОСТ ИСО 5725-6*, признаются удовлетворительными, если выполняется условие приемлемости
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
![]() , (8)
, (8)
где ![]() - критическая разность, равная 10%;
- критическая разность, равная 10%;
и
- окончательные результаты измерений, полученные в двух лабораториях в соответствии с методикой, ед. АС/г или ед. АС/см
;
- среднеарифметическое значение двух окончательных результатов измерений амилолитической активности, выполненных в двух разных лабораториях в условиях воспроизводимости, ед. АС/г или ед. АС/см
;
100 - коэффициент для пересчета в проценты.
5 Метод определения глюкоамилазной активности (ГлС)
5.1 Сущность метода
5.1.1 Метод основан на количественном определении глюкозы, образующейся при гидролизе крахмала глюкоамилазой при температуре 30°С, значении 4,7 ед. рН, продолжительности гидролиза 10 мин.
5.1.2 Глюкоамилазная активность (ГлС) характеризует способность ферментного препарата катализировать расщепление растворимого крахмала до глюкозы и выражается числом единиц активности в 1 г (1 см) препарата.
5.1.3 За единицу глюкоамилазной активности принимают такое количество фермента, которое способно катализировать гидролиз растворимого крахмала при температуре 30°С и значении 4,7 ед. рН, высвобождая за 1 мин 1 мкмоль глюкозы. Активность выражают в ед. ГлС/г (для порошкообразного) или ед. ГлС/см (для жидкого) ферментного препарата.
5.1.4 Количество глюкозы, образующейся в результате ферментативного гидролиза крахмала, определяют с использованием ферментов глюкозооксидазы и пероксидазы.
Фермент глюкозооксидаза катализирует окисление -D-глюкозы кислородом воздуха до глюконовой кислоты и перекиси водорода. Оба конечных продукта образуются в количествах, эквимолярных окисленной глюкозе. Перекись водорода под действием фермента пероксидазы окисляет ферроцианид калия (железистосинеродистый калий), который переходит в феррицианид калия, окрашенный в лимонно-желтый цвет, интенсивность окраски которого пропорциональна количеству глюкозы.
5.2 Средства измерений, вспомогательное оборудование, посуда, реактивы и материалы
Для определения глюкоамилазной активности применяют средства измерений, вспомогательное оборудование, посуду, материалы, реактивы, указанные в 4.2, со следующим дополнением:
Калий железистосинеродистый по ГОСТ 4207.
D(+)-глюкоза по ГОСТ 6038.
Калия гидроокись по ГОСТ 24363.
Глюкозооксидаза с активностью 100000-250000 ед./г.
Пероксидаза с активностью 250000-400000 ед./г.
5.3 Отбор и подготовка проб
5.3.1 Отбор проб
Отбор проб - по 4.3.1.
5.3.2 Подготовка проб
5.3.2.1 Приготовление основного раствора ферментного препарата
В стаканчик для взвешивания помещают анализируемую пробу сухого ферментного препарата массой (0,1000±0,0005) г или жидкого ферментного препарата массой (1,0000±0,0200) г и суспендируют в небольшом количестве дистиллированной воды. Суспензию количественно переносят в мерную колбу вместимостью 100 см, доводят объем до метки дистиллированной водой при температуре 20°С и тщательно перемешивают.
Приготовленный раствор является основным раствором ферментного препарата.
Срок хранения раствора в закрытой стеклянной посуде при температуре 20°С - не более 2 ч.
5.3.2.2 Приготовление рабочего раствора ферментного препарата
Рабочий раствор ферментного препарата готовят из основного раствора, приготовленного по 5.3.2.1, путем разведения его дистиллированной водой в мерных колбах вместимостью 100, 200 или 250 см в зависимости от предполагаемой активности таким образом, чтобы при ее определении оптическая плотность раствора после проведения реакции с глюкозооксидазным реактивом находилась в пределах градуировочной зависимости.
Рабочий раствор ферментного препарата готовят непосредственно перед проведением анализа.
5.4 Подготовка к анализу
5.4.1 Приготовление ацетатного буферного раствора молярной концентрации 1,0 моль/дм со значением 4,7 ед. рН
Приготовление ацетатного буферного раствора молярной концентрации 1 моль/дм со значением 4,7 ед. рН из растворов уксуснокислого натрия и уксусной кислоты осуществляют по 4.4.1.
5.4.2 Приготовление фосфатного буферного раствора молярной концентрации 1,0 моль/дм со значением 7,5 ед. рН
5.4.2.1 Приготовление раствора фосфорнокислого калия однозамещенного молярной концентрации 1,0 моль/дм (раствор Д)
В мерную колбу вместимостью 1000 см помещают (136,0000±0,0100) г безводного фосфорнокислого калия однозамещенного, растворяют в 300 см
дистиллированной воды, доводят до метки дистиллированной водой при температуре 20°С и перемешивают.
Срок хранения раствора в закрытой стеклянной посуде при температуре 4°С - не более 1 мес.
5.4.2.2 Приготовление раствора гидроокиси калия молярной концентрации 1,0 моль/дм (раствор Е)
В мерную колбу вместимостью 1000 см помещают (56,0000±0,0100) г гидроокиси калия, растворяют в 300 см
дистиллированной воды, доводят до метки дистиллированной водой при температуре 20°С и перемешивают.
Срок хранения раствора в закрытой стеклянной посуде при температуре 4°С - не более 1 мес.
5.4.2.3 Для приготовления фосфатного буферного раствора молярной концентрации 1,0 моль/дм с 7,5 ед. рН растворы Д и Е смешивают в равных объемах.
Величину рН проверяют на рН-метре. В случае отклонения рН фосфатного буферного раствора от 7,5 ед. рН его доводят до нужного значения растворами Д или Е.
Срок хранения буферного раствора в закрытой стеклянной посуде при температуре 4°С - не более 1 мес.
5.4.3 Приготовление глюкозооксидазного реактива
5.4.3.1 Глюкозооксидазный реактив готовят, используя раствор железистосинеродистого калия массовой доли 0,1% и раствор глюкозооксидазы.
5.4.3.2 Приготовление раствора железистосинеродистого калия массовой доли 0,1% (раствор Ж)
Навеску железистосинеродистого калия массой (0,0500±0,0010) г помещают в мерную колбу вместимостью 50 см и растворяют в дистиллированной воде. Объем раствора доводят до метки дистиллированной водой при температуре 20°С и перемешивают.
Раствор готовят непосредственно перед определением.
5.4.3.3 Приготовление раствора глюкозооксидазы (раствор И)
Навеску глюкозооксидазы массой 0,0050-0,0060 г растворяют фосфатным буферным раствором с 7,5 ед. рН, приготовленным по 5.4.2, в мерной колбе вместимостью 50 см и затем добавляют пероксидазу массой 0,0020-0,0030 г. Объем доводят до метки фосфатным буферным раствором.
Количество окисляемых ферментов с учетом их активности берут из такого расчета, чтобы в 50 см содержалось 500-600 ед. активности глюкозооксидазы, а пероксидазы - 200-300 ед. активности.
Срок хранения полученного раствора в темной склянке при температуре 4°С - не более 3 сут.
5.4.3.4 Глюкозооксидазный реактив готовят смешиванием равных объемов растворов Ж и И.
Срок хранения полученного раствора в темной склянке при температуре 4°С - не более 3 сут.
5.4.4 Приготовление основного раствора глюкозы массовой концентрации 1 мг/см
В мерную колбу вместимостью 100 см помещают (0,1000±0,0001) г глюкозы, растворяют в дистиллированной воде, тщательно перемешивают и доводят объем до метки дистиллированной водой при температуре 20°С.
Срок хранения раствора глюкозы в закрытой стеклянной посуде при температуре 4°С - не более 14 сут.
5.4.5 Приготовление рабочих растворов глюкозы
Из основного раствора глюкозы отбирают поочередно по 5, 10 и 15 см в мерные колбы вместимостью 100 см
каждая и доводят объем до метки дистиллированной водой при температуре 20°С. Полученные растворы соответствуют содержанию глюкозы 50, 100 и 150 мкг глюкозы в 1 см
соответственно.
Эти растворы используют для построения градуировочного графика.
Рабочие растворы глюкозы готовят в день построения градуировочного графика.
Растворы хранят в закрытой стеклянной посуде при температуре 20°С - не более 6 ч.
5.4.6 Построение градуировочного графика
В пробирки размером 14120 мм вносят по 1,0 см
рабочих растворов глюкозы разных концентраций (см. 5.4.5). Для каждой концентрации глюкозы используют три параллельные пробирки. В пробирки добавляют по 3 см
глюкозооксидазного реактива, приготовленного по 5.4.3.
Параллельно в контрольную пробирку (контроль на глюкозооксидазный реактив) вместо раствора глюкозы вносят 1 см дистиллированной воды.
Реакционную смесь выдерживают при температуре 20°С в течение 45 мин для проявления окраски. Интенсивность окраски реакционной смеси измеряют на фотоэлектроколориметре или спектрофотометре в диапазоне длины световой волны =400 нм в кюветах с толщиной поглощающего свет слоя 10 мм в сравнении с контрольной пробиркой на глюкозооксидазный реактив.
Рабочая зона градуировочного графика должна находиться в пределах от 0,1 до 0,3 единиц оптической плотности.
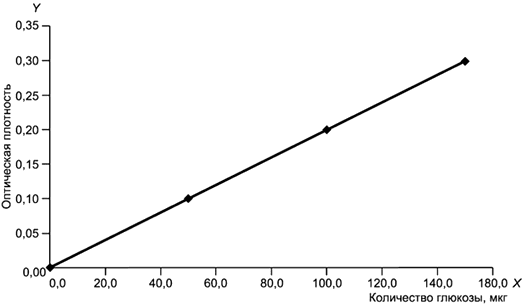
По полученным значениям строят градуировочный график зависимости оптической плотности (поглощения) от содержания глюкозы в реакционной смеси (мкг), который представлен на рисунке 1.
Для построения каждой точки градуировочного графика вычисляют среднеарифметическое значение оптической плотности трех параллельных измерений.
|
Рисунок 1
На оси абсцисс X откладывают количество глюкозы в реакционной смеси m, мкг. На оси ординат Y - соответствующие значения оптической плотности D при =400 нм.
Градуировочный график строят каждый раз при приготовлении нового глюкозооксидазного реактива (см. 5.4.3), раствора глюкозы (см. 5.4.4), а также при замене прибора.
5.4.7 Приготовление раствора крахмала массовой доли 1,0% (субстрат)
1,0000 г крахмала в пересчете на абсолютно сухое вещество (учитывая влагу, определяемую по ГОСТ 13586.5), помещают в мерную колбу вместимостью 100 см, добавляют 25 см
дистиллированной воды и перемешивают. Затем добавляют в колбу еще 25 см
дистиллированной воды, помещают колбу в кипящую водяную баню на 15-20 мин, непрерывно перемешивая содержимое до полного растворения крахмала. После этого содержимое колбы охлаждают, добавляют 10 см
ацетатного буферного раствора с 4,7 ед. рН (см. 4.4.1), объем жидкости доводят до метки дистиллированной водой при температуре 20°С и содержимое колбы перемешивают. Для полученного раствора крахмала характерна легкая опалесценция.
Раствор крахмала готовят в день проведения анализа и хранят в закрытой стеклянной посуде не более 6 ч.
5.5 Условия проведения анализа
Условия проведения анализа выполняют по 4.5.
5.6 Проведение анализа
5.6.1 Для анализа берут две параллельные навески препарата и готовят рабочие растворы ферментного препарата по 5.3.2.2. Каждое разведение рабочего раствора ферментного препарата анализируют в двух повторностях. Параллельно проводят инактивацию фермента в рабочем растворе ферментного препарата для приготовления контрольной пробы на инактивируемый фермент (см. 5.6.6).
5.6.2 В две пробирки размером 14120 мм вносят по 2,0 см
субстрата, приготовленного по 5.4.7. Содержимое пробирок прогревают в ультратермостате или водяном термостате при температуре (30,0±1,0)°С в течение 5 мин.
5.6.3 В пробирки с субстратом добавляют по 1,0 см рабочего раствора ферментного препарата, приготовленного по 5.3.2.2, предварительно прогретого в течение трех-четырех минут при температуре 30°С. Пробирки встряхивают и оставляют в ультратермостате или водяном термостате для проведения ферментативной реакции на 10 мин при температуре (30,0±1,0)°С (с точностью, определяемой по секундомеру от начала ферментативной реакции).
5.6.4 По окончании реакции отбирают 1 см смеси, вносят в чистую сухую пробирку размером 14
120 мм. Пробирку помещают в кипящую водяную баню, выдерживают в течение 4 мин по секундомеру (для остановки ферментативной реакции), после чего содержимое пробирки охлаждают в емкости с проточной холодной водой. К охлажденной смеси добавляют 3 см
глюкозооксидазного реактива, приготовленного по 5.4.3, перемешивают и выдерживают 45 мин при комнатной температуре для развития окраски.
5.6.5 Интенсивность желтой окраски соединения, образующегося в результате действия глюкозооксидазного реактива, измеряют на фотоэлектроколориметре или спектрофотометре при длине волн =400 нм в кюветах с толщиной поглощающего свет слоя 10 мм в сравнении с контрольной пробой на инактивируемый фермент (см. 5.6.6). Значение оптической плотности должно лежать в пределах, соответствующих массе глюкозы в реакционной смеси от 25 до 150 мкг.
Если при измерении интенсивности окраски в реакционной смеси полученные значения не соответствуют указанному диапазону, то анализ повторяют с меньшим или большим количеством основного раствора ферментного препарата (см. 5.3.2.1), используемого для приготовления рабочего раствора (см. 5.3.2.2).
5.6.6 Контрольная проба на инактивируемый фермент
Около 4 см рабочего раствора ферментного препарата, приготовленного по 5.3.2.2, помещают в пробирку размером 21
200 мм и выдерживают в кипящей водяной бане в течение 1 ч для инактивации фермента. Содержимое пробирки охлаждают в емкости с проточной холодной водой. К 2 см
раствора крахмала, приготовленного по 5.4.7 и помещенного в пробирку размером 14
120 мм, добавляют 1 см
охлажденного рабочего раствора ферментного препарата с инактивируемым ферментом и выдерживают в ультратермостате или водяном термостате при температуре (30,0±1,0)°С в течение 10 мин. Затем в сухую пробирку отбирают 1 см
полученной реакционной смеси и последующие операции осуществляют в соответствии с 5.6.4.
5.7 Оформление результатов
5.7.1 Глюкоамилазную активность ферментного препарата ГлС, ед. ГлС/г или ед. ГлС/см, вычисляют по формуле
![]() , (9)
, (9)
где - масса глюкозы, образовавшейся в реакционной смеси за счет действия фермента, найденная по градуировочному графику, мкг;
3 - коэффициент, учитывающий трехкратное разбавление рабочего раствора ферментного препарата непосредственно в реакционной смеси;
- масса ферментного препарата с учетом разведения по 5.3.2.2, взятая на анализ, г;
180 - молекулярная масса глюкозы, мкг/мкмоль;
10 - время гидролиза, мин;
- плотность ферментного препарата, определенная по ГОСТ 18481 (для жидкого препарата), г/см
.
Вычисления проводят до второго десятичного знака с последующим округлением до первого десятичного знака, если полученное значение глюкоамилазной активности 100 ед. ГлС/г (см) и менее. Вычисления проводят до первого десятичного знака с последующим округлением до целого числа, если полученное значение глюкоамилазной активности более 100 ед. ГлС/г (см
).
5.7.2 За окончательный результат принимают среднеарифметическое значение двух параллельных измерений, выполненных в условиях повторяемости, если выполняется условие приемлемости (12).
Границы относительной погрешности =±7% (соответствуют значению относительной расширенной неопределенности
при коэффициенте охвата
=2).
Результат анализа представляют в виде
![]() при Р=0,95, (10)
при Р=0,95, (10)
где - среднеарифметическое значение двух параллельных измерений, признанных приемлемыми, ед. ГлС/г (ед. ГлС/см
);
- границы абсолютной погрешности измерений, ед. ГлС/г (ед. ГлС/см
), вычисляемые по формуле
![]() или
или ![]() . (11)
. (11)
Наименьшие разряды численных значений результата измерения и показателей точности должны быть одинаковы.
Значащих цифр численных показателей точности измерений должно быть не более двух.
5.8 Сходимость и воспроизводимость результатов
5.8.1 Результаты измерений, полученные в условиях повторяемости (сходимости), признаются удовлетворительными, если выполняется условие приемлемости
![]() , (12)
, (12)
где и
- результаты двух параллельных измерений глюкоамилазной активности ферментного препарата, полученные в условиях повторяемости, ед. ГлС/г или ед. ГлС/см
;
0,01 - коэффициент для пересчета процентов в абсолютные значения;
- предел повторяемости (сходимости), равный 8%;
- среднеарифметическое значение двух параллельных измерений глюкоамилазной активности, ед. ГлС/г или ед. ГлС/см
.
5.8.2 Результаты измерений, полученные в условиях воспроизводимости по ГОСТ ИСО 5725-6, признаются удовлетворительными, если выполняется условие приемлемости
![]() , (13)
, (13)
где ![]() - критическая разность, равная 10%;
- критическая разность, равная 10%;
и
- окончательные результаты измерений, полученные в двух лабораториях в соответствии с методикой, ед. ГлС/г или ед. ГлС/см
;
- среднеарифметическое значение двух окончательных результатов измерений глюкоамилазной активности, выполненных в двух разных лабораториях в условиях воспроизводимости, ед. ГлС/г или ед. ГлС/см
;
100 - коэффициент для пересчета в проценты.
6 Требования безопасности
6.1 Условия безопасного проведения работ
При выполнении измерений необходимо соблюдать правила техники безопасности при работе в лаборатории с химическими веществами по ГОСТ 12.1.007 и ГОСТ 12.4.103, требования электробезопасности при работе с электроустановками - по ГОСТ 12.2.007.0 и в соответствии с требованиями, изложенными в инструкциях по эксплуатации оборудования. Требования пожарной безопасности - по ГОСТ 12.1.004 и ГОСТ 12.1.018.
Помещение, где проводят работы с реактивами, должно быть оснащено приточно-вытяжной вентиляцией по ГОСТ 12.4.021.
Содержание вредных веществ в воздухе не должно превышать допустимых значений по ГОСТ 12.1.005.
Остатки проб ферментных препаратов утилизируют в порядке, установленном в руководстве по качеству в лаборатории.
6.2 Требования к квалификации персонала
К выполнению измерений, обработке и оформлению результатов допускаются инженеры-химики и лаборанты, имеющие среднее специальное образование, опыт работы с данным оборудованием и владеющие настоящим методом.
Приложение А
(справочное)
Системные названия амилолитических ферментов
1 Амилолитическую активность ферментных препаратов (ФП) обеспечивают ферменты: -амилаза и глюкоамилаза, катализирующие гидролиз крахмала.
2 Системные названия ферментов:
- -1,4-глюкан-4-глюканогидролаза (ЕС 3.2.1.1) [1] -
-амилаза - фермент с эндогенным механизмом действия, катализирующий гидролиз
-1,4-гликозидных связей крахмала с образованием
-декстринов, олигосахаридов и мальтозы;
- -1,4-глюкан-глюкогидролаза (ЕС 3.2.1.3) [1] - глюкоамилаза - фермент с экзогенным механизмом действия, катализирующий гидролиз
-1,4- и
-1,6-гликозидных связей крахмала, декстринов, олигосахаридов, последовательно отщепляя при этом остатки молекулы глюкозы от нередуцирующих концов субстрата с образованием глюкозы.
Библиография
[1] | Номенклатура ферментов, рекомендации номенклатурного комитета IUB. Нью-Йорк, Академическое изд., 1984 (Enzyme Nomenclature, recommendations of the nomenclature Committee of the IUB, N.Y, AcademicPress, 1984) |
УДК 577.15:543.06:006.354 | МКС 07.100.30 |
Ключевые слова: препараты ферментные, активность | |
Электронный текст документа
и сверен по:
, 2018