МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ (МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ГОСТ
EN 16956—
2020
ПРОДУКЦИЯ ПАРФЮМЕРНО-КОСМЕТИЧЕСКАЯ ДЛЯ ОТБЕЛИВАНИЯ КОЖИ
Аналитические методы.
Обнаружение и количественное определение гидрохинона, эфиров гидрохинона и кортикостероидов методом ВЭЖХ/УФ
(EN 16956:2017, Cosmetics — Analytical methods — HPLC/UV method for the identification and assay of hydroquinone, ethers of hydroquinone and corticosteroids in skin whitening cosmetic products, IDT)
Издание официальное
Москва Российский институт стандартизации 2024
ГОСТ EN 16956—2020
Предисловие
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН республиканским унитарным предприятием «Белорусский государственный институт метрологии» (БелГИМ) на основе собственного перевода на русский язык англоязычной версии стандарта, указанного в пункте 5
2 ВНЕСЕН Государственным комитетом по стандартизации Республики Беларусь
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации по результатам голосования в АИС МГС (протокол от 30 января 2020 г. № 126-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166)004—97 | Код страны по МК (ИСО 3166) 004—97 | Сокращенное наименование национального органа по стандартизации |
Армения | АМ | ЗАО «Национальный орган по стандартизации и метрологии» Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
Таджикистан | TJ | Таджи кета н да рт |
Узбекистан | uz | Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 27 декабря 2023 г. № 1682-ст межгосударственный стандарт ГОСТ EN 16956—2020 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2025 г. с правом досрочного применения
5 Настоящий стандарт идентичен европейскому стандарту EN 16956:2017 «Косметика. Аналитические методы. Метод ВЭЖХ с УФ-детектированием для идентификации и анализа гидрохинона, эфиров гидрохинона и кортикостероидов в косметической продукции для отбеливания кожи» («Cosmetics— Analytical methods — HPLC/UV method for the identification and assay of hydroquinone, ethers of hydroquinone and corticosteroids in skin whitening cosmetic products», IDT).
Европейский стандарт разработан техническим комитетом CEN/TC 392 «Косметика» Европейского комитета по стандартизации (CEN).
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта с целью применения обобщающего понятия в наименовании стандарта в соответствии с ГОСТ 1.5 (подраздел 3.6)
6 ВВЕДЕН ВПЕРВЫЕ
II
ГОСТ EN 16956—2020
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случае пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге «Межгосударственные стандарты»
© Оформление. ФГБУ «Институт стандартизации», 2024
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
III
ГОСТ EN 16956—2020
Содержание
Введение.............................................................................V
1 Область применения..................................................................1
2 Сущность метода.....................................................................1
3 Реактивы............................................................................1
4 Основное и вспомогательное оборудование...............................................4
5 Методика............................................................................
5.1 Приготовление проб............................................................
5.2 Хроматографические условия....................................................
5.3 Обнаружение..................................................................
6 Определение.........................................................................
6.1 Идентификация................................................................
6.2 Количественное определение....................................................
6.3 Представление результатов......................................................
7 Протокол испытаний...................................................................
omooicnoiuicnui
Приложение А (справочное) Примеры полученных хроматограмм..............................7
Приложение В (справочное) Данные валидации метода количественного определения гидрохинона и его трех эфиров..........................................................8
Приложение С (справочное) Данные валидации метода количественного определения четырех наиболее часто встречающихся кортикостероидов.............................12
Приложение D (обязательное) Скрининговые методы для идентификации гидрохинона, трех эфиров гидрохинона и 38 кортикостероидов..............................17
Библиография........................................................................26
IV
ГОСТ EN 16956—2020
Введение
Гидрохинон не допускается к использованию в парфюмерно-косметической продукции для отбеливания и депигментации пятен на коже. Из-за цитотоксического действия использование гидрохинона регулируется. Гидрохинон и три его эфира (монометиловый эфир гидрохинона (ММЕ), моноэтиловый эфир гидрохинона (МЕЕ) и монобензиловый эфир гидрохинона (МВЕ)) регулируются Регламентом (ЕС) № 1223/2009 Европейского парламента и Совета от 30 ноября 2009 г. по косметической продукции. В настоящее время использование данных веществ в отбеливающей продукции для кожи запрещено.
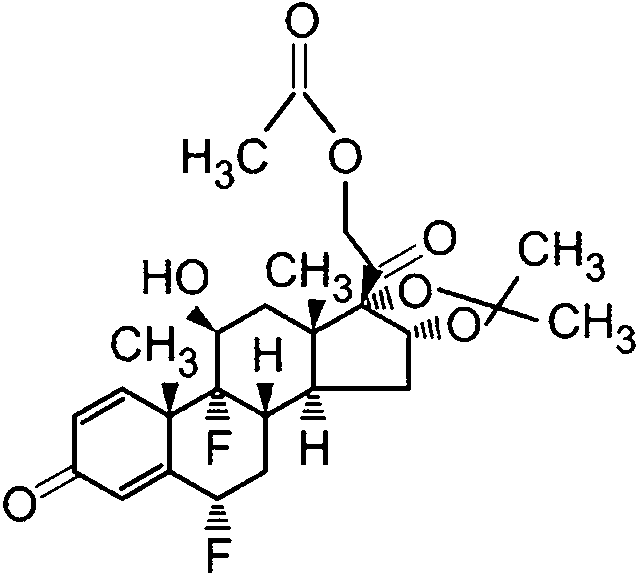
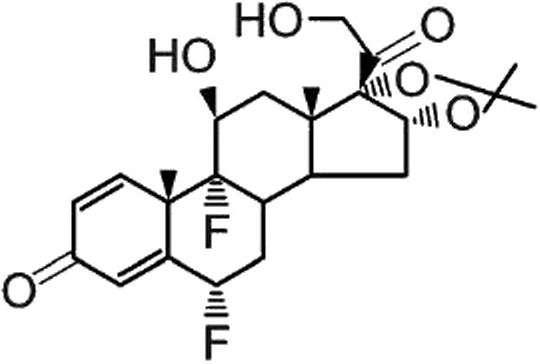
Поскольку депигментация является побочным эффектом местно применяемых стероидов, кортикостероиды могут быть использованы в качестве соединений в незаконно реализуемой парфюмернокосметической продукции. К кортикостероидам, наиболее часто встречающимся в данной продукции, относятся клобетазола пропионат, флуоцинонид, бетаметазона дипропионат и флуоцинолона ацетонид (см. рисунок 1). Кортикостероиды приведены в Регламенте (ЕС) № 1223/2009 по косметической продукции в приложении 2 «Перечень веществ, запрещенных к использованию в парфюмерно-косметической продукции» (ссылочный номер 300), их использование в парфюмерно-косметической продукции запрещено.
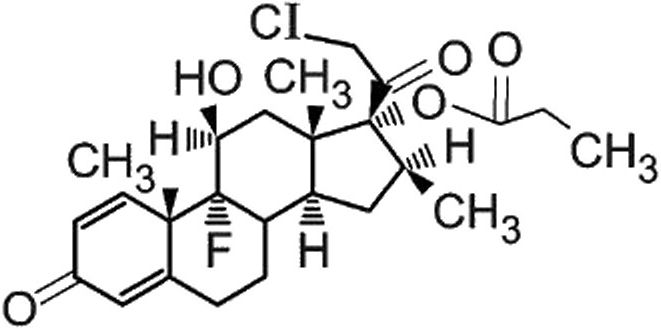

а) Клобетазола пропионат
Ь) Флуоцинонид
с) Бетаметазона дипропионат
d) Флуоцинолона ацетонид
Рисунок 1 — Кортикостероиды, содержащиеся в незаконно реализуемой парфюмерно-косметической продукции
Все указанные вещества работают по тому же принципу, что и гидрохинон, который главным образом ингибирует синтез меланина.
Косметическая директива 95/32/ЕС [2] описывает аналитический метод для определения гидрохинона и трех его эфиров (монометилового эфира гидрохинона (ММЕ), моноэтилового эфира гидрохинона (МЕЕ) и монобензилового эфира гидрохинона (МВЕ)) в парфюмерно-косметической продукции для осветления кожи. С целью усовершенствования и распространения официального метода идентификации и определения кортикостероидов в парфюмерно-косметической продукции настоящий стандарт устанавливает метод ВЭЖХ/УФ для идентификации и определения гидрохинона, эфиров гидрохинона и кортикостероидов в парфюмерно-косметической продукции.
V
ГОСТЕМ 16956—2020
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКЦИЯ ПАРФЮМЕРНО-КОСМЕТИЧЕСКАЯ ДЛЯ ОТБЕЛИВАНИЯ КОЖИ
Аналитические методы. Обнаружение и количественное определение гидрохинона, эфиров гидрохинона и кортикостероидов методом ВЭЖХ/УФ
Skin whitening cosmetics.
Analytical methods.
Detection and quantification of hydroquinone, esters hydroquinone and corticosteroids by method HPLC/UV
Дата введения — 2025—01—01 с правом досрочного применения
1 Область применения
Настоящий стандарт устанавливает метод высокоэффективной жидкостной хроматографии с детектированием в ультрафиолетовой области спектра (ВЭЖХ/УФ) для идентификации и количественного определения гидрохинона, трех эфиров гидрохинона и четырех кортикостероидов, которые наиболее часто обнаруживаются в незаконно реализуемой отбеливающей парфюмерно-косметической продукции для кожи: клобетазола пропионат, флуоцинонид, бетаметазона дипропинат, флуоцинолона ацетонид.
Настоящий стандарт также устанавливает метод ВЭЖХ/УФ для идентификации 38 кортикостероидов, которые могут быть обнаружены в отбеливающей парфюмерно-косметической продукции для кожи (см. приложение D).
Данный стандарт не предназначен для искусственных ногтей и мыла.
2 Сущность метода
Пробу экстрагируют смесью вода/метанол и осторожно нагревают для экстракции соединений, содержащихся в продукции. Полученную смесь фильтруют. Количественное определение содержащихся в растворе соединений проводят с помощью обращенно-фазовой ВЭЖХ с детектированием диодноматричным детектором (DAD).
3 Реактивы
Если не установлено иное, то должны использоваться химические вещества аналитической степени чистоты; вода должна быть дистиллированная или аналогичной чистоты. Под раствором следует понимать водный раствор, если не установлено иное.
3.1 метанол для ВЭЖХ.
3.2 вода для ВЭЖХ.
3.3 раствор для экстракции, метанол/вода (1:1).
Смешивают 500 см3 метанола и 500 см3 воды (см. 3.2) в конической колбе вместимостью 1 000 см3.
3.4 определяемые соединения (см. таблицу 1).
Издание официальное
1
ГОСТ EN 16956—2020
Таблица 1 — Определяемые соединения
Соединение | CAS | Изготовитель3) | Чистота, % | Используемый метод, раздел |
Алклометазона дипропионат (ACD) | 66734-13-2 | USP | 99,2 | Приложение D |
Амцинонид (АМС) | 51022-69-6 | Sigma | 97,9 | Приложение D |
Беклометазона дипропионат (BCD) | 5534-09-8 | Sigma | 99,0 | Приложение D |
Бетаметазона ацетат (ВМА) | 987-24-6 | Sigma | 98,6 | Приложение D |
Бетаметазон (ВМ) | 378-44-9 | Sigma | 98,4 | Приложение D |
Бетаметазона дипропионат (BMD) | 5593-20-4 | Sigma | 98,6 | Приложение D, раздел 2 |
Бетаметазона валерат (BMV) | 2152-44-5 | Sigma | 98,1 | Приложение D |
Будесонид (BUD) | 51333-22-3 | Ph. Eur. | 99,7 | Приложение D |
Клобетазола пропионат (СР) | 25122-46-7 | Sigma | 98,8 | Приложение D, раздел 2 |
Клокортолона пивалат (CLP) | 34097-16-0 | USP | 98,9 | Приложение D |
Кортизон (CS) | 53-06-5 | Sigma | 98,3 | Приложение D |
Дезонид (DSN) | 638-94-8 | Cil | 98,0 | Приложение D |
Дезоксиметазон (DXM) | 382-67-2 | Sigma | 99,0 | Приложение D |
Дексаметазона фосфат (DMPS) | 2392-39-4 | Sigma | 100,2 | Приложение D |
Дексаметазона ацетат (DMA) | 1177-87-3 | Sigma | 99,0 | Приложение D |
Дифлоразона диацетат (DFD) | 33564-31-7 | USP | 99,8 | Приложение D |
Дифлукортолона валерат (DFCV) | 59198-70-8 | Schering | / | Приложение D |
Дифлупреднат (DFP) | 23674-86-4 | Sigma | 99,5 | Приложение D |
Флуметазона пивалат (FMP) | 2002-29-1 | Farmabios | 100,4 | Приложение D |
Флуоцинолона ацетонид (FCA) | 67-73-2 | Sigma | 99,6 | Приложение D, раздел 2 |
Флуоцинонид (FCAA) | 356-12-7 | Sigma | 99,0 | Приложение D, раздел 2 |
Флуокортолона гексаноат (FCH) | 303-40-2 | Schering | / | Приложение D |
Флуокортолона пивалат(РСР) | 29205-06-9 | Ph. Eur. | / | Приложение D |
Флурандренолид (FDL) | 1524-88-5 | USP | / | Приложение D |
Хальцинонид (HAL) | 3093-35-4 | Sigma | 99,0 | Приложение D |
Гидрокортизон (НС) | 3093-25-4 | Sigma | 98,0 | Приложение D |
Гидрокортизона ацепонат (НСАР) | 74050-20-7 | Toronto Research Chemicals | 98,0 | Приложение D |
Гидрокортизона бутират (НСВ) | 13609-67-1 | Sigma | 99,1 | Приложение D |
Гидрокортизона валерат (HCV) | 57524-89-7 | Sigma | 99,0 | Приложение D |
Метилпреднизолона ацетат (MPLA) | 53-36-1 | USP | 99,8 | Приложение D |
Мометазона фуроат (MMF) | 83919-23-7 | USP | 99,8 | Приложение D |
2
Окончание таблицы 1
ГОСТ EN 16956—2020
Соединение | CAS | Изготовитель3) | Чистота, % | Используемый метод, раздел |
Предникарбат (PCN) | 73771-04-7 | Ph. Eur. | / | Приложение D |
Преднизолон (PL) | 50-24-8 | Aventis Pharma | 98,0 | Приложение D |
Преднизолона ацетат (PLA) | 52-21-1 | Dr Ehrenstrofer | 99,4 | Приложение D |
Преднизолона гексаноат (PLH) | 69164-69-8 | Schering | / | Приложение D |
Преднизолона сульфобензоат Na (PLSB) | 630-67-1 | Pharmaceutical drug | / | Приложение D |
Триамцинолон (TRI) | 124-94-7 | Sigma | 98,2 | Приложение D |
Триамцинолона ацетонид (TRA) | 76-25-5 | Sigma | 99,6 | Приложение D |
Гидрохинон (HQ) | 123-31-9 | Sigma | >99,9 | Приложение D, раздел 2 |
Монометиловый эфир гидрохинона (ММЕ) | 150-76-5 | Sigma | 99,7 | Приложение D, раздел 2 |
Моноэтиловый эфир гидрохинона (МЕЕ) | 622-62-8 | Sigma | 99,9 | Приложение D, раздел 2 |
Монобензиловый эфир гидрохинона (МВЕ) | 103-16-2 | Sigma | 99,5 | Приложение D, раздел 2 |
а) Примеры изготовителей. | ||||
3.5 подвижная фаза для ВЭЖХ, элюент А: метанол (см. 3.1); элюент В: вода (см. 3.2).
3.6 Стандартные растворы
Для приготовления исходных растворов в качестве растворителя используют метанол (см. 3.1). Стандартные растворы готовятся путем разбавления раствором для экстракции (см. 3.3).
3.6.1 Исходный стандартный раствор гидрохинона и его трех эфиров (с концентрацией от 1,2 до 2,4 мг/см3)
Взвешивают в мерной колбе вместимостью 25 см3 приблизительно:
- 0,03 г гидрохинона;
- 0,04 г монометилового эфира гидрохинона;
- 0,05 г моноэтилового эфира гидрохинона;
- 0,06 г монобензилового эфира гидрохинона.
Сначала вещества растворяют в 15 см3 метанола (см. 3.1), используя при необходимости лабораторный шейкер, а затем доводят объем раствора метанолом до метки. Раствор готовят ежедневно.
3.6.2 Исходные стандартные растворы (1 мг/см3) и рабочий стандартный раствор четырех наиболее часто обнаруживаемых кортикостероидов (10 мкг/см3)
Взвешивают каждое вещество отдельно в мерной колбе вместимостью 10 см3:
- 10 мг бетаметазона дипропионата;
-10 мг клобетазола пропионата;
-10 мг флуоцинонида;
- 10 мг флуоцинолона ацетонида.
Сначала вещества растворяют в 5 см3 метанола (см. 3.1), используя при необходимости лабораторный шейкер, а затем доводят объем раствора метанолом до метки. Данные четыре раствора могут храниться в течение 6 мес при температуре 4 °C.
Затем готовят смесь растворов 4 кортикостероидов, вводя по 1 см3 каждого исходного стандартного раствора стеклянной пипеткой в мерную колбу вместимостью 100 см3. Затем доводят объем рас-
3
ГОСТ EN 16956—2020
твора смесью метанол/вода (см. 3.3) до метки. Данный раствор может храниться в течение 6 нед при температуре 4 °C.
3.6.3 Градуировочные растворы гидрохинона и его 3 эфиров
Градуировочный раствор должен быть свежеприготовленным (см. таблицу 2). С помощью стеклянной пипетки вводят объем исходного стандартного раствора (см. 3.6.1) в мерную колбу и доводят объем смесью метанол/вода (см. 3.3) до метки.
Таблица 2 — Градуировочные растворы
Номер градуировочного раствора | Объем исходного стандартного раствора, см3 | Вместимость колбы, см3 | Концентрации градуировочных растворов, мкг/см3 |
1 | 0,5 | 100 | 6—8—10—12 |
2 | 1,0 | 50 | 24—32—40—48 |
3 | 5,0 | 120—160—200—240 | |
4 | 10,0 | 240—320—400—480 | |
5 | 20,0 | 480—640—800—960 |
3.6.4 Градуировочные растворы четырех наиболее часто обнаруживаемых кортикостероидов
Градуировочные растворы должны быть свежеприготовленными (см. таблицу 3). С помощью стеклянной пипетки вводят объем исходного стандартного раствора (см. 3.6.2) в мерную колбу и доводят объем смесью метанол/вода (см. 3.3) до метки.
Таблица 3 — Градуировочные растворы
Номер градуировочного раствора | Объем исходного стандартного раствора, см3 | Вместимость колбы,см3 | Концентрация градуировочных растворов, мкг/см3 |
6 | 5 | 100 | 0,5 |
7 | 5 | 50 | 1.0 |
8 | 10 | 2.0 | |
9 | 20 | 4.0 | |
10 | 25 | 5,0 |
4 Основное и вспомогательное оборудование
В дополнение к обычно используемому лабораторному оборудованию требуется следующее оборудование:
4.1 аналитические весы с точностью взвешивания до 0,1 мг.
4.2 лабораторный шейкер.
4.3 водяная баня, обеспечивающая нагревание при 60 °C.
4.4 высокоэффективный жидкостный хроматограф, состоящий из:
- устройства ввода проб;
- насоса, позволяющего формировать градиент элюирования;
- дегазатора;
- термостата колонок;
- детектора с фотодиодной матрицей;
- программного обеспечения.
4.5 мембранный фильтр для фильтрования пробы, например из полипропилена, размер пор 0,45 мкм.
4.6 аналитическая разделительная колонка, например Thermo Fisher Scientific Hypurity Aquastar C18)1\ длиной 0,25 м, внутренним диаметром 4,6 мм, с диаметром частиц 5 мкм.
1) Это пример продукции, имеющейся в продаже. Информация дана для удобства пользователей настоящего стандарта и не является рекламой Европейского комитета по стандартизации этого продукта. Аналогичная продукция может быть использована, если доказано, что она обеспечивает получение тех же результатов.
4
ГОСТ EN 16956—2020
4.7 бумажный фильтр для фильтрования проб, например фильтр средней скорости фильтрации диаметром 210 мм.
5 Методика
5.1 Приготовление проб
Взвешивают точно 0,5 г пробы в мерной колбе вместимостью 100 см3. Добавляют 50 см3 раствора для экстракции (см. 3.3) и встряхивают колбу при помощи лабораторного шейкера до получения однородной суспензии. Помещают смесь на водяную баню при 60 °C на 5 мин для ускорения растворения. При необходимости встряхивают его при помощи лабораторного шейкера еще раз. Охлаждают колбу до комнатной температуры и доводят объем раствора до 100 см3 раствором для экстракции (см. 3.3). Фильтруют экстракт через бумажный фильтр, а затем через мембранный фильтр (0,45 мкм). В течение следующих 24 ч фильтрат вводят в хроматограф в соответствии с 5.2.
5.2 Хроматографические условия
При использовании хроматографа (см. 4.4) и колонки (см. 4.6) были установлены следующие параметры:
- объемная скорость потока (подвижной фазы): 1,5 см3/мин;
- время анализа: 25 мин;
- объем вводимой пробы: 10 мм3;
- температура термостата: (36 ± 2) °C;
- обнаружение: диодно-матричный детектор с длиной волны: 240 нм для кортикостероидов, 295 нм для гидрохинона и его эфиров;
- подвижная фаза:
- элюент А: метанол;
- элюент В: вода.
В таблице 4 приведены условия градиентного разделения.
Таблица 4 — Условия для градиентного разделения
Время, мин | Объемная доля элюента А, % | Объемная доля элюента В, % |
0 | 5 | 95 |
20 | 80 | 20 |
21 | 5 | 95 |
25 | 5 | 95 |
5.3 Обнаружение
Обнаружение и количественное определение может быть выполнено с помощью DAD (X = 240 нм и X = 295 нм).
6 Определение
6.1 Идентификация
Гидрохинон, эфиры гидрохинона и кортикостероиды идентифицируются путем сравнения времени удерживания и УФ-спектров пробы с аналогичными параметрами стандартных растворов соединений.
В таблице 5 приведены параметры для идентификации соединений с использованием хроматографических условий, указанных в 5.2. В приложении А приведены хроматограммы градуировочных растворов при двух длинах волн.
5
ГОСТ EN 16956—2020
Таблица 5 — Хроматографические параметры для идентификации соединений
Соединения | Rt, мин | X, нм |
Гидрохинон | 4,24 | 295 |
Монометиловый эфир гидрохинона (ММЕ) | 9,34 | 295 |
Моноэтиловый эфир гидрохинона (МЕЕ) | 12,08 | 295 |
Монобензиловый эфир гидрохинона (МВЕ) | 17,54 | 295 |
Флуоцинолона ацетонид (FCA) | 17,73 | 240 |
Флуоцинонид (FCAA) | 19,60 | 240 |
Клобетазола пропионат (СР) | 20,55 | 240 |
Бетаметазона дипропионат (BMD) | 21,44 | 240 |
6.2 Количественное определение
Количественное определение проводится посредством линейной регрессии, основанной на площадях пиков внешних стандартных растворов. Градуировочная кривая должна быть линейной, а коэффициент корреляции должен быть не менее 0,995.
Массовую долю соединения, г/100 г, в пробе вычисляют по следующей формуле:
С - V-100 ■ F
R " 1000 • SW ’
где R — значение концентрации, % (г/100 г);
С — концентрация соединений, определенная в растворе пробы посредством ВЭЖХ, г/дм3 или мг/см3;
V — объем экстракта пробы, см3;
SW — масса навески пробы, г;
F— возможный коэффициент разбавления.
6.3 Представление результатов
Массовая доля выражается в процентах или г/100 г и округляется до ближайшей десятой доли процента.
В приложениях В и С приведены данные валидации.
7 Протокол испытаний
Протокол испытаний должен содержать данные в соответствии с EN ISO/IEC 17025 [1] или по крайней мере следующие данные:
а) всю информацию, необходимую для идентификации пробы (вид пробы, происхождение пробы, обозначение);
Ь) ссылку на настоящий стандарт;
с) дату и метод отбора проб (если известно);
d) дату получения;
е) дату испытания;
f) результаты испытаний и единицы, в которых они были выражены;
д) любые особенности, выявленные в ходе испытания;
h) любые операции, не указанные в методе или считающиеся необязательными, но способные повлиять на результаты.
6
ГОСТ EN 16956—2020
Приложение А (справочное)
Примеры полученных хроматограмм
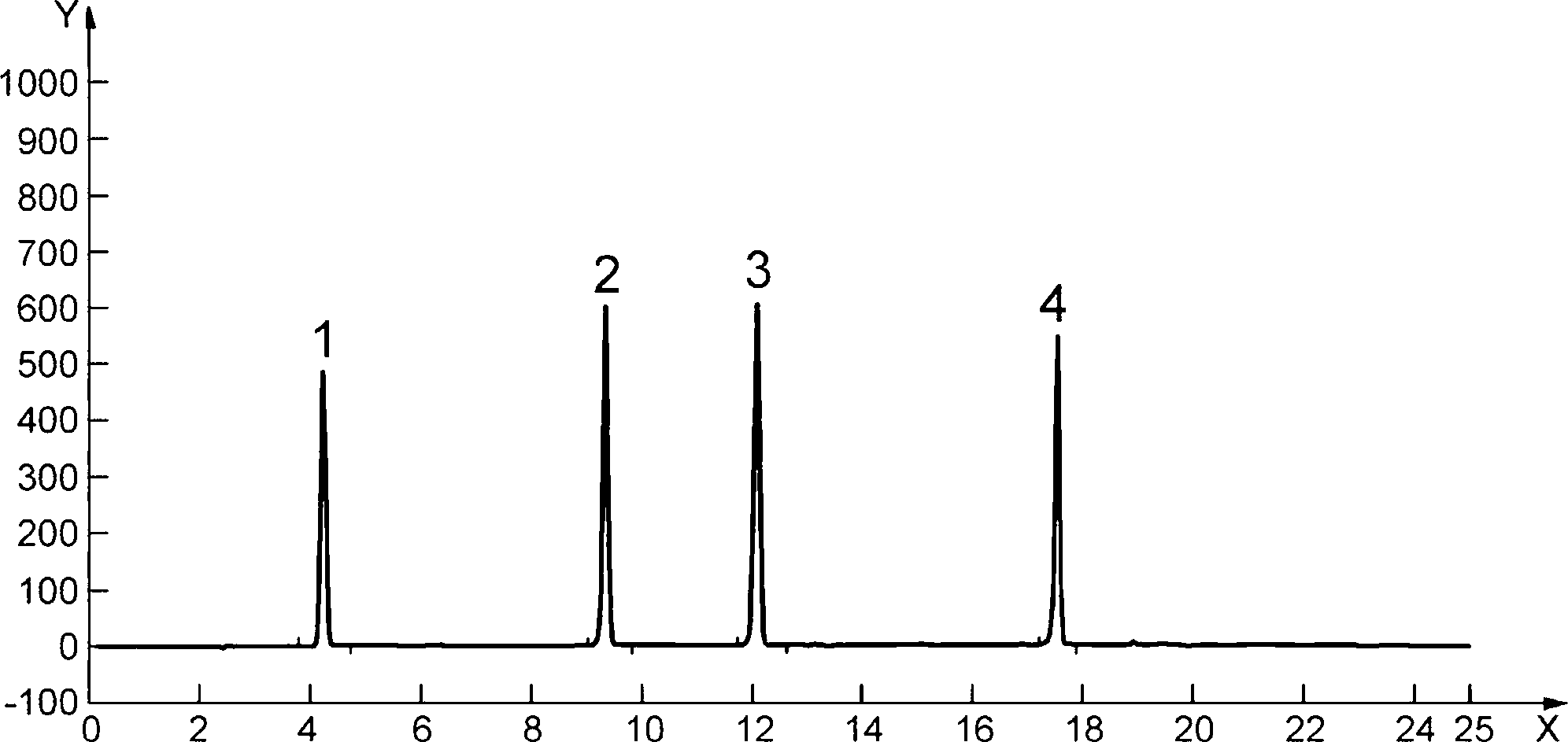
Условные обозначения:
X — время удерживания, мин;
Y — оптическая плотность (ЕОП);
1 — гидрохинон (4,235 мин);
2 — метиловый эфир гидрохинона (9,337 мин);
3 — этиловый эфир гидрохинона (12,081 мин);
4 — бензиловый эфир гидрохинона (17,544 мин)
Рисунок А.1 — Пример хроматограммы, полученной для стандартных растворов гидрохинона и его простых эфиров с концентрацией от 0,5 до 1 мг/см3
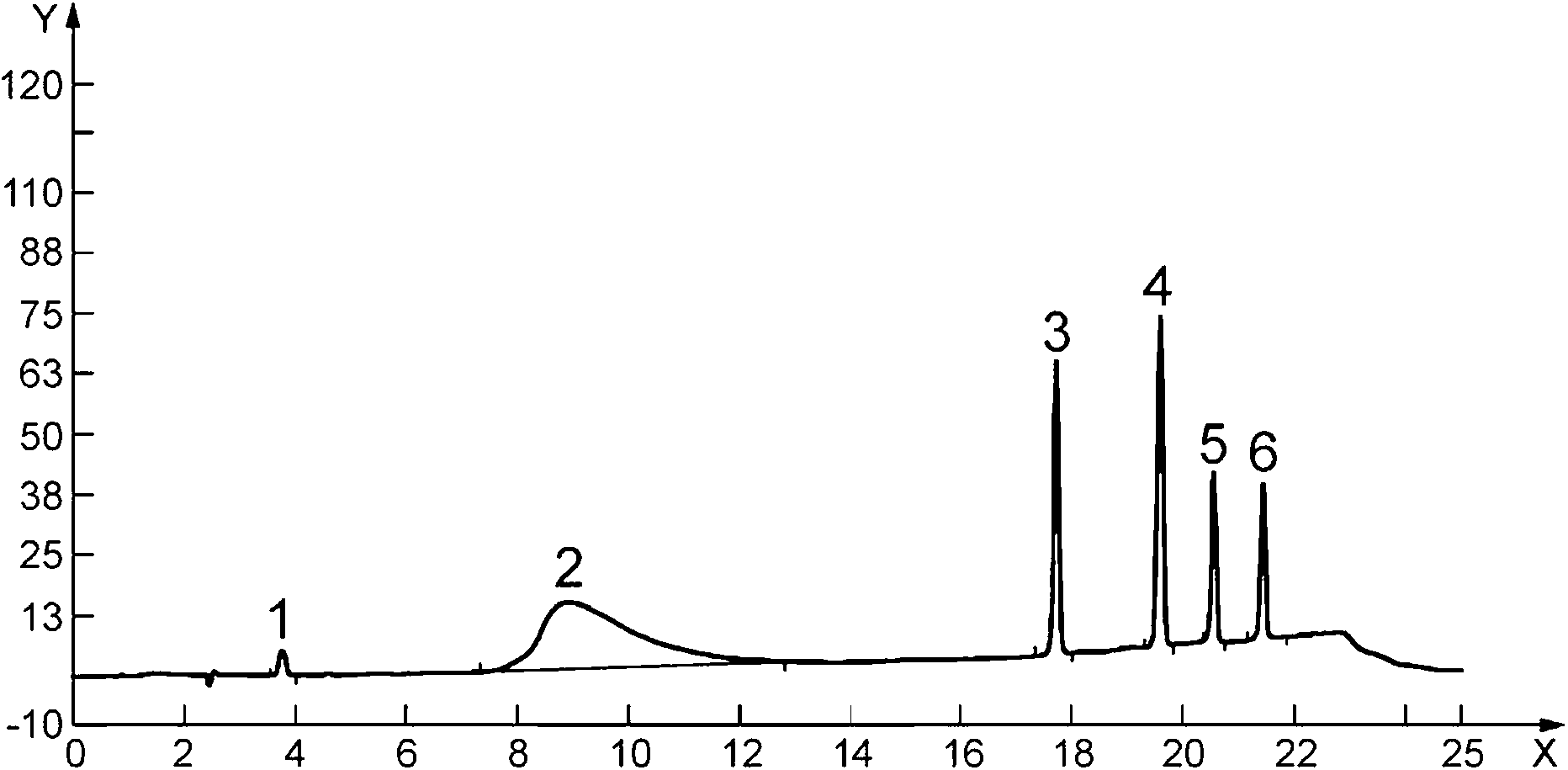
Условные обозначения:
X — время удерживания, мин;
Y — оптическая плотность (ЕОП);
1 — арбутин (3,765 мин);
2 — койевая кислота (8,898 мин);
3 — флуоцинолона ацетонид (17,726 мин);
4 —флуоцинонид (19,597 мин);
5 — клобетазола пропионат (20,551 мин);
6 — бетаметазона дипропионат (21,438 мин)
Рисунок А.2 — Пример хроматограммы, полученной для стандартных растворов кортикостероидов с концентрацией 5 мкг/см3
7
ГОСТ EN 16956—2020
Приложение В (справочное)
Данные валидации метода количественного определения гидрохинона и его трех эфиров
Данные валидации были получены Объединенной службой лабораторий (SCL) Министерства экономики и финансов — Лаборатория Lyon-Oullins — Секция Косметика.
Предел обнаружения: 0,01 % (m/m), определен при использовании стандартных растворов на трех хроматографах.
Yj
4
3

-2,51____________________I____________________I____________________I____________________I____________________I____________________I____________________I____________________I____________________1____________________I____________________I____________________I__________I_____________
0 2 4 6 8 10 12 14 16 18 20 22 25 X
Условные обозначения:
X — время удерживания, мин;
Y — оптическая плотность (ЕОП);
1 — гидрохинон (4,299 мин);
2 — метиловый эфир гидрохинона (9,458 мин);
3 — этиловый эфир гидрохинона (12,214 мин);
4 — бензиловый эфир гидрохинона (17,665 мин)
Рисунок В.1 — Хроматограмма стандартного раствора гидрохинона и его трех эфиров с концентрацией 0,01% (m/m)
Таблица В.1 — Предел количественного определения LOQ подтвержден испытаниями на образцах с точно измеренным количеством добавленных соединений четырьмя аналитиками на трех хроматографах в течение 5 дней
Соединение | Образец: отбеливающий крем | Образец: отбеливающее масло | ||||
LOQ, % (m/m) | RSD* повторяемости, % | RSD внутренней воспроизводимости, % | LOQ, % (m/m) | RSD повторяемости, % | RSD внутренней воспроизводимости, % | |
Гидрохинон | 0,1 | 2,3 | 12,6 | 0,1 | 2,8 | 25,3 |
Метиловый эфир** | 0,2 | 0,0 | 9,2 | 0,2 | 3,0 | 27,1 |
Этиловый эфир** | 0,2 | 2,2 | 10,9 | 0,2 | 2,6 | 21,0 |
Бензиловый эфир** | 0,3 | 1,3 | 7,0 | 0,2 | 3,5 | 15,6 |
Здесь и далее по тексту RSD (Relative Standard Deviation) — относительное стандартное отклонение.
** Здесь и далее по тексту под метиловым эфиром, этиловым эфиром, бензиловым эфиром подразумевается монометиловый эфир гидрохинона, моноэтиловый эфир гидрохинона, монобензиловый эфир гидрохинона.
8
ГОСТ EN 16956—2020
Таблица В.2 — Линейность, подтвержденная для восьми уровней градуировки (стандартных растворов) четырьмя аналитиками на двух различных хроматографах (№ 2 и № 3) в течение 5 дней
Соединение | Полученное максимальное относительное смещение, % | |||||||
Уровень 1 (LOQ) | Уровень 2 | Уровень 3 | Уровень 4 | Уровень 5 | Уровень 6 | Уровень 7 | Уровень 8 | |
Гидрохинон | 6,3 мкг/см3 | 12,5 мкг/см3 | 25,0 мкг/см3 | 49,9 мкг/см3 | 124,9 мкг/см3 | 249,7 мкг/см3 | 374,6 мкг/см3 | 499,4 мкг/см3 |
27,7 | 10,7 | 3,7 | -2,9 | -1,6 | 1,7 | 1,5 | -0,6 | |
Метиловый эфир | 8,1 мкг/см3 | 16,1 мкг/см3 | 32,2 мкг/см3 | 64,4 мкг/см3 | 161,1 мкг/см3 | 322,1 мкг/см3 | 483,2 мкг/см3 | 644,2 мкг/см3 |
11,1 | -7,5 | -2,5 | -1,7 | 1,8 | 1,8 | 1,5 | -0,8 | |
Этиловый эфир | 10,1 мкг/см3 | 20,2 мкг/см3 | 40,5 мкг/см3 | 81 мкг/см3 | 202,5 мкг/см3 | 405,1 мкг/см3 | 607,6 мкг/см3 | 810,2 мкг/см3 |
-11,0 | -7,0 | 3,0 | -1,8 | 1,8 | 1,7 | 1,5 | -0,8 | |
Бензиловый эфир | 12,2 мкг/см3 | 24,5 мкг/см3 | 48,9 мкг/см3 | 97,9 мкг/см3 | 244,8 мкг/см3 | 489,6 мкг/см3 | 734,3 мкг/см3 | 979,1 мкг/см3 |
-10,9 | -9,0 | -5,6 | -1,8 | 2,5 | 1,6 | 1,5 | -0,8 | |
Концентрации (мкг/см3) представляют собой усредненное значение пяти различных значений, полученных каждый день. Все анализируемые соединения были подвергнуты тесту Фишера.
Таблица В.З — Линейность, подтвержденная для пяти уровней градуировки (стандартных растворов) четырьмя аналитиками на двух различных хроматографах (№ 1 и № 2) в течение 5 дней
Соединение | Полученное максимальное относительное смещение, % | ||||
Уровень 1 (LOQ) | Уровень 2 | Уровень 3 | Уровень 4 | Уровень 5 | |
Гидрохинон | 6,4 мкг/см3 | 25,5 мкг/см3 | 127,7 мкг/см3 | 251,7 мкг/см3 | 510,6 мкг/см3 |
-40,6 | -13,2 | -3,1 | 6,9 | -1,3 | |
Метиловый эфир | 8,1 мкг/см3 | 16,1 мкг/см3 | 32,2 мкг/см3 | 64,4 мкг/см3 | 161,1 мкг/см3 |
-35,3 | -6,1 | 2,7 | -1,7 | 0,4 | |
Этиловый эфир | 10,1 мкг/см3 | 20,2 мкг/см3 | 40,5 мкг/см3 | 81 мкг/см3 | 202,5 мкг/см3 |
-31,7 | -3,9 | 2,6 | -1,7 | 0,4 | |
Бензиловый эфир | 12,2 мкг/см3 | 24,5 мкг/см3 | 48,9 мкг/см3 | 97,9 мкг/см3 | 244,8 мкг/см3 |
26,7 | -5,0 | 1,9 | -1,8 | 0,4 | |
Концентрации (мкг/см3) представляют собой усредненное значение пяти различных значений, полученных каждый день. Все анализируемые соединения были подвергнуты тесту Фишера.
9
ГОСТ EN 16956—2020
Таблица В.4 — Результативность, подтвержденная на образце отбеливающего крема с точно измеренным количеством добавленных соединений при двух уровнях содержания четырьмя аналитиками на трех различных хроматографах в течение 5 дней
Соединение | Образец: отбеливающий крем | |||||
Уровень (LOQ): | 0,1 % для гидрохинона 0,2 % для метилового и этилового эфиров 0,3 % для бензилового эфира | Уровень: | 1 % (m/m) для эфиров 2 % (m/m) для гидрохинона | |||
Результативность | RSD повторяемости, % | RSD внутренней воспроизводимости, % | Результативность | RSD повторяемости, % | RSD внутренней воспроизводимости, % | |
Гидрохинон | 112 | 2,1 | 12,2 | 99 | 1,3 | 1,6 |
Метиловый эфир | 97 | 1.6 | 9,1 | 100 | 1,4 | 2,7 |
Этиловый эфир | 98 | 1,9 | 10,8 | 101 | 1,5 | 3,4 |
Бензиловый эфир | 96 | 2,1 | 7,9 | 100 | 1,7 | 5,5 |
Таблица В.5 — Результативность, подтвержденная на образцах отбеливающего масла с точно измеренным количеством добавленных соединений при двух уровнях содержания четырьмя аналитиками на трех различных хроматографах в течение 5 дней
Соединения | Образец: отбеливающее масло | |||||
Уровень (LOQ): | 0,1 % для гидрохинона 0,2 % для метилового, этилового и бензилового эфиров | Уровень: | 1 % (m/m) для эфиров 2 % (m/m) для гидрохинона | |||
Результативность | RSD повторяемости, % | RSD внутренней воспроизводимости, % | Результативность | RSD повторяемости, % | RSD внутренней воспроизводимости, % | |
Гидрохинон | 95 | 2,8 | 25,3 | 100 | 1,5 | 3,5 |
Метиловый эфир | 89 | 3,0 | 27,1 | 98 | 2,2 | 6,9 |
Этиловый эфир | 94 | 2,6 | 21,0 | 97 | 2,0 | 10,2 |
Бензиловый эфир | 118 | 3,5 | 15,6 | 100 | 2,7 | 17,6 |
Таблица В.6 — Максимальное расхождение повторяемости MRD в абсолютном выражении двух результатов, полученных из 30 значений
Соединение | Образец: крем | Образец: масло | ||
Полученные MRD, % (m/m) | Критерий,установленный в Директиве 95/32/ЕС, % (m/m) | Полученные MRD, % (m/m) | Критерий,установленный в Директиве 95/32/ЕС, % (m/m) | |
Гидрохинон 2 % (m/m) | 0,08 | 0,13 | 0,12 | 0,13 |
Метиловый эфир 1 % (m/m) | 0,04 | 0,10 | 0,08 | 0,10 |
Этиловый эфир 1 % (m/m) | 0,05 | 0,11 | 0,09 | 0,11 |
Бензиловый эфир 1 % (m/m) | 0,07 | 0,11 | 0,14а) | 0,11 |
а)29 из 30 значений ниже либо равны 0,08, только одно значение равно 0,14.
Таблица В.7 — Максимальное расхождение внутренней воспроизводимости MIRD в абсолютном выражении двух результатов, полученных из 40 значений
Соединение | Образец: крем | Образец: масло | ||
Полученные MRD, % (m/m) | Критерий,установленный в Директиве 95/32/ЕС, % (m/m) | Полученные MRD, % (m/m) | Критерий,установленный в Директиве 95/32/ЕС, % (m/m) | |
Гидрохинон 2 % (m/m) | 0,12 | 0,37 | 0,22 | 0,37 |
Метиловый эфир 1 % (m/m) | 0,09 | 0.21 | 0,09 | 0,21 |
10
Окончание таблицы В. 7
ГОСТ EN 16956—2020
Соединение | Образец: крем | Образец: масло | ||
Полученные MRD, % (m/m) | Критерий,установленный в Директиве 95/32/ЕС, % (m/m) | Полученные MRD, % (m/m) | Критерий,установленный в Директиве 95/32/ЕС, % (m/m) | |
Этиловый эфир 1 % (m/m) | 0,10 | 0,19 | 0,24 | 0,19 |
Бензиловый эфир 1 % (m/m) | 0,17 | 0,11а) | 0,42 | 0,11 а) |
а) Данный критерий является необъяснимым по сравнению с другими критериями.
Таблица В.8 — Точность, подтвержденная на двух образцах с точно измеренным количеством добавленных соединений при двух уровнях содержания четырьмя аналитиками на трех различных хроматографах в течение 5 дней
Соединение | Образец: крем отбеливающий | Образец: масло отбеливающее | ||||||||||
Уровень (LOQ): 0,1 % для гидрохинона 0,2 % для метилового и этилового эфиров 0,3 % для бензилового эфира | Уровень: 1 % (m/m) для эфиров 2 % для гидрохинона | Уровень (LOQ): 0,1 % для гидрохинона 0,2 % для метилового, этилового и бензилового эфиров | Уровень: 1 % (m/m) для эфиров 2 % для гидрохинона | |||||||||
Точность | Т 3 о ? ^^ 2 ° н ф с О Е гс о о СП X X О о | Точность | Т 3 о н £^ 2 ° н ф с О Е гс о о си X О о | Точность | 1 а^ 2 g н ф 1- о Е гс о о го х О о | Точность | 1 1^ 2 ° н ф с О Е гс о о го х X ± О о | |||||
RSDR, % | RSDIR, % | RSDR, % | RSDIR, % | RSDR, % | RSDIR, % | RSDR, % | RSDIR, % | |||||
Гидрохинон | 2,1 | 12,2 | 13,9 | 1,3 | 1,6 | -1,5 | 28 | 25,3 | -5,0 | 1.5 | 3,5 | 0,5 |
Метиловый эфир | 1,6 | 9,1 | -3,4 | 1,4 | 2,8 | 0,1 | 3,0 | 27,1 | -10,9 | 2,2 | 6,9 | -2,5 |
Этиловый эфир | 1,9 | 10,8 | -1,7 | 1,5 | 3,4 | 0,6 | 2,6 | 21,0 | -6,5 | 2,0 | 10,2 | -3,3 |
Бензиловый эфир | 2,1 | 7,9 | -3,7 | 1,7 | 5,5 | 0,3 | 3,5 | 15,6 | 17,7 | 2,7 | 17,6 | -0,3 |
Примечание — RSDR — RSD повторяемости; RSDIR — RSD внутренней воспроизводимости.
Таблица В.9 — Стандартное круговое тестирование LGC: образец крема с гидрохиноном
Цикл | Количество лабораторий | Заданное значение, % (m/m) | Полученный результат, % (m/m) | Стандартное отклонение воспроизводимости | Z-оценка |
2012—03—05 | 10 | 2,00 | 1,90 | 0,156 | -0,64 |
2013—02—09 | 10 | 0,80 | 0,77 | 0,022 | -1,36 |
2013—09—11 | 7 | 0,50 | 0,51 | 0,05 | 0,20 |
2014—03—13 | 3 | 1,25 | 1,26 | 0,125 | 0,08 |
2015—03—17 | 7 | 0,91 | 0,90 | 0,091 | -0,11 |
2016—03—11 | 10 | 3,11 | 3,15 | 0,311 | 0,13 |
Таблица В.10 — NVWA справочный материал
Образец | Соединение | Подтвержденное значение, % (m/m) | Неопределенность, % (m/m) | Полученный результат, % (m/m) |
СНЕК RM 565 Молочко для тела | Гидрохинон | 2,57 | 0,06 | 2,63 |
СНЕК RM 604 Лосьон для тела | Гидрохинон | 2,55 | 0,06 | 2,52 |
11
ГОСТ EN 16956—2020
Приложение С (справочное)
Данные валидации метода количественного определения четырех наиболее часто встречающихся кортикостероидов
Данные валидации были получены Общей службой лаборатории (SCL) при Министерстве экономики и финансов — лаборатория Лиона-Oullins — Единая продукция — Секция Косметика и Национальным агентством безопасности медикаментов и здоровых продуктов (ANSM) при Министерстве здравоохранения (лаборатория Montpellier-Vendargues. Блок физико-химического контроля химических препаратов и других товаров медицинского назначения, Франция).
Предел обнаружения: 0,004 % (m/m) при использовании стандартных растворов на трех хроматографах.

Условные обозначения:
X — время удерживания, мин;
Y — оптическая плотность (ЕОП);
1 — флуоцинолона ацетонид (17,069 мин);
2 — флуоцинонид (18,997 мин);
3 — клобетазола пропионат (19,925 мин);
4 — бетаметазона дипропионат (20,885 мин)
Рисунок С.1 — Хроматограмма стандартного раствора четырех кортикостероидов с концентрацией 0,004 % (m/m)
Таблица С.1 — Предел количественного определения LOQ, подтвержденный на образце с точно измеренным количеством добавленных соединений четырьмя аналитиками на трех хроматографах в течение 5 дней в SCL и одним аналитиком на двух хроматографах в течение 5 дней в ANSM
Соединение | Образец: крем отбеливающий | ||
LOQ, % (m/m) | RSD повторяемости, % | RSD внутренней воспроизводимости, % | |
Флуоцинолона ацетонид | 0,01 | SCL: 9,1 | SCL: 11,6 |
ANSM: 4,5 | ANSM: 17,4 | ||
Флуоцинонид | 0,01 | SCL: 5,1 | SCL: 11,8 |
ANSM: 5,7 | ANSM: 28,2 | ||
Клобетазола пропионат | 0,01 | SCL: 8,4 | SCL: 16,2 |
ANSM: 4,3 | ANSM: 10,2 | ||
Бетаметазона дипропионат | 0,01 | SCL: 8,2 | SCL: 8,8 |
ANSM: 10,3 | ANSM: 12,6 | ||
12
ГОСТ EN 16956—2020
Таблица С.2 — Линейность подтвержденная для шести уровней градуировки (стандартных растворов) четырьмя аналитиками на трех хроматографах в течение 5 дней в SCL и одним аналитиком на двух хроматографах в течение 5 дней в ANSM
Соединение | Полученное максимальное относительное смещение, % | |||||
Уровень 1 (LOQ) | Уровень 2 | Уровень 3 | Уровень 4 | Уровень 5 | Уровень 6 | |
Флуоцинолона | 0,6 мкг/см3 | 1,1 мкг/см3 | 2,2 мкг/см3 | 4,5 мкг/см3 | 5,6 мкг/см3 | 11,2 мкг/см3 |
ацетонид | -16,3 | -6,3 | -4,5 | 4,5 | -2,1 | -0,9 |
SCL | 0,5 мкг/см3 | 1 мкг/см3 | 2 мкг/см3 | 4 мкг/см3 | 5,1 мкг/см3 | 10,1 мкг/см3 |
ANSM | 5,7 | 3,1 | -3,0 | -2,2 | 1,3 | 0,3 |
Флуоцинонид | 0,5 мкг/см3 | 1,0 мкг/см3 | 1,9 мкг/см3 | 3,9 мкг/см3 | 4,9 мкг/см3 | 9,7 мкг/см3 |
SCL | 18,4 | -9,9 | -0,8 | 3,1 | -2,3 | 0,6 |
ANSM | 0,5 мкг/см3 | 1 мкг/см3 | 2 мкг/см3 | 4,1 мкг/см3 | 5,1 мкг/см3 | 10,2 мкг/см3 |
8,4 | 3,8 | -1,6 | -1,2 | -1,3 | 0,4 | |
Клобетазола | 0,6 мкг/см3 | 1,1 мкг/см3 | 2,2 мкг/см3 | 4,4 мкг/см3 | 5,6 мкг/см3 | 11,1 мкг/см3 |
пропионат | 18,4 | -6,2 | 3,8 | 2,2 | -2,2 | 0,6 |
SCL1 | 0,5 мкг/см3 | 1,1 мкг/см3 | 2,2 мкг/см3 | 4,3 мкг/см3 | 5,4 мкг/см3 | 10,8 мкг/см3 |
ANSM | 22,2 | 9,5 | 3,3 | -2,0 | -4,7 | 1,0 |
Бетаметазона | 0,5 мкг/см3 | 1,1 мкг/см3 | 2,1 мкг/см3 | 4,2 мкг/см3 | 5,2 мкг/см3 | 10,4 мкг/см3 |
дипропионат | -21,7 | -8,9 | 4,8 | 4,4 | -2,5 | -0,9 |
SCL | 0,5 мкг/см3 | 1 мкг/см3 | 2 мкг/см3 | 4 мкг/см3 | 5,1 мкг/см3 | 10,1 мкг/см3 |
ANSM | 20,6 | 2,3 | -2,4 | -1,6 | -1,3 | 0,6 |
Концентрации, мкг/см3, представляют собой усредненное значение пяти различных значений, полученных каждый день. Тесту Фишера были подвергнуты все анализируемые соединения в SCL и флуоцинолона ацетонид и флуоцинонид в ANSM.
Для валидации пределов количественного определения, результативности и точности был изготовлен образец отбеливающего крема с добавлением точно измеренных количеств гидрохинона и его эфиров. Стандартные образцы кортикостероидов являются дорогостоящими, имеются в наличии в небольших количествах (несколько сотен мг) и мало растворимы в растворителе. Поэтому только для уровня 1 LOQ возможно было добавление небольшого объема стандартного раствора в выбранный образец перед исследованием. Для других уровней (уровней 2 и 3) перед испытанием добавлялась навеска порошкообразного стандартного образца в выбранный образец. Полученные результаты показали неэффективность добавления на уровнях 2 и 3, за исключением бетаметазона дипро-пионата. Для трех других кортикостероидов метод добавок на уровнях 2 и 3 был реализован еще раз путем добавления небольшого объема стандартного раствора при взвешивании выбранного образца в мерную колбу перед экстракцией.
Таблица С.З — Результативность, подтвержденная на образце отбеливающего крема с точно измеренным количеством добавленных соединений для одного уровня содержания четырьмя аналитиками на трех хроматографах в течение 5 дней в SCL и одним аналитиком на двух хроматографах в течение 5 дней в ANSM
Соединение | Образец: отбеливающий крем | ||
Уровень (LOQ): 0,01 % (m/m) | |||
Резул ьтати вность | RSD повторяемости, % | RSD внутренней воспроизводимости, % | |
Флуоцинолона ацетонид SCL | 96 | 9,1 | 11,6 |
ANSM | 107 | 4,5 | 17.4 |
Флуоцинонид SCL | 104 | 5,1 | 11.8 |
ANSM | 99 | 5,7 | 28,2 |
Клобетазола пропионат SCL | 99 | 8,4 | 16,2 |
ANSM | 105 | 4,3 | 10,2 |
Бетаметазона дипропионат SCL | 115 | 8,2 | 8,8 |
ANSM | 103 | 10,3 | 12,6 |
13
ГОСТ EN 16956—2020
Таблица С.4 — Результативность, подтвержденная на образце отбеливающего крема с точно измеренным количеством добавленных соединений для двух уровней содержания четырьмя аналитиками на трех хроматографах в течение 5 дней в SCL и одним аналитиком на двух хроматографах в течение 5 дней в ANSM
Соединение | Образец: отбеливающий крем. Добавление порошкообразного стандартного образца в крем перед проведением всех испытаний (SCL). Добавление стандартного раствора к массе крема в колбу перед экстракцией | |||||
Уровень: 0,05 % (m/m) | Уровень: 0,1 % (m/m) | |||||
Результативность | RSD повторяемости, % | RSD внутренней воспроизводимости, % | Результативность | RSD повторяемости, % | RSD внутренней воспроизводимости, % | |
Флуоцинолона ацетонид SCL ANSM | 124 | 13,3 | 18,1 | 119 | 3,6 | 11,4 |
109 | 2,4 | 3,6 | 105 | 2,5 | 5,1 | |
114 | 7,0 | 19,7 | 115 | 6,7 | 16,8 | |
Флуоцинонид SCL ANSM | 118,5 | 4,0 | 11,4 | 97 | 2,0 | 17,2 |
106 | 1,8 | 7,0 | 108 | 1,7 | 5.8 | |
88 | 8,4 | 16,6 | 81 | 6,1 | 18,7 | |
Клобетазола пропионат SCL ANSM | 78,1 | 20,2 | 22,4 | 79 | 9,5 | 9,6 |
96 | 1,4 | 7,5 | 102 | 1,7 | 6,1 | |
98 | 6.0 | 8,5 | 95 | 6,8 | 7,1 | |
Бетаметазона дипропионат SCL ANSM | 107 | 3,7 | 5,6 | 102 | 2,2 | 4,5 |
97 | 2,5 | 2,9 | 104 | 1,6 | 4,3 | |
95 | 7,3 | 8,9 | 92 | 5,4 | 8.5 | |
Таблица С.5 — Точность подтвержденная на образце с точно измеренным количеством добавленных соединений для трех уровней содержания четырьмя аналитиками на трех хроматографах в течение 5 дней в SCL и одним аналитиком на двух хроматографах в течение 5 дней в ANSM
Соединение | Образец: отбеливающий крем Добавление стандартного раствора или порошкообразного стандартного образца в крем перед проведением всех испытаний (SCL). Добавление стандартного раствора к массе крема в колбу перед экстракцией. | ||||||||
Уровень (LOQ): 0,01 % (m/m) | Уровень: 0,05 % (m/m) | Уровень: 0,1 % (m/m) | |||||||
Точность | Система-тическая погрешность, % | Точность | Система-тическая погрешность, % | Точность | Система-тическая погрешность, % | ||||
RSDR, % | RSDIR, % | RSDR, % | RSDIR, % | RSDR, % | RSDIR, % | ||||
Флуоцинолона ацетонид SCL ANSM | 9,1 | 11,6 | -3,6 | 13,3 | 18,1 | 24,1 | 3,6 | 11,4 | 18,7 |
2,4 | 3,6 | 8,7 | 2,5 | 5,1 | 5,5 | ||||
4,5 | 17,4 | 6,8 | 6.9 | 19,1 | 15,7 | 6,7 | 16,4 | 15,3 | |
Флуоцинонид SCL ANSM | 5,1 | 11,8 | 3,5 | 4,0 | 11,4 | 18,5 | 2,0 | 17,2 | -3,1 |
1,8 | 6,0 | 7,1 | 1,7 | 5,0 | 8,7 | ||||
5,7 | 28,2 | -1,5 | 8,5 | 15,1 | -12,8 | 6,1 | 17,3 | -19,6 | |
14
Окончание таблицы С. 5
ГОСТ EN 16956—2020
Соединение | Образец: отбеливающий крем Добавление стандартного раствора или порошкообразного стандартного образца в крем перед проведением всех испытаний (SCL). Добавление стандартного раствора к массе крема в колбу перед экстракцией. | ||||||||
Уровень (LOQ): 0,01 % (m/m) | Уровень: 0,05 % (m/m) | Уровень: 0,1 % (m/m) | |||||||
Точность | Система-тическая погрешность, % | Точность | Система-тическая погрешность, % | Точность | Система-тическая погрешность, % | ||||
RSDR, % | RSDIR, % | RSDR. % | RSDIR, % | RSDR, % | RSDIR, % | ||||
Клобетазола пропионат SCL ANSM | 8,4 | 16,2 | -1,5 | 20,2 | 22,4 | -21,9 | 9,5 | 9,6 | -21,0 |
1,4 | 7,5 | -4,0 | 1,7 | 5,9 | 2,2 | ||||
4,3 | 10,2 | 5,0 | 5,9 | 9.5 | -1,3 | 6,8 | 8,8 | -4,9 | |
Бетаметазона дипропионат SCL ANSM | 8,2 | 8,8 | 15,0 | 3,7 | 5,6 | 7,3 | 2,2 | 4,5 | 2,1 |
2,5 | 3,1 | "2,1 | 1,6 | 3,3 | 4,9 | ||||
10,3 | 12,6 | 3,0 | 7,3 | 9.4 | -5,6 | 5,4 | 8,8 | -8.2 | |
Примечание — RSDR — RSD повторяемости; RSDIR — RSD внутренней воспроизводимости.
Таблица С.6 — Точность, подтвержденная на коммерческом лекарственном средстве для одного уровня содержания четырьмя аналитиками на трех хроматографах в течение 5 дней в SCL и одним аналитиком на двух хроматографах в течение 5 дней в ANSM
Соединение | Образец: крем (коммерческое лекарственное средство) | |||||
Уровень: 0,05 % (m/m) | Уровень: 0,064 % (m/m) | |||||
Точность | Систематиче-ская погрешность, % | Точность | Систематиче-ская погрешность, % | |||
RSDR, % | RSDIR, % | RSDR, % | RSDIR, % | |||
Клобетазола пропионат SCL ANSM | 5,4 | 6,1 | -8,0 | |||
8.0 | -3,7 | |||||
Бетаметазона дипропионат SCL ANSM | 4,7 | 10,2 | -7,6 | |||
2,3 | 3,1 | -5,3 | ||||
Примечание — RSDR — RSD повторяемости; RSDIR — RSD внутренней воспроизводимости.
Данный метод был опробован при проведении межлабораторных сличений с участием восьми участников с использованием коммерческих доступных кремообразных лекарственных средств с известными концентрациями этих двух веществ.
Таблица С.7 — Надежность метода
Параметры | Образцы крема | |
Клобетазола пропионат | Бетаметазона дипропионат | |
Число участвовавших лабораторий | 8 | 8 |
Число лабораторий, представивших результаты | 7 | 6 |
Число выбросов | 0 | 0 |
15
ГОСТ EN 16956—2020
Окончание таблицы С. 7
Параметры | Образцы крема | |
Клобетазола пропионат | Бетаметазона дипропионат | |
Заданное значение, г/100 г | 0,050 | 0,064 |
Среднее арифметическое значение х, г/100 г | 0,047 | 0,062 |
Степень обнаружения, % | 94,8 | 97,0 |
Предел повторяемости г, г/100 г | 0,006 | 0,003 |
Стандартное отклонение повторяемости sr, г/100 г | 0,002 | 0,001 |
Относительное стандартное отклонение повторяемости sr ге|, % | 4,2 | 1.5 |
Предел воспроизводимости R, г/100 г | 0,010 | 0,016 |
Стандартное отклонение воспроизводимости sR, г/100 г | 0,004 | 0,006 |
Относительное стандартное отклонение воспроизводимости sR rei, % | 7,5 | 9,3 |
Коэффициент Хорвитца (Хорвитц-И-Индекс) | 1,2 | 1,5 |
16
ГОСТ EN 16956—2020
Приложение D (обязательное)
Скрининговые методы для идентификации гидрохинона, трех эфиров гидрохинона и 38 кортикостероидов
D.1 Сущность метода
Поскольку кортикостероиды не должны использоваться в парфюмерно-косметической продукции и не должны присутствовать в качестве загрязнителей или примесей, идентификация одного из этих запрещенных соединений, преднамеренно введенных в парфюмерно-косметическую продукцию, может быть достаточной для проведения контроля рынка. После идентификации запрещенных кортикостероидов, если необходимо, точное количественное определение этих соединений затем может быть выполнено с использованием установленных методов.
Образец экстрагируют смесью вода/метанол, затем осторожно нагревают, чтобы экстрагировать соединения, присутствующие в продукции. Полученную смесь фильтруют. Идентификацию присутствующих соединений в растворе проводят с помощью обращенно-фазовой ВЭЖХ с детектированием диодно-матричным детектором.
Для разделения всех соединений необходимы два различных градиента элюирования. Основной градиент элюирования позволяет выделить 39 соединений из 43 соединений в течение 45 мин. Для неразделенных соединений предусмотрено дополнительное градиентное элюирование с использованием тех же растворителей.
D.2 Реактивы
Используются химические вещества аналитической степени чистоты; вода должна быть дистиллированная или аналогичной чистоты, если не установлено иное. Под раствором следует понимать водный раствор, если не установлено иное.
Используют реактивы 3.1—3.4, 3.6 и указанные ниже.
D.2.1 ацетонитрил для ВЖХ.
D.2.2 муравьиная кислота, чистота >98 %.
D.2.3 этанол для ВЭЖХ.
D.2.4 Подвижная фаза для ВЭЖХ
Элюент А: добавляют 1,0 см3 муравьиной кислоты (см. D.2.2) в 500 см3 воды (см. 3.2) в мерной колбе вместимостью 1 дм3. Взбалтывают до растворения и доводят объем до метки водой (см. 3.2). Конечная концентрация водного раствора муравьиной кислоты — 0,1 %.
Элюент В: добавляют 1,0 см3 муравьиной кислоты (см. D.2.2) к 500 см3 ацетонитрила (см. D.2.1) в мерной колбе вместимостью 1 дм3. Взбалтывают до растворения, и доводят объем до метки ацетонитрилом (см. D.2.1). Конечная концентрация муравьиной кислоты в ацетонитриле — 0,1 %.
D.2.5 Исходный раствор внутреннего стандарта (1 000 мкг/см3)
Для определения относительного времени удерживания (RR) содержащихся веществ готовят исходный раствор внутреннего стандарта путем взвешивания приблизительно 10 мг пропилпарабена в мерную колбу вместимостью 10 см3. Сначала растворяют в небольшом количестве метанола (3.1), а затем доводят объем до метки метанолом.
В методе настоящего стандарта гидрохинон, эфиры гидрохинона и кортикостероиды идентифицируют путем сравнения относительного времени удерживания (RR), рассчитанного для веществ, содержащихся в пробе, с RR соответствующих соединений в стандартных растворах. Если в пробе содержится пропилпарабен или другое мешающее соединение, идентификация может быть выполнена непосредственно по времени удерживания (вместо RR). При необходимости подтверждение идентичности соединения также может быть выполнено с использованием образца с точно измеренным количеством добавленного соединения или с использованием масс-спектрометрии (т. е. используют элюенты, совместимые с анализом LC-MS (жидкостная хроматография/масс-спектрометрия)).
D.2.6 Исходные стандартные растворы (1 000 мкг/см3)
Готовят исходные стандартные растворы каждого вещества в соответствии с таблицей D.2, взвесив приблизительно по 10,0 мг каждого вещества в мерную колбу вместимостью 10 см3. Сначала растворяют навеску в небольшом количестве метанола (см. 3.1) и затем доводят объем метанолом до метки.
D.2.7 Качественный анализ (идентификация)
D.2.7.1 Исходные растворы для скрининга
Готовят 4 стандартных раствора (смеси А, В, С и D) путем смешения 250 мм3 каждого выбранного исходного раствора в мерной колбе вместимостью 5 см3. Доводят объем метанолом до метки.
D.2.7.2 Смесь стандартных растворов А (50 мкг/см3): гидрохинон (HQ), клобетазола пропионат (СР), флу-цинонид (FCAA), монометиловый эфир гидрохинона (ММЕ), монобензиловый эфир гидрохинона (МВЕ), моноэтиловый эфир гидрохинона (МЕЕ), бетаметазона дипропионат (BMD), флуоцинолона ацетонид (FCA).
17
ГОСТ EN 16956—2020
D.2.7.3 Смесь стандартных растворов В (50 мкг/см3): гидрокортизон (НС), преднизолона сульфобензоат (PLSB), триамцинолона ацетонид (TRA), преднизолона ацетат (PLA), дексаметазона ацетат (DMA), гидрокортизона валерат (HCV), дифлупреднат (DFP), амцинонид (АМС), дифлуокортолона валерат (DFCV), флукортолона пивалат (FCP), флуокортолона гексаноат (FCH).
D.2.7.4 Смесь стандартных растворов С (50 мкг/см3): триамцинолон (TRI), преднизолон (PL), бетаметазон (ВМ), дезоксиметазон (DXM), бетаметазона ацетат (ВМА), гидрокортизона бутират (НСВ), дифлоразона диацетат (DFD), хальцинонид (HAL), преднизолона гексаноат (PLH), предникарбат (PCN), беклометазона дипропионат (BCD).
D.2.7.5 Смесь стандартных растворов D (50 мкг/см3): дексаметазона фосфат (DMPS), кортизон (CS), флу-рандренолид (FDL), дезонид (DSN), будесонид (BUD), бетаметазона валерат (BMV), флуметазона пивалат (FMP), алклометазона дипропионат (ACD), мометазона фуроат (MMF), клокортолона пивалат (CLP).
Для целей идентификации готовят общий раствор веществ путем смешения 1 см3 каждого предварительно приготовленного стандартного раствора (А, В, С и D) в мерной колбе вместимостью 5 см3. К полученному раствору добавляют 100 мм3 исходного раствора пропилпарабена (ISTD) (внутреннего стандарта) (см. D.2.5). Доводят объем раствора метанолом до метки и используют его для идентификации кортикостероидов, которые могут содержаться в пробе. Полученный стандартный раствор содержит каждый кортикостероид в концентрации 10 мкг/см3 и ISTD в концентрации 20 мкг/см3.
В качестве альтернативы может быть приготовлен стандартный раствор путем смешения 100 мм3 каждого отдельно взятого исходного раствора (см. D.2.6) в мерной колбе вместимостью 10 см3. Затем добавляют 200 мм3 исходного раствора ISTD (см. D.2.5). Доводят объем раствора в колбе до метки метанолом и используют его для идентификации кортикостероидов, которые могут содержаться в анализируемой пробе.
D.3 Аппаратура и оборудование
В дополнение к обычно используемому лабораторному оборудованию и вспомогательным устройствам, указанным в 4.1—4.5, требуется следующее оборудование.
D.3.1 ультразвуковая баня с терморегулятором.
D.3.2 магнитная мешалка.
D.3.3 аналитическая хроматографическая колонка, например Zorbax Phenyl, длиной 0,25 м, внутренним диаметром 4,6 мм, с диаметром частиц 5 мкм1\
D.4 Процедура
D.4.1 Подготовка пробы
Взвешивают точно 1 г пробы в мерную колбу. Диспергируют пробу в половине объема раствора для экстра-ции (см. 3.3, приблизительно 25 см3) путем энергичного перемешивания с помощью лабораторного шейкера до получения однородной суспензии (ультразвуковая баня может быть использована для ускорения экстракции). При необходимости помещают смесь в водяную баню при 60 °C в течение 5 мин, чтобы улучшить диспергирование, затем охлаждают и доводят объем до 50 см3 раствором для экстракции (см. 3.3). Перемешивают пробу магнитной мешалкой в течение от 30 мин до 1 ч и фильтруют через мембранный фильтр премиум-класса с диаметром пор 0,45 мкм. Вводят фильтрат в систему ВЭЖХ.
D.4.2 Условия хроматографирования
При использовании аппаратуры (см. 4.4) и колонки (см. D.3.3) рекомендуется придерживаться следующих условий:
- объемная скорость потока: 1,0 см3/мин;
- время анализа: 45 мин;
- объем вводимой пробы: 10 мм3;
- температура автодозатора: 5 °C;
- температура термостата колонок: 45 °C;
- обнаружение: DAD с длиной волны: 240 нм (кортикостероиды), 295 нм (гидрохинон и его эфиры);
- подвижные фазы:
- элюент А: раствор муравьиной кислоты с массовой долей 0,1 % в воде;
- элюент В: раствор муравьиной кислоты с массовой долей 0,1 % в ацетонитриле.
В таблице D.1 приведены условия градиентного разделения.
1) Это пример продукции, имеющейся в продаже. Информация дана для удобства пользователей настоящего стандарта и не является рекламой Европейского комитета по стандартизации этого продукта. Аналогичная продукция может быть использована, если доказано, что она обеспечивает получение тех же результатов.
18
Таблица D.1—Градиентное разделение
ГОСТ EN 16956—2020
Время, мин | Объемная доля элюента А, % | Объемная доля элюента В, % |
0 | 95 | 5 |
2 | 95 | 5 |
7 | 60 | 40 |
25 | 60 | 40 |
45 | 30 | 70 |
46 | 95 | 5 |
50 | 95 | 5 |
D.4.3 Обнаружение
См. 5.3.
D.5 Оценка методов скрининга
D.5.1 Идентификация
Гидрохинон и кортикостероиды идентифицируют, сравнивая относительное время удерживания (RR) проб и стандартных растворов. В таблице D.2 приведены хроматографические параметры для идентификации соединений с применением предложенного аналитического метода.
Чтобы обеспечить специфичность обнаружения, идентификация соединения для отбеливания кожи должна выполняться в два этапа. На первом этапе идентификация отбеливающего соединения, содержащегося в экстракте пробы, выполняется с использованием RR и при необходимости DAD спектров. В случае обнаружения соединения, для обеспечения правильной идентификации рекомендуется введение стандартного раствора этого идентифицированного отбеливающего соединения (второй этап). При необходимости, для подтверждения идентификации соединений можно также использовать образец с точно измеренным количеством добавленного соединения или масс-спектрометрическое обнаружение (например, используемые элюенты, совместимые с анализом LC-MS).
Отбеливающие соединения в парфюмерно-косметической продукции для кожи чаще присутствуют отдельно или в паре, поэтому неполное разделение некоторых хроматографических пиков можно считать достаточным. Кроме того, хроматографическое разделение может допускать только идентификацию пиков и разрешение между пиками не обязательно должно быть выше 1,5. Полученное с помощью основного метода полное разделение (RS (коэффициент разрешения) >1.5) 9 соединений для отбеливания кожи уже описаны в литературе (HQ, ММЕ, МЕЕ, FCA, МВЕ, FCAA, BMV, СР и BMD).
В таблице D.2 приведены хроматографические параметры для идентификации соединений.
Таблица D.2 — Хроматографические параметры для идентификации соединений
Соединение | Rt, мин | RR | X, нм |
Гидрохинон (HQ)a) | 5,90 | 0,41 | 295 |
Гидрокортизона ацепонат (НСАР)Ь) | 9,87 | 0,68 | 240 |
Метоксифенол (ММЕ)а> | 10,14 | 0,70 | 295 |
Триамцинолон (TRI) | 11,15 | 0,77 | 240 |
Дексаметазона фосфат (DMPS) | 11,36 | 0,78 | 240 |
Этоксифенол (МЕЕ)а) | 11,28 | 0,78 | 295 |
Гидрокортизон (НС) | 12,64 | 0,87 | 240 |
Преднизолон (PL) | 12,81 | 0,88 | 240 |
Кортизон (CS) | 13,11 | 0,90 | 240 |
19
ГОСТ EN 16956—2020
Продолжение таблицы D.2
Соединение | Rt, мин | RR | X, нм |
Бетаметазон (ВМ) | 14,22 | 0,98 | 240 |
Преднизолона сульфобензоат (PLSB) | 14,76 | 1,01 | 240 |
Флурандренолид (FDL) | 16,75 | 1,15 | 240 |
Флуоцинолона ацетонид (FCA)a) | 16,96 | 1,17 | 240 |
Триамцинолона ацетонид (TRA) | 17,25 | 1,19 | 240 |
Монобензон (МВЕ)а) | 17,74 | 1,22 | 295 |
Дезоксиметазон (DXM) | 18,47 | 1,27 | 240 |
Дезонид (DSN) | 18,75 | 1,29 | 240 |
Преднизолона ацетат (PLA) | 18,97 | 1,30 | 240 |
Бетаметазона ацетат (ВМА) | 21,35 | 1,47 | 240 |
Метилпреднизолона ацетат (MPLA)b> | 21,87 | 1,50 | 240 |
Дексаметазона ацетат (DMA) | 22,97 | 1,58 | 240 |
Гидрокортизона бутират (НСВ) | 25,66 | 1,76 | 240 |
Будесонид 1 (BUD1) | 27,67 | 1,90 | 240 |
Будесонид 2 (BUD2) | 30,16 | 2,07 | 240 |
Флуоцинонид (FCAA)a) | 31,49 | 2,16 | 240 |
Гидрокортизона валерат (HCV) | 31,93 | 2,19 | 240 |
Дифлоразона диацетат (DFD) | 32,41 | 2,23 | 240 |
Бетаметазона валерат (BMV) | 35,15 | 2,42 | 240 |
Дифлупреднат (DFP)C) | 35,71 | 2,45 | 240 |
Хальцинонид (HAL)C) | 35,71 | 2,45 | 240 |
Флуметазона пивалат (FMP) | 37,86 | 2,60 | 240 |
Амцинонид (АМС) | 38,22 | 2,63 | 240 |
Клобетазола пропионат (СР)а^ | 38,89 | 2,67 | 240 |
Преднизолона гексаноат (PLH) | 39,31 | 2,70 | 240 |
Алклометазона дипропионат (ACD) | 39,98 | 2,75 | 240 |
Бетаметазона дипропионат (BMD)a) | 40,18 | 2,76 | 240 |
Предникарбат (PCN) | 40,46 | 2,78 | 240 |
Мометазона фуроат (MMF) | 41,22 | 2,83 | 240 |
Дифлукортолона валерат (DFCV) | 41,50 | 2,85 | 240 |
Флуокортолона пивалат (FCP)C) | 42,25 | 2,90 | 240 |
Беклометазона дипропионат (BCD)C) | 42,25 | 2,90 | 240 |
Клокортолона пивалат (CLP) | 42,93 | 2,95 | 240 |
20
Окончание таблицы D.2
ГОСТ EN 16956—2020
Соединение | Rt, мин | RR | X, нм |
Флуокортолона гексаноат (FCH) | 44,54 | 3,06 | 240 |
Пропилпарабен (ISTD) | 14,55 | 1,00 | 240 |
а) Наиболее часто встречающееся отбеливающее соединение в незаконно реализуемой парфюмернокосметической продукции. ь) Соединение вводится отдельно от смеси стандартных растворов. с) Совместно элюируемые соединения. Идентификация может быть осуществлена с использованием процедуры, описанной в D.8.* | |||
D.6 Протокол испытания
См. раздел 7.
D.7 Примеры хроматограмм, полученных для стандартных растворов с концентрацией 50 мкг/см3
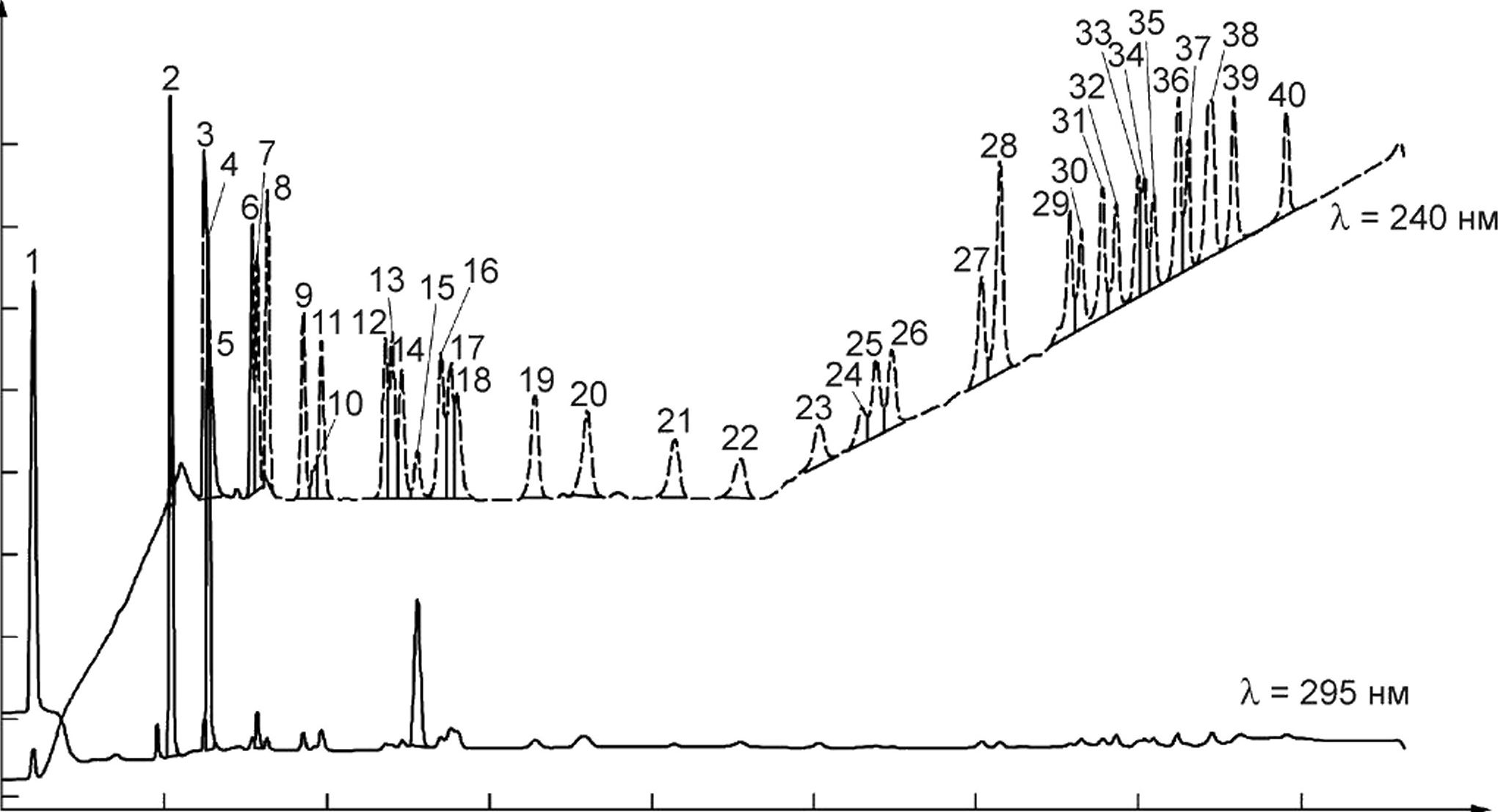
Примеры хроматограмм, полученных для стандартных растворов с концентрацией 50 мкг/см3, приведены на рисунках D.1—D.5.
80
70
60
50
40
30
20
10
0
5
10
15
20
25
30
35
40
45
X
Условные обозначения:
X
1
2
3
4
5
6
7
8
9
10
11
12
— время удерживания, мин;
— оптическая плотность (ЕОП);
— HQ (5,896 мин);
— ММЕ (10,140 мин);
— TRI (11,152 мин);
— ММЕ (11,284 мин);
— DMPS (11,364 мин);
— НС (12,644 мин);
— PL (12,809 мин);
— CS (13,113 мин);
— ВМ (14,215 мин);
— ISTD (14,544 мин);
— PLSB (14,760 мин);
— FDL (16,747 мин);
13
14
15
16
17
18
19
20
21
22
23
24
25
26
— FCA (16,955 мин);
— TRA (17,250 мин);
— МВЕ (17,736 мин);
— DXM (18,467 мин);
— DSN (18,751 мин);
— PLA (18,972 мин);
— ВМА (21,351 мин);
— DMA (22,970 мин);
— НСВ (25,658 мин);
— BUD1 (27,673 мин);
— BUD2 (30,157 мин);
— FCAA (31,489 мин);
— HCV (31,923 мин);
— DFD (32,410 мин);
27
28
29
30
31
32
33
34
35
36
37
38
39
40
— BMV (35,150 мин);
— HAL + DFP (35,713 мин);
— FMP (37,864 мин);
— АМС (38,224 мин);
— СР (38,887 мин);
— PLH (39,307 мин);
— ACD (39,977 мин);
— BMD (40,147 мин);
— PCN (40,457 мин);
— MMF (41,217 мин);
— DFCV (41,498 мин);
— FCP+BCD (42,250 мин);
— CLP (42,930 мин);
— FCH (44,538 мин)
Рисунок D.1 —Хроматограмма для общей смеси стандартных растворов
Устранена опечатка в части ссылки на приложение Е (слова «приложение Е» заменены на «D.8»).
21
ГОСТ EN 16956—2020
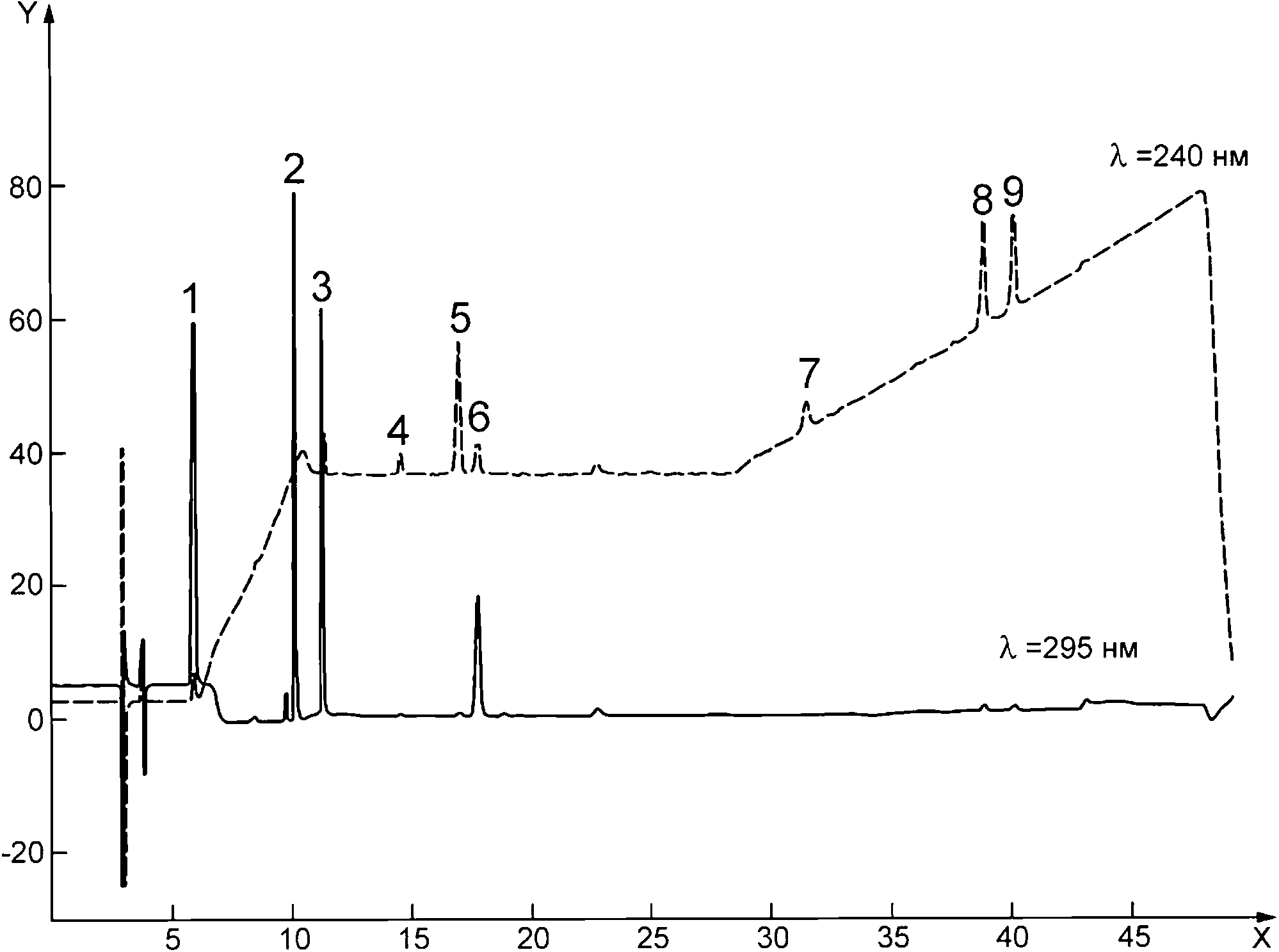
Условные обозначения:
X — время удерживания, мин;
Y — оптическая плотность (ЕОП);
1 —HQ (5,912 мин);
2 — ММЕ (10,142 мин);
3 —МЕЕ (11,289 мин);
4 —ISTD (14,564 мин);
5 —FCA (16,989 мин);
6 — МВЕ (17,767 мин);
7 — FCAA(31,530 мин);
8 —СР (38,920 мин);
9 — BMD (40,175 мин)
Рисунок D.2 — Хроматограмма стандартного раствора А
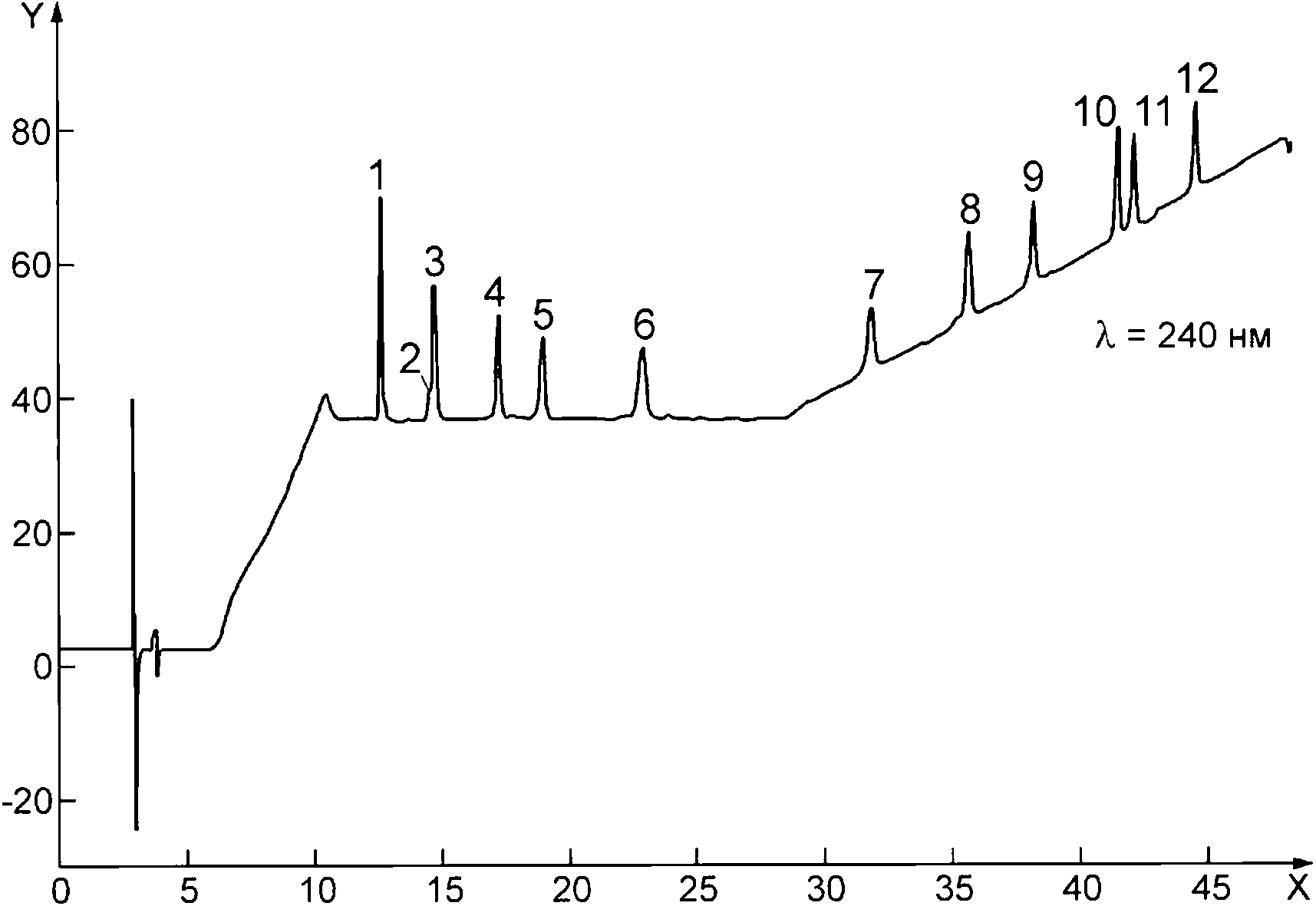
Условные обозначения:
X — время удерживания, мин;
Y — оптическая плотность (ЕОП);
1 —НС (12,629 мин);
2 — PLSB (14,535 мин);
3 — ISTD (14,721 мин);
4 —TRA (17,226 мин);
5 —PLA (18,953 мин);
6 —DMA (22,926 мин);
7 —HCV (31,860 мин);
8 — DFP (35,665 мин);
9 —АМС (38,218 мин);
10 —DFCV (41,510 мин);
11 — FCP(42,242 мин);
12 — FCH (44,551 мин)
Рисунок D.3 — Хроматограмма стандартного раствора В
22
ГОСТ EN 16956—2020
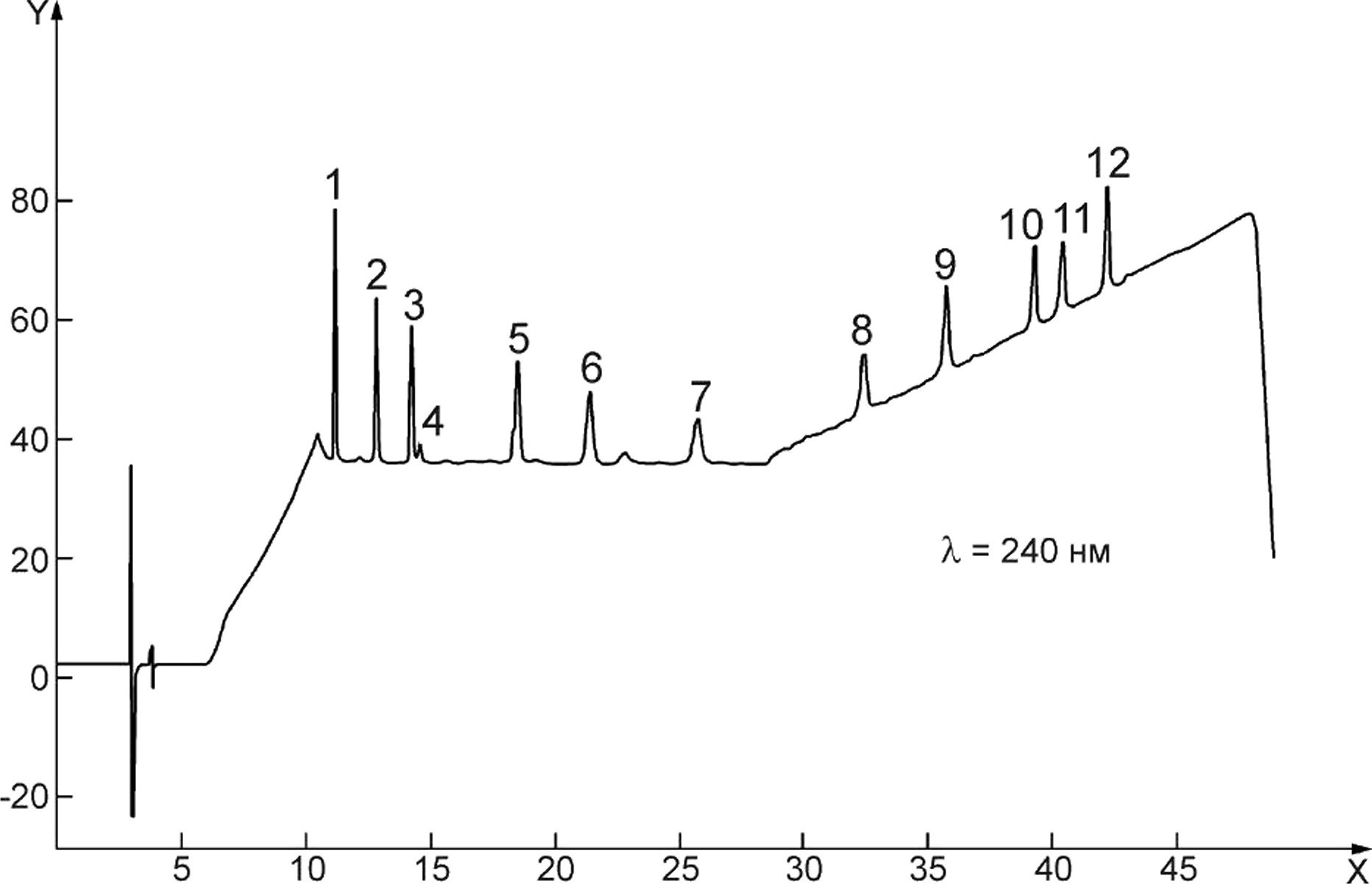
Условные обозначения:
X — время удерживания, мин;
Y — оптическая плотность (ЕОП);
1 —TRI (11,161 мин);
2 —PL (12,827 мин);
3 —ВМ (14,236 мин);
4 —1STD (14,569 мин);
5 — DXM (18,507 мин);
6 — ВМА (21,408 мин);
7 — НСВ (25,735 мин);
8 — DFD (32,469 мин);
9 — HAL (35,784 мин);
10 — PLH (39,331 мин);
11 — PCN (40,475 мин);
12 — BCD (42,273 мин)
Рисунок D.4 — Хроматограмма стандартного раствора С
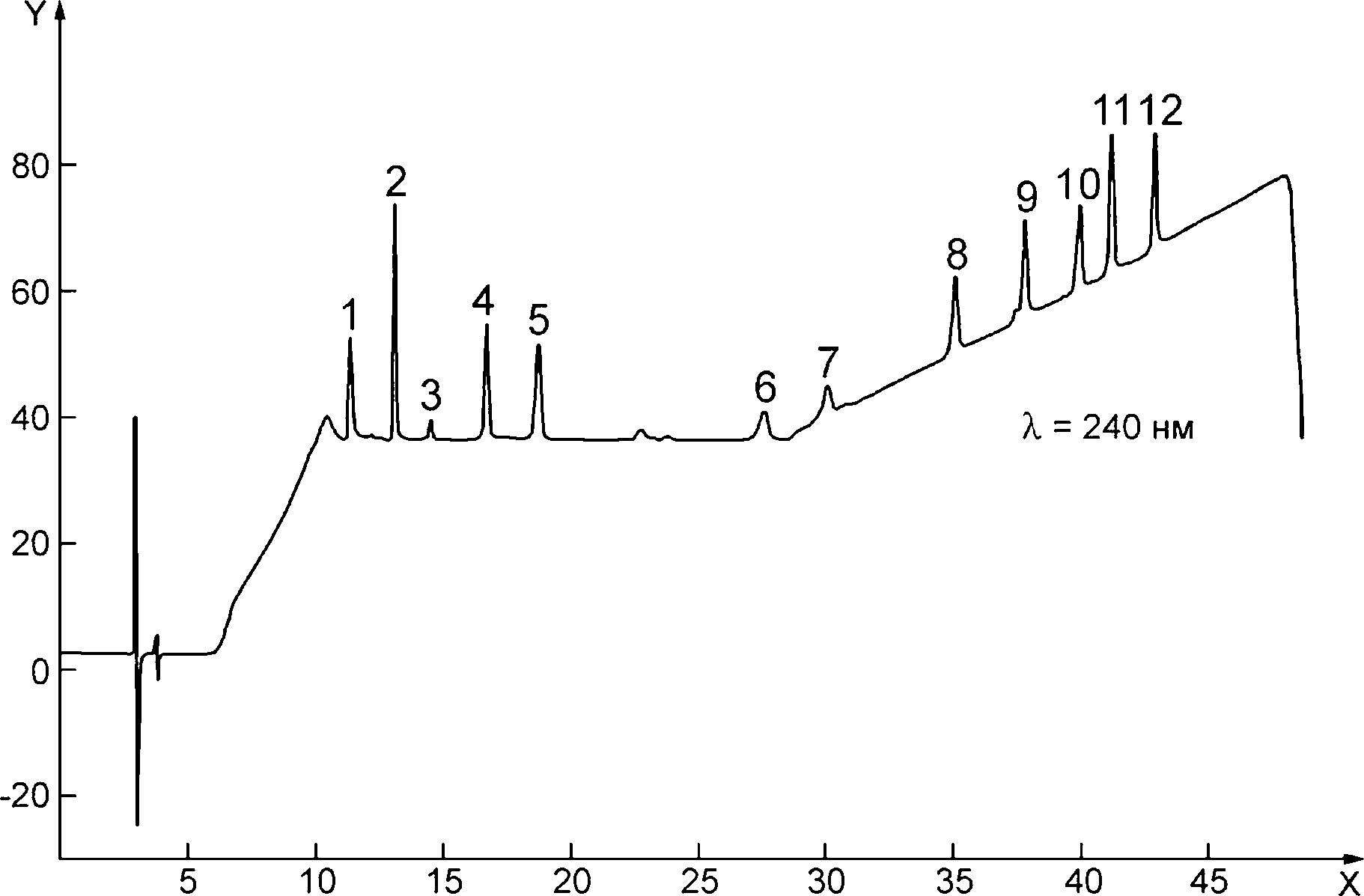
Условные обозначения: | ||||
X — время удерживания, мин; | 4 | — FDL (16,724 мин); | 9 | — FMP (37,854 мин); |
Y — оптическая плотность (ЕОП); | 5 | — DSN (18,731 мин); | 10 | — ACD (39,971 мин); |
1 —DMPS (11,351 мин); | 6 | — BUD1 (27,629 мин); | 11 | — MMF (41,225 мин); |
2 —CS (13,099 мин); | 7 | — BUD2 (30,119 мин); | 12 | — CLP (42,940 мин) |
3 — ISTD (14,533 мин); | 8 | — BMV (35,120 мин); | ||
Рисунок D.5 — Хроматограмма стандартного раствора D
23
ГОСТ EN 16956—2020
D.8 Альтернативный метод ВЭЖХ/УФ для идентификации неразделяемых соединений
Были разработаны дополнительные условия хроматографирования для разделения двух соединений, неразделяемых в ранее предложенных условиях (DFP + HAL, FCP + BCD).
Условия хроматографирования:
- аналитическая колонка: Zorbax Phenyl длиной 250 см, внутренним диаметром 4,6 мм, с диаметром частиц 5 мкм;
- объемная скорость потока (расход элюента): 1,0 см3/мин;
- длина волны: 240 нм для кортикостероидов, 295 нм для гидрохинона и его эфиров;
- время анализа: 45 мин;
- объем вводимой пробы: 10 мм3;
- температура автодозатора: 5 °C;
- температура термостата: 45 °C;
- обнаружение: DAD;
- градиентное элюирование:
- элюент А: раствор муравьиной кислоты с массовой долей 0,1 % в воде;
- элюент В: раствор муравьиной кислоты с массовой долей 0,1 % в ацетонитриле (CH3CN).
- раствор для экстракции: метанол/вода (1:1) (для приготовления стандартных растворов и экстрагирования проб).
Таблица D.3 — Градиентное разделение
Время, мин | Объемная доля элюента А, % | Объемная доля элюента В, % |
0 | 90 | 10 |
2 | 90 | 10 |
45 | 70 | 30 |
46 | 90 | 10 |
50 | 90 | 10 |
Таблица D.4 — Результаты, полученные для неразделяемых соединений
Соединение | RT, мин | RR | X, нм |
Дифлупреднат (DFP) | 38,16 | 1,31 | 240 |
Хальцинонид (HAL) | 38,44 | 1,32 | 240 |
Флуокортолона пивалат (FCP) | 42,98 | 1,48 | 240 |
Беклометазона дипропионат (BCD) | 43,16 | 1,49 | 240 |
Пропилпарабен (ISTD) | 29,17 | 1,00 | 240 |
D.9 Полученные данные валидации
Пределы обнаружения, определенные для большинства кортикостероидов в разных образцах парфюмернокосметической продукции, приведены в таблице D.5.
Таблица D.5 — Значение предела обнаружения в парфюмерно-косметической продукции
Соединения | Молочко для тела, % | Масло для тела, % | Крем для тела, % |
Этоксифенол (МЕЕ) | <0,005 | <0,005 | <0,005 |
Гидрохинон (HQ) | / | / | <0,005 |
Метоксифенол (ММЕ) | <0,005 | <0,005 | <0,005 |
Монобензон (МВЕ) | <0,005 | <0,005 | 0,010 |
Бетаметазон (ВМ) | 0,010 | 0,010 | 0,010 |
Кортизон (CS) | 0,010 | 0,010 | 0,010 |
24
Окончание таблицы D.5
ГОСТ EN 16956—2020
Соединения | Молочко для тела, % | Масло для тела, % | Крем для тела, % |
Флуоцинолона ацетонид (FCA) | 0,010 | 0,010 | 0,010 |
Гидрокортизон (НС) | 0,010 | 0,010 | 0,010 |
Преднизолон (PL) | 0,010 | 0,010 | 0,010 |
Преднизолона сульфобензоат (PLSB) | 0,010 | / | |
Триамцинолон (TRI) | / | 0,010 | / |
Алклометазона дипропионат (ACD) | 0,050 | 0,020 | 0,020 |
Амцинонид (АМС) | 0,020 | 0,050 | 0,020 |
Беклометазона дипроприонат (BCD) | 0,020 | 0,020 | 0,020 |
Бетаметазона ацетат (ВМА) | 0,050 | 0,020 | 0,020 |
Бетаметазона дипроприонат (BMD) | 0,020 | 0,020 | 0,020 |
Бетаметазона валерат (BMV) | 0,050 | 0,020 | 0,020 |
Клобетазола пропионат (СР) | 0,020 | 0,020 | 0,020 |
Клокортолона пивалат (CLP) | 0,020 | 0,010 | 0,020 |
Дезоксиметазон (DXM) | 0,020 | 0,020 | 0,010 |
Дексаметазона ацетат (DMA) | 0,050 | 0,010 | / |
Дексаметазона фосфат(ОМРБ) | 0,050 | 0,020 | 0,020 |
Дифлукортолона BanepaT(DFCV) | 0,020 | 0,020 | 0,020 |
Дифлупреднат (DFP) | 0,020 | 0,050 | 0,020 |
Флукотортона гексаноат (FCH) | 0,020 | 0,020 | 0,050 |
Флуокортолона пивалат (FCP) | 0,020 | 0,020 | 0,020 |
Флурандренолид (FDL) | 0,020 | 0,020 | 0,020 |
Хальцинонид (HAL) | 0,020 | 0,020 | 0,020 |
Гидрокортизона бутират (НСВ) | 0,050 | 0,020 | 0,020 |
Мометазона фуроат (MMF) | 0,020 | 0,010 | 0,020 |
Предникарбат (PCN) | 0,050 | 0,020 | 0,020 |
Преднизолона ацетат (PLA) | 0,020 | / | 0,020 |
Преднизолона гексаноат (PLH) | 0,050 | 0,020 | 0,020 |
Триамцинолона ацетонид (TRA) | 0,020 | 0,020 | 0,020 |
Будезонид (BUD) | 0,100 | 0,050 | 0,050 |
Дезонид (DSN) | 0,050 | / | 0,020 |
Дифлоразона диацетат (DFD) | 0,050 | 0,020 | 0,050 |
Флуметазона пивалат (FMP) | 0,050 | 0,020 | / |
Флуоцинонид (FCAA) | 0,050 | 0,020 | 0,050 |
Гидрокортизона валерат (HCV) | 0,050 | 0,050 | 0,050 |
Для гидрокортизона ацетата (НСАР) и метилпреднизолона ацетата (MPLA) значения не определялись.
25
ГОСТ EN 16956—2020
Библиография
[1] EN ISO/IEC 17025 General requirements forthe competence of testing and calibration laboratories (ISO/IEC17025) (Общие требования к компетентности испытательных и поверочных лабораторий (ISO/IEC 17025))
[2] Cosmetic directive 95/32/ЕС «Identification and determination of hydroquinone in cosmetics» (Идентификация и определение гидрохинона в косметике)
[3] GIMENO Р., MAGGIO A.-F., BANCILHON М. et al. HPLC/UV method for the identification of hydroquinone, ethers of hydroquinone and corticosteroids possibly used as skin whitening agents in illicit cosmetic products. J. Chromatogr. Sci. 2015, pp. 1—10. DOI:10.1093/chromsci/bmv147 (Метод ВЭЖХ/УФ для идентификации гидрохинона, эфиров гидрохинона и кортикостероидов, используемых в качестве агентов в незаконно реализуемой косметической парфюмерно-косметической продукции отбеливания кожи)
УДК 665.584.014:543.544.5.068.7(083.74)(476)
МКС 71.100.70
IDT
Ключевые слова: продукция парфюмерно-косметическая, отбеливающая продукция, гидрохинон, эфиры гидрохинона, кортикостероиды, масс-спектрометрия
Технический редактор В.Н. Прусакова
Корректор С.И. Фирсова Компьютерная верстка М.В. Малеевой
Сдано в набор 09.01.2024. Подписано в печать 18.01.2024. Формат 60x84%. Гарнитура Ариал.
Усл. печ. л. 3,72. Уч.-изд. л. 2,98.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
Создано в единичном исполнении в ФГБУ «Институт стандартизации» , 117418 Москва, Нахимовский пр-т, д. 31, к. 2.

