ГОСТ EN 14164-2014
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ
Определение витамина с помощью высокоэффективной жидкостной хроматографии
Foodstuffs. Determination of vitamin B6 by high performance chromatography
МКС 67.050
Дата введения 2017-07-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-2015 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2015 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Республиканским государственным предприятием "Казахстанский институт стандартизации и сертификации" Комитета технического регулирования и метрологии и Техническим комитетом по стандартизации ТК N 71 "Экологическая безопасность сырья, материалов, веществ и сооружений"*
_______________
* На основе собственного перевода немецкоязычной версии стандарта, указанного в пункте 5.
2 ВНЕСЕН Комитетом технического регулирования и метрологии Министерства индустрии и новых технологий Республики Казахстан
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 29 августа 2014 г. N 69-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Молдова | MD | Молдова-Стандарт |
Россия | RU | Росстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 11 мая 2016 г. N 295-ст межгосударственный стандарт ГОСТ EN 14164-2014 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2017 г.
5 Настоящий стандарт идентичен европейскому стандарту EN 14164:2008* "Продукты пищевые. Определение витамина с помощью высокоэффективной жидкостной хроматографии" ("Foodstuffs - Determination of vitamin B6 by HPLC", IDT).
________________
* Доступ к международным и зарубежным документам, упомянутым здесь и далее по тексту, можно получить, перейдя по ссылке на сайт . - .
Европейский стандарт EN 14164:2008 подготовлен Техническим комитетом CEN/TC 275 "Анализ пищевых продуктов. Горизонтальные методы" Европейского комитета по стандартизации (CEN).
Официальный экземпляр европейского стандарта, на основе которого подготовлен настоящий межгосударственный стандарт, и европейского стандарта, на который дана ссылка, имеются в Федеральном информационном фонде технических регламентов и стандартов.
Сведения о соответствии ссылочных европейских региональных стандартов межгосударственным стандартам приведены в дополнительном приложении ДА.
Степень соответствия - идентичная (IDT)
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
1 Область применения
1 Область применения
Настоящий стандарт устанавливает метод определения витамина в пищевых продуктах с помощью высокоэффективной жидкостной хроматографии (далее - ВЭЖХ). Витамин
представляет собой сумму массовых долей пиридоксина, пиридоксаля, пиридоксамина, включая их фосфорилированные продукты замещения, в пересчете на пиридоксин. Они определяются по методу, указанному в [1], при помощи которого могут быть разделены и количественно определены как индивидуальные соединения - различные витамеры витамина
(пиридоксаль, пиридоксамин, пиридоксин). В [2] определяется общее содержание витамина
микробиологическим методом.
2 Нормативные ссылки
Для применения настоящего стандарта необходим следующий ссылочный нормативный документ*. Для датированных ссылок применяют только указанное издание ссылочного документа, для недатированных ссылок применяют последнее издание ссылочного документа (включая все его изменения):
_______________
* Таблицу соответствия национальных стандартов международным см. по ссылке. - .
EN ISO 3696:1997 Water for analytical laboratory use - Specification and test methods (Вода для лабораторного анализа. Технические требования и методы испытаний)
3 Сущность метода
Пиридоксаль, пиридоксамин, пиридоксин извлекают из продуктов питания в ходе гидролиза в кислой среде и дефосфорилируют ферментативным путем, используя кислую фосфатазу. В результате реакции с глиоксиловой кислотой в присутствии в качестве катализатора пиридоксамин превращается в пиридоксаль, который далее переходит в пиридоксин под воздействием борогидрида натрия в щелочной среде.
Затем пиридоксин количественно определяют в растворе пробы с помощью высокоэффективной жидкостной хроматографии с флуориметрическим детектором [3], [4].
4 Реактивы
4.1 Общие положения
Для испытаний используют реактивы гарантированной чистоты и воду не ниже 1-й степени чистоты в соответствии с EN ISO 3696.
4.2 Реактивы
4.2.1 Кислая фосфатаза из картофеля, ферментная активность составляет 33 нанокатал/мг с субстратом нитрофенилфосфатом (при рН = 4,8 и температуре 37°С), например, производства Boehringer или Sigma. Активность 33 нанокатал/мг соответствует 2 U/мг.
_______________ Катал (обозначается "кат") - единица измерения активности катализатора в системе СИ. Активность катализатора в один катал увеличивает скорость реакции на один моль/с в заданных условиях.
4.2.1.1 Раствор кислой фосфатазы
Готовят раствор кислой фосфатазы в растворе ацетата натрия (см. 4.2.14) массовой концентрации 20 мг/см.
Необходимо использовать кислую фосфатазу, а не Така-диастазу для достижения полного гидролиза фосфорилированных форм витамина . Там, где требуется 300 мг Така-диастазы для получения хорошего дефосфорилирования, кислой фосфатазы потребуется всего 0,5 мг (см. [5]).
4.2.1.2 Проверка активности кислой фосфатазы
Проверяют активность каждой новой партии кислой фосфатазы следующим образом. Готовят исходный раствор пиридоксальфосфата массовой концентрации 0,1 мг/см (см. 4.2.9) в воде. Отбирают для экстракции 5,0 см
этого раствора и проводят операции, предусмотренные в 6.2.1, 6.2.2, 6.2.3, 6.2.4 и 7.
Рассчитывают коэффициент извлечения пиридоксина из этого раствора и делят на теоретическое количество пиридоксина, выделенного из пиридоксальфосфата. Вычисляют теоретическую массовую концентрацию пиридоксина , мг/см
, выделенного из пиридоксальфосфата по формуле:
![]() , (1)
, (1)
где ![]() - массовая концентрация пиридоксальфосфата, определенная спектрофотометрическим методом в УФ-области;
- массовая концентрация пиридоксальфосфата, определенная спектрофотометрическим методом в УФ-области; - молярная масса образца сравнения витамина
- пиридоксина (
![]() 169,1), г/моль;
169,1), г/моль;
2 - коэффициент разбавления при реакции с борогидритом натрия;
5,0 - объем раствора, взятого для экстракции (см. 4.2.1.2), см;
100 - общий объем исследуемого раствора пробы, см;
![]() - молярная масса пиридоксальфосфата (
- молярная масса пиридоксальфосфата (![]() 265,16), г/моль.
265,16), г/моль.
Смешивают 3,0 см исходного раствора пиридоксальфосфата и 10 см
соляной кислоты (см. 2.21) в мерной колбе вместимостью 20 см
и разбавляют до метки водой. Проверяют концентрацию пиридоксальфосфата путем измерения поглощения при 295 нм в кювете с толщиной слоя 1 см, используя спектрофотометр для УФ-области спектра (см. 5.2) относительно раствора соляной кислоты (см. 4.2.20). Молярный коэффициент поглощения (
) пиридоксальфосфата в растворе соляной кислоты молярной концентрации 0,1 моль/дм
равен 8353.
Рассчитывают массовую концентрацию исходного раствора пиридоксальфосфата , мг/см
, по формуле:
![]() , (2)
, (2)
где - оптическая плотность раствора при 295 нм;
![]() - молярная масса пиридоксальфосфата (
- молярная масса пиридоксальфосфата (![]() 265,16), г/моль;
265,16), г/моль; - коэффициент разбавления (в данном случае
20/3);
- молярный коэффициент поглощения пиридоксальфосфата в 0,1 моль/дм
соляной кислоты при 295 нм, дм
мол
см
(
8353).
4.2.2 Ацетат натрия трехводный (тригидрат), с массовой долей (
![]() )
)99,0%.
4.2.3 Ледяная уксусная кислота, с массовой долей (
![]() )
)99,8%.
4.2.4 Глиоксиловая кислота, с массовой долей (
![]() )
)97,0%.
4.2.5 Сульфат железа (II) 7-водный (гептагидрат), с массовой долей (
![]() )
)99,5%.
4.2.6 Гидроксид натрия, с массовой долей (NaOH)
99,0%.
4.2.7 Борогидрид натрия, с массовой долей (
![]() )
)97,0%.
4.2.8 Дигидрофосфат калия, с массовой долей (
![]() )
)99,0%.
4.2.9 Пиридоксальфосфат (PLP), с массовой долей 99,0%.
4.2.10 Ортофосфорная кислота, с массовой долей (
![]() )
)84,0%.
4.2.11 1-октансульфонат натрия, с массовой долей (
![]() )
)98,0% или 1-гептансульфонат натрия, с массовой долей
(
![]() )
)98,0%.
4.2.12 Ацетонитрил (квалификации "для ВЭЖХ"), с массовой долей (
![]() )
)99,8%.
4.2.13 Раствор ацетата натрия, массовой концентрации c(![]() )=2,5 моль/дм
)=2,5 моль/дм.
Растворяют 170,1 г ацетата натрия трехводного (см. 4.2.2) в 500 см воды.
4.2.14 Раствор ацетата натрия, c(![]() )=0,05 моль/дм
)=0,05 моль/дм (рН = 4,5).
Растворяют 6,8 г ацетата натрия трехводного (см. 4.2.2) в 1 дм воды. Устанавливают рН = 4,5, используя ледяную уксусную кислоту (см. 4.2.3).
4.2.15 Раствор сульфата железа, c(![]() )=0,0132 моль/дм
)=0,0132 моль/дм.
Растворяют 36,6 мг сульфата железа (II) 7-водного (см. 4.2.5) в 10 см раствора ацетата натрия (см. 4.2.14). Раствор готовят в день использования.
Примечание - В исследовании, описанном в [10], использовался раствор сульфата железа с массовой концентрацией 10 г/дм. Эта концентрация была выбрана для осуществления полного превращения пиридоксамина в пиридоксаль на уровне содержания пиридоксамина в 8 раз большего минимального уровня витамина
, установленного законодательством США о детских смесях (см. [9]). Такая концентрация не является обязательной для европейских стран.
4.2.16 Раствор гидроксида натрия, c(NaOH)=0,2 моль/дм.
Растворяют 800 мг гидроксида натрия (см. 4.2.6) в 100 см воды.
4.2.17 Раствор гидроксида натрия, c(NaOH)=6,0 моль/дм.
Растворяют 24 г гидроксида натрия (см. 4.2.6) в 100 см воды.
4.2.18 Раствор борогидрида натрия, c(![]() )=0,1 моль/дм
)=0,1 моль/дм.
Растворяют 378 мг борогидрида натрия (см. 4.2.7) в 100 см раствора гидроксида натрия (см. 4.2.16). Раствор готовят в день использования.
4.2.19 Раствор глиоксиловой кислоты, с(![]() )=1 моль/дм
)=1 моль/дм (рН=4,5).
Растворяют 4,7 г моногидрата глиоксиловой кислоты (см. 4.2.4) в 30 см раствора ацетата натрия (см. 4.2.13).
Устанавливают значение рН 4,5, используя раствор гидроксида натрия (см. 4.2.17), и доводят водой до метки в мерной колбе вместимостью 50 см. Раствор готовят в день использования.
4.2.20 Соляная кислота, c(HCI)=0,1 моль/дм.
4.2.21 Соляная кислота, c(HCI)=0,2 моль/дм.
4.2.22 Подвижная фаза для ВЭЖХ.
В лабораторный стакан добавляют 940 см воды, 40 см
ацетонитрила (см. 4.2.12), 160 мг 1-октансульфоната натрия или 1-гептансульфоната натрия (см. 4.2.11) и 6,8 г дигидрофосфата калия (см. 4.2.8).
После растворения 1-октансульфоната натрия или 1-гептансульфоната натрия и дигидрофосфата калия устанавливают значение рН 2,5, используя ортофосфорную кислоту (см. 4.2.10). Раствор переносят в мерную колбу вместимостью 1 дм. Доводят до метки водой. Фильтруют через фильтр с размером пор 0,45 мкм.
4.3 Пиридоксина гидрохлорид (образец сравнения витамина ),
(
![]() )
)99%
4.4 Исходный раствор пиридоксина гидрохлорида с массовой концентрацией 0,5 мг/см
Растворяют 50 мг пиридоксина гидрохлорида в 100 см воды. Исходный раствор стабилен в течение четырех недель при хранении при температуре 4°С в темном месте.
Для определения массовой концентрации разбавляют 0,5 см исходного раствора пиридоксина гидрохлорида в 20 см
раствора соляной кислоты (см. 4.2.20) молярной концентрации 0,1 моль/дм
и измеряют оптическую плотность при 290 нм в кювете с толщиной поглощающего слоя 1 см, используя спектрофотометр для УФ-области спектра (см. 5.2) относительно раствора соляной кислоты молярной концентрации 0,1 моль/дм
. Рассчитывают массовую концентрацию исходного раствора, мкг/см
, по формуле:
![]() , (3)
, (3)
где - оптическая плотность раствора при 290 нм;
- молярная масса стандартного вещества витамина
, в г/моль (
![]() 205,64);
205,64); - коэффициент разбавления (
40);
- молярный коэффициент поглощения пиридоксина гидрохлорида в растворе соляной кислоты молярной концентрации 0,1 моль/дм
при 291 нм, в дм
/моль
см
(
8600 по [6]).
Дополнительная информация о молярных коэффициентах поглощения в других растворах, кроме раствора соляной кислоты молярной концентрации 0,1 моль/дм HCI (рН = 1), приведена в приложении D.
4.5 Стандартные растворы
4.5.1 Стандартный раствор пиридоксина гидрохлорида, c(![]() )=10 мкг/см
)=10 мкг/см
При помощи пипетки переносят 1 см исходного раствора витамина
(см. 4.4) в мерную колбу вместимостью 50 см
и доводят водой до метки. Раствор готовят в день использования.
4.5.2 Стандартные рабочие растворы пиридоксина гидрохлорида для ВЭЖХ, c(![]() ) от 0,1 до 1 мкг/см
) от 0,1 до 1 мкг/см
Готовят ряд соответствующих стандартных рабочих растворов пиридоксина гидрохлорида, массовая концентрация которых варьируется от 0,1 до 1 мкг/см, используя стандартный раствор пиридоксина (см. 4.5.1). Эти растворы готовят в день использования.
Проводят проверку пригодности хроматографической системы путем инжектирования смешанного стандартного рабочего раствора пиридоксина (PN) и пиридоксаля (PL). Пиридоксин (PN) и пиридоксаль (PL) должны иметь известную концентрацию в стандартном рабочем растворе для ВЭЖХ. Пиридоксаль (PL) элюируется перед пиридоксином (PN). Пара PN/PL должна иметь разделение до базовой линии. К отдельной пробе добавляют пиридоксамин (РМ), чтобы удостовериться в полноте дезаминирования и окисления.
5 Оборудование
Используется следующее лабораторное оборудование:
5.1 Стеклянная посуда.
5.2 Спектрофотометр для УФ-области спектра, предназначенный для измерений оптической плотности при заданных длинах волн.
5.3 Нагревательный прибор.
Печь или водяная баня с приспособлениями для встряхивания.
5.4 Система для высокоэффективной жидкостной хроматографии, состоящая из насоса, устройства для ввода пробы, флуоресцентного детектора с длинами волн возбуждения и регистрации, установленными на 290 и 395 нм соответственно, и системы обработки данных, например, интегратора.
5.5 ВЭЖХ-колонка, например, колонка для обращенно-фазовой хроматографии, такая как LiChrosper®60 RP С8 Select В, размер частиц 5 мкм, диаметр 4,0 мм, длина 250 мм.
Помимо указанных в настоящем стандарте, могут использоваться колонки других типоразмеров и с частицами другого размера. Параметры разделения должны быть адаптированы для таких материалов, чтобы гарантировать получение объективных результатов. Критерий эффективности для аналитических колонок - это полное разделение пиков рассматриваемых анализируемых веществ.
5.6 Фильтровальный прибор.
Фильтрование подвижной фазы, а также исследуемого раствора пробы через мембранный фильтр, например с размером пор фильтра 0,45 мкм, перед использованием или впрыскиванием продлит срок службы колонок.
6 Проведение испытаний
6.1 Подготовка проб для испытаний
Пробу гомогенизируют. Измельчают крупнозернистый материал, используя подходящий измельчитель, и снова перемешивают. Необходимо проводить предварительное охлаждение для избежания длительного воздействия высоких температур.
6.2 Подготовка раствора пробы
6.2.1 Извлечение
Взвешивают соответствующее количество пробы с точностью до 1 мг, например 2,5 г (если содержание витамина превышает 2 мкг/г) или 5 г (если содержание витамина менее 2 мкг/г), в конической колбе. Добавляют 50 см
раствора соляной кислоты (см. 4.2.20). Нагревают в течение 30 мин в кипящей водяной бане.
Примечания
1 - Для проб с высоким содержанием воды или низким содержанием витамина будет полезно увеличить массу пробы, например до 20 г, добавить соответствующий ей объем воды, например 25 см
, и сразу же добавить непосредственно 5 см
соляной кислоты массовой концентрацией c(HCI)=1 моль/дм
.
2 - Для проб с высоким содержанием жира желательно удалить его при помощи, например, петролейного эфира перед проведением кислотного гидролиза.
3 - Главным преимуществом предварительного кислотного гидролиза является улучшение этапа фильтрации для проб, содержащих крахмал. Имеющиеся в приложении В данные были в основном получены без проведения кислотного гидролиза. Модификация процедуры (без кислотного гидролиза) приведена в приложении С.
6.2.2 Ферментативная обработка
После охлаждения до комнатной температуры устанавливают в экстракте значение рН, равное 4,5, используя раствор ацетата натрия (см. 2.13), и добавляют 2,5 см раствора глиоксиловой кислоты массовой концентрации 1 моль/дм
(см. 4.2.19), 400 мм
раствора сульфата железа (см. 4.2.15) и 1 см
раствора кислой фосфатазы (см. 4.1.1). Оставляют раствор на ночь при температуре 37°С при непрерывном перемешивании.
После охлаждения до комнатной температуры доводят раствор водой до метки в мерной колбе вместимостью 100 см. Встряхивают и фильтруют. Смешивают 5,0 см
отфильтрованного раствора и 4,5 см
раствора борогидрида натрия молярной концентрации 0,1 моль/дм
(см. 4.2.18). Встряхивают в течение 3 мин. Для обеспечения полного разложения остатка борогидрида натрия можно добавить 0,5 см
ледяной уксусной кислоты (см. 4.2.3). При этом принимают во внимание коэффициент разбавления. Встряхивают в течение 1 мин.
Фильтруют через фильтр с размером пор 0,45 мкм. Используют этот отфильтрованный раствор для хроматографического анализа.
6.2.3 Идентификация
Идентифицируют пиридоксин путем сравнения времени удерживания отдельных пиков на хроматограммах раствора анализируемой пробы и стандартного раствора. Идентификацию пиков также можно провести путем добавления образца сравнения витамина в исследуемый раствор пробы.
Разделение и количественное определение являются удовлетворительными при соблюдении следующих условий испытаний (см. также рисунок А.1).
Неподвижная фаза: | LiChrosper®60 RP С8 Select В, размер частиц 5 мкм, 250 мм |
Подвижная фаза: | В соответствии с 4.2.22 |
Скорость потока: | 1 см |
Объем впрыскивания: | 30 мм |
Детектирование: флуориметрическое | Возбуждение: 290 нм, регистрация: 395 нм |
6.2.4 Определение методом ВЭЖХ
В хроматографическую систему последовательно вводят равные объемы (до 50 мм) стандартного рабочего раствора и раствора анализируемой пробы. При использовании внешнего стандарта вычисляют площадь пика путем интегрирования или же определяют его высоту и сравнивают полученные значения с соответствующими значениями для образца сравнения.
7 Обработка результатов
Вычисление результата проводят либо при помощи градуировочной характеристики, либо с использованием соответствующих программ интегратора или же применяют следующую упрощенную процедуру.
Вычисляют массовую долю витамина в пересчете на пиридоксин в мг/100 г пробы (
) по формуле:
![]() , (4)
, (4)
где - площадь или высота пика пиридоксина, полученная для исследуемого раствора исследуемой пробы, в единицах площади или высоты;
- массовая концентрация пиридоксина гидрохлорида в стандартном рабочем растворе, мкг/см
;
- площадь или высота пика пиридоксина, полученная при использовании стандартного рабочего раствора, в единицах площади или высоты;
- масса пробы, г;
100 - общий объем исследуемого раствора пробы, см;
2 - коэффициент разбавления реакции с борогидридом натрия при добавлении уксусной кислоты, в противном случае коэффициент разбавления равен 1,9;
1000 - коэффициент для перевода микрограммов в миллиграммы;
100 - коэффициент для приведения массовой доли к 100 г пробы;
0,822 - коэффициент для пересчета содержания пиридоксина гидрохлорида на пиридоксин.
В протоколе испытаний результат для витамина представляют в пересчете на пиридоксин и выражают в мг/100 г.
8 Протокол испытаний
В протоколе испытания должны содержаться следующие данные:
a) информация об идентификации пробы;
b) ссылка на настоящий стандарт;
c) дата отбора проб и процедура (если известны);
d) дата поступления пробы;
e) дата проведения испытания;
f) результаты и единицы измерений, в которых выражены результаты;
g) любые особенности, которые наблюдались в ходе испытания;
h) любые операции, не указанные в методе, или относящиеся к факультативным, которые могли повлиять на результаты.
Приложение А (справочное). Пример хроматограммы
Приложение А
(справочное)
Рисунок А.1 - Пример количественного определения пиридоксина в сухом молоке методом ВЭЖХ
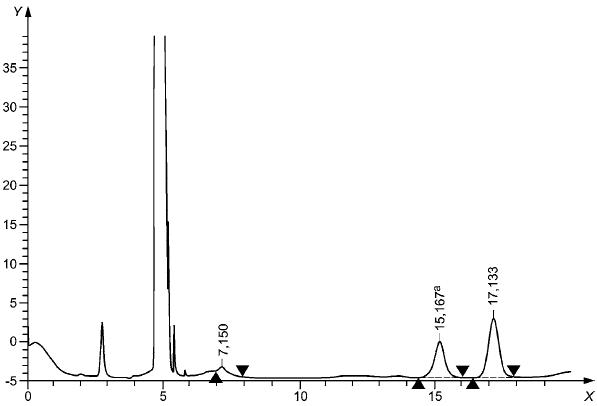
Ось - время в минутах
Ось - мВ
- пиридоксин
Неподвижная фаза: | LiChrosper®60 RP С8 Select В, размер частиц 5 мкм, 250х4,0 мм |
Подвижная фаза: | В соответствии с 4.2.22 |
Скорость потока: | 1 см |
Объем впрыскивания: | 30 мм |
Детектирование: флуориметрическое | Возбуждение: 290 нм, регистрация: 395 нм |
Рисунок А.1 - Пример количественного определения пиридоксина в сухом молоке методом ВЭЖХ
Приложение В (справочное). Данные о прецизионности
Приложение В
(справочное)
Данные были получены главным образом при использовании метода, описанного в приложении С, который не предусматривает гидролиза. Кислотный гидролиз не влияет на результаты испытания.
Данные о прецизионности для определения витамина в таблице В.1 были установлены в ходе межлабораторного испытания в соответствии с [7], которое проводилось Главным управлением в области конкуренции, потребления и преследования мошенничества законом (DGCCRF).
При межлабораторном испытании была использована аналитическая колонка LiChrosper®60 RP 8 Select В, размер частиц 5 мкм, диаметр 4,0 мм, длина 250 мм.
Данные о прецизионности для определения содержания витамина в таблице В.2 были установлены в ходе межлабораторного испытания в соответствии с положениями Ассоциации химиков-аналитиков, работающих в государственных организациях (АОАС Guidelines), для проведения совместного изучения для подтверждения характеристик метода анализа (см. [8]), (см. [9], [10] и основанные на методе (см. [3]). Совместное изучение проводилось с использованием Luna ® 5 мкм фенил-гексиловой колонки для ВЭЖХ
.
_______________ Luna ® 5 мкм фенил-гексиловая колонка для ВЭЖХ - это пример подходящего продукта, имеющегося в продаже. Данная информация приведена только для удобства пользователей и не является рекламированием CEN названного продукта. Можно использовать эквивалентные продукты, если они приводят к получению аналогичных результатов.
Таблица В.1 - Данные о прецизионности для определения содержания витамина
Проба | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Год проведения межлабораторного испытания | 1993 | 1993 | 1993 | 1993 | 1993 | 1993 | 1993 | 1993 |
Количество лабораторий | 12 | 12 | 12 | 12 | 12 | 12 | 12 | 12 |
Количество лабораторий, оставшихся после удаления выбросов | 11 | 10 | 11 | 12 | 11 | 11 | 12 | 11 |
Количество оставшихся результатов | 32 | 29 | 31 | 36 | 33 | 33 | 35 | 33 |
Среднее значение, | 0,06 | 0,14 | 0,22 | 0,53 | 0,55 | 0,67 | 1,50 | 3,28 |
Стандартное отклонение повторяемости | 0,01 | 0,02 | 0,02 | 0,04 | 0,02 | 0,03 | 0,10 | 0,09 |
Относительное стандартное отклонение повторяемости | 18 | 3 | 10 | 8 | 4 | 4 | 6 | 3 |
Предел повторяемости | 0,03 | 0,05 | 0,06 | 0,12 | 0,06 | 0,08 | 0,27 | 0,26 |
Стандартное отклонение воспроизводимости | 0,02 | 0,05 | 0,07 | 0,14 | 0,07 | 0,08 | 0,18 | 0,43 |
Относительное стандартное отклонение воспроизводимости | 30 | 35 | 30 | 26 | 1 | 12 | 12 | 13 |
Предел воспроизводимости | 0,05 | 0,14 | 0,19 | 0,39 | 0,20 | 0,23 | 0,51 | 1,22 |
Индекс Горвица [11] | 1,7 | 2,3 | 2,1 | 2,1 | 1,1 | 1,1 | 1,1 | 1,4 |
|
Таблица В.2 - Данные о прецизионности для определения содержания витамина в восстановленных детских смесях
Проба | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Год проведения межлабораторного испытания | 2003 | 2003 | 2003 | 2003 | 2003 | 2003 | 2003 | 2003 |
Количество лабораторий | 11 | 11 | 11 | 11 | 11 | 11 | 11 | 11 |
Количество лабораторий, оставшихся после удаления выбросов | 9 | 9 | 8 | 9 | 7 | 9 | 9 | 9 |
Количество оставшихся результатов | 18 | 18 | 16 | 18 | 14 | 18 | 18 | 18 |
Среднее значение | 0,013 | 0,036 | 0,057 | 0,101 | 0,005 | 0,028 | 0,056 | 0,106 |
Стандартное отклонение повторяемости | 0,001 | 0,001 | 0,001 | 0,004 | 0,001 | 0,002 | 0,003 | 0,004 |
Относительное стандартное отклонение повторяемости | 10 | 3,3 | 2,0 | 4,0 | 16,4 | 5,9 | 4,5 | 3,5 |
Предел повторяемости | 0,0028 | 0,0028 | 0,0028 | 0,0112 | 0,0028 | 0,0056 | 0,0084 | 0,0112 |
Стандартное отклонение воспроизводимости | 0,002 | 0,003 | 0,005 | 0,006 | 0,002 | 0,003 | 0,004 | 0,007 |
Относительное стандартное отклонение воспроизводимости | 17,5 | 8,2 | 8,4 | 8,4 | 52,1 | 11,2 | 7,4 | 6,4 |
Предел воспроизводимости | 0,0056 | 0,0084 | 0,014 | 0,0168 | 0,0056 | 0,0084 | 0,0112 | 0,0196 |
Индекс Горвица [11] | 0,81 | 0,44 | 0,48 | 0,53 | 2,06 | 0,58 | 0,42 | 0,43 |
|
Приложение С (справочное). Факультативный способ подготовки пробы без кислотного гидролиза
Приложение С
(справочное)
Пункты 6.2.1-6.2.2 настоящего стандарта могут быть заменены следующей процедурой:
Взвешивают в конической колбе необходимое количество пробы с точностью до 1 мг, например, 2,5 г (если содержание витамина превышает 2 мкг/г) или 5,0 г (если содержание витамина менее 2 мкг/г). Добавляют 25 см
раствора ацетата натрия массовой концентрации 0,05 моль/дм
(см. 4.2.14), 2,5 см
раствора глиоксиловой кислоты молярной концентрации 1 моль/дм
(см. 4.2.19), 400 мм
раствора сульфата железа (см. 4.2.15) и 20 мг раствора кислой фосфатазы (см. 4.2.1). Оставляют раствор на ночь при температуре 37°С при непрерывном перемешивании.
После охлаждения до комнатной температуры доводят водой до метки в мерной колбе вместимостью 50 см. Встряхивают и фильтруют. Смешивают 5,0 см
отфильтрованного раствора и 4,5 см
раствора борогидрида натрия молярной концентрации 0,1 моль/дм
(см. 4.2.18). Встряхивают в течение 3 мин. Добавляют 0,5 см
ледяной уксусной кислоты (см. 4.2.3). Встряхивают в течение 1 мин. Фильтруют через фильтр с размером пор 0,45 мкм. Этот отфильтрованный раствор используют для хроматографического анализа.
При проведении вычислений в формуле (4) заменяют общий объем исследуемого раствора пробы 100 см на 50 см
.
Приложение D (справочное). Примеры молярных коэффициентов поглощения
Приложение D
(справочное)
D.1 Примеры молярных коэффициентов поглощения () производных витамина
[6], [12] приведены в таблице D.1.
Таблица D.1
Соединения | Растворитель |
|
|
|
Пиридоксина гидрохлорид | 0,1 моль/дм | 291 | 8600 | 205,6 |
Пиридоксина гидрохлорид | 0,1 моль/дм | 323,8 | 7300 | 205,6 |
Пиридоксаля гидрохлорид | 0,1 моль/дм | 288 | 8960 (9000) | 203,6 |
Пиридоксаль-5'-фосфат | 0,1 моль/дм | 388 | 5020 | 247,1 |
Пиридоксамина дигидрохлорид | 0,1 моль/дм | 292 | 8200 | 241,1 |
Пиридоксамина дигидрохлорид | 0,1 моль/дм | 253 | 4600 | 241,1 |
Пиридоксамин-5'-фосфат гидрохлорид | 0,1 моль/дм | 326 | 8370 | 241,1 |
Приложение ДА (справочное). Сведения о соответствии ссылочных европейских стандартов межгосударственным стандартам
Приложение ДА
(справочное)
Таблица ДА.1
Обозначение и наименование европейского стандарта | Степень соответствия | Обозначение и наименование межгосударственного стандарта |
EN ISO 369 | - | * |
* Соответствующий межгосударственный стандарт отсутствует. До его утверждения рекомендуется использовать перевод на русский язык данного европейского стандарта. Перевод данного европейского стандарта находится в Федеральном информационном фонде технических регламентов и стандартов. |
Библиография
[1] | EN 14663 Foodstuffs - Determination of vitamin B6 (including its glycosylated forms) by HPLC [Продукты пищевые. Определение витамина В6 (включая гликозилированные формы) методом высокоэффективной жидкостной хроматографии] |
[2] | EN 14166 Foodstuffs - Determination of vitamin B6 by microbiological assay (Продукты пищевые. Определение содержания витамина |
[3] | Bergaentzle М., Arella F, Bourguignon J.В., Hasselmann С. Determination of vitamin B6 in foods by HPLC: a collaborative study. Food Chem (1995), 52, 81-86 (Определение витамина B6 в пищевых продуктах методом высокоэффективной жидкостной хроматографии: совместное изучение, Food Chem (1995), 52, 81-86) |
[4] | Reitzer-Bergaentzle М., Marchioni Е., Hasselmann С. HPLC determination of vitamin B6 in foods after pre-column derivatization of free and phosphorylated vitamers into pyridoxol. Food Chem (1993), 48, 321-324 (Определение витамина |
[5] | Ndaw S., Bergaentzle M., Aoude-Werner D., Hasselmann С. Extraction procedures for the Liquid hromatographic determination of thiamin, riboflavin and vitamin B6 in foodstuffs. Food Chem, (2000), 71, 129-138 (Процедуры экстракции для жидкостно-хроматографического определения тиамина, рибофлавина и витамина |
[6] | Metzlerand Snell (1955): Spectra and ionisation constants of the vitamin B6 group and related 3-hydroxypyridine derivates. Journal of the American Chemical Society 77:2431-2437 (Константы спектра и ионизации витаминов группы |
[7] | ISO 5725 Accuracy (trueness and precision) of measurement methods and results [Точность (правильность и прецизионность) методов и результатов измерений] |
[8] | International 1995. АОАС Official Methods Program, Associate Referee's Manual on development, Study, Review, and Approval Process. Part IV AOAC Guidelines for Collaborative Studies, p.23-51 (Международная Ассоциация химиков-аналитиков, состоящих на государственной службе. 1995, Программа официальных методов, руководство по разработке, изучению обзору и процессу одобрения. Часть IV. Рекомендации АОАС по совместным изучениям, стр.23-51) |
[9] | Mann D.L., Chase G.W., Eitenmiller R.R. Liquid Chromatographic analysis of vitamin B6 in soy-based infant formula. JAOAC (2001). 84, 5:1596 (Жидкостно-хроматографический анализ витамина |
[10] | Mann D.L., Ware G.W., Bonnin E. Liquid Chromatographic analysis of vitamin B6 in reconstituted infant formula: Collaborative Study. JAOAC (2005), 88,1:30-37 (Жидкостно-хроматографический анализ витамина |
[11] | Evaluation of Analylical Methods used for Regulation of Foods and Drugs, W. Horwitz, Anal. Chem. 1982,54 (1). 67A-76A) Оценка аналитических методов, используемых в регулировании пищевых продуктов и лекарственных средств) |
[12] | Oiliiainen V (1999): HPL Canalysisofvitamin В6 infoods. Agriculturaland Food Sciencein Finland 8.559 (Анализ методом высокоэффективной жидкостной хроматографии витамина |
УДК 641.1:577.164.13:543.544.5:006.354 | МКС 67.050 | IDT |
Ключевые слова: витамин |
Электронный текст документа
и сверен по:
официальное издание
М.: Стандартинформ, 2016

