ГОСТ Р 53133.2-2008
Группа Р20
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Технологии лабораторные клинические
КОНТРОЛЬ КАЧЕСТВА КЛИНИЧЕСКИХ ЛАБОРАТОРНЫХ ИССЛЕДОВАНИЙ
Часть 2
Правила проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований с использованием контрольных материалов
Clinical laboratory technologies. Quality control of clinical laboratory tests. Part 2. Rules for intra-laboratory quality control of quantitative methods of clinical laboratory tests using control materials
ОКС 11.020
Дата введения 2010-01-01
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. N 184-ФЗ "О техническом регулировании", а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 РАЗРАБОТАН Лабораторией проблем клинико-лабораторной диагностики Московской медицинской академии им. И.М.Сеченова, отделом сертификации и контроля качества клинических лабораторных исследований Государственного научного центра профилактической медицины, лабораторией клинической химии Научно-исследовательского института нейрохирургии Российской академии медицинских наук, Закрытым акционерным обществом "Аналитика"
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 466 "Медицинские технологии"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии Российской Федерации от 18 декабря 2008 г. N 559-ст
4 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячно издаваемых информационных указателях "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
1 Область применения
Настоящий стандарт устанавливает общие требования к проведению внутрилабораторного контроля качества количественных исследований, выполняемых в клинико-диагностических лабораториях, организациях здравоохранения, в составе которых действуют указанные лаборатории.
Настоящий стандарт предназначен для применения всеми организациями, учреждениями и предприятиями, а также индивидуальными предпринимателями, деятельность которых связана с оказанием медицинской помощи гражданам Российской Федерации.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р ИСО 5725-1-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения
ГОСТ Р ИСО 5725-3-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 3. Промежуточные показатели прецизионности стандартного метода измерений
ГОСТ Р ИСО 15189-2006 Лаборатории медицинские. Частные требования к качеству и компетентности
ГОСТ Р ИСО/МЭК 17025-2006 Общие требования к компетентности испытательных и калибровочных лабораторий
ГОСТ Р ИСО 17511-2006 Изделия медицинские для диагностики in vitro. Измерение величин в пробах биологического происхождения. Метрологическая прослеживаемость значений, приписанных калибраторам и контрольным материалам
ГОСТ Р 52361-2005 Контроль объекта аналитический. Термины и определения
ГОСТ Р 53079.2-2008 Технологии лабораторные клинические. Обеспечение качества клинических лабораторных исследований. Часть 2. Руководство по качеству исследований в клинико-диагностической лаборатории. Типовая модель
ГОСТ Р 53133.3-2008 Технологии лабораторные клинические. Контроль качества клинических лабораторных исследований. Часть 3. Описание материалов для контроля качества клинических лабораторных исследований
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодно издаваемому указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1
аналит (analyte): Компонент, представленный в наименовании измеряемой величины. [ГОСТ Р ИСО 17511-2006, пункт 3.2] |
Примечание - В ГОСТ Р 52361, статья 17, приведено следующее определение этого термина: "Компонент, искомый или определяемый в пробе вещества или материала объекта аналитического контроля".
ПРИМЕР - В наименовании величины "масса белка в 24-часовой моче" "белок" является аналитом. В наименовании величины "количество вещества глюкозы в плазме" "глюкоза" является аналитом. В обоих случаях вся фраза представляет собой измеряемую величину.
ПРИМЕР - В наименовании величины "каталитическая концентрация изофермента 1 лактат-дегидрогеназы в плазме" "изофермент 1 лактатдегидрогеназы" является аналитом. Все выражение обозначает измеряемую величину).
3.2 аналитический этап (analytical period, analytical phase): Совокупность действий в соответствии с установленным и описанным процессом проведения лабораторного анализа проб пациентов и контрольных материалов.
Примечание - Данный этап лабораторного исследования завершается получением результата измерения.
3.3 аналитическая серия (analytical run): Совокупность измерений аналита, выполненных в одних и тех же условиях без перенастройки и калибровки аналитической системы, при которых характеристики аналитической системы остаются стабильными.
Примечание - Продолжительность аналитической серии (по числу измерений) определяется рекомендациями изготовителей средств измерения, условиями данной лаборатории. Рекомендуемая максимальная продолжительность аналитической серии по времени - 24 ч (без перенастройки и калибровки).
3.4 аналитическая система (analytical run): Совокупность приборов (включая программное обеспечение), калибраторов, реагентов и расходных материалов, необходимых для выполнения измерения аналита.
3.5
значение (величины) [value (of quantity)]: Числовое выражение величины, обычно в виде некоторого числа и единицы измерения. [[1], статья 1.18] |
Примечания
1 Значение величины может быть положительным, отрицательным, равным нулю.
2 Значение величины может выражаться более чем одним способом.
3 Значения величин с размерностью единица обычно выражаются отвлеченными числами.
4 Значение, которое не может быть выражено в виде числа и единицы измерения, может быть выражено путем отнесения к условной опорной шкале измерений, или ссылкой на методику измерения, или обоими способами.
3.6
измеряемая величина (mesurand): Конкретная величина, являющаяся объектом измерения. [[1], статья 2.6] |
3.7 исследование (examination): Комплекс операций, результатом которых является определение значения величины или характеристики ее свойств.
3.8
истинное значение (величины) [true value (of a quantity)]: Значение, адекватное определению данной конкретной величины. [[1], статья 1.19] |
Примечания
1 Это значение, которое может быть получено путем идеального измерения.
2 Истинные значения по своей природе неопределимы.
3 В иностранных языках с понятием "истинное значение" используют, как правило, неопределенные артикли (a, une, ein, un), а не определенные (the, la, der, el), так как может быть несколько значений, соответствующих определению данной конкретной величины.
3.9
калибратор (calibrator), [калибровочный материал (calibrator material)]: Стандартный образец, числовое значение которого используется как независимая переменная в калибровочной функции. [ГОСТ Р ИСО 17511-2006, пункт 3.7] |
3.10
калибровка (calibration): Совокупность операций, устанавливающих в заданных условиях соотношения между значениями величин, показанных средством измерений или измерительной системой и значениями, представленными материальной мерой или стандартным образцом, и соответствующими значениями, воспроизводимыми эталонами. [[1], статья 6.11] |
3.11 контрольный материал (control material): Однородный материал человеческого или животного происхождения или искусственный материал, приближающийся, насколько это возможно, по своим наиболее существенным свойствам к исследуемому биологическому материалу пробы и предназначенный для оценки качества измерений аналитов в пробах пациентов, выполняемых в клинико-диагностических лабораториях медицинских организаций.
Примечание - Термин "контрольный материал" может быть использован для материалов, реализующих номинальные свойства, например цвет.
3.12
матрица (материальной системы) [matrix (of a material system)]: Совокупность компонентов материальной системы за исключением аналита. [ГОСТ Р ИСО 15194-2007, пункт 3.3] |
Примечание - В ГОСТ Р 52361, пункте 40 приведено следующее определение данного термина: "Компонент или совокупность компонентов, образующих данное вещество или материал объекта аналитического контроля и являющихся его основой".
3.13
методика измерения (measurement procedure): Совокупность конкретно описанных операций, используемых при выполнении конкретных измерений в соответствии с данным методом. [[1], статья 2.5] |
Примечания
1 Метод измерения, будучи описан в общем виде, не имеет заданных числовых характеристик выполнения. Данный метод может быть основой одной или нескольких методик измерения, каждая из которых имеет присущие ей числовые значения характеристик выполнения.
2 Измерительную процедуру обычно записывают в документ, который иногда называется "Методика измерений" и обычно достаточно детально обеспечивает информацией оператора, выполняющего измерения, без привлечения дополнительной информации.
3.14
неопределенность измерения (uncertainty of measurement): Параметр результата измерения, характеризующий дисперсию значений, которые могут быть обоснованно приписаны измеряемой величине. [[1], статья 3.9] |
Примечания
1 В качестве параметра может быть, например, среднеквадратическое отклонение (или кратное ему) или половина интервала с заданным уровнем доверительной вероятности.
2 Неопределенность измерения, в общем виде, включает в себя множество составляющих. Некоторые из них могут быть оценены по статистическому распределению результатов ряда измерений и охарактеризованы экспериментальными среднеквадратическими отклонениями. Другие составляющие, которые могут быть охарактеризованы среднеквадратическими отклонениями, оцениваются по предполагаемым распределениям вероятностей, основанных на опыте или другой информации.
3 Здесь понимается, что результат измерения является наилучшей оценкой значения измеряемой величины, а все составляющие неопределенности, включая и те, которые возникают из-за систематических эффектов, таких как составляющие, связанные с внесением поправок и исходными эталонами, вносят свой вклад в разброс ([2], пункт 2.2.4 и приложение D).
3.15 оперативный контроль качества (operative quality control): Выполнение повседневных (ежесерийных) процедур внутрилабораторного контроля качества с использованием контрольных материалов.
3.16
повторяемость (результата проверки); сходимость (repeatability): Прецизионность в условиях повторяемости. [ГОСТ Р 50779.10-2000, статья 3.15] |
3.17
условия повторяемости (repeatability conditions): Условия, при которых независимые результаты проверки получены одним методом на идентичных испытательных образцах, в одной лаборатории, одним оператором, с использованием одинакового оборудования и за короткий интервал времени. [ГОСТ Р ИСО 50779.10-2000, статья 3.16] |
3.18
принятое опорное значение (accepted reference value): Значение, которое может служить в качестве согласованного для сравнения и получено как: a) теоретическое или установленное значение, базирующееся на научных принципах; b) приписанное или аттестованное значение, базирующееся на экспериментальных работах какой-либо национальной или международной организации; c) согласованное или аттестованное значение, базирующееся на совместных экспериментальных работах под руководством научной или инженерной группы; d) математическое ожидание измеряемой характеристики, то есть среднее значение заданной совокупности результатов измерений - лишь в случае, когда перечисления а), b) и с) недоступны. [ГОСТ Р ИСО 5725-1-2002, пункт 3.5] |
3.19
правильность (trueness): Степень близости среднего значения, полученного на основании большой серии результатов измерений (или результатов испытаний), к принятому опорному значению. Примечание - Показателем правильности обычно является значение систематической погрешности. [ГОСТ Р ИСО 5725-1-2002, пункт 3.7] |
3.20 предельно допускаемые значения характеристик погрешностей (limiting permissible maximum value of errors characteristics): Крайние значения погрешностей, допускаемые нормативными документами для результата измерения аналита в контрольных материалах.
3.21
прецизионность (precision): Степень близости друг к другу независимых результатов измерений, полученных в конкретных регламентированных условиях. [ГОСТ Р ИСО 5725-1-2002, пункт 3.12] |
Примечания
1 Прецизионность зависит только от случайных погрешностей и не имеет отношения к истинному или установленному значению измеряемой величины.
2 Меру прецизионности обычно выражают в терминах неточности и вычисляют как стандартное отклонение результатов измерений. Меньшая прецизионность соответствует большему стандартному отклонению.
3 Независимые результаты измерений (или испытаний) - результаты, полученные способом, на который не оказывает влияние предшествующий результат, полученный при испытаниях того же самого или подобного объекта. Количественные значения мер прецизионности существенно зависят от регламентированных условий. Крайними случаями совокупностей таких условий являются условия повторяемости и условия воспроизводимости.
3.22
промежуточная прецизионность (intermediate precision): Характеризует вариацию результатов, наблюдающуюся при изменении одного или более факторов, таких как время, оборудование или оператор в пределах одной лаборатории. [ГОСТ Р ИСО 5725-1-2002, статья 3.12] |
Примечание - Воспроизводимость (reproducibility), характеризующую прецизионность измерений, выполненных в неодинаковых условиях, то есть в разных лабораториях, различными операторами, с использованием различных аналитических систем (включая различную калибровку, различные партии реагентов), часто обозначают как межлабораторную прецизионность.
3.23
случайная погрешность (random error): Разность между результатом измерения и средним значением многократных измерений одной и той же измеряемой величины, выполненных в условиях сходимости. [[1], статья 3.13] |
3.24
систематическая погрешность (bias): Разность между математическим ожиданием результатов измерений и истинным (или в его отсутствии - принятым опорным) значением. [ГОСТ Р ИСО 5725-1-2002, статья 3.8] |
Примечания
1 Большое систематическое отклонение от принятого опорного значения находит свое отражение в большом значении систематической погрешности.
2 Определение термина "bias", содержащееся в ГОСТ Р ИСО 5725-1, статья 3.8 и примечании 1, фактически соответствует понятию "систематическая погрешность" (systematic error), приведенному в [1], статья 3.14. Термин "bias (of measuring instrument)" в [1], статья 5.25 определен как "смещение (неправильность средства измерений)" - систематическая погрешность в показаниях средства измерений.
3 В качестве составляющих систематической погрешности выделяют неисключенную систематическую погрешность, составляющую систематической погрешности измерений, обусловленную несовершенством реализации принятого принципа измерений (ГОСТ Р ИСО 5725-1, подраздел 3.10), погрешность градуировки применяемого средства измерений и др.
4 Если математическое ожидание систематической погрешности известно и постоянно, то в результат измерений вносят поправку. Знак поправки противоположен знаку погрешности.
Когда систематическая погрешность пропорциональна значению измеряемой величины, то для исключения влияния систематической погрешности используют поправочный множитель (числовой коэффициент - correction factor), на который умножают неисправленный результат [[1], статья 3.16].
3.25
точность (accuracy): Степень близости результата измерений к принятому опорному значению. [ГОСТ Р ИСО 5725-1-2002, статья 3.6] |
Примечание - Термин "точность", когда он относится к серии результатов измерений (испытаний), включает в себя сочетание случайных составляющих и общей систематической погрешности.
4 Внутрилабораторный контроль в системе управления качеством клинических лабораторных исследований
4.1 Общие положения
4.1.1 Настоящий стандарт разработан для нормативного обеспечения повседневных внутрилабораторных процедур контроля качества (оперативного контроля качества), направленных на выявление недопустимых случайных и систематических погрешностей на аналитическом этапе клинических лабораторных исследований, выполняемых количественными методами с помощью контрольных материалов.
4.1.2 Контроль качества аналитического этапа клинических лабораторных исследований является неотъемлемой частью системы взаимосвязанных мер по управлению качеством клинических лабораторных исследований.
4.1.3 Контроль качества аналитического этапа клинических лабораторных исследований существует в двух взаимодополняющих формах: внутрилабораторного контроля качества и внешней оценки качества.
4.1.4 Комплексную систему контроля качества клинических лабораторных исследований осуществляют путем:
- установления единых требований к аналитическому качеству количественных методов;
- ежесерийного выполнения процедур внутрилабораторного контроля качества с использованием контрольных материалов (оперативный контроль качества);
- регулярного участия в программах внешней оценки качества.
4.1.5 В настоящем стандарте приведены единые требования к аналитическому качеству количественных методов измерения аналитов в биологических жидкостях (приложение А).
Предельные допускаемые значения характеристик погрешностей установлены путем экспертной оценки данных и нахождения компромисса между:
а) клинически обоснованными требованиями к качеству лабораторных исследований;
б) фактическими характеристиками качества, полученными в результате деятельности системы внешней оценки качества;
в) сведениями о биологической вариации компонентов биологических жидкостей [3], [4].
Примечания
1 Расчет клинически обоснованных допустимых значений погрешностей был произведен в соответствии с рекомендациями Европейской рабочей группы организаторов внешнего контроля качества клинических лабораторных исследований [5].
2 Пределы погрешностей, рассчитанные на основе данных внешней оценки качества, отражают реально достигаемый уровень точности в большинстве лабораторий, использующих доступные методы исследования аналитов, реагенты, приборы.
4.2 Общие принципы организации и проведения внутрилабораторного контроля качества в клинико-диагностических лабораториях
Наличие системы внутрилабораторного контроля качества является необходимым условием получения достоверной аналитической информации.
Проверку наличия системы внутрилабораторного контроля качества в клинико-диагностических лабораториях осуществляют территориальные органы управления здравоохранением.
Организация и обеспечение внутрилабораторного контроля качества количественных методов клинических лабораторных исследований являются обязанностью заведующего лабораторией или сотрудника, ответственного за обеспечение качества исследований.
Внутрилабораторный контроль качества клинических лабораторных исследований выполняется сотрудниками каждой клинико-диагностической лаборатории для поддержания стабильности аналитической системы.
Внутрилабораторный контроль качества обязателен в отношении всех видов количественных исследований, выполняемых в лаборатории, для которых разработаны контрольные материалы.
Примечание - Если для количественного метода контрольные материалы недоступны, рекомендуется использование других способов контроля качества с использованием проб пациентов: метод оценки воспроизводимости измерений аналита "по дубликатам", "по ежедневным средним" и др.
Порядок и технология проведения внутрилабораторного контроля качества измерений лабораторных показателей должны выполняться в соответствии с настоящим стандартом.
Рекомендуется использование лабораторией компьютерных программ для ведения внутрилабораторного контроля качества, разрешенных к использованию в установленном порядке в клинико-диагностических лабораториях Российской Федерации.
Примеры регистрационных форм для внесения результатов внутрилабораторного контроля качества приведены в приложениях к настоящему стандарту:
а) регистрационная форма "Оценка повторяемости результатов измерения" (приложение Б);
б) регистрационная форма "Результаты установочных серий измерений показателя в контрольных материалах" (приложение В);
в) журнал "Регистрации отбракованных результатов внутрилабораторного контроля качества" (приложение Г).
Отчеты о выполнении оперативного контроля качества должны оформляться в виде контрольных карт (согласно 5.4.2.1), таблиц, журналов на бумажных или электронных носителях и архивируются на срок не менее трех лет. Все регистрационные формы и журналы должны быть представлены в "Руководстве по качеству" клинико-диагностической лаборатории в соответствии с требованиями, установленными в ГОСТ Р 53079.2.
5 Правила проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований с использованием контрольных материалов
5.1 Контрольные материалы
Контрольные материалы должны быть аттестованы, зарегистрированы и разрешены к использованию в установленном порядке федеральным органом исполнительной власти в сфере здравоохранения.
В настоящем стандарте рассматривают правила применения следующих контрольных материалов:
- с аттестованными (принятыми, опорными) значениями контролируемых аналитов, которые должны использоваться для оценки прецизионности (воспроизводимости) измерений и расчета относительного смещения (правильности измерений) по результатам измерения аналитов в установочной серии;
- аттестованных на наличие аналита и диапазон его значений (нормальный, патологический), которые должны использоваться для оценки прецизионности (контрольные материалы прецизионности).
Примечание - Уровни исследуемых компонентов в контрольном материале должны соответствовать значениям показателей в нормальном и патологическом диапазонах; за нормальный принимается диапазон значений лабораторного показателя, соответствующий состоянию здоровья обследуемого, за патологический - диапазон, соответствующий состоянию болезни пациента.
В инструкции (паспорте) к контрольному материалу в соответствии с ГОСТ Р ИСО 17025* и ГОСТ Р ИСО 17511 должны быть указаны:
_______________
* Вероятно ошибка оригинала. Следует читать ГОСТ Р ИСО/МЭК 17025. - .
Аттестованное значение аналита и пределы неопределенности аттестованного значения аналита или наличие аналита и диапазон его измерений; перечень аналитов и методы их исследования; матрица контрольного материала; условия его хранения и срок годности и другие характеристики (по ГОСТ Р 53133.3).
Примечания
1 Для одного и того же показателя в документах на контрольный материал может быть указано несколько значений отдельно по каждому методу измерения или для каждой аналитической системы.
2 Аттестованное значение контрольного материала нельзя использовать в качестве среднеарифметического значения () для построения контрольной карты.
5.2 Использование контрольных материалов
Внутрилабораторный контроль качества с использованием контрольных материалов должен выполняться в течение достаточно длительного времени с использованием одного и того же контрольного материала (одного пула/лота) - на протяжении не менее 200 аналитических серий (для гематологических анализаторов - не менее 40 серий). Количество закупаемого контрольного материала зависит от стабильности, срока годности контрольного материала и числа исследований, подлежащих контролю в данной лаборатории.
Подготовка контрольного материала к исследованию и хранение после приготовления проводится в соответствии с инструкцией изготовителя. Для хранения замороженного контрольного материала при минус 20 °С и более низких температурах рекомендуется использовать специальные лабораторные морозильные камеры.
Контрольные материалы должны исследоваться так же, как пробы пациентов, то есть в тех же аналитических сериях.
Контрольный материал нельзя использовать в качестве калибровочного материала.
При реконструкции лиофилизированных форм для уменьшения значения погрешности дозирования необходимо использовать одно и то же поверенное дозирующее устройство (допускается использование стеклянной пипетки класса А).
Примечание - Для экономного использования реконструированного контрольного материала допускается разлить содержимое флакона на аликвоты. Объем аликвот (не менее 0,5 миллилитра) должен помещаться в пробирки или флаконы соответствующей вместимости с герметичными крышками. Материал, из которого изготовлены пробирки, не должен адсорбировать компоненты контрольного материала (кальций, альбумин и др.). Хранение аликвот проводят в соответствии с рекомендациями изготовителя.
5.3 Статистические основы оценки погрешностей количественных методов исследования с применением контрольных материалов
Статистической основой оценки погрешностей при внутрилабораторном контроле качества количественных методов лабораторных исследований является допущение о том, что частотные распределения результатов многократного измерения одного и того же контрольного материала одним и тем же аналитическим методом имеют вид нормального распределения. Для оценки случайных и систематических погрешностей измерения используются следующие статистические характеристики:
- среднеарифметическое значение (среднеарифметическое)
![]() , (1)
, (1)
где - результат
-го измерения из
выполненных;
- число измерений;
![]() - сумма результатов измерений
- сумма результатов измерений ,
, ...,
;
- среднеквадратическое отклонение :
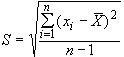 , (2)
, (2)
где ![]() - сумма квадратов отклонений результатов измерений
- сумма квадратов отклонений результатов измерений ,
, …,
от среднеарифметического
;
- коэффициент вариации :
![]() . (3)
. (3)
Среднеквадратическое отклонение и коэффициент вариации
служат характеристикой случайных погрешностей и используются для оценки повторяемости и прецизионности измерений.
Среднеарифметическое значение используется при расчете смещения
в установочной серии измерений. Смещение
определяется близостью среднеарифметического значения результатов установочной серии измерений контрольного материала
к аттестованному значению (
) измеряемой величины (см. 5.1) и может быть выражено в абсолютных и/или относительных величинах. Относительную систематическую погрешность или смещение
рассчитывают по формуле
![]() . (4)
. (4)
В полученном результате обязательно указывают знак числа ("+" или "-").
5.4 Порядок проведения внутрилабораторного контроля качества
Выявление недопустимых случайных погрешностей выполняют путем оценки повторяемости и промежуточной прецизионности (далее - прецизионности) результатов измерения аналитов в контрольном материале (по результатам установочной серии измерений); систематических погрешностей с помощью оценки относительного смещения. Систематическое выполнение процедур оперативного контроля качества позволяет с помощью контрольных правил и установленных контрольных пределов для каждого аналита выявить недопустимые погрешности и провести работу по их устранению (см. 5.4.1 и 5.4.2).
Порядок проведения внутрилабораторного контроля качества для каждой выполняемой в лаборатории количественной методики исследования состоит из трех последовательных стадий:
Стадия 1 - оценка повторяемости результатов измерений.
Стадия 2 - оценка прецизионности и относительного смещения по результатам установочной серии измерений, построение контрольных карт.
Стадия 3 - проведение оперативного внутрилабораторного контроля качества.
Примечание - Предварительную оценку повторяемости, прецизионности и относительного смещения (правильности измерений) лабораторного показателя (1 и 2 стадии внутрилабораторного контроля качества) выполняют при внедрении в работу лаборатории каждой новой методики. В случае внесения существенных изменений в аналитическую систему, а именно, принципа аналитического измерения (приборов, реактивов, калибраторов, технологической процедуры и др.) стадии 1 и 2 внутрилабораторного контроля качества следует повторить. При использовании контрольного материала того же изготовителя введение нового лота требует выполнения только стадий 2 и 3.
Принятые обозначения в тексте - результаты измерений лабораторного показателя, получаемые в лаборатории, оцениваются по значениям коэффициента вариации и относительного смещения, в тексте настоящего стандарта обозначаются следующими символами:
- повторяемость, индекс "
" - within run (внутри серии);
- прецизионность, соответственно в 10 аналитических сериях;
- прецизионность, соответственно в 20 аналитических сериях;
- относительное смещение (правильность), соответственно в 20 аналитических сериях.
Формулы расчета (1-4) приведены выше.
5.4.1 Стадия 1 - оценка повторяемости результатов измерений*
________________
* Оценку повторяемости рекомендуется выполнять не только при замене компонентов аналитической системы, но и при анализе причин неудовлетворительной прецизионности результатов исследования аналита.
Цель: проверка соответствия повторяемости результатов измерения установленным нормам.
Исследуемый материал: контрольный материал или проба пациента со значением аналита в нормальном диапазоне.
Последовательность выполнения:
а) провести 10 измерений на одном и том же материале в одной аналитической серии;
б) результаты измерений внести в регистрационную форму "Оценка повторяемости результатов измерения" (приложение Б);
в) по формулам 1-3 рассчитать значение коэффициента вариации ;
г) проверить, что полученное значение не превышает половины значения
(приложение А):
![]() ; (6)
; (6)
д) если значение превышает
![]() , необходимо выявить источники недопустимо больших случайных погрешностей и провести работу по их устранению. Затем следует повторить стадию 1;
, необходимо выявить источники недопустимо больших случайных погрешностей и провести работу по их устранению. Затем следует повторить стадию 1;
е) при соответствии повторяемости установленным нормам переходят к следующей стадии.
5.4.2 Стадия 2 - оценка прецизионности и относительного смещения по результатам установочной серии измерений, построение контрольных карт
Цель: оценка соответствия значений коэффициента вариации и относительного смещения
установленным нормам.
Исследуемый материал: контрольные материалы с аттестованными значениями аналитов - для оценки значений коэффициента вариации и относительного смещения
; контрольные материалы прецизионности - для оценки значений коэффициента вариации
.
Примечание - Все контрольные материалы могут использоваться в стадии 3 для проведения оперативного контроля качества.
Последовательность выполнения:
а) провести измерение показателя в 20 аналитических сериях; в каждой серии по одному измерению одновременно в двух контрольных материалах.
Примечание - После выполнения 10 аналитических серий из 10 полученных результатов измерения для каждого контрольного материала следует рассчитать значения и
и сравнить с предельно допустимыми значениями, указанными в приложении А. Если полученные значения
и
превышают допустимые, следует выявить источники погрешностей и провести работу по их устранению. Затем следует повторить перечисление а); если полученные значения не превышают установленных норм, выполняют следующие 10 аналитических серий. Указанный расчет по 10 измерениям аналита в контрольных материалах следует проводить для предварительной оценки погрешностей в установочной серии измерений (см. таблицу 1);
Таблица 1 - Последовательность процедур при введении внутрилабораторного контроля качества (установочная серия измерений)
Наименование процедуры | Исследуемый материал | Число серий | Число измерений в серии для каждого материала | Рассчи- |
Стадия 1 | ||||
Оценка повторяемости измерений | Контрольный материал или проба пациента | 1 | 10 | |
Стадия 2 | ||||
Предварительная оценка относительного смещения | Аттестованные контрольные материалы | 10 | 1 | |
Предварительная оценка прецизионности измерений | Контрольные материалы для текущего ежесерийного контроля | 10 | 1 | |
Окончательная оценка относительного смещения | Аттестованные контрольные материалы | 20 | 1 | |
Окончательная оценка прецизионности измерений | Контрольные материалы для текущего ежесерийного контроля | 20 | 1 | |
Построение контрольной карты | Контрольные материалы для текущего ежесерийного контроля | 20 | 1 |
|
б) результаты внести в регистрационную форму "Результаты установочных серий измерений показателя в контрольных материалах" (приложение Г);
в) из полученных для каждого из контрольных материалов 20 результатов с использованием формул 1-3 рассчитать значения коэффициента вариации и сравнить его с предельно допустимым значением (приложение А);
г) если полученное значение превышает допустимое, следует выявить источники погрешностей и провести работу по их устранению. Затем следует повторить перечисления а), б), в);
д) если значения коэффициента вариации не превышают установленных норм, следует рассчитать относительное смещение
по формуле 4 и сравнить его с предельно допустимым значением
(приложение А);
е) если полученное значение превышает допустимое, следует установить причину отклонения и устранить ее. Затем следует повторить перечисления а), б), в), г);
ж) если полученное значение не превышает допустимое, делают окончательный вывод о возможности использования рассматриваемой методики для целей лабораторной диагностики и переходят к следующему этапу - построению контрольных карт.
5.4.2.1 Построение контрольных карт
Выполнение в стадии 2 двадцати измерений лабораторного показателя в контрольных материалах называют установочными сериями измерений, по результатам которых рассчитывают среднеарифметическое значение , среднеквадратическое отклонение
и контрольные пределы для каждого контрольного материала.
Цель: построение контрольных карт.
Последовательность выполнения:
- Из полученных в установочной серии 20 результатов измерений определяемого показателя рассчитывают: среднеарифметическое значение (формула 1), среднеквадратическое отклонение
(формула 2), контрольные пределы:
![]() ,
, ![]() и
и ![]() .
.
- Если в ряду результатов оказалось значение, выходящее за пределы , то его не учитывают; выполняют еще одну аналитическую серию, после чего снова подсчитывают значения
и
.
Контрольная карта, построенная по установочной серии измерений, представляет собой график, на оси абсцисс которого откладывается номер аналитической серии (или дата ее выполнения), а на оси ординат - значения определяемого показателя в контрольном материале (рисунок 1).
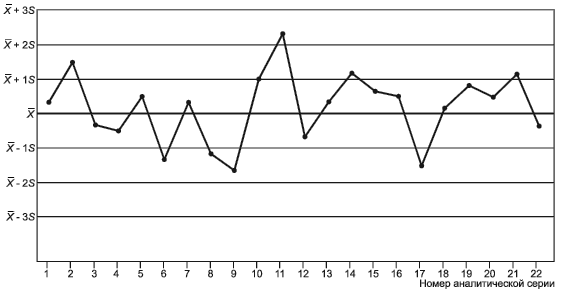
Рисунок 1 - Пример контрольной карты
- Через середину оси ординат проводится линия, соответствующая среднеарифметическому значению , и параллельно этой линии отмечаются линии, соответствующие контрольным пределам:
![]() - контрольный предел "1 среднеквадратическое отклонение";
- контрольный предел "1 среднеквадратическое отклонение";
![]() - контрольный предел "2 среднеквадратических отклонения";
- контрольный предел "2 среднеквадратических отклонения";
![]() - контрольный предел "3 среднеквадратических отклонения".
- контрольный предел "3 среднеквадратических отклонения".
- Контрольные карты строят для каждого лабораторного показателя и для каждого контрольного материала, предназначенного для оперативного контроля качества.
Контрольные карты оформляют и архивируют в виде графиков, таблиц в бумажном или электронном виде.
5.4.3 Стадия 3 - проведение оперативного внутрилабораторного контроля качества
Проведение оперативного контроля качества количественных методов лабораторных исследований предполагает измерение аналита в контрольных материалах и оценку приемлемости результатов исследования проб пациентов в каждой аналитической серии. Приемлемость результатов измерений проб пациентов в каждой аналитической серии оценивают по результатам исследования контрольных материалов с помощью контрольных правил. Окончательное решение о приемлемости проб пациентов в данной аналитической серии принимает специалист по клинической лабораторной диагностике, исходя из допускаемых значений пределов погрешностей для данного аналита и его клинической значимости.
Цель: оценка приемлемости результатов исследования проб пациентов и подтверждение стабильности аналитической системы по результатам исследования контрольных материалов в каждой аналитической серии.
Исследуемый материал: для оперативного контроля качества лаборатория должна использовать контрольный материал промышленного производства в двух диапазонах определяемых показателей.
Последовательность выполнения:
- в каждой аналитической серии проводится однократное (как минимум) измерение показателя в каждом контрольном материале. Число образцов пациентов в аналитической серии не ограничивается;
- образцы контрольных материалов следует равномерно распределять среди анализируемых проб пациентов при отсутствии иных указаний изготовителей приборов и реагентов;
- наносят точки, соответствующие результатам контрольных измерений, на соответствующие контрольные карты;
- при отклонении результатов контрольных измерений за контрольные пределы оценить приемлемость результатов проб пациентов в данной аналитической серии с помощью контрольных правил*:
- проверить присутствие на обеих контрольных картах предупредительного контрольного правила ;
- если один из результатов анализа контрольных материалов выходит за пределы ![]() , последовательно проверить наличие контрольных правил
, последовательно проверить наличие контрольных правил ,
,
,
и
; аналитическая серия признается неудовлетворительной при наличии одного из них:
- одно из контрольных измерений выходит за пределы
![]() .
.
- два последних контрольных измерения превышают предел
![]() или лежат ниже предела
или лежат ниже предела ![]() ;
;
- два контрольных измерения в рассматриваемой аналитической серии расположены по разные стороны от коридора
![]() ;
;
- четыре последних контрольных измерения превышают
![]() или лежат ниже предела
или лежат ниже предела ![]() ;
;
- десять последних контрольных измерений располагаются по одну сторону от линии, соответствующей
;
- если в дополнение к нарушению признака обнаруживается хотя бы один из указанных признаков:
,
,
,
или
, все результаты, полученные в данной аналитической серии, следует считать неприемлемыми (рисунок 2);
- контрольные признаки ,
,
следует проверять на одной контрольной карте и/или на обеих контрольных картах (рисунок 3);
- проведение анализа приостановить, выявить и устранить причины возникновения повышенных погрешностей. Все пробы, проанализированные в этой серии (и пациентов, и контрольные), исследовать повторно;
- результаты измерения контрольных материалов в серии, признанной неприемлемой, не должны использоваться при оценке по контрольным правилам повторной и последующих серий;
- в случае, если ни один из признаков, перечисленных выше, не обнаруживается ни на одной контрольной карте, проведение исследований следует продолжить;
- решение о приемлемости результатов измерения аналита в биологическом материале пациентов принимается сотрудником, отвечающим за качество исследований. Если результаты аналитической серии признаются неприемлемыми, делается соответствующая запись в журнале "Регистрация отбракованных результатов внутрилабораторного контроля качества" (приложение Г).
________________
* Контрольное правило включает в себя контрольный предел (![]() ,
,![]() ,
,![]() ) и число контрольных измерений в аналитической серии. Контрольные правила обозначаются символами типа
) и число контрольных измерений в аналитической серии. Контрольные правила обозначаются символами типа , где
- число контрольных результатов,
- контрольный предел.
Рисунок 2 - Схема последовательного применения контрольных правил
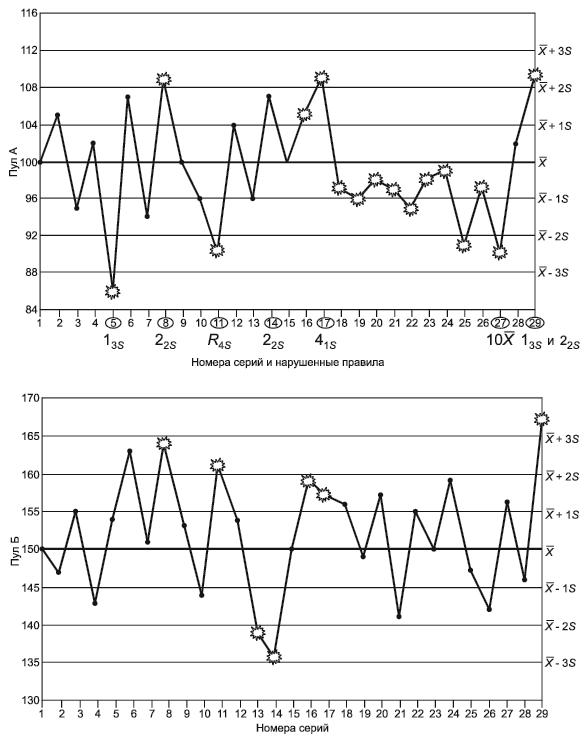
Рисунок 3 - Примеры нарушения контрольных правил в случае двух контрольных материалов
Пул А - контрольный материал с нормальными значениями: 100,
4.
Пул Б - контрольный материал с патологическими значениями: 150,
5.
Обведены номера неудовлетворительных серий и указаны нарушенные в них правила.
Контрольный признак является предупредительным, выявление его не должно приводить к отбраковке результатов аналитической серии и повторному исследованию проб. Выявление контрольных признаков:
- свидетельствует о наличии грубой погрешности,
- о появлении случайной ошибки, а признаки
,
и
- об увеличении систематической ошибки методики.
Для установления надежных контрольных пределов после проведения не менее 50 аналитических серий (включая установочную серию) рекомендуется пересчитать значения и
и, если необходимо, построить новую контрольную карту. Из расчета должны быть исключены значения контрольного материала тех серий, которые не учитывались.
Статистические расчеты и выполнение оперативного контроля качества в повседневной работе лаборатории рекомендуется выполнять с помощью компьютерных программ. Пример контрольных карт для двух контрольных материалов, на которых представлены серии, являющиеся неудовлетворительными ввиду нарушения разных контрольных правил, приведен на рисунке 3.
5.4.4 Смена контрольного материала
Для сохранения непрерывности внутрилабораторного контроля в период, когда используемого контрольного материала остается только на 20 аналитических серий, необходим переход на новый контрольный материал путем проведения так называемого "перекрывания".
Перекрывание состоит в том, что в течение 20* серий (периода перекрывания) лаборатория исследует одновременно заканчивающийся материал ("используемый"), по которому продолжается осуществление текущего контроля, и материал, который его заменяет ("вводимый"). При этом пробы вводимого контрольного материала располагают в положениях, отстоящих на две или более позиции от положений, в которых расположены пробы используемого контрольного материала. Например, если пробы используемого контрольного материала находятся в положениях 07, 36, то пробы вводимого контрольного материала можно разместить в положениях 04, 33.
________________
* Число серий периода перекрывания может быть больше 20. Для гематологических анализаторов период перекрывания составляет 4 аналитические серии.
По результатам, полученным для вводимого контрольного материала, рассчитывают среднее арифметическое значение и среднеквадратическое отклонение, по которым строится новая контрольная карта.
Приложение А
(рекомендуемое)
Предельно допускаемые значения смещения и коэффициента вариации
определения лабораторных показателей в контрольном материале
В таблице А.1 приведены сведения о предельно допускаемых погрешностях, на которые даны ссылки в 4.5.1 и 4.5.2 настоящего стандарта.
Таблица А.1 - Предельно допускаемые значения погрешностей
Исследование биологических жидкостей | Код ОКПМУ* |
|
|
|
|
Исследование уровня аланинтрансаминазы* в крови | 09.05.042 | ±17 | 16 | ±15 | 15 |
Исследование уровня альбумина в крови | 09.05.011 | ±5 | 4 | ±4 | 4 |
Исследование уровня амилазы* в крови | 09.05.045 | ±16 | 11 | ±15 | 10 |
Исследование уровня аспартатрансаминазы* в крови | 09.05.041 | ±11 | 11 | ±10 | 10 |
Исследование уровня общего белка в крови | 09.05.010 | ±5 | 3 | ±5 | 3 |
Исследование уровня общего билирубина в крови | 09.05.021 | ±17 | 16 | ±15 | 15 |
Исследование уровня гамма-глутамилтрансферазы* в крови | 09.05.044 | ±16 | 11 | ±15 | 10 |
Исследование уровня глюкозы в крови | 09.05.023 | ±6 | 5 | ±5 | 5 |
Исследование уровня железа в крови | 09.05.007 | ±12 | 17 | ±10 | 16 |
Исследование уровня калия в крови | 09.05.031 | ±5 | 4 | ±4 | 4 |
Исследование уровня кальция в крови | 09.05.032 | ±3,4 | 3,3 | ±3,0 | 3,0 |
Исследование уровня креатинина в крови | 09.05.020 | ±11 | 8 | ±10 | 7 |
Исследование уровня креатинкиназы* в крови | 09.05.043 | ±23 | 22 | ±20 | 20 |
Исследование уровня лактатдегидрогеназы* и ее изоферментов в крови | 09.05.039 | ±11 | 11 | ±10 | 10 |
Исследование уровня магния в крови | 09.05.132 | ±7 | 7 | ±6 | 6 |
Исследование уровня мочевой кислоты в крови | 09.05.018 | ±11 | 8 | ±10 | 7 |
Исследование уровня мочевины в крови | 09.05.017 | ±11 | 11 | ±10 | 10 |
Исследование уровня натрия в крови | 09.05.030 | ±1,8 | 2,2 | ±1,5 | 2,0 |
Исследование уровня нейтральных жиров и триглицеридов плазмы крови | 09.05.025 | ±17 | 16 | ±15 | 15 |
Исследование уровня фосфатов (неорганических) в крови | 09.05.033 | ±8 | 8 | ±7 | 7 |
Исследование уровня хлоридов в крови | 09.05.034 | ±3,4 | 3,3 | ±3,0 | 3,0 |
Исследование уровня холестерина в крови | 09.05.026 | ±9 | 8 | ±8 | 7 |
Исследование уровня щелочной фосфатазы* в крови | 09.05.046 | ±16 | 11 | ±15 | 10 |
Определение белка в моче | 09.28.003 | ±24 | 27 | ±20 | 25 |
Исследование уровня глюкозы в моче | 09.28.011 | ±22 | 16 | ±20 | 15 |
Исследование уровня общего гемоглобина в крови | 09.05.003 | ±5 | 4 | ±4 | 4 |
Исследование уровня эритроцитов в крови | 08.05.003 | ±7 | 4 | ±6 | 4 |
* Обозначения услуг даны в соответствии с ОКПМУ - отраслевым классификатором простых медицинских услуг. | |||||
Приложение Б
(рекомендуемое)
Форма регистрации результатов оценки повторяемости результатов измерения
В форму регистрации результатов оценки повторяемости результатов измерения аналита в одной аналитической серии вносят рассчитанное по формулам 1-3 среднеквадратическое отклонение и значение коэффициента вариации , которое сравнивают со значением 0,5
(приложение А).
Повторяемость результатов измерения аналита
Лаборатория: Отдел: | Показатель: | |||
Дата измерения: | Исследуемый материал (нужное подчеркнуть): | |||
проба пациента, | контрольный материал | |||
Методика измерения: | Контрольный материал (наименование, диапазон значений): | |||
Исполнитель: | Изготовитель контрольного материала: | N партии контрольного материала: | Срок годности контрольного материала: | |
Порядковый номер измерения | Результат измерения показателя ( |
|
|
1 | |||
2 | |||
3 | |||
4 | |||
5 | |||
6 | |||
7 | |||
8 | |||
9 | |||
10 | |||
Число результатов |
|
| |
|
| Повторяемость приемлема: | |
да | нет | ||
- знак суммы результатов.
Заведующий клинико-диагностической лабораторией ___________________ | подпись |
Приложение В
(рекомендуемое)
Форма регистрации результатов установочных серий измерений показателя в контрольных материалах
Данная форма регистрации результатов оценки прецизионности и относительного смещения (правильности) результатов измерения контрольных материалов в установочных аналитических сериях заполняется для каждого лабораторного показателя, исследуемого в лаборатории.
Прецизионность и правильность результатов измерения контрольных материалов
Лаборатория: | Показатель: | Дата проведения измерений | |||||||||||||||
Контрольный материал: (наименования) | Срок годности: | Изготовитель: | N партии | Паспортное значение (диапазон значений): | |||||||||||||
1 | |||||||||||||||||
2 | |||||||||||||||||
Прибор и его метрологические характеристики*: | Методика измерения: | Реактивы: | |||||||||||||||
Серия исследований | Контрольный материал 1 | Контрольный материал 2 | |||||||||||||||
Результат измерения |
|
| Результат измерения |
|
| ||||||||||||
1 | |||||||||||||||||
2 | |||||||||||||||||
3 | |||||||||||||||||
4 | |||||||||||||||||
5 | |||||||||||||||||
6 | |||||||||||||||||
7 | |||||||||||||||||
8 | |||||||||||||||||
9 | |||||||||||||||||
10 | |||||||||||||||||
11 | |||||||||||||||||
12 | |||||||||||||||||
13 | |||||||||||||||||
14 | |||||||||||||||||
15 | |||||||||||||||||
16 | |||||||||||||||||
17 | |||||||||||||||||
18 | |||||||||||||||||
19 | |||||||||||||||||
20 | |||||||||||||||||
|
|
|
| ||||||||||||||
|
|
| |||||||||||||||
|
|
| |||||||||||||||
Прецизионность в 20 сериях | Прецизионность в 20 сериях | ||||||||||||||||
приемлема: | да | нет | приемлема: | да | нет | ||||||||||||
Правильность по 20 сериям | Правильность по 20 сериям | ||||||||||||||||
приемлема: | да | нет | приемлема: | да | нет | ||||||||||||
* Прецизионность средства измерения, диапазон измерений (рабочий диапазон) устанавливается калибровкой средства измерения, что подтверждает его пригодность для предполагаемого использования. | |||||||||||||||||
Заведующий клинико-диагностической лабораторией ____________________ | (подпись) |
Приложение Г
(рекомендуемое)
Форма регистрации отбракованных результатов внутрилабораторного контроля качества
В данную форму регистрации заносят данные об отбракованных при проведении оперативного контроля аналитических сериях (по датам, с указанием причин выбраковки)
Данные об отбракованных аналитических сериях
Лаборатория: Отдел: | Показатель: | Методика выполнения измерений: | ||
Прибор: | Реактивы: | Контрольный материал (название, диапазон значений): | ||
Изготовитель: | N партии: | Срок годности: | ||
День | Запись* | Подпись |
________________
* При выбраковке результатов сотрудник делает запись о произведенных действиях: проверка калибровки, инструментов, дозирования, повторное измерение результатов отбракованной аналитической серии. В конце каждого месяца заведующий лабораторией просматривает регистрационные листы и делает выводы с соответствующими комментариями по поводу предпринятых действий и решений.
Дата: | Обзор результатов за месяц: комментарии, действия, решения: | Подпись заведующего лабораторией |
Библиография
[1] | Международный словарь основных и общих терминов в метрологии 2-е издание ИСО, Женева, 1993 | Русско-англо-французский-немецко-испанский словарь основных и общих терминов в метрологии - М.: ИПК Издательство стандартов: 1998 - 160 с. | |
[2] | Руководство для выражения неопределенности при измерении ИСО, Женева, 1993 | Руководство ЕВРАХИМ/СИТАК Количественное описание неопределенности в аналитических измерениях (второе издание) - С.-Петербург: Пер. с англ., ВНИИМ им. Д.И.Менделеева, 2002, 141 с. | |
[3] | M.A.Sebastian-Gambaro, F.J.Liron-Hernandez, X.Fuentes-Arderiu. - Intra- and Inter Individual Biological Variability Data Bank. - Eur.J.Clin.Chem.Clin.Biochem., 1997, 35, 11, 845-852 | ||
[4] | Ricos C., Alvares V., Cava F., Garcia-Lario J.V., Hernandez A., Jimenz C.V., Minchinela J., Perich C., Simon M. - Current databases on biologic variation: pros, cons and progress. - Scand J.Clin.Lab Invest 1999, V.59, p.491-500. | ||
[5] | Compendium on Advanced External Quality Assurance in Clinical Biochemistry. Editor A.Uldall, Denmark, 2000. | ||
Электронный текст документа
и сверен по:
, 2009