ГОСТ Р ИСО 15473-2016
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
КАЧЕСТВО ПОЧВЫ
Оценка анаэробной биоразлагаемости органических химических веществ в почве
Soil quality. Evaluation of anaerobic biodegradation of organic chemicals in soil
ОКС 13.080.30
Дата введения 2017-02-01
Предисловие
1 ПОДГОТОВЛЕН Некоммерческим партнерством "Координационно-информационный центр содействия предприятиям по вопросам безопасности химической продукции" (НП "КИЦ") на основе собственного перевода на русский язык англоязычной версии стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 326 "Биотехнологии"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 29 июня 2016 г. N 742-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 15473:2002* "Качество почвы. Оценка анаэробной биоразлагаемости органических химических веществ в почве" (ISO 15473:2002 "Soil quality - Guidance on laboratory testing for biodegradation of organic chemicals in soil under anaerobic conditions", IDT).
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные и межгосударственные стандарты, сведения о которых приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
6 ПЕРЕИЗДАНИЕ. Август 2019 г.
Правила применения настоящего стандарта установлены в статье 26 Федерального закона от 29 июня 2015 г. N 162-ФЗ "О стандартизации в Российской Федерации". Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе "Национальные стандарты", а официальный текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
Введение
Органические химические вещества могут быть введены в почву как намеренно, так и попасть случайно, после чего они могут разлагаться в результате биологического воздействия. Для разлагаемых химических веществ скорость разложения может значительно различаться в зависимости не только от молекулярной структуры химического вещества, но и также от условий в почве, таких как температура, вода, доступ кислорода, что влияет на деятельность микроорганизмов. Деятельность микроорганизмов часто играет важную роль в процессах разложения.
ИСО 11266 [3] дает общие указания по выбору и методам испытания для определения биоразложения органических химических веществ в почвах в аэробных условиях.
Для оценки скорости и степени биоразложения в анаэробных условиях, а также для оценки способность* почвы разлагать органические химические вещества в этих условиях необходимы соответствующие методы испытаний.
________________
* Текст документа соответствует оригиналу. - .
В настоящем стандарте приведен метод испытания для определения биоразложения органических химических веществ в почвах в анаэробных условиях.
1 Область применения
Настоящий стандарт устанавливает метод определения биоразложения органических химических веществ в почвах в анаэробных условиях.
Примечание - Если метод будет использоваться для проведения испытания в рамках регистрации химических веществ, в Руководстве OECD по определению разложения в почве [20] приведена полезная информация по дополнительным требованиям к испытанию.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты. Для датированных ссылок применяют только указанное издание ссылочного стандарта, для недатированных - последнее издание (включая все изменения).
ISO 10381-6:1993 Soil quality - Sampling - Part 6: Guidance on the collection, handling and storage of soil for the assessment of aerobic microbial processes in the laboratory (Качество почвы. Отбор образцов. Часть 6. Руководство по отбору, транспортировке и хранению образцов почвы для лабораторной оценки аэробных микробных процессов)
ISO 10390:1994 Soil quality - Determination of pH (Качество почвы. Определение pH)
ISO 10694:1995 Soil quality - Determination of organic and total carbon after dry combustion (elementary analysis) [Качество почвы. Определение содержания органического и общего углерода после сухого сжигания (элементарный анализ)]
ISO 11260:1994 Soil quality - Determination of effective cation exchange capacity and base saturation level using barium chloride solution (Качество почвы. Определение эффективной катионообменной способности и порога насыщения с применением раствора хлорида бария)
ISO 11261:1995 Soil quality - Determination of total nitrogen - Modified Kjeldahl method (Качество почвы. Определение содержания общего азота. Модифицированный метод Кьельдаля)
ISO 11271 Soil quality - Determination of redox potential - Field method [Качество почвы. Определение окислительно-восстановительного (редокс) потенциала. Полевой метод]
ISO 11274:1998 Soil quality - Determination of the water retention characteristic - Laboratory methods (Качество почвы. Определение водоудерживающей способности. Лабораторные методы)
ISO 11277:1998 Soil quality - Determination of particle size distribution in mineral soil material - Method by sieving and sedimentation (Качество почвы. Определение гранулометрического состава минеральных почв. Метод просеивания и осаждения)
ISO 14239:1997 Soil quality - Laboratory incubation systems for measuring the mineralization of organic chemicals in soil under aerobic conditions (Качество почвы. Лабораторные инкубационные системы для измерения минерализации органических соединений в почве в аэробных условиях)
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 биоразложение (biodegradation): Разложение на молекулярном уровне органических соединений, происходящее в результате комплексного воздействия живых организмов.
[ИCO 11266]
3.2 первичное биоразложение (primary biodegradation): Разложение вещества в степени, достаточной, чтобы исчезли некоторые характерные свойства исходной молекулы. На практике это определяется таким анализом, как потеря из исходного соединения или некоторые специфические функции исходного соединения.
[ИСО 11266]
3.3 полное биоразложение (ultimate biodegradation): Разрушение органического соединения диоксидом углерода, водой, оксидами или минеральными солями каких-либо присутствующих элементов и продуктов, связанных с обычными процессами метаболизма микроорганизмов.
[ИСО 11266]
3.4 анаэробная трансформация (anaerobic transformation): Реакция, протекающая в условиях отсутствия кислорода (условия восстановления).
Примечание - Такие реакции обычно протекают, когда окислительно-восстановительный потенциал () менее 200 мВ [17].
3.5 персистентность (persistente): Продолжительность пребывания химических веществ в конкретном определенном объекте окружающей природной среды.
[ИСО 11266]
3.6 время исчезновения DT-50 (the disappearance time DT-50): Время, за которое концентрация данного соединения уменьшается на 50% от исходного значения.
[ИСО 11266]
3.7 время исчезновения DT-90 (the disappearance time DT-90): Время, за которое концентрация данного соединения уменьшается на 90% от исходного значения.
[ИСО 11266]
3.8 связанные остатки, неэкстрагируемые остатки (bound residues; non-extractable residues): Химические соединения в растениях и почвах, образовавшиеся, например, из органических молекул, которые не извлекаются методами, которые существенно не изменяют химическую природу этих остатков.
Примечание - Такие неэкстрагируемые остатки рассматривают для учета недостающих фрагментов метаболических процессов, приводящих к образованию конечных продуктов [12].
3.9 почва (soil): Верхний слой земной коры, состоящий из минеральных частей, органических веществ, воды, воздуха и живой материи.
[ИСО 11074-1]
3.10 испытуемое вещество (test substance): Исследуемое химическое вещество, добавленное в тест-систему.
3.11 насыщенные почвы (saturated soil): Часть почвы, полностью насыщенная водой.
4 Сущность метода
Настоящий стандарт устанавливает два метода испытания:
a) инкубирование испытуемого соединения в почве в метаногенных условиях и мониторинг его биоразложения;
b) инкубирование испытуемого соединения в почве в условиях переувлажнения и мониторинг его биоразложения.
Последний метод воспроизводит условия естественного анаэробного состояния, при котором предшествующий метод применяет химические вещества для образования низкого окислительно-восстановительного потенциала в почве и является методом выбора измерения потенциального разложения в почве в метаногенных условиях. В методе переувлажненной почвы установление низкого окислительно-восстановительного потенциала занимает больше времени, чем в метаногенных условиях испытания.
Если выбраны условия переувлажнения ("затопление"), то почва будет формировать условия в зависимости от природы почвы. Такие условия могут быть нитратовосстанавливающими (от 450 мВ до 200 мВ, pH 7), железовосстанавливающими (от +150 мВ до -100 мВ, pH 7) или сульфатвосстанавливающими (от -50 мВ до -200 мВ, pH 7). Если выбраны метаногенные условия, окислительно-восстановительный потенциал будет менее -200 мВ.
Метод переувлажнения подходит для аэробных почв, которые временно могут быть анаэробными. Метаногенные условия подходят для поверхностных почв органического болота (постоянно затопленные почвы), почв полигонов захоронения отходов и почв, загрязненных осадками сточных вод.
Примечание - Органические почвы, содержащие легко разлагаемые органические вещества, могут в конечном итоге достичь метаногенных условий в условиях испытания при переувлажнении.
После добавления испытуемого соединения в выбранную почву (см.5.1) биоразложение измеряют в анаэробных условиях путем последующего выделения диоксида углерода, метана и других летучих соединений. Если должны быть определены такие летучие соединения, рекомендуется использование помеченных изотопом веществ (радиоактивные). Исчезновение испытуемого соединения может также быть вызвано специфичным для вещества анализом.
Также возможно использование меченых радиоизотопами соединений для определения скорости исчезновения испытуемого вещества и образования метаболитов и связанных неэкстрагируемых остатков. Метаболиты можно идентифицировать при помощи соответствующих аналитических методов.
5 Материалы
5.1 Почва
5.1.1 Отбор проб
Выбранные почвы для испытания следует отбирать непосредственно с места предполагаемого контакта с химическим веществом.
В случае невозможности обнаружения образцов по причине загрязнения, которое уже введено, выбранные почвы должны иметь свойства, максимально приближенные к загрязненной почве.
Следует принять во внимание и зафиксировать историю поля конкретной почвы, последние изменения (например, применение пестицидов) и методы обработки почвы. Должны быть приведены точные данные о месте отбора проб, его расположении, состоянии аэрации (например, цвет, содержание воды, запах), присутствие растений или предыдущих культур, дата забора образца с поля, глубина отбора.
5.1.2 Характеристики почвы
Знание характеристик почвы необходимо для полной интерпретации результатов исследования. Поэтому рекомендуется, чтобы на выбранных почвах были проведены по меньшей мере следующие испытания:
a) физические свойства:
1) анализ размера частиц в соответствии с ИСО 11277; | |
2) содержание воды подходящим методом; | |
3) общая водоудерживающая способность и/или характеристики водоудержания в соответствии с ИСО 11274; |
b) химические свойства:
1) pH почвы в соответствии с ИСО 10390, или pH в растворе KCl или | |
2) содержание органических веществ в соответствии с ИСО 10694; | |
3) катионообменная емкость (CEC) в соответствии с ИСО 11260; | |
4) содержание азота в соответствии с ИСО 11261; | |
5) окислительно-восстановительный потенциал в соответствии с ИСО 11271; |
c) биологические свойства:
Может потребоваться определение микробной биомассы почвы с помощью соответствующего метода, например, метода дыхания субстрата [4]. Однако если в отобранной почве преобладает анаэробное биоразложение, следует использовать метод фумигации [5].
5.2 Испытуемое вещество
Вещества, которые необходимо испытать, должны быть химически чистыми веществами (химическая чистота более 95% массовой доли). Влияние любых носителей или ингредиентов состава следует принимать во внимание.
Для интерпретации результатов важны следующие данные о соединении:
- наименование (IUPAC);
- структура;
- относительная молекулярная масса;
- данные о чистоте и химической природе основных примесей;
- стабильность в воде и органических растворителях;
- растворимость в воде;
- давление паров;
- коэффициент разделения октанол/вода;
- постоянная сорбции;
- константа кислотной диссоциации;
- для химических веществ, меченных радиоизотопом:
- природа и размещение метки;
- особая активность;
- радиохимическая чистота.
Примечание - Результаты исследований, где используют меченные радиоизотопом вещества, зависят от расположения радиоактивной метки. Поэтому расположение введенной метки в молекулярную структуру необходимо тщательно рассматривать.
5.3 Посуда и оборудование
Требуется следующее основное лабораторное оборудование и посуда.
5.3.1 Круглодонная колба вместимостью 250 и 500 см.
5.3.2 Ледяная ванна.
5.3.3 Колонка, содержащая восстановленную медь.
5.3.4 Система подачи газа со шприцем и иглой.
5.3.5 Пробирки или колбы с пробкой из бутилового каучука.
5.3.6 Пипетки с ПВХ - трубками с внутренним диаметром от 0,5 до 1 мм.
5.3.7 Газонепроницаемые шприцы вместимостью 10, 20, 50 и 100 см.
5.3.8 Приборы и электроды для измерения окислительно-восстановительного потенциала. Дополнительно для исследования испытуемых материалов с меткой необходимы:
5.3.9 Сцинтилляционные коктейли.
5.3.10 Жидкостный сцинтилляционный счетчик.
5.3.11 Сцинтилляционные флаконы.
5.4 Реактивы
Все реактивы должны быть известной степени чистоты.
5.4.1 Азот без примеси кислорода, гелий (чистый) или аргон.
5.4.2 Титана (III) хлорид.
5.4.3 Натрия цитрат.
5.4.4 Калия дигидрогенфосфат (![]() ).
).
5.4.5 Динатрия дигидрат гидрогенфосфата (![]() ).
).
5.4.6 Натрия карбонат.
5.4.7 Титана (III) цитрат.
Готовят цитрат титана, как указано ниже. Нейтрализуют 5 см хлорида титана (III) (15%) (см.5.4.2) в 50 см
раствора цитрата натрия (см.5.4.3) 0,2 моль/л с насыщенным раствором карбоната натрия (см.5.4.6), фильтруют при необходимости и хранят в бескислородном газе.
6 Отбор проб
Отбор проб осуществляют в соответствии с ИСО 10381-6, что позволяет обеспечить максимальную жизнеспособность микроорганизмов почвы в случае, если отбирают почвы, в которых протекают преимущественно аэробные процессы. Если почвы собраны в условиях, где преобладает анаэробное биоразложение, то при отборе, обращении и хранении проб следует минимизировать воздействие кислорода на образцы почвы.
7 Проведение испытания
7.1 Введение испытуемого вещества
Концентрация испытуемого вещества зависит от целей эксперимента (например, ожидается такая концентрация как в условиях поля), и испытуемое вещество следует вводить:
- в почву либо
- в водную фазу, покрывающую почву.
Анаэробные условия следует создавать в тест-системе перед помещением испытуемого вещества в водную фазу.
Испытуемое вещество может быть добавлено следующими способами:
а) как водный раствор (в зависимости от растворимости в воде);
b) растворенное в органических водорастворимых растворителях (в зависимости от растворимости в растворителе). Количество используемого растворителя должно поддерживаться на уровне минимально необходимого (менее 1%) для применения соединения. Следует принять во внимание возможную токсичность и биоразлагаемость растворителя;
c) твердое вещество, например нанесенное на кварцевый песок (перед смешиванием с почвой).
С осторожностью следует добавлять испытуемый материал при высоких уровнях токсичности. Токсичные соединения или соединения, которые оказывают ингибирующее воздействие на почвенные микроорганизмы при примененной концентрации, будут мешать определению биоразложения.
7.2 Инкубация в метаногенных условиях
7.2.1 Подготовка свободной от кислорода инкубационной среды
Помещают примерно 100 см воды в круглодонную колбу объемом 250 или 500 см
(см.5.3.1), помещают иглы для ввода газа (см.5.3.4) в воду и промывают несильным потоком кислородсвободного азота или гелия (см.5.4.1), который проходит через колонку нагретой меди (350°C) (см.5.3.3). Доводят воду до интенсивного кипения в условиях продувания свободным от кислорода газом в течении одной минуты. Впоследствии воду сохраняют анаэробной, замещая пар кислородсвободного азота или гелия, пока контейнер охлаждается во льду. После охлаждения цитрат титана (III) (см.5.4.7) с молярной долей 0,8 ммоль/л
![]() (см.5.4.4) с плотностью 0,27 г/л и
(см.5.4.4) с плотностью 0,27 г/л и ![]() (см.5.4.5) с плотностью 0,56 г/л добавляют и растворяют (здесь и далее упоминается как "бескислородный буфер") [7].
(см.5.4.5) с плотностью 0,56 г/л добавляют и растворяют (здесь и далее упоминается как "бескислородный буфер") [7].
7.2.2 Инкубационная система
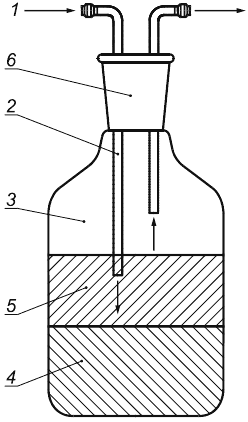
Инкубационная система должна обеспечивать поддержание анаэробных условий. Доступно небольшое количество систем [7], [8], [9], [13], [14], [16], [18]. Система, представленная в настоящем стандарте, состоит из стеклянной колбы (250 см) (см.5.3.5) и системы подвода газа со шприцами и иглами для ввода газа (см.5.3.4). Для примера приведена система на рисунке 1. При использовании трубки должна обеспечиваться непроницаемость для газов (например, это может быть достигнуто при применении плотной бутилкаучуковой пробки). Однако любые другие подходящие системы могут использоваться при условии следования настоящему стандарту.
Если необходимо измерить содержание таких летучих веществ, как ![]() , следует использовать проточные или биометрические инкубационные системы, они описаны в ИСО 14239. В проточной системе следует использовать инертный газ. На рисунке 1 приведена проточная система.
, следует использовать проточные или биометрические инкубационные системы, они описаны в ИСО 14239. В проточной системе следует использовать инертный газ. На рисунке 1 приведена проточная система.
7.2.3 Инкубация
7.2.3.1 Подготовка
Обработанный образец почвы разделяют на равные части по 40 г (сухая масса эквивалента) и помещают в инкубационные колбы (см.5.3.5). Переносят достаточное количество подготовленного бескислородного буфера (уровень жидкости должен быть выше поверхности почвы по меньшей мере на 1 см) в каждую колбу, содержащую почву, которые следует продолжительно промыть во время приготовления бескислородным потоком инертного газа с помощью иглы для ввода газа. Буфер следует переносить с помощью пипеток, оснащенных длинной тонкой трубкой из ПВХ (см.5.3.6 и [7]). После извлечения иглы колбу сразу закрывают пробкой из бутилкаучука. Пробку прокалывают иглой, присоединенной к герметичному шприцу для предотвращения избыточного давления и для обеспечения отвода образцов газа для анализа или соединяют с трубкой, как показано на рисунке 1.
Проводят инкубацию не менее двух проб для каждого определения. При увеличении количества повторов повышается точность испытания.
|
1 - азот без примеси кислорода; 2 - стеклянная трубка или игла; 3 - колба; 4 - почва; 5 - буфер; 6 - пробка
Рисунок 1 - Пример инкубационной системы для исследования разложения в анаэробных условиях в почве
Контрольные образцы следует запустить одновременно и следует содержать почву с количеством буфера, который использовался для применения испытуемого вещества в обрабатываемых образцах.
Почва без каких-либо добавок может быть использована для дополнительного контроля.
7.2.3.2 Условия инкубации
7.2.3.2.1 Поддержание анаэробности
Считается, что анаэробное биоразложение в почвах преобладает, если окислительно-восстановительный потенциал менее 200 мВ. Для проверки анаэробности см. 7.2.3.3.
7.2.3.2.2 Температура
Температуру инкубации следует подбирать в соответствии с особыми целями исследования. Обнаружено, что максимальная микробная активность в почве наблюдается в диапазоне от 25°С до 35°С. Для почв зон умеренного климата температура от 10°С до 25°С является предпочтительнее естественных условий.
Минимум и максимум температур следует измерить и записать с регулярными интервалами в течение процесса инкубации, он не должен отличаться более чем на ±2°С.
7.2.3.2.3 Освещение
Испытание следует проводить в темноте.
7.2.3.3 Проверка анаэробности
Анаэробность проверяют по мере необходимости во время исследования путем измерения окислительно-восстановительного потенциала в соответствии с ИСО 11271.
В конце испытания измеряют растворенное Fe, растворенный Mn и концентрации /
/
.
7.2.3.4 Продолжительность испытания
Рекомендуемой минимальной продолжительности для испытания не существует, так как активность микроорганизмов в почве возрастает при длительных инкубационных периодах, при этом рекомендуется, что испытание не следует продолжать более 100 дней.
7.2.3.5 Отбор проб
Пробы следует отбирать в течение инкубационного периода через регулярные интервалы времени, в зависимости от продолжительности испытания и скорости биоразложения испытуемого материала. Требуется по меньшей мере пять точек отбора проб для построения кривой разложения. Поскольку многие материалы разлагаются намного быстрее во время ранних этапов инкубации, рекомендуется следующая частота отбора проб: 0, 2, 4, 8, 16, 40 и 100 после начала инкубации. Для разрушающих методов отбора проб, например прямой анализ почвы, рекомендуется постепенно отбирать все содержимое индивидуальной инкубационной колбы.
7.3 Инкубация в условиях переувлажнения
Для достижения анаэробных условий в почве применяют практику покрытия почвы водой (примерно 1 см над почвой) [19], [20].
Далее следует продолжать проведение испытания в соответствии с 7.2.1-7.2.3.5, но вместо использования буфера (см.7.2.3) следует использовать воду.
Эта переувлажненная система имеет намного более высокий окислительно-восстановительный потенциал, в то время как бескислородная буферная система имеет отрицательное значение.
7.4 Мониторинг разложения
7.4.1 Общее
Тип выбранного анализа для мониторинга процесса разложения будет зависеть от целей исследования и того, какие данные требуются - по первичному и/или по полному биоразложению.
Анализы зависят от самих химических веществ и от наличия радиоизотопной метки.
Рекомендуется рассмотреть следующие виды анализа:
a) для первичного разложения (вещества, не меченные радиоизотопом):
- распад исходного соединения;
b) для метаболизма, включающего полное разложение (помеченные вещества):
- определение летучих соединений и исходного соединения и метаболитов;
- определение извлекаемости воды и/или растворителя;
- определение "связанных", неэкстрагируемых остатков.
Для определения экстрагируемых веществ следует применять растворители, которые не преобразуют исходное соединение, или его метаболиты. С осторожностью необходимо отнестись к последующим процедурам экстракции, при которых будет удаляться много экстрагируемых веществ. Анализ метаболитов и исходного соединения может быть проведен с использованием тонкослойной хроматографии (ТСХ), высокоэффективной жидкостной хроматографии (ВЭЖХ) и газовой хроматографии (ГХ).
7.4.2 Измерение выделения ![]()
Выделение ![]() измеряют в соответствии с ИСО 14239.
измеряют в соответствии с ИСО 14239.
7.4.3 Измерение выделения ![]()
Выделение ![]() может быть установлено путем окисления
может быть установлено путем окисления ![]() с использованием оксида меди. Перед проведением этой процедуры должны быть созданы условия для улавливания натриевой известью естественных
с использованием оксида меди. Перед проведением этой процедуры должны быть созданы условия для улавливания натриевой известью естественных , выделенных в этом эксперименте.
8 Представление результатов
Все данные следует представлять в табличной или графической форме (кривая разложения).
Значения DT-50 и DT-90 следует вычислять с использованием модели, приведенной, например, в [15], или других подходящих моделей.
Дополнительная полезная информация включает определение летучих соединений, образование и персистентность метаболитов и неэкстрагируемых остатков.
Примечание - Если биоразложения не наблюдается, наиболее вероятными являются следующие причины:
a) испытуемое вещество токсично;
b) испытуемое вещество не является биоразлагаемым;
c) деятельность микроорганизмов в почве равна нулю;
d) испытуемое вещество не биодоступно (из-за адсорбции или испарения).
9 Протокол испытания
Протокол испытания должен включать следующую информацию:
a) данные об испытуемом веществе (см. 5.2);
b) данные об используемой почве (см. 5.1);
c) данные по испытательной процедуре, методе испытания, используемой концентрации, методам введения, данные по представлению испытания, проверка анаэробности, отбор проб и т.п. (см.5);
d) данные по используемым аналитическим методам, например пределы обнаружения, процедуры контроля качества, анализированные вещества сравнения;
e) черновые результаты анализа;
f) материальный баланс при использовании испытуемого вещества, помеченного изотопом , (если требуется);
g) расчеты и заключения.
Приложение ДА
(справочное)
Сведения о соответствии ссылочных международных стандартов национальным стандартам
Таблица ДА.1
Обозначение ссылочного международного стандарта | Степень соответствия | Обозначение и наименование соответствующего национального стандарта |
ISO 10381-6:1993 | - | * |
ISO 10390:1994 | - | * |
ISO 10694:1995 | - | * |
ISO 11260:1994 | - | * |
ISO 11261:1995 | - | * |
ISO 11271 | - | * |
ISO 11277:1998 | - | * |
ISO 11274:1998 | - | * |
ISO 14239:1997 | - | * |
* Соответствующий национальный стандарт отсутствует. До его принятия рекомендуется использовать перевод на русский язык указанных международных стандартов.
| ||
Библиография
[1] | ISO 9408:1999, Water quality - Evaluation of ultimate aerobic biodegradability of organic compounds in aqueous medium by determination of oxygen demand in a closed respirometer |
[2] | ISO 11074-1:1996, Soil quality - Vocabulary - Part 1: Terms and definitions relating to the protection and pollution of the soil |
[3] | ISO 11266:1994, Soil quality - Guidance on laboratory testing for biodegradation of organic chemicals in soil under aerobic conditions |
[4] | ISO 14240-1:1997, Soil quality - Determination of soil microbial biomass - Part 1: Substrate-induced respiration method |
[5] | ISO 14240-2:1997, Soil quality - Determination of soil microbial biomass - Part 2: Fumigation-extraction method |
[6] | AHLRICHS J.L. in: Organic Chemicals in the Soil Environment, Goring C.A.I., and Hamaker J.W., eds., Dekker, New York, 1972, p.40 |
[7] | ALEF K., NANNIPIERI P. Methods in applied soil microbiology and biochemistry, Academic Press, London, 1995, p.271-310 |
[8] | ATTAWAY H.H., PAYNTER M.J.B. and CAMPER N.D. Degradation of selected phenylurea herbicides by anaerobic pond sediment, J.Environ. Sci.Health, B17 (6), 1982, pp.683-699 |
[9] | BE LAND F.A., FARWELL S.O. and GEER R.D. Anaerobic degradation of 1,1,1,2-Tetrachloro-2,2- bis(p-chlorophenyl)ethane (DTE), J.Agr.Food Chem., 22, 1974, pp.1148-1149 |
[10] | GOWDA T.K.S and SETHUNATHAN N. Persistence of Endrin in Indian soils under flooded conditions, J.Agric. Food Chem., 24, 1976, pp.750-753 |
[11] | HEALY J.B. and YOUNG L.Y. Anaerobic biodegradation of eleven aromatic compounds to methane, Appl. and Environ. Microbiol., 38, 1979, pp.84-89 |
[12] | KEARNE, Ph.CIUPAC Pesticide Commission Report, Technical Communication, J.Assoc. Off. Anal. Chem., 65, 1982, pp.1030-1032 |
[13] | MADSEN T., BECK-RASSMUSSEN H., NILSSON L. Methods for screening anaerobic biodegradability and toxicity of organic chemicals, Miljoprojekt No.336, 1996 |
[14] | SHELTON D.R. and TIEDJE J.M. General method for determining anaerobic biodegradation potential, Appl. Environ. Microbiol., 47 (4), 1984, pp.850-857 |
[15] | TIMME G., FREHSE H. and LASKA V. Interpretation and graphischen Darstellung des Abbauverhaltens von Pflanzenschutzmittel- |
[16] | WARD T.E. Aerobic and anaerobic biodegradation of nitrilotriacetate in subsurface soils, Ecotoxicol. Environmental Safety, 11, 1986, pp.112-125 |
[17] | WOLFE N.L., MINGELGRIN U., MILLER G. Abiotic transformations in water, sediments and soils. In: Cheng, H.H. (ed.), Pesticides in the soil environment: processes, impacts and modelling, SSSA Book Series 2, 1990, pp.103-168 |
[18] | ZORO J.A., HUNTER J.M., EGLINTON G. and WARE G.C. Degradation of p,p'-DDT in reducing environments, Nature, 247, 1974, pp.235-237 |
[19] | U.S.Environmental Protection Agency, Washington DC, Pesticide Assessment Guidelines, Subdivision N Chemistry: Environmental Fate, Oct.18, 1982, §162-2 Anaerobic soil metabolism studies |
[20] | OECD Guideline 307 for Testing of Chemicals, Final Document (2000), Aerobic and Anaerobic Transformation in Soil |
УДК 631.423.4:006.354 | ОКС 13.080.30 | ||
Ключевые слова: качество почвы, анаэробная биоразлагаемость, органические химические вещества | |||
Электронный текст документа
и сверен по:
, 2019