ГОСТ Р ИСО 10808-2015
Группа Т58
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
НАНОТЕХНОЛОГИИ
Наноаэрозоли для оценки токсичности при ингаляционном поступлении в организм. Контроль характеристик
Nanotechnologies. Nanoaerosols for inhalation toxicity testing. Monitoring characteristics
ОКС 07.030
Дата введения 2016-07-01
Предисловие
1 ПОДГОТОВЛЕН Федеральным государственным учреждением "Федеральный исследовательский центр "Фундаментальные основы биотехнологии" Российской академии наук" (ФИЦ Биотехнологии РАН) на основе собственного аутентичного перевода на русский язык стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 441 "Нанотехнологии"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 6 ноября 2015 г. N 1710-ст
4 Настоящий стандарт идентичен международному стандарту ISO 10808:2010* "Нанотехнологии. Определение параметров наночастиц в ингаляционной камере для испытаний токсичности ингаляции" (ISO 10808:2010 "Nanotechnologies - Characterization of nanoparticles in inhalation exposure chambers for inhalation toxicity testing").
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ Р 1.5-2012 (пункт 3.5).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации (и действующие в этом качестве межгосударственные стандарты), сведения о которых приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе "Национальные стандарты", а официальный текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
Введение
Ежегодно происходит увеличение производства нанопродукции, содержащей наночастицы серебра, золота, углерода, оксида цинка, диоксида титана и диоксида кремния. По мере расширения сфер применения нанопродукции увеличивается риск воздействия наночастиц на здоровье человека. Работники нанотехнологических производств подвержены риску воздействия наночастиц на рабочих местах, а потребители - при высвобождении наночастиц из готовой продукции. Токсикологические испытания с использованием инстилляции наноматериалов не позволяют получить реальную картину ингаляционного поступления наноматериалов в организм и, соответственно, объективные данные для оценки их риска. Также необходимо заменить существующие методы испытаний, применяемые для оценки ингаляционной токсичности с использованием крыс, на более подходящие для человеческого организма методы [10].
Особое внимание следует уделять вредному воздействию наночастиц, поступающих в организм при вдыхании, на изготовителей и потребителей нанопродукции. Во время проведения испытаний по оценке токсичности аэрозоля, состоящего из наночастиц, в камере для ингаляционной экспозиции необходимо осуществлять контроль следующих его характеристик: концентрации наночастиц, размеров наночастиц и их распределения по размерам. Стандартные методы контроля характеристик аэрозолей, состоящих из мелких и крупных частиц, таких как массовая концентрация частиц, не подходят для контроля характеристик аэрозолей, состоящих из наночастиц, таких как удельная площадь поверхности или счетная концентрация наночастиц. Данные характеристики необходимы для оценки токсичности аэрозолей, состоящих из наночастиц, поэтому во время проведения испытаний необходимо осуществлять их контроль.
В настоящем стандарте установлены требования к контролю характеристик аэрозолей, состоящих из наночастиц и используемых для оценки токсичности при ингаляционном поступлении в организм, с применением системы анализа дифференциальной электрической подвижности частиц, с помощью которой контролируют счетную концентрацию наночастиц, размеры наночастиц и их распределение по размерам, удельную площадь поверхности и массовую концентрацию наночастиц, а также требования к контролю химического состава наночастиц с помощью просвечивающего электронного микроскопа, растрового электронного микроскопа или энергодисперсионного рентгеновского анализатора [13], [17], [18].
1 Область применения
Настоящий стандарт распространяется на аэрозоли, состоящие из наночастиц (далее - наноаэрозоли), для оценки токсичности при ингаляционном поступлении в организм и устанавливает требования к контролю характеристик наноаэрозолей.
В приложении A приведен пример контроля характеристик наноаэрозоля, состоящего из наночастиц серебра, применяемого для оценки токсичности при ингаляционном поступлении в организм.
2 Нормативные ссылки
Нижеуказанные документы содержат положения, которые посредством ссылок в данном тексте составляют положения настоящего стандарта*.
________________
* Таблицу соответствия национальных стандартов международным см. по ссылке. - .
Для датированных ссылок применяют только ту версию, которая была упомянута в тексте. Для недатированных ссылок необходимо использовать самое последнее издание документа (включая любые поправки).
ИСО 10312 Воздух окружающий. Определение концентрации асбестовых волокон. Метод электронной микроскопии с прямым просвечиванием (ISO 10312, Ambient air - Determination of asbestos fibres - Direct transfer transmission electron microscopy method)
ИСО 15900 Определение распределения частиц по размеру. Анализ дифференциальной подвижности частиц аэрозолей в электрическом поле (ISO 15900, Determination of particle size distribution - Differential electrical mobility analysis for aerosol particles)
ИСО/ТС 27687 Нанотехнологии. Термины и определения нанообъектов. Наночастица, нановолокно и нанопластина (ISO/TS 27687, Nanotechnologies - Terminology and definitions for nano-objects - Nanoparticle, nanofibre and nanoplate)
ОЭСР Тест N 403 Руководство по проведению тестирования химических веществ. Острая токсичность при ингаляционном поступлении (OECD Test Guideline (TG) 403, Acute Inhalation Toxicity)
ОЭСР Тест N 412 Руководство по проведению тестирования химических веществ. Подострая ингаляционная токсичность: 28-дневное исследование (OECD Test Guideline 412 (TG) 412, Subacute Inhalation Toxicity: 28-Day Study)
ОЭСР Тест N 413 Руководство по проведению тестирования химических веществ. Субхроническая ингаляционная токсичность: 90-дневное исследование (OECD Test Guideline 413 (TG) 413, Subchronic Inhalation Toxicity: 90-day Study)
ОЭСР Руководящий документ N 39 Руководство по исследованию острой ингаляционной токсичности (OECD Guidance Document 39 (GD 39), Acute Inhalation Toxicity Testing)
3 Термины и определения
В настоящем стандарте применены термины по ИСО/ТС 27687, ИСО 15900, а также следующие термины с соответствующими определениями:
3.1 Термины и определения понятий, относящихся к оборудованию, применяемому для определения характеристик наноаэрозоля
3.1.1
классификатор дифференциальной электрической подвижности частиц; КДЭП (differential electrical mobility classifier, DEMC); спектрометр дифференциальной электрической подвижности частиц; СДЭП (differential electrical mobility spectrometer, DEMS): Устройство, распределяющее аэрозольные частицы по размерам в соответствии с их электрической подвижностью и регистрирующее частицы только определенных размеров. Примечание - Принцип распределения частиц по размерам в КДЭП основан на уравновешивании электрического заряда каждой частицы с силой ее аэродинамического сопротивления при прохождении через электрическое поле. Электрическая подвижность частиц зависит от их размеров, режимов работы и формы КДЭП. Размер частицы можно определить по числу зарядов на ней. [ИСО 15900:2009, статья 2.7] |
3.1.2
система анализа дифференциальной электрической подвижности частиц; САДЭП (differential mobility analyzing system; DMAS): Система, применяемая для измерения распределения субмикронных частиц аэрозоля по размерам, состоящая из классификатора дифференциальной электрической подвижности частиц, нейтрализатора, счетчика частиц, соединительных трубок, компьютера и программного обеспечения. [ИСО 15900:2009, статья 2.8] |
3.1.3
счетчик конденсированных частиц; СКЧ (condensation particle counter, СРС): Устройство, регистрирующее частицы и измеряющее их счетную концентрацию в аэрозоле при заданной скорости потока частиц. Примечания 1 Диапазон размеров частиц регистрируемых СКЧ, - от нескольких нанометров до нескольких сотен нанометров. СКЧ можно использовать совместно с КДЭП. 2 В некоторых случаях СКЧ называют счетчиком ядер конденсации (СЯК). [ИСО 15900:2009, статья 2.5, определение термина изменено] |
3.2
камера для ингаляционной экспозиции (inhalation exposure chamber); ингаляционная камера (inhalation chamber); камера для экспозиции (exposure chamber): Устройство, предназначенное для введения установленной дозы испытуемого газообразного вещества в организм экспериментального животного через его дыхательные пути, воздействуя "только через нос" или "через все тело", в течение заданного периода времени. Примечание - Термин "только через нос" является синонимом терминов "только через голову" и "только через мордочку". [ОЭСР Тест N 403, ОЭСР Тест N 412, ОЭСР Тест N 413] |
3.3 система генерирования наноаэрозоля (nanoparticle generator system): Устройство, применяемое для получения аэрозоля, состоящего из наночастиц, с контролируемыми значениями концентрации наночастиц и распределения их по размерам.
3.4 зона дыхания (breathing zone): Пространство вокруг экспериментального животного, из которого поступает вдыхаемый воздух.
Примечания
1 Зоной дыхания животных, не помещенных в клетки, считают все пространство ингаляционной камеры. Зоной дыхания животных, помещенных в клетки, считают пространство вблизи носа животного. Зоной дыхания животных в масках считают небольшое пространство перед ноздрями.
2 Термин "зона дыхания" применяют с целью обозначения места отбора проб воздуха, вдыхаемого животными. В случае если экспозицию экспериментального животного осуществляют в нижней части ингаляционной камеры, то отбор проб воздуха для определения концентрации наночастиц нельзя проводить в верхней части ингаляционной камеры.
3.5 средний геометрический диаметр; СГД (geometric mean diameter; GMD): Среднее значение распределения частиц по размерам, выраженное в виде логарифма и вычисленное по логарифму диаметров частиц, определенных с помощью САДЭП, по формуле
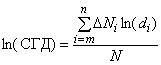 , (1)
, (1)
где - среднее геометрическое значение нижней и верхней границы диаметров частиц i-го диапазона размеров;
- общая концентрация наночастиц;
- концентрация частиц i-го диапазона размеров;
m - нижняя граница диаметра частиц в размерном диапазоне;
n - верхняя граница диаметра частиц в размерном диапазоне.
Примечание - СГД можно вычислить по числу частиц, зная площадь поверхности или объемную концентрацию частиц в аэрозоле.
3.6 стандартное геометрическое отклонение; СГО (geometric standard deviation; GSD): Значение, характеризующее диапазон распределения наночастиц по размерам, вычисляемое для САДЭП по формуле
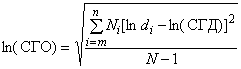 . (2)
. (2)
3.7 счетный медианный диаметр; СМД (count median diameter, CMD): Диаметр, равный СГД, вычисленный при подсчете частиц с предполагаемым нормальным распределением.
Примечание - Формула для вычисления СМД представлена в [1].
![]() , (3)
, (3)
где e - основание натурального логарифма, e=2,71828;
p - размерность распределения,
где p=0 - число;
p=1 - длина;
p=2 - площадь;
p=3 - объем или масса;
r - размерность распределения,
где r=0 - число;
r=1 - длина;
r=2 - площадь;
r=3 - объем или масса;
s - стандартное отклонение плотности распределения;
- медианный размер частиц из кумулятивного распределения частиц по размерам r.
4 Контролируемые параметры процесса испытаний по оценке токсичности наноаэрозоля при ингаляционном поступлении в организм
4.1 Основные параметры
4.1.1 Экспозиция
В процессе проведения испытаний по оценке токсичности наноаэрозоля при ингаляционном поступлении в организм определяют и контролируют характеристики экспозиции, устанавливают количественное соотношение полученных токсикологических показателей и показателей экспозиционной дозы, зависящих от физико-химических характеристик наноаэрозоля.
4.1.2 Характеристики наноаэрозоля
Перед проведением испытаний по оценке токсичности наноаэрозоля определяют как можно больше его физико-химических характеристик, включая:
- состав наноаэрозоля;
- форму наночастиц;
- счетную концентрацию наночастиц;
- массовую концентрацию наночастиц;
- СГД наночастиц;
- СМД наночастиц;
- распределение наночастиц по размерам;
- удельную площадь поверхности наночастиц;
- электрический заряд наноаэрозоля;
- химический состав наночастиц;
- гигроскопичность наночастиц.
4.2 Параметры оборудования
4.2.1 Систему генерирования наноаэрозоля проверяют на соответствие установленным в программах и методиках испытаний требованиям. Перед подачей наноаэрозоля в камеру(-ы) для ингаляционной экспозиции (далее - ингаляционная камера) определяют следующие характеристики наноаэрозоля:
- счетную концентрацию наночастиц;
- массовую концентрацию наночастиц;
- распределение наночастиц по размерам;
- стабильность наноаэрозоля.
В процессе испытаний в ингаляционной камере постоянно и/или периодически определяют распределение наночастиц по размерам, не прерывая процесс экспозиции.
При необходимости дополнительно определяют такую характеристику наноаэрозоля, как распределение электрических зарядов на наночастицах, в этом случае значение данной характеристики регистрируют в протоколе. Значения распределения электрических зарядов на наночастицах должны быть установлены в соответствующих программах и методиках испытаний.
Примечание - Система генерирования наноаэрозолей, состоящих из наночастиц серебра и других металлов, описана в [3].
4.2.2 Ингаляционные камеры и вспомогательное оборудование должны соответствовать ОЭСР Тест N 403, ОЭСР Тест N 412, ОЭСР Тест N 413.
4.2.3 Ингаляционные камеры и вспомогательное оборудование должны быть подготовлены для проведения испытаний по оценке токсичности наноаэрозолей при ингаляционном поступлении в организм.
Примечания
1 Осаждение аэрозольных наночастиц на стенках ингаляционной камеры происходит вследствие броуновского движения, а изменение размеров наночастиц - их агрегации/агломерации. Процесс осаждения зависит от размеров наночастиц, значений электростатического заряда, концентрации наночастиц и времени их нахождения в камере [11], [19], [20].
2 В зависимости от цели исследования может возникнуть необходимость выполнить нейтрализацию заряда наноаэрозоля.
3 С целью уменьшения потерь наночастиц при их осаждении необходимо в оборудовании применять соединительные трубки минимальных длины и диаметра.
4.2.4 В целях получения достоверных результатов оценки токсичности наноаэрозолей ингаляционную камеру (или камеры) и вспомогательное оборудование (пробоотборники и система соединительных трубок) перед проведением испытаний проверяют на соответствие требованиям ОЭСР Тест N 403, ОЭСР Тест N 412, ОЭСР Тест N 413.
Примечание - Следует учитывать, что в пробоотборниках и соединительных трубках, электромагнитных клапанах и/или другом оборудовании, предназначенном для транспортирования проб наноаэрозоля из ингаляционной камеры к устройству, с помощью которого выполняют измерения и осуществляют контроль, могут произойти потери наночастиц, что приведет к изменению результатов определения распределения наночастиц по размерам.
4.2.5 Измерительное оборудование должно быть откалибровано и/или поверено в соответствии с ИСО 15900.
Система анализа дифференциальной электрической подвижности частиц (САДЭП) должна быть откалибрована на заводе-изготовителе. Сведения о калибровке САДЭП должны быть указаны в протоколе.
Примечание - В процессе эксплуатации САДЭП выполняют ее периодическую калибровку.
4.3 Параметры процесса испытаний
4.3.1 Оценку токсичности наноаэрозоля при ингаляционном поступлении в организм выполняют в соответствии с ОЭСР Тест N 403, ОЭСР Тест N 412, ОЭСР Тест N 413 и ОЭСР Руководящий документ N 39.
4.3.2 Во время проведения испытаний счетная и массовая концентрации наночастиц должны быть стабильны. Контроль осуществляют постоянно и/или периодически в зависимости от методов испытаний.
4.3.3 Для определения характеристик экспозиции выполняют отбор проб в зоне дыхания животных.
4.3.4 В процессе испытаний осуществляют контроль скорости потоков воздуха и наноаэрозоля, подаваемого в ингаляционную(-ые) камеру(-ы), в соответствии с ОЭСР Тест N 403, ОЭСР Тест N 412, ОЭСР Тест N 413 и ОЭСР Руководящий документ N 39.
С помощью расходомера контролируют соответствие скорости потоков воздуха и наноаэрозоля заданным значениям.
4.3.5 В процессе испытаний осуществляют постоянный контроль температуры и влажности внутри ингаляционной камеры.
С помощью измерительного оборудования контролируют соответствие температуры и влажности внутри ингаляционной камеры заданным значениям.
4.3.6 Отработанный воздух, выходящий из камеры в атмосферу и содержащий наночастицы, должен быть очищен с помощью фильтров и/или, при необходимости, химических веществ.
5 Общие требования к методам контроля
5.1 Основные характеристики наноаэрозоля
К основным характеристикам наноаэрозоля при оценке его токсичности относят счетную и массовую концентрации наночастиц и распределение наночастиц по размерам. Значения счетной концентрации наночастиц, массовой концентрации наночастиц и распределения наночастиц по размерам определяют и контролируют методами, установленными в соответствующих программах и методиках испытаний.
5.2 Требования к методам контроля, применяемым для определения счетной концентрации наночастиц и распределения наночастиц по размерам
5.2.1 Для определения счетной концентрации наночастиц и распределения наночастиц по размерам применяют методы, позволяющие осуществлять непрерывный контроль характеристик и стабильности наноаэрозоля в период экспозиции, и оборудование с соответствующей разрешающей способностью.
5.2.2 Диапазоны значений счетной концентрации наночастиц и распределения наночастиц по размерам в зоне дыхания экспериментальных животных должны соответствовать требованиям, необходимым для оценки токсичности наноаэрозоля при ингаляционном поступлении в организм.
5.2.3 Для определения счетной концентрации наночастиц и распределения наночастиц по размерам в зоне дыхания экспериментальных животных применяют методы, обеспечивающие точность измерений, соответствующую требованиям, необходимым для оценки токсичности наноаэрозоля при ингаляционном поступлении в организм. Процесс измерений должен быть валидирован посредством калибровки по эталонным мерам [6].
5.2.4 Диапазон измерений применяемого оборудования должен быть достаточным для определения размеров различных частиц и вычисления удельной площади поверхности наноаэрозоля по его массе или объему. Диапазон измерений применяемого оборудования должен быть установлен в соответствующих программах и методиках испытаний.
Примечание - Метод измерений с помощью САДЭП является единственным методом, удовлетворяющим всем требованиям и применяемым для определения распределения наночастиц диаметром менее 100 нм по размерам (см. ИСО 15900).
Размеры наночастиц диаметром более 100 нм определяют по их оптическим или электрическим характеристикам, времени пролета или другим аэродинамическим характеристикам с помощью различного оборудования [8].
5.3 Требования к методам контроля, применяемым для определения массовой
концентрации наночастиц
Для определения массовой концентрации наночастиц применяют методы, обеспечивающие точность измерений и имеющие предел обнаружения, соответствующие требованиям, необходимым для оценки токсичности наноаэрозоля при ингаляционном поступлении в организм.
Примечания
1 Массовую концентрацию наночастиц можно определять методом измерения массы наночастиц, содержащихся в исследуемом воздухе, основанном на поглощении бета-лучей твердыми частицами, методами с использованием вибрационных микровесов с коническим элементом и пьезоэлектрических микровесов, а также другими методами, основанными на химическом анализе частиц, отобранных на фильтре [4].
2 Массовую концентрацию наночастиц можно определить по значениям счетной концентрации наночастиц при условии, что известны (точно или предположительно) заряд и плотность наночастиц [14]. При этом следует учитывать, что если плотность наночастиц неизвестна или определена неточно, то могут быть получены ошибочные результаты.
Определять значения массовой концентрации наночастиц по значениям счетной концентрации наночастиц следует только в том случае, если невозможно применить другие методы измерений.
5.4 Требования к ингаляционным камерам
5.4.1 При экспозиции животного "через все тело" смену воздуха в ингаляционной камере осуществляют 10-15 раз в час. При экспозиции животных "только через нос" смену воздуха в ингаляционной камере осуществляют не менее двух раз за минутный объем дыхания животного (в опытах с крысами - не менее 0,5 л/мин на одну ингаляционную камеру).
Распределение наночастиц в ингаляционной камере должно быть равномерным.
5.4.2 Температура и влажность внутри ингаляционной камеры должны соответствовать значениям, установленным в соответствующих программах и методиках испытаний.
Примечание - В соответствии с ОЭСР Тест N 413 испытания проводят при температуре (22±3)°С.
Относительную влажность воздуха желательно поддерживать в диапазоне от 30% до 70%.
5.4.3 Для предотвращения выброса наноаэрозоля в окружающую среду и воздействия его на персонал давление в ингаляционной камере должно быть ниже давления окружающей среды. Перепад давления - не менее 49 Па.
Для экспозиции экспериментальных животных "только через нос" давление в ингаляционной камере должно быть выше давления окружающей среды. В этом случае для предотвращения выброса наноаэрозоля в окружающую среду испытания проводят в специальном закрытом помещении, оборудованном вытяжной вентиляцией (см. ОЭСР Руководящий документ N 39).
5.4.4 Распределение кислорода в ингаляционной камере должно быть равномерным, а его содержание - не менее 19%.
6 Сведения о характеристиках наноаэрозоля, необходимых для обработки результатов испытаний по оценке токсичности наноаэрозоля
6.1 Для обработки результатов испытаний по оценке токсичности наноаэрозоля при ингаляционном поступлении в организм необходимы значения следующих его характеристик:
a) распределение наночастиц по размерам, нм, СГД, нм, и СГО в каждой ингаляционной камере, определяемые с помощью САДЭП, просвечивающего электронного микроскопа (ПЭМ), растрового электронного микроскопа (РЭМ) и др.;
b) морфология наночастиц, определяемая с помощью ПЭМ или РЭМ с учетом требований ИСО 10312;
c) счетная концентрация наночастиц, наночастиц/м, в каждой ингаляционной камере, определяемая с помощью САДЭП и др.;
d) массовая концентрация наночастиц (в каждой ингаляционной камере), мг/м, определяемая гравиметрическим методом с использованием мембранных фильтров или другими методами, например с использованием САДЭП;
e) химический состав наночастиц.
Не рекомендуется определять значения счетной концентрации наночастиц и распределения наночастиц по размерам в наноаэрозолях, состоящих из наночастиц несферической формы, с помощью САДЭП, так как существует вероятность получения ошибочных результатов.
Также могут быть получены ошибочные результаты при определении значений массовой концентрации наночастиц в наноаэрозолях, состоящих из наночастиц несферической формы, по значениям счетной концентрации наночастиц, полученным с помощью САДЭП.
6.2 Для обработки результатов испытаний по оценке токсичности наноаэрозоля при ингаляционном поступлении в организм необходимы значения следующих дополнительных характеристик:
a) площадь поверхности наночастиц [15], [16], определяемая в соответствии с ИСО 10312 или [5];
b) объемная концентрация наночастиц, определяемая в соответствии с ИСО 10312;
c) форма наночастиц и дисперсность наноаэрозоля, определяемые с помощью ПЭМ и РЭМ [5] и [2];
d) химический состав поверхности наночастиц, определяемый с помощью энергодисперсионного рентгеновского анализатора (см. ИСО 10312, [5]) или электронного спектрометра [7];
e) электрический заряд наночастиц или его отсутствие (в этом случае в протокол вносят сведения о применении нейтрализатора заряда и его месторасположении в испытательной установке).
7 Требования к протоколу испытаний
7.1 В протоколе указывают сведения о применяемых методах, средствах и условиях испытаний.
7.2 В протокол включают:
a) описание характеристик наноаэрозоля, используемого в каждой ингаляционной камере, в соответствии с разделом 6;
b) информацию об исходном материале (код изготовителя, химическое наименование или химическая формула, номер партии и дата изготовления, торговое наименование и др.), а в случае повторного эмульгирования наночастиц - сведения о процессе обработки;
c) перечень использованного оборудования (с указанием модели, изготовителя, серийного номера или даты выпуска, торгового наименования и др.);
d) значение скорости потока воздуха, проходящего через ингаляционную камеру;
e) значения температуры и влажности воздуха в ингаляционной камере;
f) информацию о подготовке к проведению испытаний (сведения о потерях наночастиц при отборе проб и др.).
7.3 В качестве дополнительной информации в протокол включают:
a) сведения о химическом составе поверхности, определенном в соответствии с ИСО 10312 или другими методами;
b) сведения об электрическом заряде наночастиц или о нейтрализации заряда.
Приложение A
(справочное)
Пример контроля характеристик наноаэрозоля, состоящего из наночастиц серебра, применяемого для оценки токсичности при ингаляционном поступлении в организм
А.1 Требования к испытательной установке, применяемой для оценки токсичности наноаэрозоля при ингаляционном поступлении в организм
А.1.1 Общие требования
На рисунке А.1 представлена схема испытательной установки, применяемой для оценки токсичности наноаэрозоля при ингаляционном поступлении в организм (далее - испытательная установка).
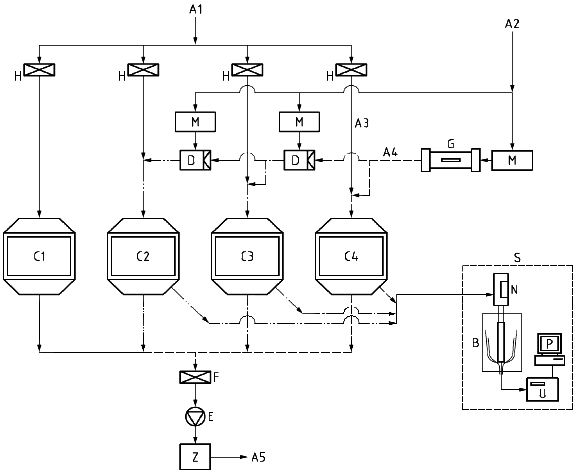
Компоненты испытательной установки:
B - КДЭП;
C2 - ингаляционная камера с низкой концентрацией наночастиц; C4 - ингаляционная камера с высокой концентрацией наночастиц; E - вытяжной вентилятор; G - система генерирования наноаэрозоля; M - регулятор расхода воздуха (РРВ); P - персональный компьютер; U - СКЧ; C1 - контрольная ингаляционная камера; C3 - ингаляционная камера со средней концентрацией наночастиц; D - дилютор; F - пылеуловитель; Н - НЕРА фильтр; N - нейтрализатор электрического заряда (Po); S - САДЭП; Z - химический газоочиститель
Потоки воздуха:
A1 - предварительно очищенный атмосферный воздух; A2 - газ-носитель; A3 - воздух, очищенный НЕРА фильтром и подаваемый со скоростью 200 л/мин; A4 - наноаэрозоль, подаваемый со скоростью 30 л/мин; A5 - очищенный отработанный воздух.

Рисунок А.1 - Схема испытательной установки, применяемой для оценки токсичности наноаэрозоля при ингаляционном поступлении в организм
С помощью системы генерирования получают наноаэрозоли с тремя (высокой, средней и низкой) концентрациями наночастиц, в качестве исходного материала применяют серебряную проволоку (массовая доля серебра не менее 99,9%). В испытательной установке использован дилютор типа трубы Вентури и пробоотборник наночастиц, состоящий из двух концентрических трубок, между которыми пропускают поток воздуха [9]. Высокая скорость потока воздуха, проходящего между стенками двух концентрических трубок, приводит к понижению давления вокруг отверстия, расположенного в конце пробоотборника. За счет снижения давления наноаэрозоль попадает внутрь пробоотборника, в котором происходит его смешивание с находящимся там воздухом, предварительно очищенным с помощью НЕРА фильтров. На фоне понижения давления вокруг отверстия, расположенного в конце пробоотборника, и увеличения скорости потока воздуха возрастает скорость наноаэрозоля, выходящего из дилютера. В данной испытательной установке получают наноаэрозоли с различными (высокой, средней и низкой) концентрациями наночастиц в трех разных ингаляционных камерах. В дилюторе 1 с помощью РРВ 2 перемешивают воздух с наноаэрозолем, поступающим из ингаляционной камеры с высокой концентрацией наночастиц, получая таким образом наноаэрозоли со средней концентрацией наночастиц. В дилюторе 2 с помощью РРВ 3 перемешивают воздух с наноаэрозолем, поступающим из ингаляционной камеры со средней концентрацией наночастиц, получая таким образом наноаэрозоли с низкой концентрацией наночастиц. Скорость наноаэрозоля, получаемого в системе генерирования, - 30 л/мин, скорость воздуха, предназначенного для смешивания с наноаэрозолем, - 200 л/мин [12], [13]. При использовании трех систем генерирования наноаэрозолей, по одной для каждой ингаляционной камеры, применение дилюторов не обязательно. Для проведения контроля характеристик наноаэрозоля из каждой ингаляционной камеры отбирают по две пробы. Пробы следует отбирать в соответствии с требованиями, установленными для отбора проб с помощью дилюторов. Процессом отбора проб из каждой ингаляционной камеры управляют с помощью электромагнитного клапана, установленного в системе соединительных трубок перед САДЭП.
A.1.2 Требования к оборудованию, применяемому для контроля характеристик наноаэрозоля
Характеристики наноаэрозоля определяют в каждой ингаляционной камере с различной концентрацией наночастиц. Измерения выполняют с помощью САДЭП, включающей нейтрализатор электрического заряда (Po), КДЭП и СКЧ. Наночастицы размером от 1,98 до 64,9 нм измеряют при скорости потока воздуха 15 л/мин и скорости потока наноаэрозоля 1,5 л/мин (данные значения являются рабочими характеристиками КДЭП и СКЧ) [13]. Фильтры, на которые отбирают наночастицы, должны иметь покрытие из углеродных материалов. Фильтры помещают на специальные сеточки (200 ячеек) и просматривают на ПЭМ. Для определения размеров наночастиц используют 100000-кратное увеличение ПЭМ и энергодисперсионный рентгеновский спектрометр с ускоряющим напряжением 75 кВ [13].
A.2 Результаты контроля характеристик наноаэрозоля
На рисунках A.2 и A.3 представлены диаграммы распределения наночастиц по размерам в ингаляционных камерах с высокой, средней и низкой концентрацией наночастиц.
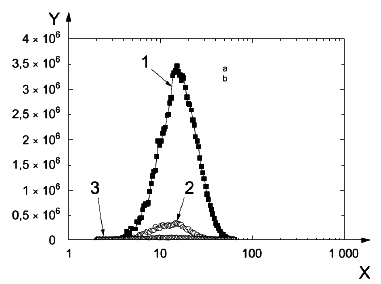
X - диаметр подвижности, Dp, нм; Y - счетная концентрация наночастиц, dN/dlog(Dp), наночастиц/см; 1 - значения, полученные в ингаляционной камере с высокой концентрацией наночастиц; 2 - значения, полученные в ингаляционной камере со средней концентрацией наночастиц; 3 - значения, полученные в ингаляционной камере с низкой концентрацией наночастиц; a - скорость потока воздуха в дилюторе 1, 5,75 л/мин; b - скорость потока воздуха в дилюторе 2, 7,50 л/мин
Рисунок А.2 - Диаграмма распределения наночастиц по размерам в камерах с высокой, средней и низкой концентрацией наночастиц, построенная в линейном/логарифмическом масштабе [13]
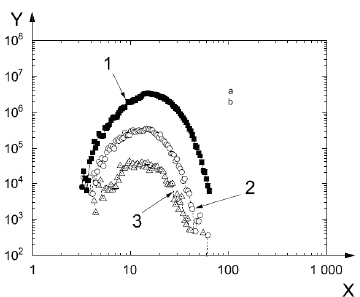
X - диаметр подвижности, Dp, нм; Y - счетная концентрация наночастиц, dN/dlog(Dp), наночастиц/см; 1 - значения, полученные в ингаляционной камере с высокой концентрацией наночастиц; 2 - значения, полученные в ингаляционной камере со средней концентрацией наночастиц; 3 - значения, полученные в ингаляционной камере с низкой концентрацией наночастиц; a - скорость потока воздуха в дилюторе 1, 5,75 л/мин; b - скорость потока воздуха в дилюторе 2, 7,50 л/мин
Рисунок A.3 - Диаграмма распределения наночастиц по размерам в камерах с высокой, средней и низкой концентрацией наночастиц, построенная в логарифмическом масштабе [13]
Давление в ингаляционных камерах должно быть ниже давления окружающей среды. Рабочие характеристики системы генерирования наноаэрозоля: электрическое напряжение, подаваемое на нагреватель с исходным материалом, - 85 В; температура в зоне испарения исходного материала - 1130°С; скорость потока наноаэрозоля - 30 л/мин. В ингаляционной камере с высокой концентрацией наночастиц получены следующие значения: СГД - 15,38 нм; СГО - 1,58; счетная концентрация наночастиц - 1,63·10 частиц/см
. В ингаляционной камере со средней концентрацией наночастиц получены следующие значения: СГД - 12,60 нм; СГО - 1,53; счетная концентрация наночастиц - 1,60·10 частиц/см
. В ингаляционной камере с низкой концентрацией наночастиц получены следующие значения: СГД - 12,61 нм; СГО - 1,52; счетная концентрация наночастиц - 1,66·10
частиц/см
.
На рисунке A.4 представлен график зависимости значений счетной концентрации наночастиц, СГД и СГО в ингаляционной камере со средней концентрацией наночастиц от значений скорости потока воздуха в пробоотборнике.
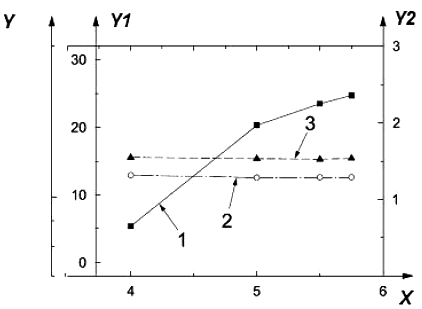
X - скорость потока воздуха в пробоотборнике 1, л/мин; Y - счетная концентрация наночастиц, наночастиц/см; Y1 - СГД, нм; Y2 - СГО; 1 - значения счетной концентрации наночастиц, наночастиц/см
; 2 - значения СГД, нм; 3 - значения СГО
Рисунок А.4 - График зависимости значений счетной концентрации наночастиц, СГД и СГО в ингаляционной камере со средней концентрацией наночастиц от значений скорости потока воздуха в пробоотборнике [13]
На рисунке А.5 представлен график зависимости значений счетной концентрации наночастиц, СГД и СГО в ингаляционной камере с низкой концентрацией наночастиц от значений скорости потока воздуха в пробоотборнике.
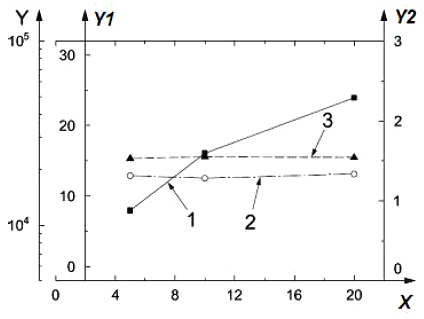
X - скорость потока воздуха в пробоотборнике 2, л/мин; Y - счетная концентрация наночастиц, наночастиц/см; Y1 - СГД, нм; Y2 - СГО; 1 - значения счетной концентрации наночастиц, наночастиц/см
; 2 - значения СГД, нм; 3 - значения СГО
Рисунок А.5 - График зависимости значений счетной концентрации наночастиц, СГД и СГО в ингаляционной камере с низкой концентрацией наночастиц от значений скорости потока воздуха в пробоотборнике [13]
Графики, представленные на рисунках A.4 и A.5, демонстрируют незначительные различия значений СГД и СГО при изменении значений скорости потока воздуха в каждом пробоотборнике.
С целью подтверждения стабильности характеристик наноаэрозоля осуществлен их непрерывный контроль в каждой ингаляционной камере в течение 18 ч в ходе испытаний по оценке токсичности при ингаляционном поступлении в организм. На рисунке A.6 представлена диаграмма, показывающая изменения значений счетной концентрации наночастиц и интенсивности образования наночастиц в течение времени проведения испытаний.
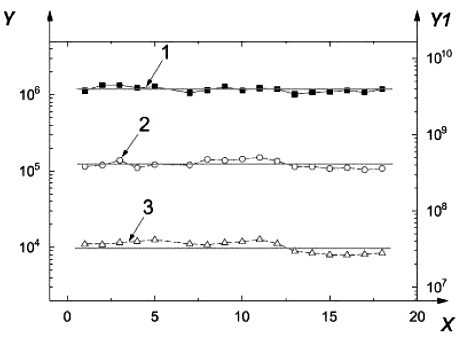
X - время проведения испытаний, ч; Y - счетная концентрация наночастиц, частиц/см; Y1 - интенсивность образования наночастиц (наночастиц/с); 1 - значения, полученные в ингаляционной камере с высокой концентрацией наночастиц, 8,2%; 2 - значения, полученные в ингаляционной камере со средней концентрацией наночастиц, 12,1%; 3 - значения, полученные в ингаляционной камере с низкой концентрацией наночастиц, 16,2%
Рисунок A.6 - Диаграмма, показывающая изменения значений счетной концентрации наночастиц и интенсивности образования наночастиц в течение времени проведения испытаний [13]
На рисунке A.7 представлена диаграмма, показывающая изменения значений СГД в течение времени проведения испытаний.
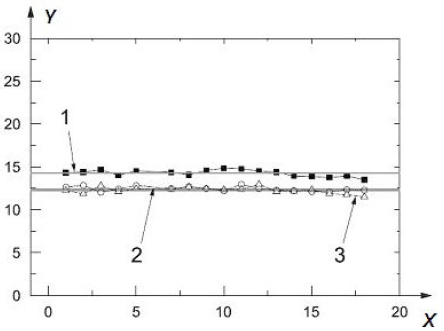
X - время проведения испытаний, ч; Y - СГД, нм; 1 - значения, полученные в ингаляционной камере с высокой концентрацией наночастиц, 2,6%; 2 - значения, полученные в ингаляционной камере со средней концентрацией наночастиц, 2,2%; 3 - значения, полученные в ингаляционной камере с низкой концентрацией наночастиц, 3,0%
Рисунок А.7 - Диаграмма, показывающая изменения значений СГД в течение времени проведения испытаний [13]
На рисунке A.8 представлена диаграмма, показывающая изменения значений СГО в течение времени проведения испытаний.
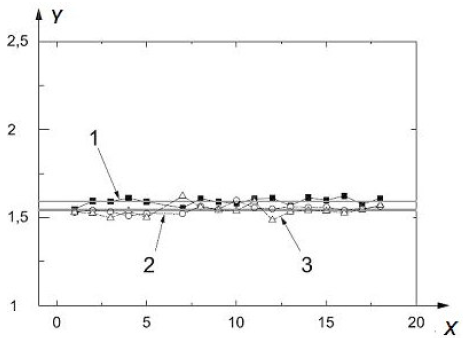
X - время проведения испытаний, ч; Y - СГО; 1 - значения, полученные в ингаляционной камере с высокой концентрацией наночастиц; 2 - значения, полученные в ингаляционной камере со средней концентрацией наночастиц; 3 - значения, полученные в ингаляционной камере с низкой концентрацией наночастиц
Рисунок А.8 - Диаграмма, показывающая изменения значений СГО в течение времени проведения испытаний [13]
На рисунке A.9 представлены рентгеновские энергодисперсионные спектры химического состава наночастиц серебра.
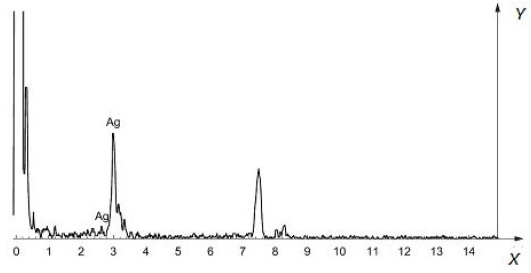
X - энергия рентгеновского излучения, кэВ; Y - интенсивность рентгеновского излучения
Рисунок A.9 - Энергодисперсионные рентгеновские спектры химического состава наночастиц серебра [13]
На рисунке A.9 представлены пики энергодисперсионных рентгеновских спектров химического состава не только наночастиц серебра, но и материала подложки. Неагломерированные наночастицы выявляют с помощью ПЭМ.
На рисунке A.10 представлен график зависимости значений кумулятивного распределения наночастиц по размерам от значений СМД.
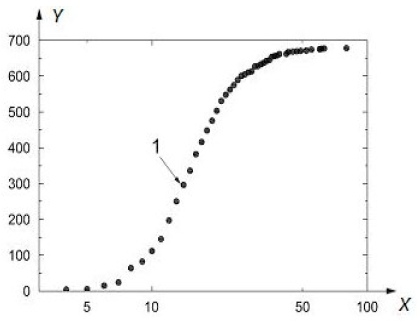
X - СМД, нм; Y - кумулятивная частота; 1 - значение СМД, 18 нм при СГО - 2,1
Рисунок А.10 - График зависимости значений кумулятивного распределения наночастиц по размерам от значений СМД [13]
В ходе испытаний в каждой ингаляционной камере осуществляют контроль следующих характеристик наноаэрозоля: СГД, счетной концентрации наночастиц, удельной площади поверхности, объемной и массовой концентраций наночастиц. Значения удельной площади поверхности, объемной и массовой концентраций наночастиц рассчитывают с помощью компьютерного обеспечения САДЭП по значениям СГД наночастиц при условии, что наночастицы имеют сферическую форму и известна (точно или предположительно) плотность наночастиц серебра. Приблизительные значения объемной концентрации наночастиц и удельной площади поверхности получают при условии, что наночастицы имеют почти сферическую форму и не агрегированы. Значения характеристик наноаэрозоля, полученные в ходе 28-дневных испытаний по оценке его токсичности при ингаляционном поступлении в организм, представлены в таблице A.1.
Таблица A.1 - Значения характеристик наноаэрозоля, полученные в ходе 28-дневных испытаний по оценке его токсичности при ингаляционном поступлении в организм [13]
Место отбора пробы | Зона отбора пробы | СГД, нм (среднее значение ± допустимое отклонение) | Счетная концент- | Удельная площадь поверхности, нм | Объемная концент- | Массовая концент- |
Контрольная ингаляционная камера | - | 0 | 0 | 0 | 0 | 0 |
Ингаляционная камера с низкой концентрацией наночастиц | Вверху | 11,80±0,17 | 2,21·10 | 1,75·10 | 6,27·10 | 0,65±0,41 |
±1,12·10 | ±1,03·10 | ±3,95·10 | ||||
Внизу | 12,13±0,47 | 1,03·10 | 6,83·10 | 2,18·10 | 0,22±0,01 | |
±3,60·10 | ±2,72·10 | ±9,85·10 | ||||
Общая | 11,93±0,22 | 1,73·10 | 1,32·10 | 4,60·10 | 0,48±0,25 | |
±6,64·10 | ±2,34·10 | ±2,34·10 | ||||
Ингаляционная камера со средней концентрацией ночастиц | Вверху | 12,57±0,23 | 1,31·10 | 1,04·10 | 3,72·10 | 3,89±0,79 |
±1,33·10 | ±1,65·10 | ±7,58·10 | ||||
Внизу | 12,15±0,13 | 1,21·10 | 8,60·10 | 2,74·10 | 2,88±0,28 | |
±7,23·10 | ±8,16·10 | ±2,71·10 | ||||
Общая | 12,40±0,15 | 1,27·10 | 9,68·10 | 3,33·10 | 3,48±0,49 | |
±8,45·10 | ±1,04·10 | ±4,66·10 | ||||
Ингаляционная камера с высокой концентрацией наночастиц | Вверху | 14,74±0,14 | 1,35·10 | 1,43·10 | 5,92·10 | 62,12±2,02 |
±2,58·10 | ±3,86·10 | ±1,93·10 | ||||
Внизу | 14,82±0,18 | 1,28·10 | 1,38·10 | 5,73·10 | 60,00±2,31 | |
±2,24·10 | ±4,25·10 | ±2,21·10 | ||||
Общая | 14,77±0,11 | 1,32·10 | 1,41·10 | 5,84·10 | 61,24±1,52 | |
±1,79·10 | ±2,87·10 | ±1,45·10 | ||||
| ||||||
Приложение ДА
(справочное)
Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации (и действующим в этом качестве межгосударственным стандартам)
Таблица ДА.1
Обозначение ссылочного международного стандарта и документа | Степень соответствия | Обозначение и наименование соответствующего национального или межгосударственного стандарта |
ИСО 10312:1995 | - | * |
ИСО 15900:2009 | NEQ | ГОСТ Р 8.775-2011 "Государственная система обеспечения единства измерений. Дисперсный состав газовых сред. Определение размеров наночастиц по методу дифференциальной электрической подвижности аэрозольных частиц" |
ИСО/ТС 27687:2008 | IDT | ГОСТ ISO/TS 27687-2014 |
ОЭСР Тест N 403 | IDT | ГОСТ 32542-2013 "Методы испытаний по воздействию химической продукции на организм человека. Основные требования к проведению испытаний по оценке острой токсичности при ингаляционном поступлении" |
ОЭСР Тест N 412 | IDT | ГОСТ 32643-2014 "Методы испытания по воздействию химической продукции на организм человека. Токсичность подострая ингаляционная: 28-дневное исследование" |
ОЭСР Тест N 413 | IDT | ГОСТ 32636-2014 "Методы испытания по воздействию химической продукции на организм человека. Субхроническая ингаляционная токсичность: 90-дневное исследование" |
ОЭСР Руководящий документ N 39 | - | * |
* Соответствующий национальный или межгосударственный стандарт отсутствует. До его утверждения рекомендуется использовать перевод на русский язык данного международного документа. Перевод данного международного документа находится в Федеральном информационном фонде технических регламентов и стандартов. Примечание - В настоящей таблице использованы следующие условные обозначения степени соответствия стандартов: - IDT - идентичный стандарт; - NEQ - неэквивалентный стандарт. | ||
Библиография
[1] | ISO 9276-5 | Representation of results of particle size analysis - Part 5: Methods of calculation relating to particle size analyses using logarithmic normal probability distribution (Гранулометрический анализ. Представление результатов. Часть 5. Методы расчета при гранулометрическом анализе с использованием логарифмического нормального распределения вероятностей) |
[2] | ISO 9276-6 | Representation of results of particle size analysis - Part 6: Descriptive and quantitative representation of particle shape and morphology (Гранулометрический анализ. Представление результатов. Часть 6. Описательное и количественное представление формы и морфологии частиц) |
[3] | ISO 10801 | Nanotechnologies - Generation of metal nanoparticles for inhalation toxicity testing using the evaporation/condensation method (Нанотехнологии. Генерирование наноаэрозолей, применяемых для оценки токсичности при ингаляционном поступлении в организм, методом испарения/конденсации) |
[4] | ISO/AWI TR 12885 | Nanotechnologies - Health and safety practices in occupational settings relevant to nanotechnologies (Нанотехнологии. Методы здравоохранения и безопасности в профессиональном окружении в связи с нанотехнологиями) |
[5] | ISO/TR 13014 | Nanotechnologies - Guidance on physico-chemical characterization of engineered nanoscale materials for toxicologic assessment (Нанотехнологии. Руководство по физико-химическому описанию материалов с заданной наношкалой для токсикологической оценки) |
[6] | ISO/IEC 17025 | General requirements for the competence of testing and calibration laboratories (Общие требования к компетентности испытательных и калибровочных лабораторий) |
[7] | ISO/TR 18394 | Surface chemical analysis - Auger electron spectroscopy - Derivation of chemical information (Химический анализ поверхности. Оже-электронная спектроскопия. Источник химической информации) |
[8] | ISO/TR 27628 | Workplace atmosphers - Ultrafine, nanoparticle and nano-structured aerosols - Inhalation exposure characterization and assessment (Атмосферы на рабочем месте. Очень мелкие аэрозоли, аэрозоли с наночастицами и наноструктурой. Определение характеристик и оценка воздействия при вдыхании) |
[9] | Ahn, K.H., Jung, C.H., Choi, M., and Lee, J.S. Particle sampling and real time size distribution measurement inH2/O2/TEOS diffusion flame. J. Nanoparticle Res., 3, pp.161-170 (2001) | |
[10] | Goldberg, A.M. and Hartung, T. Protecting more than animals. Sci. Am., 294, pp.84-91 (2006) | |
[11] | Hinds, W.C., Aerosol Technology, Wiley Interscience (1999) | |
[12] | Ji, J.H., Jung, J.H., Yu, I.J. and Kim, S.S. Long-term stability characteristics of a nanoparticle generator using a small ceramic heater for inhalation toxicity study. Inhalation Toxicology, 19, pp.745-751 (2007) | |
[13] | Ji, J.H., Jung, J.H., Kim, S.S., Yoon, J.U., Park, J.D., Choi, B.S., Chung, Y.H., Kwon, I.H., Jeong, J., Han, B.S., Shin, J.H., Sung, J.H., Song, K.S. and YU, I.J. Twenty-eight-day inhalation toxicity study of silver nanoparticles in Sprague Dawley Rats. Inhalation Toxicology, 19(10), pp.857-871 (2007) | |
[14] | Ku, B.K and De LA Mora, J.F. Relation between Electrical Mobility, Mass, and Size for Nanodrops 1-6.5 nm in Diameter in Air. Aerosol Science and Technology, 43:3, pp.241-249 (2009) | |
[15] | Ku, B.K. and Maynard, A.D. Comparing aerosol surface-area measurement of monodisperse ultrafine silver agglomerates using mobility analysis, transmission electron microscopy and diffusion charging. J. Aerosol Sci., 36 pp.1108-1124 (2005) | |
[16] | Fissan, H., Neumann, S., Trampe, A., Pui, D.Y.H. and Shin, W.G Rationale and principle of an instrument measuring lung deposited nanoparticle surface area. J. Nanoparticle R, 9, pp.53-59 (2007) | |
[17] | Sung, J.H., Ji, J.H., Yun, J.U., Kim, D.S., Song, M.Y, Jeong, J, Han, B.S., Han, J.H., Chung, Y.H., Kim, J., Kim, T.S., Chang, H.K., Lee, E.J., Lee, J.H. and Yu, I.J. Lung function changes in Sprague-Dawley rats after prolonged inhalation exposure to silver nanoparticles. Inhalation Toxicology, 20, pp.567-574 (2008) | |
[18] | Sung, J.H., Ji, J.H., Park, J.D., Yoon, J.U., Kim, D.S., Jeon, K.S., Song, M.Y, Jeong, J., Han, B.S., Han, J.H., Chung, Y.H., Chang, H.K., Lee, J.H., Cho, M.H., Kelman, B.J. and Yu, I.J. Subchronic inhalation toxicity of silver nanoparticles. Toxicol Sci 108 (2), pp.452-61 (2009) | |
[19] | Friedlander, S.K., Smoke Dust and Haze, Wiley Interscience, New York (2000) | |
[20] | Willeke, K., and Baron, P.A. Aerosol Measurement: Principles, Techniques, and Applications, Van Nostrand Reinhold, New York (1993) | |
[21] | United States Environmental Protection Agency, Prevention, pesticides and toxic substances (7101), EPA712-C-98-204, EPA Health Effects Test Guidelines OPPTS 870.3465 (1998) 90-Day Inhalation Toxicity, US EPA | |
УДК 57.08:006.354 | ОКС 07.030 | Т 58 |
Ключевые слова: нанотехнологии, наноаэрозоль, наночастица, оценка токсичности при ингаляционном поступлении, контроль характеристик | ||
Электронный текст документа
и сверен по:
, 2016

