ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ

НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ГОСТ Р
ИСО 14375—
2023
УПАКОВКА ДЛЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ, НЕ ПРЕДНАЗНАЧЕННАЯ ДЛЯ МНОГОРАЗОВОГО ОТКРЫВАНИЯ И ЗАКРЫВАНИЯ, С ЗАЩИТОЙ ОТ ВСКРЫТИЯ ДЕТЬМИ
Требования и испытания
(ISO 14375:2018, IDT)
Издание официальное
Москва Российский институт стандартизации 2023
Предисловие
1 ПОДГОТОВЛЕН Федеральным государственным автономным образовательным учреждением высшего образования Первый Московский государственный медицинский университет имени И.М. Сеченова Министерства здравоохранения Российской Федерации [ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет)] на основе официального перевода на русский язык англоязычной версии указанного в пункте 4 стандарта, который выполнен Федеральным государственным бюджетным учреждением «Российский институт стандартизации» (ФГБУ «Институт стандартизации»)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 458 «Разработка, производство и контроль качества лекарственных средств»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 29 июня 2023 г. № 456-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 14375:2018 «Упаковка для лекарственных препаратов, не предназначенная для многоразового открывания и закрывания, с защитой от вскрытия детьми. Требования и испытания» (ISO 14375:2018 «Child-resistant non-reclosable packaging for pharmaceutical products. Requirements and testing», IDT).
Международный стандарт разработан Европейским комитетом по стандартизации (CEN) (как EN 14375) и принят подкомитетом ПК 3 «Требования к эксплуатации и методам испытаний упаковочных средств, упаковки и единичных грузов» Технического комитета ИСО/ТК 122 «Упаковка».
Дополнительные сноски в тексте стандарта, выделенные курсивом, приведены для пояснения текста оригинала
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в статье 26 Федерального закона от 29 июня 2015 г. № 162-ФЗ «О стандартизации в Российской Федерации». Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.rst.gov.ru)
© ISO, 2018 © Оформление. ФГБУ «Институт стандартизации», 2023
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
Содержание
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Требования
5 Проведение испытаний
6 Отчет об испытании
Приложение А (справочное) Руководство для лиц, выполняющих функции контролеров испытаний с участием детей
Приложение В (обязательное) Графики испытаний
Приложение С (справочное) Пригодность выбранных процедур ступенчатых испытаний
Библиография
Введение
Упаковка с защитой от вскрытия детьми используется для создания физического барьера между ребенком и потенциально опасным продуктом. Различные типы упаковки признаются защищенными от вскрытия детьми на основании тестирования их эффективности по стандартам для определенных категорий продукции и типов упаковки.
С момента появления упаковки, защищенной от вскрытия детьми, значительно уменьшилось количество случаев, связанных с проглатыванием детьми в возрасте до пяти лет потенциально опасных продуктов. И хотя трудно дать количественную оценку того, насколько это обусловлено использованием защищенной от вскрытия детьми упаковки, а не другими факторами, такими как повышение степени информированности общества об опасностях, можно с уверенностью сказать, что упаковка данного типа внесла значительный вклад в снижение количества таких случаев.
Защищенную от вскрытия детьми упаковку следует использовать только для тех продуктов, которые являются потенциально опасными, или там, где этого требует законодательство, так как если использовать эту упаковку в иных обстоятельствах, то это может привести к введению в заблуждение потребителей в отношении степени опасности, связанной с тем или иным продуктом.
В любом случае, правильная маркировка и информация от производителя играют важную роль для безопасного использования продуктов в быту.
Упаковка с защитой от вскрытия детьми функционирует как последнее средство защиты, когда другие барьеры, отделяющие ребенка от опасного вещества, уже преодолены. Однако следует признать, что невозможно рассчитывать на то, что любая защитная упаковка может быть абсолютно устойчива к вскрытию ребенком в возрасте от 42 до 51 мес включительно, и такая сложная для вскрытия детьми упаковка не может служить заменой другим разумным мерам предосторожности.
Поскольку использование упаковки, защищенной от вскрытия детьми, возрастает, то во избежание путаницы и разногласий в области, имеющей большое значение для безопасности детей младшего возраста, желательно достичь согласия по методикам испытаний.
Непрерывное развитие и совершенствование упаковки, защищенной от вскрытия детьми, открывает большие возможности для инноваций в этой области. Стили защищенной от вскрытия детьми упаковки могут быть самыми разнообразными по конструкционному исполнению или дизайну.
Настоящий документ направлен на сокращение количества детей, «подвергающихся обучению» во время групповых испытаний. С момента появления испытаний эффективности стало доступно много информации о проведении испытаний упаковки, защищенной от вскрытия детьми, с участием детей, и внимание было сосредоточено на том, каким образом можно уменьшить количество детей, привлекаемых к проведению испытаний. Дальнейшая разработка стандартов, основанных на методах механических испытаний, необходима во избежание ненужных групповых испытаний с участием детей, а также для совершенствования физических качеств упаковки, используемой изготовителями.
Упаковка с защитой от вскрытия детьми является последней в серии средств защиты, поэтому ответственность за безопасность детей все равно лежит на родителях или на тех взрослых, в обязанности которых входит присматривать за детьми.
ГОСТ Р ИСО 14375—2023
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
УПАКОВКА ДЛЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ, НЕ ПРЕДНАЗНАЧЕННАЯ ДЛЯ МНОГОРАЗОВОГО ОТКРЫВАНИЯ И ЗАКРЫВАНИЯ, С ЗАЩИТОЙ ОТ ВСКРЫТИЯ ДЕТЬМИ
Требования и испытания
Child-resistant non-reclosable packaging for pharmaceutical products. Requirements and testing
Дата введения — 2024—07—01
1 Область применения
Настоящий стандарт устанавливает требования и методы испытаний упаковки для лекарственных препаратов с защитой от вскрытия детьми, без возможности повторного закрытия. Настоящий стандарт предназначен только для подтверждения соответствия типа упаковки (см. 3.5) и не применяется в целях обеспечения качества.
2 Нормативные ссылки
В настоящем стандарте нормативные ссылки отсутствуют.
3 Термины и определения
В настоящем стандарте применены следующие термины и определения.
ИСО и МЭК поддерживают терминологические базы данных, используемые в стандартизации по следующим адресам:
- платформа онлайн-просмотра ИСО: доступна по адресу https://www.iso.org/obp
- Электропедия МЭК: доступна по адресу http://www.electropedia.org/
3.1 упаковка с защитой от вскрытия детьми* (child-resistant package): Упаковка, которую трудно открыть (или получить доступ к ее содержимому) маленьким детям, но которой не трудно правильно пользоваться взрослым.
3.2 упаковка с защитой от вскрытия детьми, не предназначенная для многоразового открывания и закрывания* (non-reclosable child-resistant package): Упаковка с защитой от вскрытия детьми (см. 3.1) или ее часть, которая после вскрытия и полного или частичного извлечения ее содержимого не может быть снова надлежащим образом закрыта.
3.3 имитирующая продукция** (substitute product): Нейтральная продукция (заменитель), имитирующая продукцию, вместо которой она используется.
Примечание — Иногда его называют плацебо.
Пример — Порошок, таблетки или жидкости (бесцветная вода) и т. д.
* Термин применяют только для упаковки лекарственных препаратов — в соответствии с Решением Коллегии ЕЭК от 25.10.2022 г. № 150 «О внесении изменений в Фармакопею Евразийского экономического союза». Для упаковки любой другой продукции используют термин «упаковка, недоступная для открывания детьми».
* * Это продукт, не обладающий фармакологическим действием, близкий по своим характеристикам к лекарственному препарату. Термин применяют только для упаковки лекарственных препаратов. Для упаковки любой другой продукции используют термин «имитация (муляж) продукции» по ГОСТ ИСО 28862.
Издание официальное
3.4 единица лекарственной формы (unit dose): Дозированная единица продукта, полностью извлекаемая из первичной упаковки.
3.5 подтверждение соответствия типа упаковки (type approval): Процедура подтверждения соответствия в качестве определенного типа упаковки с защитой от вскрытия детьми1, не предназначенной для многоразового открывания и закрывания, произведенной из определенных материалов.
4 Требования
4.1 Общие требования
При проведении испытаний на соответствие требованиям настоящего стандарта упаковки с защитой от вскрытия детьми, не предназначенной для многоразового открывания и закрывания, необходимо подтвердить удовлетворительную степень сложности ее вскрытия детьми (см. 4.2.1) и возможность взрослых людей достаточно легко получить доступ к ее содержимому (см. 4.2.2).
Кроме соответствия требованиям настоящего стандарта (см. 4.2) такая упаковка должна быть пригодной для хранения в ней лекарственных препаратов, обеспечивать защиту от механических повреждений и функционировать надлежащим образом на протяжении всего срока годности препарата и самой упаковки.
Производители первичной упаковки и ее элементов, предприятия, осуществляющие упаковывание лекарственных препаратов в первичную упаковку, должны разработать и выполнять процедуры по контролю качества упаковочных материалов так, чтобы упаковка данного типа отвечала требованиям настоящего стандарта.
Примечание — ИСО 9001 устанавливает требования к системам менеджмента качества для организаций, которым необходимо демонстрировать свою способность поставлять потребителям продукцию, соответствующую установленным требованиям.
4.2 Требования к эффективности защиты от вскрытия (функциональные требования)
4.2.1 Испытание с участием детейИндивидуальный результат испытания с участием детей считают отрицательным, если ребенок в течение 10 мин получает доступ к более чем восьми единицам лекарственной формы, содержащимся в испытуемой упаковке, представляющей собой однодозовую упаковку, контурную ячейковую (блистер) или безъячейковую (стрип) упаковку.
Если упаковка подверглась испытанию в соответствии с 5.3.2 и оценена в соответствии с 5.4.1.3, считают, что она имеет защиту от вскрытия детьми.
Примечание — Требование в отношении восьми единиц лекарственной формы основывается на действующих национальных стандартах, опубликованных рядом членов ЕКС (CEN), и не учитывает выраженность токсических эффектов продукта. Некоторые лекарственные препараты, имеющиеся на рынке, могут причинить вред детям при проглатывании ими меньшего количества единиц лекарственной формы. Однако достоверные данные по токсичности у детей имеются лишь для незначительного количества лекарственных препаратов. Можно определить опасную для здоровья дозу для некоторых имеющихся лекарственных препаратов и тем или иным образом определить максимальную безопасную дозу каждого препарата. Такая информация в настоящее время недоступна для всех препаратов, а единый реестр, содержащий такую информацию, отсутствует. В отсутствие общего законодательства разработчики настоящего стандарта осознают актуальность данной проблемы и полагают, что в более поздней версии стандарта появится более точная информация в отношении оценочных критериев по токсичности препаратов применительно к групповым испытаниям с участием детей.
4.2.2 Испытание с участием взрослых людей
При испытаниях в соответствии с 5.3.3.2 не менее 90 % взрослых людей, участвовавших в испытаниях, должны в течение 1 мин суметь получить доступ хотя бы к одной единице лекарственной формы без предварительной демонстрации (показа) способа вскрытия упаковки.
Чтобы не подвергать детей ненужным испытаниям, испытание с участием взрослых людей следует проводить до испытаний с участием детей.
5 Проведение испытаний
5.1 Принцип испытания
Подтверждение соответствия типа упаковки с защитой от вскрытия детьми, не предназначенной для многоразового открывания и закрывания, проводят путем проведения испытаний с участием детей по последовательной методике или при участии всей группы (панели) испытуемых, а для взрослых — при участии всей группы (панели) испытуемых. Группу испытуемых в количестве до 200 детей в возрасте от 42 до 51 мес разбивают на пары. Каждому ребенку дают несколько упаковок, не предназначенных для многоразового открывания и закрывания, и просят открыть их любым способом, которым они пожелают воспользоваться. Ребенку, не справившемуся с заданием в течение 5 мин, контролер должен показать, как вскрывается упаковка. Затем ребенку предоставляют еще 5 мин для вскрытия упаковки. Результаты регистрируют (вносят в графики) последовательно по мере их получения. Упаковку считают защищенной от вскрытия детьми, если результаты испытаний на соответствующих графиках испытаний попадают в зону приемлемости, или же если не менее 80 % всех детей, участвовавших в испытании, не смогли получить доступ к более чем восьми единицам лекарственной формы в течение 10 мин и если не менее 85 % всех детей, участвовавших в испытании, не смогли получить доступ к более чем восьми единицам лекарственной формы в течение первых 5 мин. Степень сложности доступа к содержимому упаковки также оценивают с участием группы из 100 взрослых испытуемых. Каждому взрослому выдают упаковку, не предназначенную для многоразового открывания и закрывания, со всеми прилагаемыми к упаковке вспомогательными средствами и инструкцией по вскрытию. Участникам испытания в течение 5 мин предлагают ознакомиться с данной упаковкой, а затем правильно вскрыть упаковку и получить доступ к ее содержимому. Регистрируют количество взрослых, вскрывших упаковку в течение 1 мин. Упаковка считается отвечающей требованиям настоящего стандарта, если не менее 90 % взрослых участников смогли за 1 мин получить доступ хотя бы к одной единице лекарственной формы.
5.2 Образцы упаковки и их подготовка
Необходимо произвести достаточное количество упаковок с лекарственным препаратом, позволяющее контролеру провести отбор репрезентативных образцов и обеспечить резерв для архивных образцов. Высокоактивные и токсичные препараты должны быть заменены на подходящие препараты-плацебо. Материал и конструктивное исполнение испытуемых образцов упаковки должны соответствовать требованиям спецификации, и они должны быть репрезентативны по отношению к обычной серии производимой продукции.
Упаковки, предназначенные для испытания с участием детей, должны быть незапечатанными.
Для каждого испытания предусматривают новую упаковку для каждого участника. Для испытаний с участием как детей, так и взрослых, каждый участник получает упаковку, содержащую не менее десяти единиц лекарственной формы.
Перед испытанием должна проверяться целостность каждой упаковки. Детям следует выдавать первичные упаковки с лекарственными препаратами (без вторичной упаковки), обеспечивая им доступ к единицам лекарственной формы.
5.3 Процедура испытания
5.3.1 Общие положенияИспытание проводят в два этапа:
а) испытание с участием детей (см. 5.3.2);
Ь) испытание с участием взрослых (см. 5.3.3).
5.3.2 Испытание с участием детей
5.3.2.1 Формирование детской испытуемой группы
Группа должна включать не более 200 детей в возрасте от 42 до 51 мес включительно с равномерным распределением по возрасту и полу. Детей отбирают случайным образом. Критерии отбора должны включать условие отсутствия физических или ментальных отклонений, которые могли бы повлиять на ловкость рук. Также не следует включать в испытуемую группу детей, участвовавших в испытаниях упаковки более одного раза, при условии, что в тех испытаниях тестировалась упаковка с другим принципом вскрытия и конструкцией. При повторном участии ребенка в испытаниях рекомендуется обеспечить перерыв между испытаниями не менее четырех недель. Для включения ребенка в состав испытательной группы должно быть получено согласие от родителей или опекуна (законного представителя) ребенка. В испытании не должны участвовать дети, в отношении которых имеются сведения о случаях отравления.
Детей следует отбирать таким образом, чтобы они представляли различные социальные, этнические и культурные слои населения страны в целом, а не только того района или местности, где проводят испытания.
5.3.2.2 Порядок проведения испытания
Испытания должны проводиться в присутствии контролера. Испытание с участием детей проводят в знакомой для детей обстановке.
Персонал, участвующий в испытании, должен заранее посетить место проведения испытания и встретиться с детьми для того, чтобы они испытывали к нему доверие. При проведении испытаний должны присутствовать только контролеры, присутствие родителей не допускается.
Испытание должно проводиться по последовательной методике (см. 5.4.1.1—5.4.1.3). Таким образом, количество детей, участвующих в испытании, будет зависеть от полученных результатов. При этом должны соблюдаться ограничения по возрасту и полу, указанные в 5.3.2.1.
Дети участвуют в испытании парами и каждая пара находится под наблюдением одного контролера. Если ребенок ушел со своего места во время испытания, действия контролера должны ограничиться тем, чтобы вернуть ребенка на место и попросить его продолжить испытание, не давая дополнительных инструкций по вскрытию упаковки; такое событие должно быть отражено в отчете об испытании (см. раздел 6).
В одном помещении одновременно в испытаниях могут участвовать несколько пар (до пяти) при условии, что это не будет отвлекать другие пары испытуемых. Дети могут принимать любое положение или позицию, которую сочтут для себя удобной. Во время испытания детей следует по возможности оградить от внешних отвлекающих факторов. При использовании других средств наблюдения за детьми контролер может стоять на расстоянии от детей.
Каждому ребенку дают достаточное количество упаковок с лекарственным препаратом (см. 5.2) и просят открыть ее любым удобным для него способом в течение 10 мин. Испытание не останавливают, если ребенок пытается открыть упаковку зубами или любым другим способом. Однако ребенок не должен иметь доступа к каким-либо инструментам или подручным средствам для вскрытия упаковки, кроме тех инструментов и устройств, которые прилагаются производителем упаковки или производителем лекарственного препарата, в том числе осуществляющим только стадии упаковки.
Детям, не сумевшим вскрыть упаковку или получить доступ хотя бы к одной единице лекарственной формы в течение первых 5 мин, контролер должен, не акцентируя внимания на своих действиях, один раз показать, как открывается упаковка, не поясняя словами свои действия. Затем ребенку дают еще 5 мин для открытия упаковки или получения доступа к ее содержимому.
Если ребенок покидает зону испытаний во время испытательного периода (5 мин или 10 мин) или отказывается участвовать в испытании несмотря на просьбы, такой результат не учитывается, но данное событие следует зарегистрировать.
Если для вскрытия упаковки необходимы инструменты, которые не поставляются производителем вместе с упаковкой, демонстрацию вскрытия упаковки не проводят. В этих случаях продолжительность испытания ограничивается первыми 5 мин.
По завершении каждого испытания детей нужно предупредить, чтобы они не играли с упаковками или не пытались их вскрывать.
Примечание — В приложении А приведено руководство для контролеров испытаний, включая ряд обязательных требований. По требованию регуляторного органа при испытании может присутствовать официальный наблюдатель, тем не менее руководство, изложенное в приложении А, должно соблюдаться.
5.3.3 Испытание с участием взрослых
5.3.3.1 Формирование взрослой испытуемой группы
Группа должна включать 100 испытуемых; при отборе потенциальных участников испытания опрашивают по следующим вопросам:
- не связана ли его трудовая деятельность с конструированием, производством или использованием упаковки с защитой от вскрытия детьми;
- принимал ли он в предыдущие 6 мес участие в тестировании упаковки с защитой от вскрытия детьми более одного раза.
Для участия в испытании отбирают только лица, давшие отрицательные ответы на эти вопросы.
Для регистрации ответов, а также проверки грамотности, опрос проводят в письменном виде.
Критерии отбора должны включать условия отсутствия физических или ментальных отклонений, которые могли бы повлиять на ловкость рук, и способность понимать письменные инструкции по вскрытию упаковки.
Испытуемым доступно объясняют цель испытания, но демонстрацию вскрытия упаковки не проводят.
Случайным образом отбирают 100 участников в возрасте от 50 до 70 лет в соответствии с требованиями, указанными в таблице 1. Не допускается отбирать или включать в испытание более 30 испытуемых взрослых из одного места (района, региона). Если одновременно в испытании принимают участие менее 35 взрослых испытуемых, то проводить испытание может один контролер.
Таблица 1 — Состав взрослой испытательной группы
Возрастной диапазон, лет | Мужчины, число участников | Женщины, число участников | Всего, число участников | |
50—54 | 8 или 7 | 17 или 18 | 25 | |
55—59 | 7 или 8 | 18 или 17 | 25 | |
60—70 | 15 | 35 | 50 | |
Всего | — | 30 | 70 | 100 |
5.3.3.2 Порядок проведения испытаний
Не требуется проводить испытания с участием взрослых исключительно в каком-либо определенном месте или в определенном времени. Испытание выполняет один человек в конкретный период времени в присутствии только контролера.
Каждому взрослому участнику выдают упаковку со всеми вспомогательными средствами, которые вложены в потребительскую (вторичную) упаковку, и письменными инструкциями по вскрытию упаковки, которые могут быть напечатаны на упаковке или включены в инструкцию по применению лекарственного препарата.
Задание выполняется каждым участником индивидуально. Демонстрацию вскрытия упаковки не проводят. Участнику испытания в течение 5 мин предлагают ознакомиться с упаковкой, прочитать соответствующую инструкцию, а затем правильно вскрыть упаковку. Участникам испытания не разрешают консультироваться с контролером или другими участниками испытания.
Тем участникам, которым удалось в течение 5 мин вскрыть испытуемую упаковку, выдают новую идентичную упаковку с просьбой вскрыть ее максимально быстро в течение не более 1 мин.
Если же в течение 5 мин участник не смог вскрыть первую испытуемую упаковку, то проводят дополнительное тестирование. Дополнительный тест включает открытие и закрытие упаковки в течение 1 мин каждое с помощью двух обычных укупорочных средств (без защиты от вскрытия детьми):
- крышка диаметром 28 мм с винтовой резьбой, навинчиваемая с крутящим моментом на 1,1 Нм на полимерный контейнер объемом от 25 до 50 мл с цилиндрической горловиной;
- крышка диаметром 28 мм, надеваемая на полимерный контейнер объемом от 25 до 50 мл с круглой горловиной.
У частники, не способные открыть и повторно закрыть обе такие упаковки в течение 1 мин, исключаются из состава группы, и их результаты не учитывают.
Результаты участников, способных открыть и повторно закрыть только упаковки с обычными укупорочными средствами, считают отрицательными.
5.4 Оценка результатов
5.4.1 Испытание с участием детей5.4.1.1 Общие положения
Результат каждого испытания заносят в графики испытания упаковки, представленные на рисунках В.1 и В.2 в соответствии с 5.4.1.2. Данные результаты оценивают в соответствии с 5.4.1.3.
Примечание — Статистические параметры, регулирующие процедуры отбора образцов упаковки для графиков их испытаний, приведены в приложении С.
Результат испытания считают отрицательным, если ребенок в течение 10 мин сможет получить доступ более чем к восьми единицам лекарственной формы, содержащимся в испытуемой упаковке, представляющей собой однодозовую упаковку, контурную ячейковую (блистер) или безъячейковую (стрип).
5.4.1.2 Графики испытаний
Каждый полученный результат заносят в соответствующий график, заполняя клетку графика, приведенного на рисунке В.1 или на рисунке В.2, следующим образом:
а) если ребенок не смог получить доступ к более чем восьми единицам лекарственной формы в течение первых 5 мин, то заполняют клетку, расположенную справа от предыдущего результата на графике рисунка В.1, и на графике рисунка В.2, если ребенок не смог получить доступ к более чем восьми единицам лекарственной формы в течение последующих 5 мин;
Ь) если ребенок смог получить доступ к более чем восьми единицам лекарственной формы в течение первых 5 мин, то заполняют клетку, расположенную непосредственно над предыдущим результатом на графиках рисунков В.1 и В.2, и только на графике рисунка В.2, если ребенок смог получить доступ к более чем восьми единицам лекарственной формы в течение последующих 5 мин.
Примечание — При регистрации результата «предыдущим результатом» считают незаполненную клетку.
5.4.1.3 Представление результатов
5.4.1.3.1 Последовательная методика
Упаковку считают:
- прошедшей испытание, если при заполнении клеток текущий результат попадает в зону приемлемости как на рисунке В.1, так и на рисунке В.2;
- не прошедшей испытание, если при заполнении клеток текущий результат попадает в зону не-приемлемости/отклонения или на рисунке В.1, или на рисунке В.2.
Если не происходит ни того ни другого, результаты оценивают в соответствии с требованиями, изложенными в 5.4.1.3.2.
5.4.1.3.2 Проведение испытаний с участием всей группы
Если испытания проводят с участием всех 200 детей из испытательной группы, упаковку считают защищенной от вскрытия детьми при выполнении следующих требований:
а) не менее 85 % детей не смогли получить доступ к более чем восьми единицам лекарственной формы в течение 5 мин при отсутствии демонстрации способа вскрытия упаковки;
Ь) не менее 80 % детей не смогли получить доступ к более чем восьми единицам лекарственной формы в течение 10 мин (в течение 5 мин при отсутствии демонстрации способа вскрытия упаковки и в течение 5 мин после демонстрации, если она потребовалась).
5.4.2 Испытание с участием взрослых
При проведении испытаний согласно 5.3.3.2 результат испытания для любого взрослого считают отрицательным, если последний не сумел получить доступ хотя бы к одной единице лекарственной формы в течение одной минуты, за исключением лиц, не справившихся с дополнительным тестированием (не сумевших вскрыть упаковки с обычными укупорочными средствами).
5.5 Общий результат испытаний
Только упаковка, отвечающая требованиям испытаний как в отношении детей, так и в отношении взрослых, указанным в 4.2, может считаться соответствующей настоящему стандарту.
6 Отчет об испытании
6.1 Общие положения
В отчете должна содержаться следующая информация:
а) наименование организации, проводящей испытания;
Ь) дата(ы) проведения испытания;
с) наименование и адрес производителя и/или поставщика испытуемой упаковки;
d) фамилия лица/лиц, выполняющего(их) функции контролеров;
е) спецификации на материалы, входящие в состав упаковки, чертежи или фотографии, когда это нужно, а также полное описание испытуемой упаковки;
f) перечень точных инструкций, даваемых контролером взрослым участникам и детям во время испытания;
д) копия инструкции производителя по вскрытию упаковки, предоставляемой взрослым участникам во время испытания;
h) описание препарата-плацебо (имитирующей продукции), используемого при проведении испытания.
6.2 Испытание с участием детей
В отчете должна содержаться следующая информация:
а) место(а) проведения испытания;
Ь) количество, возраст и пол детей, участвовавших в испытании;
с) количество детей с указанием возраста и пола, успешно вскрывших и получивших доступ к содержимому упаковки, как это указано в 5.4.1.1—5.4.1.3:
1) до демонстрации способа вскрытия упаковки,
2) после демонстрации способа вскрытия упаковки;
d) время, затраченное на вскрытие упаковки;
е) количество единиц лекарственной формы, к которым смог получить доступ каждый ребенок;
f) использованный способ вскрытия упаковки.
6.3 Испытание с участием взрослых
В отчете должна содержаться следующая информация:
а) количество, возраст и пол взрослых, участвовавших в испытании;
Ь) количество взрослых, которые в ходе испытания вскрыли упаковку в течение 1 мин;
с) количество взрослых, которые в ходе испытания не смогли вскрыть упаковку в течение 1 мин;
d) количество, возраст и пол взрослых, которые в ходе испытания не смогли вскрыть упаковку в течение 5 мин;
е) время, затраченное на вскрытие упаковки;
f) причина, помешавшая вскрытию упаковки.
6.4 Дополнительная информация, включаемая в отчет
В отчет об испытании следует включать любую дополнительную информацию, которая будет полезной при оценивании и интерпретации результата.
6.5 Общий результат испытаний
В отчете об испытании необходимо указать, является ли общий результат испытания положительным или отрицательным в соответствии с 5.5.
Приложение А (справочное)
Руководство для лиц, выполняющих функции контролеров испытаний с участием детей
А.1 Согласие родителей/опекунов
До включения ребенка в состав испытуемой группы должно быть получено согласие от родителей или опекуна ребенка.
А.2 Окружение и персонал
Испытание с участием детей проводят в знакомой и дружелюбной обстановке. Персонал, участвующий в испытаниях, должен заранее посетить место проведения испытаний и встретиться с детьми для того, чтобы они испытывали к нему доверие. При испытаниях должны присутствовать только контролеры, присутствие родителей при испытаниях не допускается.
А.З Социальное положение детей
Детей следует отбирать таким образом, чтобы они представляли различные социальные, этнические и культурные слои населения страны в целом, а не только того района или местности, где проводят испытания.
А.4 Сведения о имевших место случаях отравления
В испытании не должны участвовать дети, в отношении которых имеются сведения о случаях отравления лекарственными средствами.
А.5 Исключение внешних отвлекающих факторов
Во время испытания детей следует по возможности огородить от внешних отвлекающих факторов.
А.6 Размещение детей
Дети могут принимать любое положение или позицию.
А.7 Поведение контролера во время испытаний
а) Контролер обращается к детям с просьбой вскрыть упаковку.
Ь) Инструкции по вскрытию упаковки не предоставляют, за исключением визуальной демонстрации способа вскрытия в случаях, когда такая демонстрация предусмотрена.
с) Детей не следует сдерживать или отвлекать.
d) Если дети теряют интерес к испытуемому объекту, контролеру следует повторить просьбу о вскрытии упаковки.
е) При использовании других средств наблюдения за детьми контролер может стоять на некотором расстоянии от детей.
f) Контролеру следует побуждать детей получить доступ к содержимому упаковки любым способом, не упоминая какого-либо конкретного способа.
д) По завершении каждого испытания детей нужно предупредить, чтобы они не играли с упаковками или не пытались их открывать.
Приложение В (обязательное)
Графики испытаний
Результаты должны отмечаться на графиках, представленных на рисунках В.1 и В.2, в соответствии с 5.4.1.2.
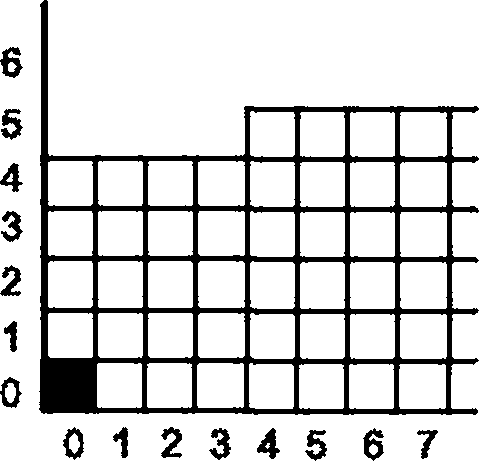

1
1 — количество неоткрытых единиц упаковки (положительный результат); 2 — количество открытых единиц упаковки (отрицательный результат); 3 — разметка в увеличенном масштабе; 4 — зона неприемлемости/отклонения; 5 — зона приемлемости
Рисунок В.1 — График испытания упаковки с участием детей по последовательной методике (результаты после 5 мин испытания до демонстрации способа вскрытия упаковки)
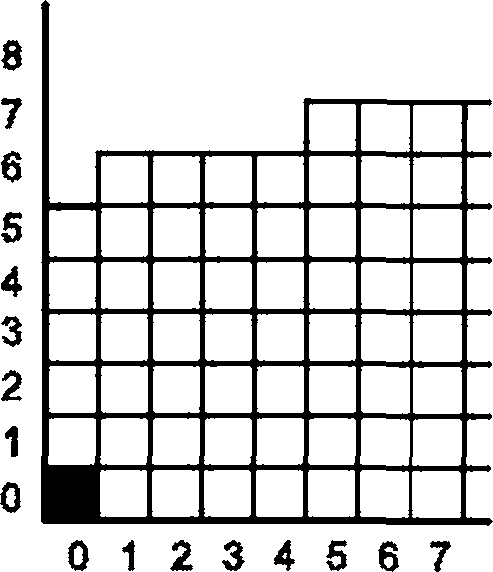

0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 150 160
1 — количество неоткрытых единиц упаковки (положительный результат); 2 — количество открытых единиц упаковки (отрицательный результат); 3 — разметка в увеличенном масштабе; 4 — зона неприемлемости/отклонения; 5 — зона приемлемости
Рисунок В.2 — График испытания упаковки с участием детей по последовательной методике (результаты после всего периода испытания)
Приложение С (справочное)
Пригодность выбранных процедур ступенчатых испытаний
Пригодность процедуры отбора обычно определяется координатами двух точек на операционной кривой: точка для риска производителя и точка для риска потребителя. Приемлемый уровень качества (AQL) и предельный уровень качества (LQ) для двух процедур отбора, используемых в настоящем стандарте, следующие:
- дети (до демонстрации способа вскрытия упаковки) (см. рисунок В.1):
Приемлемый уровень качества а = 5 %
(AQL): рА = уровень качества по риску производителя = 10 %
Предельный уровень качества р = 5 %
(LQ): pR = уровень качества по риску потребителя = 20 %
- дети (после демонстрации способа вскрытия упаковки) (см. рисунок В.2):
AQL=15% а = 5%
LQ = 25 % р = 5 %
где а — риск производителя;
Р — риск потребителя.
Приведенные значения являются достаточно точными для используемых процедур отбора и их оценки, они не подходят для вычисления нового набора показателей приемлемости и неприемлемости. Указанные на графиках и в таблицах значения также учитывают другие критерии и на практике их можно считать стандартными.
Библиография
[1] ISO 9001 Quality management systems — Requirements (Системы менеджмента качества. Требования)
[2] ISO/IEC 17025 General requirements for the competence of testing and calibration laboratories (Общие требования к компетентности испытательных и калибровочных лабораторий)
УДК 615.014.83:006.354
ОКС 55.020
Ключевые слова: первичная упаковка, лекарственные препараты, защита от вскрытия детьми
Редактор Е.Ю. Митрофанова Технический редактор В.Н. Прусакова Корректор М.В. Бучная Компьютерная верстка И.А. Налейкиной
Сдано в набор 30.06.2023. Подписано в печать 06.07.2023. Формат 60х841/8. Гарнитура Ариал. Усл. печ. л. 1,86. Уч.-изд. л. 1,30.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
Создано в единичном исполнении в ФГБУ «Институт стандартизации» , 117418 Москва, Нахимовский пр-т, д. 31, к. 2.
1
Термин применяют только для упаковки лекарственных препаратов — в соответствии с Решением Коллегии ЕЭК от 25.10.2022 г. № 150 «О внесении изменений в Фармакопею Евразийского экономического союза». Для упаковки любой другой продукции используют термин «упаковка, недоступная для открывания детьми».

