А
ГОСТ Р 57525-2017
Группа Р24
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИКО-ЭКОНОМИЧЕСКИЕ ИССЛЕДОВАНИЯ
Общие требования
Clinical and economic analysis. General requirements
ОКС 11.160
ОКП 94 4000
Дата введения 2018-06-01
Предисловие
1 РАЗРАБОТАН Межрегиональной общественной организацией "Общество фармакоэкономических исследований"
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 466 "Медицинские технологии"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 6 июля 2017 г. N 655-ст
4 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в статье 26 Федерального закона от 29 июня 2015 г. N 162-ФЗ "О стандартизации в Российской Федерации". Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе "Национальные стандарты", а официальный текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru).
1 Область применения
Настоящий стандарт устанавливает общие положения по проведению и использованию результатов клинико-экономических исследований, а также формату представления их результатов. Соблюдение этих правил служит гарантией достоверности результатов клинико-экономических исследований.
Настоящий стандарт предназначен для применения в качестве основы для проведения клинико-экономических исследований исследователями в системе здравоохранения Российской Федерации.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р 52379 Надлежащая клиническая практика
ГОСТ Р 56044 Оценка медицинских технологий. Общие положения
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если заменен ссылочный стандарт, на который дана недатированная ссылка, то рекомендуется использовать действующую версию этого стандарта с учетом всех внесенных в данную версию изменений. Если заменен ссылочный стандарт, на который дана датированная ссылка, то рекомендуется использовать версию этого стандарта с указанным выше годом утверждения (принятия). Если после утверждения настоящего стандарта в ссылочный стандарт, на который дана датированная ссылка, внесено изменение, затрагивающее положение, на которое дана ссылка, то это положение рекомендуется применять без учета данного изменения. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, рекомендуется применять в части, не затрагивающей эту ссылку.
3 Общие положения
Настоящий стандарт разработан для решения следующих задач:
- унификации подходов к проведению и использованию результатов клинико-экономических исследований;
- обоснования выбора лекарственных средств и медицинских технологий при разработке нормативных документов, обеспечивающих их рациональное применение;
- формирования взаимосвязанных клинических и экономических требований к эффективности, безопасности, совместимости и взаимозаменяемости медицинских технологий и критериев их оценки;
- экономического обоснования актуализации нормативных документов системы стандартизации в здравоохранении, регулирующих доступность и качество медицинской помощи в субъектах Российской Федерации, учреждениях здравоохранения, медицинских организациях.
Клинико-экономическое исследование представляет собой изучение в клинической практике методов диагностики, профилактики, лекарственного и нелекарственного лечения, реабилитации, выполняемое с целью оценки соотношения результатов и связанных с ними затрат.
Клинико-экономический анализ - методология оценки медицинских технологий: методов профилактики, диагностики, лекарственного и нелекарственного лечения на основе комплексного взаимосвязанного учета результатов применения медицинской технологии и связанных с этим затрат, в том числе - для сравнения двух и более медицинских технологий. Методология клинико-экономического анализа применима к любым технологиям здравоохранения - лекарственным (в узком понимании слова - фармакоэкономика) и нелекарственным способам лечения, методам диагностики, профилактики и реабилитации, и в равной мере - к административным медицинским технологиям, оказывающим влияние на здоровье.
4 Характеристика требований к проведению и использованию результатов клинико-экономических исследований, а также формату представления их результатов
4.1 Получение информации для клинико-экономических исследований
Целью клинико-экономического исследования является получение информации об эффективности и безопасности медицинских технологий с учетом затрат на их использование.
Получение информации для клинико-экономических исследований возможно с помощью:
а) анализа данных опубликованных клинических исследований и данных о затратах;
б) клинико-экономического компонента в рамках клинических исследований новых лекарственных средств или нелекарственных медицинских технологий одновременно с изучением их эффективности и безопасности, проводимых в рамках пред- или пострегистрационных клинических исследований;
в) самостоятельного клинико-экономического исследования в случае изучения экономических аспектов зарегистрированной или применяемой в практике технологии (если ее регистрация не предусмотрена действующими нормативно-правовыми актами):
- ретроспективного клинико-экономического наблюдения - изучение медицинской документации, связанной с применением изучаемой или альтернативной медицинской технологии, типичной практики применения медицинской технологии;
- проспективного клинико-экономического наблюдения - изучение эффективности, безопасности и затратности применения медицинской технологии без влияния на тактику ведения больного лечащим врачом или поведение больного со стороны исследователя (оценка реального мира, типичная практика);
- проспективного клинико-экономического исследования - проведение исследования эффективности, безопасности и затратности медицинской технологии с применением протокола исследования (например, рандомизации исследуемых групп или стандартизации применяемых доз или показаний для лекарственных средств);
г) клинико-экономического анализа с применением моделирования эффективности, безопасности и затрат (например, при использовании стандартов медицинской помощи или результатов опроса экспертов);
д) смешанных видов исследования.
4.2 Типы клинико-экономического анализа
Используются следующие основные типы клинико-экономического анализа:
- анализ "затраты на болезнь" (cost of illness, COI);
- анализ "затраты - эффективность" (cost-effectiveness analysis, СЕА);
- анализ "минимизация затрат" (cost-minimizaition* analysis, СМА);
- анализ "затраты - полезность (утилитарность)" (cost-utility analysis, CUA);
- анализ "затраты - выгода (польза)" (cost-benefit analysis, СВА).
Анализ "затраты на болезнь" - метод изучения всех затрат, связанных с ведением больных с определенным заболеванием, как на определенном этапе (отрезке времени), так и на всех этапах оказания медицинской помощи. При этом не предполагается сравнения эффективности медицинских технологий. Данный анализ допускается применять для изучения типичной практики ведения больных с конкретным заболеванием и следует использовать для достижения задач планирования затрат на определенную болезнь или программу, определения тарифов на медицинские услуги и т.п.
Анализ "затраты - эффективность" - сравнительная оценка результатов и затрат при двух и более медицинских технологиях, эффективность которых различна. Эффективность оценивают с позиции результатов, отражающих течение болезни (например, суррогатные точки - симптомы болезни, лабораторные показатели и т.д.; конечные точки - клинические необратимые состояния: мягкие (ампутация, хроническая недостаточность органа, инфаркт миокарда, инсульт) и твердые, связанные со смертью (продолжительность жизни, частота смертельных событий, обусловленных сердечно-сосудистыми заболеваниями). Обязательным требованием является использование одинаковых показателей результативности и затратности для всех анализируемых медицинских технологий.
Анализ "минимизация затрат" - вариант исследования "затраты - эффективность", при котором проводят сравнительную оценку медицинских технологий, характеризующихся идентичной эффективностью и безопасностью, но разными затратами. Рекомендуется применять анализ минимизации затрат при сравнительном исследовании разных форм или разных условий применения одного лекарственного средства или одной медицинской технологии. В некоторых случаях допустимо, при доказанных несущественных различиях в эффективности, применение данного вида анализа и при сравнении различных медицинских технологий.
Анализ "затраты - полезность (утилитарность)" - вариант исследования "затраты - эффективность", при котором результаты применения медицинской технологии оценивают в единицах "полезности" с точки зрения потребителя медицинской помощи (как правило - в показателях качества жизни); при этом часто используют показатель "сохраненные годы качественной жизни" (QALY). Обязательным требованием является использование одинаковых показателей результативности (например, метода оценки качества жизни) и затратности для всех анализируемых медицинских технологий.
Анализ "затраты - выгода (польза)" - вариант анализа "затраты - эффективность", при котором результаты (эффективность) представлены в денежном выражении, что позволяет сравнивать экономическую эффективность различных, в первую очередь, административных медицинских технологий (например, программу вакцинации против гриппа с организацией системы интенсивной неонатальной помощи для выхаживания детей, рожденных с низкой массой тела).
Анализ влияния на бюджет является частным случаем анализа затраты на болезнь. Анализ проводят с целью оценки экономических последствий повсеместного распространения в системе здравоохранения, региона, медицинской организации новой медицинской технологии - метода профилактики, диагностики, лечения или реабилитации. В ходе анализа влияния на бюджет оценивают прямые медицинские затраты, связанные как с применением новой медицинской технологии, так и с развитием нежелательных явлений при применении анализируемой технологии. Анализ влияния на бюджет выполняют с помощью построения моделей - древа решений, модели Маркова.
Моделирование - вид клинико-экономического исследования, основанный на использовании формализованных описаний изучаемого объекта (например, пациента, заболевания, эпидемиологической ситуации, затрат) или процессов (например, динамики состояния) при применении медицинских технологий. Основными видами моделирования, применяемых в клинико-экономических исследованиях, являются древо решений, Марковский анализ, моделирование затрат, влияние на бюджет, моделирование Монте-Карло.
Анализ чувствительности - анализ степени изменения результатов клинико-экономического исследования при изменении величины исходных параметров [например, изменения цен на лекарственные препараты (максимальные и минимальные цены), изменение показателей эффективности, частоты побочных эффектов и т.п.].
Дисконтирование - введение поправочного коэффициента при расчете затрат с учетом влияния временного фактора: затраты, которые предстоит понести в будущем менее значимы, чем понесенные сегодня, и, напротив, выгода, приобретенная сегодня, более ценна, чем предстоящая в будущем. Коэффициент ориентировочно определяют равным предстоящему уровню инфляции за анализируемый период или ставке кредитования.
Маржинальность - введение поправочного коэффициента при расчете затрат с учетом одновременного выполнения нескольких медицинских услуг или при моделировании затрат по стандартам медицинской помощи с учетом коморбидности заболевания (наличия одновременно нескольких заболеваний).
4.3 Общие требования к представлению результатов клинико-экономического анализа
Результаты анализа "затраты на болезнь" представляют в виде абсолютных значений затрат либо на всех этапах лечения болезни, либо на отдельных этапах (например, этап диагностики, амбулаторного лечения, стационарного лечения, реабилитации).
Результаты анализа "затраты - эффективность" и "затраты - полезность (утилитарность)" представляются в форме показателей соотношения затрат и достигнутого эффекта или коэффициента приращения затрат (дополнительные затраты, приходящиеся на достижение единицы дополнительного эффекта).
Результаты анализа "минимизация затрат" представляются в форме абсолютной разницы в затратах при применении исследуемой технологии по сравнению с альтернативной.
Результаты анализа "затраты - выгода (польза)" представляют в форме абсолютной разницы между затратами и выгодой в денежном выражении либо в форме коэффициента соотношения затрат и достигнутого эффекта в денежном выражении.
Рекомендуется при представлении отчета о клинико-экономическом исследовании указывать затраты на применение всех исследуемых технологий, источники их получения, величины тарифов на услуги, цен на лекарства и др. и формулы расчетов затрат.
4.4 Требования к структуре и методология клинико-экономического анализа
При составлении протокола клинико-экономического исследования необходимо учитывать, что клинико-экономический анализ состоит из следующих шести обязательных этапов:
а) оценка исследуемой медицинской технологии согласно ГОСТ Р 56044 с поиском доказательств эффективности и безопасности медицинской технологии;
б) разработка плана и программы исследования, выбор типа анализа включает:
- формулировку целей и задач анализа;
- выбор медицинской технологии сравнения;
- выбор критериев оценки эффективности и безопасности исследуемых медицинских технологий;
- разработку протокола клинико-экономического исследования;
- выбор типа клинико-экономического анализа;
в) собственно проведение исследования;
г) учет и оценка затрат;
д) экономические расчеты (клинико-экономический анализ);
е) исследование чувствительности;
ж) выводы и предложения с учетом слабых сторон анализа, ограничивающих применение его результатов.
4.4.1 Критерии оценки эффективности и безопасности медицинских технологий
Оценку медицинских технологий проводят согласно требованиям ГОСТ Р 56044.
Критерии эффективности медицинских технологий:
а) твердые точки - изменение показателей здоровья или качества жизни, обусловленного здоровьем (например, частота сердечно-сосудистых событий или сердечно-сосудистой смертности, ампутации конечностей, нарушения функции, смертность, выживаемость, продолжительность жизни, инвалидизация, число сохраненных лет без инвалидности (DALY), число сохраненных лет качественной жизни - QALY и др.).
б) суррогатные точки - опосредованные клинические эффекты (например, снижение частоты осложнений, сокращение числа повторных госпитализаций и др.), прямые клинические эффекты (например, сдвиг физикальных или биохимических параметров, исчезновение хрипов, снижение артериального давления, прирост гемоглобина, изменение симптомов заболевания).
Предпочтительным является оценка с использованием критериев группы а), однако при отсутствии данных допускается использование критериев б). Возможно использование критерия "число больных, которых необходимо пролечить для получения одной единицы эффекта" (показатель Number-Needed-to-Treat (NNT), например, сколько больных надо пролечить, чтобы избежать одного смертельного исхода).
4.4.2 Разработка плана и программы исследования, выбор типа анализа
1) Цели и задачи формулируются исследователем или спонсором исследования, при этом обязательно формулируется экономическая позиция исследования (чей экономический интерес будет приниматься во внимание при планировании и проведении исследования):
- интересы общества в целом (включая не только систему здравоохранения, но и социальные службы и другие задействованные сферы);
- экономические интересы системы здравоохранения на федеральном уровне (например, Федерального фонда обязательного медицинского страхования), субъекта Российской Федерации, муниципального звена здравоохранения;
- интересы провайдера медицинской помощи (медицинской организации, частнопрактикующего медицинского работника);
- интересы страховой медицинской организации;
- интересы отдельного пациента или его семьи и др.
2) Выбор медицинской технологии сравнения проводят:
- с технологией, чаще всего использующейся по аналогичным показаниям [с "типичной практикой" ведения больных с данным заболеванием; при этом для анализа типичной практики применяется исследование медицинских (амбулаторных и стационарных) карт пациентов, опрос экспертов - специалистов в исследуемой области медицины или опрос пациентов];
- с технологией, являющейся наиболее эффективной среди использующихся по аналогичным показаниям с учетом результатов и уровня доказательности, полученных в ходе оценки медицинской технологии;
- с наименее затратной технологией среди использующихся по аналогичным показаниям;
- с технологией, рекомендуемой стандартом, клиническими рекомендациями (протоколами лечения), иным нормативным документом;
- с отсутствием применения технологии (диагностики или лечения) в тех случаях, когда это допустимо в клинической практике.
Выбор технологии для сравнения зависит от позиции исследования, целей и задач исследования и должен быть обоснован исследователем как в протоколе, так и в отчете.
4.4.3 Выбор критериев оценки эффективности и безопасности исследуемых медицинских технологий
При выборе критериев оценки медицинской технологии используют результаты проведенной оценки технологии и степень (сила) полученных доказательств. Значимость оценок последовательно снижается в ряду типа проведенных предшествующих клинических исследований:
- доказательства, полученные при проведении метаанализа и систематического обзора;
- доказательства, полученные в проспективных рандомизированных исследованиях;
- доказательства, полученные в больших проспективных сравнительных не рандомизированных исследованиях;
- доказательства, полученные в ретроспективных сравнительных исследованиях;
- доказательства, полученные в не сравнительных исследованиях или исследованиях на ограниченном числе больных;
- доказательства, полученные на отдельных больных;
- формализованное мнение экспертов (например, полученное дельфийским методом, в ходе формализованного опроса экспертов или интервью).
При выборе критериев для клинико-экономического исследования базироваться на ниже стоящих в ряду доказательствах можно только при отсутствии вышестоящих в иерархии доказательств.
Рекомендуется сопоставить результаты разных исследований и выбрать наилучшие для выбора критериев эффективности. Одновременно возможно, что использование критериев, полученных в качественных клинических исследованиях, невозможно в рамках предполагаемого клинико-экономического исследования, что должно быть четко указано и обосновано исследователем при составлении программы, протокола исследования и в отчете.
4.4.4 Разработка протокола клинико-экономического исследования
Протокол исследования должен содержать результаты оценки медицинской технологии, цели и задачи, описание и обоснование дизайна исследования, его плана, и, при необходимости, клинико-экономической карты, формы информированного согласия пациента, опросника экспертов, источники учета затрат, обоснование выбора клинико-экономического анализа и др.
4.4.5 Учет и оценка затрат
Следует максимально полно учесть все прямые медицинские затраты на медицинскую технологию согласно видам затрат.
Затраты делятся:
1 на прямые - издержки, понесенные системой здравоохранения, пациентом, иным плательщиком, непосредственно связанные с оказанием медицинских услуг. Прямые затраты могут быть:
а) медицинские - издержки, понесенные системой здравоохранения, связанные непосредственно с оказанием медицинской помощи. Они разделяются:
1) на переменные - зависят от количества оказанных медицинских услуг. Это затраты:
- на диагностические, лечебные, реабилитационные и профилактические медицинские услуги, манипуляции и процедуры, в том числе оказываемые на дому (включая оплату рабочего времени медицинских работников, непосредственно оказывающих медицинскую помощь);
- транспортировку больного санитарным транспортом (скорая помощь) или выезд бригад неотложной помощи;
- лекарственные препараты;
- кровь и ее компоненты;
- диетическое питание (если это планируется);
- имплантируемые человеку приборы и приспособления;
- выполнение отдельных услуг, выполняемых сторонними исполнителями (аутсорсинг);
2) постоянные - их величина не зависит от количества оказанных медицинских услуг. Это затраты:
- на содержание пациента в лечебном учреждении ("гостиничные услуги");
- оплату покупки дорогостоящего медицинского оборудования;
- оплату за использование медицинского оборудования, площадей и средств (амортизация);
- оплату коммунальных услуг;
- оплату работы административно-хозяйственного аппарата;
- оплату за ремонт зданий, сооружений и техники;
- оплату обучения персонала
- и др.;
б) немедицинские - расходы, которые несут другие общественные службы и организации, а также пациенты и их семьи:
- наличные ("карманные") расходы пациентов, не связанные с оплатой лекарственных средств или медицинских услуг (например, оплата сервисных услуг в медицинской организации);
- затраты на немедицинские услуги, оказываемые пациентам на дому (например, услуги социальных служб);
- затраты на перемещение пациентов не санитарным транспортом (личным, общественным) и т.п.;
- затраты членов семьи, связанные с оказанием помощи пациенту;
2 непрямые или косвенные (альтернативные) затраты (издержки упущенных возможностей):
- фрикционные затраты - связанные с непроизведенным национальным продуктом за период болезни (или утраты трудоспособности) пациента, пока его функции не компенсированы новым сотрудником, в том числе затраты на обучение нового сотрудника;
- затраты на оплату листков нетрудоспособности, пособия по инвалидности и иные социальные выплаты, предусмотренные действующим законодательством из-за болезни или выхода на инвалидность;
- затраты, связанные с отсутствием на работе членов его семьи или друзей, непосредственно связанные с его болезнью;
- экономические потери от преждевременного наступления смерти;
3 нематериальные (неосязаемые) затраты - затраты, связанные с болью, страданиями, дискомфортом, которые испытывает пациент вследствие проходимого им курса лечения, - из-за трудностей с точным количественным измерением в денежном выражении на сегодняшний день обычно остаются за рамками выполняемого анализа.
В большинстве случаев клинико-экономического исследования используется анализ медицинских затрат. При оценке влияния медицинской технологии на бюджет используют и другие виды затрат.
Учет затрат следует проводить за фиксированный период времени (например, за период госпитализации или за месяц, или за год болезни). Необходимо принимать во внимание, что в тех случаях, когда эффект применения медицинской технологии растягивается во времени, период учета затрат может в несколько раз превышать продолжительность непосредственного лечения. Выбор временного периода (временного горизонта) для анализа затрат обосновывается в протоколе исследования и отчете.
Оценка структуры затрат на лекарства и услуги имеют самостоятельную ценность. Используются следующие варианты оценки структуры затрат:
- ABC анализ: группа A - 80% затрат, группа B - 15%, группа C - 5%;
- VEN анализ: V - важные, обычно - входящие в нормативные документы, например, перечень основных лекарственных средств, стандарты медицинской помощи, клинические рекомендации (протоколы лечения), E - необходимые, обычно симптоматические технологии и N - второстепенные для изучаемой патологии, например, лекарственные средства, не имеющие доказательств эффективности;
- частотный анализ - частота применения медицинских технологий в группе больных или в медицинской организации.
Следует проводить комплексную оценку структуры затрат на медицинские технологии, в процессе которого медицинские технологии ранжируются по группам A, B и C, каждой из них присваивается индекс по системе VEN, показатель частоты применения;
- DDD-анализ лекарственных средств (defined daily dose) - число больных, которые могут получить лечение определенным лекарственным средством за определенный период с учетом установленных Всемирной организацией здравоохранения дневных доз лекарственного средства. DDD-анализ имеет самостоятельное значение и используется для прогнозирования затрат на определенные лекарственные средства.
4.4.6 Источники информации о денежном выражении прямых затрат
При определении размера прямых затрат на медицинские услуги в денежном выражении используют:
- тарифы на медицинские услуги (например, действующие в регионе в рамках системы обязательного медицинского страхования или усредненные тарифы в платных медицинских организациях, в последнем случае представляется выборка трех-пяти организаций с обоснованием их выбора);
- результаты собственных экономических расчетов расценок на медицинские услуги (с описанием методики расчета, например, с учетом среднемесячной зарплаты персонала и числа процедур, которые может выполнить один человек за месяц с учетом условных единиц трудозатрат (УЕТ) на каждую процедуру (1 УЕТ принимается за величину в 10 мин).
При определении размера прямых затрат на лекарственные средства в денежном выражении используют:
- розничные цены на лекарственные средства в аптечной сети (при анализе расходов на амбулаторное лечение, а также в случаях, когда лекарственные средства приобретаются непосредственно пациентом);
- оптовые цены фирм-дистрибьюторов при анализе расходов на лечение в стационаре (не менее трех-пяти дистрибьюторов с обоснованием выбора);
- данные с сайтов закупок, в которых указаны цены на лекарства в лотах.
Не рекомендуется использование цен, зарегистрированных в нормативных документах, так как эти цены могут существенно отличаться от реальных цен продаж.
Предпочтительно использовать усредненные показатели цен.
Источники информации о ценах на лекарственные средства и медицинские услуги должны быть представлены в отчете.
Величина иных затрат анализируется по доступным источникам, в первую очередь - в сети Интернет. Для учета постоянных медицинских затрат возможно использование поправочных коэффициентов, отражающих долю прямых затрат в общих затратах медицинской организации (например, переменные затраты на оказание услуг в рамках обязательного медицинского страхования, по данным экспертной оценки, составляют 30% от общих затрат и компенсируются из бюджета, следовательно, тариф по медицинскому страхованию следует умножить на три для получения истинной величины затрат на услугу).
4.4.7 Расчет затрат
Расчет затрат (определение размера расходов) в процессе экономического анализа включает в свой состав четыре этапа:
1) идентификация и описание использованных ресурсов (например, перечень методов диагностики и лечения, лекарственных средств, показатель койко-дней в отделении определенного профиля и др.);
2) количественная оценка указанных ресурсов в физических единицах (например, число каждой услуги за определенный промежуток времени, число посещений врачом больного, число консультаций специалистов, инструментальных и лабораторных услуг, операций, процедур сестринского ухода, определение времени (в койко-днях) в отделении определенного профиля и т.д.);
3) оценка каждого из использованных ресурсов в денежном выражении (например, затраты на один день содержания койки, тариф на медицинскую услугу, цена лекарственного средства);
4) внесение поправок и коэффициентов:
- на неопределенность и время (дисконтирование). Рекомендуемый уровень дисконтирования без учета инфляции - 5% в год;
- инфляцию (определяется по официальным документам, устанавливающим уровень инфляции за предшествующий исследованию год, возможно введение иного - прогнозируемого - коэффициента инфляции);
- маржинальность (одновременное выполнение нескольких медицинских услуг снижает затраты на каждую из них, следует сложить затраты на каждую услугу и сумму затрат перемножить на коэффициент); значения коэффициента маржинальности, установленного эмпирически, представлены в таблице 1.
Таблица 1 - Значение коэффициента маржинальности
Количество услуг | Значение коэффициента маржинальности |
2 | 1,5 |
3 | 1,2 |
4 | 1,0 |
5 | 0,8 |
6 | 0,6 |
7 | 0,5 |
8 | 0,42 |
9 | 0,38 |
10 | 0,34 |
11 | 0,3 |
12 | 0,26 |
13 | 0,22 |
14 | 0,18 |
15 | 0,16 |
16 | 0,14 |
17 | 0,12 |
18 | 0,1 |
19 | 0,08 |
20 | 0,06 |
21 | 0,04 |
22 | 0,02 |
Более 22 | 0,01 |
Использование коэффициента маржинальности возможно при оценке затрат методом моделирования на основе стандартов медицинской помощи при наличии высокой степени коморбидности заболевания (например, у пожилых нередко сочетание болезней с коронарной патологией, артериальной гипертонией, сахарным диабетом, все эти болезни могут обостряться одновременно и, соответственно, требовать дополнительных издержек). Полный перечень видов затрат, учтенных при проведении исследования, приводится в отчете наряду с указанием источников информации о ценах. Рекомендуется также приводить в приложении цены на услуги и лекарственные средства, использованные исследователями при проведении анализа с их ABC-, VEN- и частотным анализами.
Рекомендуемая методика расчета затрат на простые медицинские услуги представлена в приложении A.
4.4.8 Выбор типа клинико-экономического анализа
Выбор типа клинико-экономического анализа зависит:
- от цели исследования;
- экономической позиции исследования, заказчика, для которого выполняется данное исследование;
- временного горизонта;
- исследуемой медицинской технологии;
- вида оцениваемой эффективности ее применения.
Выбор типа клинико-экономического анализа должен быть обоснован исследователем при формировании программы исследования и в отчете.
4.4.9 Требования к проведению клинико-экономического исследования
Все клинико-экономические исследования должны проводиться специалистами, имеющими образование, профессиональную подготовку и квалификацию, позволяющие им принять ответственность за надлежащее проведение исследования. Рекомендуется дополнительное (по необходимости) привлечение к проведению исследования врачей, медицинских сестер, экономистов, программистов, специалистов по обработке данных, пациентов.
4.4.9.1 Руководитель исследования, персонал
Исследование возглавляет руководитель - специалист в области клинической медицины, имеющий опыт в области клинической фармакологии и клинической эпидемиологии, знающий требования настоящего стандарта.
Руководитель привлекает в клинико-экономическое исследование достаточное число квалифицированных сотрудников (персонал исследования), имеющих профессиональное образование или опыт, соответствующие поставленным задачам.
Персонал проводит исследование в помещениях, обеспечивающих его проведение в течение всего срока надлежащим и безопасным для испытуемых образом и с соблюдением действующего законодательства.
Персонал, принимающий участие в проведении исследования, знакомится с протоколом, информацией об исследуемой медицинской технологии, а также со своими функциями и обязанностями в исследовании.
4.4.9.2 Информация, полученная в ходе исследования
Сбор, обработка и хранение информации, полученной в ходе исследования, должны обеспечивать точное и правильное представление, объяснение и подтверждение данных и проводиться в соответствии с требованиями настоящего стандарта и законодательства о защите персональных данных.
4.4.9.3 Декларация конфликта интересов
Руководитель исследования и ответственные исполнители, привлекаемые к работе группы эксперты должны избегать конфликта интересов - наличия интересов, противоречащих общественным интересам, которые могут привести к заключениям, не отвечающим интересам пациентов, групп пациентов, системы здравоохранения, общества в целом.
Профессиональная активность руководителя исследования и ответственного исполнителя, привлекаемых к работе группы экспертов (далее - члены рабочей группы), связанная с его сотрудничеством с государственными структурами, частными и общественными организациями, сопряженная с возможностью возникновения конфликта интересов, не должна влиять на объективность заключений об эффективности, безопасности, экономической целесообразности (приемлемости) медицинской технологии.
В целях предотвращения (ограничения) возникновения конфликта интересов, связанного с профессиональной, государственной, коммерческой, общественной и иной деятельностью членов рабочей группы, а также с родственными, дружескими связями членов рабочей группы по клинико-экономическому анализу заранее в письменной форме объявляют об имеющемся у них потенциальном конфликте интересов.
Информация о потенциальном конфликте интересов или отсутствии конфликта интересов членов рабочей группы по клинико-экономическом анализу публикуется вместе с планом (протоколом) клинико-экономической оценки медицинских технологий и отчетом.
Руководитель исследования при возникновении потенциально существенных для деятельности группы в целом или при рассмотрении отдельных вопросов конфликтов интересов предпринимает меры к предотвращению их влияния на заключения рабочей группы. Лица с существенным конфликтом интересов (представители или сотрудники производителя лекарственного средства или изделия медицинского назначения), а также иные лица, или их близкие связанные с производителем лекарственного средства или изделием медицинского назначения или иным заинтересованным лицом владением долями собственности (акций) или получением систематического дохода или значительного дохода (суммы более четверти годового дохода эксперта), могут участвовать в анализе исходных данных для клинико-экономического исследования, но не могут принимать участия в формировании выводов и решений.
4.4.10 Кпинико-экономическое исследование, совмещенное с клиническим исследованием
Клинико-экономическое исследование, совмещенное с клиническим исследованием, следует осуществлять в соответствии с основополагающими этическими принципами Хельсинкской декларации, нормами и правилами качественной клинической практики согласно ГОСТ Р 52379, настоящему стандарту и иным действующим в этой области нормативным документам.
Данные о планируемом проведении клинико-экономического исследования одновременно с клиническим исследованием должны быть включены в протокол исследования и представлены на рассмотрение независимому Комитету по этике вместе с формой информированного согласия и другими документами, предусмотренными действующей нормативно-правовой документацией.
Данные, сбор и регистрацию которых проводят в целях клинико-экономического исследования, допускается вносить как в основную расширенную карту испытуемого, так и в отдельную карту, разработанную специально с учетом целей и задач данного исследования. Форму расширенной или дополнительной карты испытуемого согласуют в соответствии с требованиями действующей нормативно-правовой базы.
4.4.10.1 Участие испытуемого в исследовании
Испытуемый - участник клинико-экономического исследования, к которому применяют исследуемую или альтернативную медицинскую технологию, может быть включен в исследование только на основании добровольного информированного согласия, полученного после детального ознакомления с материалами исследования. Данные о проведении клинико-экономического исследования одновременно с клиническими исследованиями включают в форму информированного согласия. При получении и документальном оформлении информированного согласия исследователь должен соблюдать действующие нормативные требования, придерживаться основополагающих этических принципов Хельсинкской Декларации, сохранять анонимность испытуемого.
4.4.10.2 Результаты клинико-экономического исследования
Результаты клинико-экономического исследования, проходящего одновременно с клиническими исследованиями, следует представлять в виде отдельного отчета одновременно с отчетом по результатам клинических исследований, включая подробное описание методологии исследования (в том числе наличие или отсутствие рандомизации, плацебо контроля и ослепления, критерии включения и не включения пациентов в исследование, число единиц наблюдения по группам и характеристики групп), оценку эффективности исследуемой медицинской технологии, данные о частоте зарегистрированных побочных эффектов, число и причины исключения пациентов из исследования в процессе его выполнения, данные о нарушениях протокола, причинах прекращения или приостановки исследования. Рекомендуемая форма отчета о результатах клинико-экономического исследования представлена в приложении Б.
4.4.11 Клинико-экономическое наблюдение (ретроспективное или проспективное)
Клинико-экономическое наблюдение (ретроспективное или проспективное) не подразумевает дополнительного активного вмешательства в процессы оказания помощи пациентам. Назначение диагностики и лечения проводится лечащим врачом независимо от исследователей; информация собирается путем выкопировки данных из медицинской документации или опроса (анкетирования, интервьюирования) пациентов, родственников пациентов, медицинских работников, иных субъектов в зависимости от поставленных задач. Отказ от участия пациента в исследовании не может влиять на процесс оказания медицинской помощи пациенту.
С целью гарантии прав лиц, информация о которых будет подвергаться анализу, протокол исследования до его начала должен быть одобрен Комитетом по этике медицинской организации, на базе которой будет проходить исследование. При проведении клинико-экономических наблюдений в нескольких медицинских организациях одновременно, протокол исследования одобряется Комитетом по этике каждой медицинской организации.
Доступ к медицинской документации предоставляется лицам с медицинским образованием с соблюдением положений законодательства о врачебной тайне. Протокол исследования должен гарантировать, что вся информация, полученная из медицинской документации, не подлежит разглашению, распространению или передаче посторонним лицам. Посторонними в данном случае считаются лица, не имеющие непосредственного отношения к оказанию медицинской помощи пациенту. Ответственность за соблюдение протокола лежит на руководителе исследования.
Для анализа и отчетности предоставляется обезличенная информация (без указания персональных данных включенного в исследование). Исследователь не обязан оповещать пациентов и получать их согласие на выкопировку данных, касающихся состояния их здоровья, из имеющейся медицинской документации (медицинской карты больного).
4.4.11.1 Получение информации методом опроса
При проведении опроса (анкетирования, интервьюирования пациентов, членов их семей, экспертов, иных лиц) участник вправе отказаться от участия в исследовании на любом из этапов. Информацию о числе лиц, отказавшихся от участия в ходе исследования, приводят в отчете без их идентификации.
Исследователь должен ознакомить анкетируемых с целями и задачами исследования, представив им информацию в доступной форме, по возможности избегая специальных терминов. Протокол исследования должен гарантировать, что информация о персональных данных, полученная при опросе, не подлежит разглашению, распространению или передаче посторонним лицам. Для анализа и отчетности предоставляется обезличенная информация (без указания имени, включенного в исследование).
4.4.12 Проспективное клинико-экономическое исследование
Клинико-экономическое исследование подразумевает активное вмешательство исследователя в лечебно-диагностический процесс (внесение изменений и дополнений в обычную традиционную схему лечения, в том числе соответствующую клиническую рекомендацию (протокол лечения). Под это определение подходят все исследования, в программу которых входит планирование применения медицинской технологии исследователем.
При проведении клинико-экономического исследования лечение проводят строго в соответствии с протоколом исследования. Отклонение от протокола, обусловленное состоянием здоровья и интересами пациента, влечет за собой исключение из исследования.
Клинико-экономическое исследование должно соответствовать основополагающим этическим принципам Хельсинкской декларации и действующим нормативным актам Российской Федерации, регулирующим проведение экспериментов с участием человека в роли испытуемого.
Клинико-экономическое исследование допускается проводить с использованием медицинских технологий, зарегистрированных в Российской Федерации в установленном порядке и по зарегистрированным показаниям, если это предусмотрено действующим законодательством (например, для лекарственных средств). В случае проведения клинико-экономического исследования с использованием медицинских технологий, не зарегистрированных в Российской Федерации при наличии законодательного требования, или по незарегистрированным показаниям, исследование рассматривается как клиническое дорегистрационное исследование и должно проводиться в соответствии с требованиями действующего законодательства в данной области.
При проведении клинико-экономического исследования необходимо для защиты прав и обеспечения безопасности испытуемых, участвующих в исследовании, и обеспечения профессиональных интересов и защиты прав исследователей необходимо:
- одобрение Комитета по этике;
- информированное согласие пациентов, участвующих в исследовании.
На рассмотрение Комитета по этике представляются документы в соответствии со стандартными операционными процедурами (СОПами).
Процедура получения рецензии Комитета по этике определяется утвержденными правилами, СОПами или уставом (положением) о Комитете по этике. Руководитель исследования должен выяснить все подробности процедуры рецензирования Комитета по этике и несет ответственность за взаимодействие с Комитетом по этике и за предоставление ему информации об исследовании, а также за получение документального подтверждения соответствующего одобрения.
Критерии включения пациентов в исследование и не включения в исследование должны быть определены таким образом, чтобы риск возможного вреда был сведен к минимуму.
В течение и после окончания участия испытуемого в исследовании исследователь или медицинская организация должны обеспечить оказание испытуемому необходимой медицинской помощи в случае любых проявившихся в ходе исследования негативных проявлений, включая клинически значимые изменения лабораторных показателей.
Вся информация, полученная в ходе исследования, не подлежит разглашению, распространению или передаче посторонним лицам (непосредственно не связанным с оказанием медицинской помощи пациентам). Для исследования и отчетности предоставляется обезличенная информация (без указания имени испытуемого).
4.4.12.1 Информированное добровольное согласие
Информированное добровольное согласие представляет собой документально оформленное согласие испытуемого на участие в клинико-экономическом исследовании после ознакомления со всеми его особенностями.
Проспективное клинико-экономическое исследование допускается проводить только с письменного информированного добровольного согласия пациента или его законных представителей.
При получении и документальном оформлении информированного добровольного согласия исследователь должен соблюдать действующие нормативные требования и основополагающие этические принципы Хельсинкской декларации.
Информация для потенциального участника исследования состоит из двух составляющих:
- информации о планируемом исследовании (включая сведения об исследуемой медицинской технологии с указанием возможных рисков ее применения);
- информации о правах пациента.
Основную информацию потенциальный участник получает на этапе включения в исследование. Эта информация представляется в виде документа из двух частей: собственно информационной и формы информированного согласия, которую должен подписать доброволец - потенциальный участник исследования.
Независимые комитеты по этике должны оценить соответствие этого документа существующим требованиям.
В ходе исследования участник должен в обязательном порядке получать информацию, касающуюся дополнений в протокол исследования, его изменений, вновь полученных данных о действии медицинской технологии в той мере, в которой эта информация может повлиять на решение пациента продолжать свое участие в исследовании. Способствовать текущему информированию участника, одобрять новые версии информированного согласия или дополнения к нему входит в функции Комитета по этике.
К информированию участника исследования предъявляют следующие требования:
1) потенциальному участнику исследования должна предоставляться письменная информация и форма информированного согласия только после одобрения этих документов Комитетом по этике;
2) потенциальный участник или его законные представители должны иметь достаточно времени для обдумывания и принятия решения;
3) информация, предоставляемая участнику, должна быть достоверной и актуальной; в ней следует избегать непонятных участнику научных терминов, либо эти термины должны быть объяснены;
4) при появлении новой информации об исследуемой медицинской технологии, ходе исследования и др. ее также следует доводить до сведения испытуемого в письменном виде (в виде новой дополненной версии информированного согласия или дополнения к нему) после одобрения Комитетом по этике;
5) врач-исследователь или его коллеги не должны оказывать давления на потенциального участника исследования с целью добиться его согласия; врач-исследователь должен предоставить участнику исследования на любом его этапе всю информацию по запросам участника;
6) информация для участника исследования и информированное добровольное согласие должны составлять единый документ, желательно с единой нумерацией страниц с указанием на каждой странице ее текущего номера и общего их числа (1 из 5; 2 из 5 и т.д.); испытуемый должен расписаться в получении одного экземпляра этого документа, подписанного врачом-исследователем.
Информационный документ, предоставляемый потенциальному участнику исследования, должен содержать следующие сведения:
- название исследования (номер протокола);
- компания-спонсор (если она есть);
- цели и задачи исследования, обоснование его необходимости;
- вид исследования, его продолжительность для каждого участника (желательно указать, сколько человек участвует в исследовании); вероятность попадания участника в одну из групп;
- характеристика исследуемой медицинской технологии и технологий для сравнения;
- процедуры исследования, включая инвазивные методы;
- возможная польза для участника, риск и неудобства; если исследование не имеет терапевтических целей, необходимо сообщить об этом участнику;
- действия участника в случае непредвиденных воздействий на состояние здоровья - к кому он должен обратиться и в какие сроки;
- альтернативные методы лечения;
- расходы участника, если таковые ожидаются в связи с его участием в исследовании; порядок и размер выплат по компенсации расходов, если таковая предусмотрена;
- обязанности участника исследования;
- компенсация, на которую участник может рассчитывать в случае нанесения вреда его здоровью в ходе исследования, если таковая предусмотрена;
- информация об анонимности участия в исследовании и о возможности и пределах раскрытия информации об участнике определенным лицам (аудиторам, мониторам и т.д.);
- обязательства врача-исследователя довести до участника новые сведения об исследовании, которые могут повлиять на желание участника продолжить исследование;
- сведения об одобрении протокола исследования Комитетом по этике;
- куда может обратиться участник для получения дополнительной информации;
- возможные обстоятельства или причины, по которым участие в исследовании может быть прекращено.
Информация для участника исследования должна обладать следующими свойствами:
- быть полной, правдивой (объективной) и достоверной;
- быть актуальной, что достигается за счет текущего оперативного информирования;
- быть доступной, т.е. понятной для читателя-неспециалиста;
- текст должен быть составлен грамотно, перевод - хорошо отредактирован и адаптирован;
- информацию следует подавать с деликатностью и чувством такта.
Качество содержания документа контролирует Комитет по этике.
Таким образом, информированное добровольное согласие пациента - участника исследования имеет следующее значение:
- доказывает факт информирования и подтверждает факт согласия пациента;
- формализует содержание сообщенной пациенту информации;
- формализует согласие между исследователем и пациентом-участником;
- позволяет осознать риск нанесения ущерба здоровью пациента и риск профессиональной ответственности со стороны врача-исследователя и минимизировать зависящие от врача и пациента обстоятельства, способствующие нежелательным событиям;
- служит защите прав испытуемых и защищает врача от необоснованных претензий.
Если испытуемый способен, он подписывает и датирует форму письменного согласия собственноручно. Когда в исследовании участвуют испытуемые, которые могут быть включены только на основании согласия их законных представителей (например, несовершеннолетние, пациенты с выраженным слабоумием, находящиеся в бессознательном состоянии), то за них подписывает добровольное информированное согласие законный представитель пациента.
Если испытуемый нуждается в неотложной помощи и у него невозможно получить согласие до включения в исследование, оно должно быть получено у его близких, если последний при этом присутствует.
Испытуемый или его законные представители должны быть поставлены в известность об исследовании в кратчайшие сроки, и у них должно быть получено согласие на продолжение клинико-экономического исследования в соответствии с представленными выше положениями.
4.4.13 Клинико-экономическое моделирование
Моделирование проводят при невозможности получить реальные данные, необходимые для проведения клинико-экономических расчетов в исследовании или наблюдении.
Моделирование допускается использовать:
- в случае, когда в клинических исследованиях не изучались опосредованные и отдаленные результаты лечения - результаты клинических исследований дополняются данными из других источников (нерандомизированные исследования, исследования-наблюдения, экспертное мнение и др.);
- при использовании результатов исследований, проведенных в других странах, для принятия клинических и управленческих решений в России;
- при необходимости сделать заключение о целесообразности применения лекарственных средств, схем и методов лечения у групп пациентов, не включавшихся ранее в исследования (например, пациенты с осложненным течением заболевания, тогда как в клинических исследования отбирались пациенты с неосложненным течением);
- при необходимости учесть различия в потреблении ресурсов в исследовании и на практике.
Наиболее часто используют следующие виды моделирования:
- построение древа решений;
- модель Маркова.
При использовании других видов моделирования в отчете должно представляться подробное описание методики и способов математической обработки данных.
При представлении результатов клинико-экономических расчетов, основанных на моделировании, исследователи должны обосновать необходимость выбора этого типа анализа, сформулировать все условия построения модели (допуски, гипотезы), описать и обосновать выбор литературных источников, данные которых были положены в основу анализа.
Результаты экономического анализа, основанного на моделировании, рассматривают как предварительные, однако их допускается использовать для обоснования экономической целесообразности применения лекарственных средств, схем и методов лечения при отсутствии исследований или наблюдений.
4.5 Интерпретация результатов клинико-экономических исследований
Клинико-экономические обоснования целесообразности применения медицинских технологий следует принимать во внимание при разработке:
- клинических рекомендаций (протоколов лечения);
- стандартов медицинской помощи;
- перечня жизненно необходимых и важнейших лекарственных средств;
- формулярных перечней и списков;
- других нормативных документов, регламентирующих качество и объемы медицинской помощи населению.
Оценку достоверности и практической значимости результатов клинико-экономических исследований проводят эксперты, участвующие в разработке соответствующих нормативных документов.
При оценке результатов клинико-экономического анализа следует обращать внимание на следующие позиции:
- ясное определение цели и задач исследования;
- формулировка экономической позиции исследования - ее соответствие целям лиц, принимающих решение о целесообразности использования исследуемого вмешательства;
- обоснование выбора медицинской технологии для сравнения с исследуемой технологией; соответствие выбранной альтернативы для сравнения целям лиц, принимающих решение о целесообразности использования исследуемой технологии;
- однозначность выбранных критериев эффективности и безопасности и их оценки (клиническая и социальная значимость критерия, уровень научной обоснованности данных о наличии и размере эффекта);
- наличие необходимых сведений о методологии учета затрат (перечень учтенных ресурсов, анализ затрат, источники информации о ценах);
- обоснованность выбранного типа клинико-экономического анализа;
- использование дополнительных методов анализа - моделирование, дисконтирование, маржинальность, анализ чувствительности, - повышающих достоверность и практическую значимость результатов исследования;
- степень соответствия выводов использованной методологии.
Минимальный перечень вопросов, на которые должны быть даны положительные ответы при критическом анализе результатов клинико-экономических исследований, представлен в приложении В.
Приложение А
(рекомендуемое)
Расчет затрат на простые медицинские услуги
А.1 Общие затраты на простую медицинскую услугу
В основе расчета затрат на простую медицинскую услугу ![]() лежит учет затрат времени на осуществление данной услуги с приведением затрат к единице времени:
лежит учет затрат времени на осуществление данной услуги с приведением затрат к единице времени:
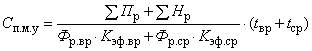 , (А.1)
, (А.1)
где - сумма прямых расходов организации здравоохранения за анализируемый период времени;
![]() - сумма накладных расходов организации здравоохранения за тот же период времени;
- сумма накладных расходов организации здравоохранения за тот же период времени;
- фонд рабочего времени врачей в условных единицах трудоемкости (трудозатрат);
- фонд рабочего времени среднего медицинского и вспомогательного персонала в условных единицах трудоемкости (трудозатрат);
![]() ,
, - нормативный коэффициент использования рабочего времени медицинского персонала (соответственно врача и среднего медицинского персонала), установленный настоящей методикой;
- время, затрачиваемое врачами на оказание услуги;
- время, затрачиваемое средним медицинским и вспомогательным персоналом на оказание услуги.
А.2 Прямые затраты на простую медицинскую услугу
Для определения расходов на оплату труда всего основного персонала организации здравоохранения за анализируемый период раздельно рассчитывают основную заработную плату, т.е. величину заработной платы, установленной в соответствии со штатными должностями организации здравоохранения, начисленную согласно всем основаниям, и дополнительную заработную плату, т.е. суммы выплат компенсационного характера. В дополнительную заработную плату включают затраты на выплаты:
- за работу в ночное время;
- за работу в праздничные и выходные дни;
- оплата очередных ежегодных и дополнительных отпусков (компенсаций за неиспользованный отпуск);
- оплата льготных часов работы подростков;
- доплата за работу с интернами;
- оплата времени прохождения обязательных медицинских осмотров;
- компенсация женщинам, находящимся в частично оплачиваемом отпуске по уходу за ребенком;
- оплата времени выполнения государственных обязанностей;
- выходные пособия;
- оплата приглашенных специалистов (консультантов);
- оплата отпусков молодым специалистам перед началом работы;
- оплата времени учебы с отрывом от производства в системе повышения квалификации и переподготовки кадров.
В расчетах не учитывают:
- премии и материальную помощь работникам;
- оплату дополнительно предоставляемых (сверх предусмотренных законодательством) отпусков работникам.
Основную заработную плату основного (медицинского) персонала рассчитывают по формуле
![]() , (А.2)
, (А.2)
где ![]() - основная заработная плата врачей;
- основная заработная плата врачей;
![]() - основная заработная плата среднего медицинского и вспомогательного персонала.
- основная заработная плата среднего медицинского и вспомогательного персонала.
Коэффициент дополнительной заработной платы рассчитывают по формуле
![]() , (А.3)
, (А.3)
где - дополнительная заработная плата;
- основная заработная плата.
Расходы на заработную плату основного персонала с учетом дополнительной заработной платы рассчитывают по формуле
![]() , (А.4)
, (А.4)
где - основная заработная плата;
- коэффициент дополнительной заработной платы.
Начисления на фонд заработной платы устанавливаются законодательством Российской Федерации в процентах от фонда заработной платы.
При расчете расходов на материальные ресурсы, полностью потребляемые в процессе оказания услуги: лекарственные средства, реактивы, перевязочные средства, одноразовые шприцы и инструментарий, сосудистые и иные протезы, шунты, вживляемые в организм больного приспособления, шовный материал, продукты питания и др., учитывают затраты на медикаменты, перевязочные средства, химические реактивы, одноразовые принадлежности, приобретение минеральных вод, сывороток, вакцин, витаминов и т.п., пленок для рентгеновских снимков. Объем и номенклатура материальных ресурсов должны обеспечивать качественное выполнение простой медицинской услуги и могут корректироваться путем внесения недостающих элементов в соответствии с требованиями стандарта технологии выполнения услуги. Учет расходов проводится согласно порядку, установленному в настоящей методике.
Расчет затрат на лекарственные средства и перевязочные материалы проводится на основании данных о фактических расходах по организации здравоохранения в целом и по его структурным подразделениям в соответствии с действующими нормативными документами.
Расчет потребляемой в процессе оказания услуги доли износа мягкого инвентаря проводят по нормативу его износа в соответствии с действующими нормативными документами в этой области и ценами на период расчета.
Расчет потребляемой в процессе осуществления услуги доли износа медицинского оборудования проводят путем расчета износа оборудования, числящегося в составе основных средств. Износ учитывается пропорционально продолжительности выполнения услуги. Годовую сумму износа каждого вида оборудования, используемого в процессе выполнения медицинской услуги, рассчитывают по формуле
![]() , (А.5)
, (А.5)
где - балансовая стоимость основных средств;
- норматив годового износа.
А.3 Накладные затраты
Накладные затраты не могут быть прямо отнесены на затраты на услугу, их рассчитывают следующими способами:
Коэффициент заработной платы общеучрежденческого (немедицинского) персонала рассчитывают по формуле
![]() , (А.6)
, (А.6)
где - заработная плата общеучрежденческого (немедицинского) персонала;
- основная заработная плата медицинского персонала.
Заработную плату общеучрежденческого (немедицинского) персонала рассчитывают по формуле
![]() . (А.7)
. (А.7)
Начисления на заработную плату немедицинского персонала рассчитываются аналогично начислениям на заработную плату основного персонала.
Прочие накладные расходы в расчете на услугу (приобретение предметов снабжения и расходных материалов; оплата горюче-смазочных материалов, прочих расходных материалов и предметов снабжения; командировки и служебные разъезды; транспортные услуги; оплата услуг связи; оплата коммунальных услуг; оплата содержания помещений; оплата потребления тепловой энергии; оплата отопления и технологических нужд; оплата потребления газа; оплата потребления котельно-печного топлива; оплата потребления электрической энергии; оплата водоснабжения помещений; оплата аренды помещений, земли и др. имущества; прочие коммунальные услуги; прочие текущие расходы на закупки товаров и оплату услуг; оплата научно-исследовательских, опытно-конструкторских и технологических работ; оплата текущего ремонта оборудования и инвентаря; оплата текущего ремонта зданий и сооружений; прочие текущие расходы; прочие специальные расходы; прочие непредвиденные расходы; износ не медицинского оборудования и мягкого инвентаря, затраты, связанные с лицензированием, аккредитацией, сертификацией, текущим ремонтом, обеспечением санитарных и противопожарных норм, обучением персонала; налоги, не относимые к начислениям на заработную плату), рассчитывают исходя из фактических затрат по учреждению в целом за календарный год с поправкой на период времени, за который учитывают затраты (квартал, полугодие). Коэффициент накладных расходов , связанных с выполнением услуги, рассчитывают по формуле
![]() , (А.8)
, (А.8)
где ![]() - суммы накладных расходов;
- суммы накладных расходов;
![]() - сумма основной заработной платы основного персонала по организации здравоохранения за анализируемый период.
- сумма основной заработной платы основного персонала по организации здравоохранения за анализируемый период.
Сумму накладных расходов в составе затрат на медицинскую услугу ![]() рассчитывают по формуле
рассчитывают по формуле
![]() . (А.9)
. (А.9)
А.4 Учет прибыли в затратах на медицинскую услугу
В расчет затрат на медицинскую услугу дополнительно включается прибыль организации здравоохранения. Затраты на медицинскую услугу с учетом рентабельности рассчитывают по формуле
![]() , (А.10)
, (А.10)
где - сумма затрат на оказание медицинской помощи;
- рентабельность (в величинах от 0 до 1).
Показатель уровня рентабельности определяется на основании нормативных документов.
А.5 Учет инфляции при расчете затрат на медицинскую услугу
При расчете затрат на медицинскую услугу рекомендуется проводить корректировку на инфляцию. Для этого используют показатель "индекс цен валового национального продукта" ![]() за анализируемый период времени, который рассчитывают по формуле
за анализируемый период времени, который рассчитывают по формуле
![]() , (А.11)
, (А.11)
где - затраты на медицинскую услугу с учетом инфляции;
- сумма затрат на оказание медицинской помощи;
![]() - индекс цен валового национального продукта.
- индекс цен валового национального продукта.
А.6 Трудоемкость услуги
Показатель времени, затрачиваемого врачами, средним медицинским и вспомогательным персоналом в процессе оказания услуги, устанавливается путем измерения не менее чем в 10 случаях выполнения одноименных услуг с вычислением среднего значения или путем экспертной оценки - опроса нескольких специалистов, выполняющих однотипные услуги. При этом считается, что весь персонал, участвующий в оказании услуги, затрачивает одинаковое время. Расчет трудоемкости (трудозатрат, затрат времени) проводят на основании фонда рабочего времени медицинского персонала.
Трудоемкость услуги измеряют в условных единицах труда. Одна условная единица труда приравнивается к 10 мин рабочего времени.
При определении трудоемкости услуги учитывают время, затрачиваемое на непосредственное оказание услуги. При расчете определенной условной единицы труда время, затрачиваемое специалистами на выполнение услуги, умножается на нормативные коэффициенты использования рабочего времени , представленные в таблице А.1.
Таблица А.1 - Нормативные коэффициенты использования рабочего времени
Наименование должности (специальности) | Нормативный коэффициент |
Врач терапевтического или хирургического профиля | 0,923 |
Врач клинической лабораторной диагностики | 0,750 |
Медицинская сестра по специальности "Лабораторная диагностика" | 0,800 |
Врач-рентгенолог, медицинская сестра по специальности "Рентгенология" | 0,900 |
Врач-радиолог | 1,000 |
Врач функциональной диагностики | 0,840 |
Врач ультразвуковой диагностики | 0,850 |
Врач-эндоскопист | 0,850 |
Врач по лечебной физкультуре, врач-физиотерапевт | 0,923 |
Медицинская сестра по специальности "Медицинский массаж" | 0,770 |
Медицинская сестра по специальности "Физиотерапия" | 1,120 |
Врач-психиатр, врач психиатр-нарколог | 0,923 |
Врач-судебно-медицинский эксперт | 0,900 |
Для врачебных специальностей, не указанных в таблице А.1, коэффициент использования рабочего времени принимается равным коэффициенту, рассчитанному для врача терапевтического и хирургического профиля, для медицинских сестер, работающих с врачами, используется коэффициент, рассчитанный для врачей соответствующей специальности.
А.7 Затраты на сложные и комплексные медицинские услуги
Затраты на оказание сложных и комплексных медицинских услуг определяются суммированием затрат на простые услуги и кратностью проведения простых медицинских услуг, входящих в состав сложной и комплексной медицинской услуги.
При расчете затрат на сложные и комплексные медицинские услуги учитывают маржинальные составляющие затрат, характеризующиеся величиной дополнительных затрат, необходимых для одновременного выполнения одной дополнительной простой медицинской услуги согласно составу сложной или комплексной услуги.
При расчете затрат на сложные и комплексные услуги учитывают расходы по оплате услуг, выполняемых в других организациях здравоохранения (аутсорсинг, при отсутствии возможности их выполнения в данной организации здравоохранения); оплате доноров, включая питание.
А.8 Поправочные коэффициенты
Поправочные коэффициенты необходимы в случаях, когда имеющиеся условные единицы трудозатрат (УЕТ) не коррелируются со значением нормативов выполнения той или иной услуги. Это может быть связано с изменением условий предоставления услуг (например, выполнение услуги "на дому" по отношению к выполнению той же услуги в поликлинике), усложнением или упрощением технологии предоставления услуги (например, исследование аналита ручным способом по отношению к исследованию с помощью анализатора или анализатора, упрощающего выполнение услуги), применением для формирования УЕТ сложной и комплексной услуги суммации УЕТ простых услуг ее составляющих. Основная задача поправочных коэффициентов - нивелировать такие погрешности. Выделяют следующие виды поправочных коэффициентов:
- коэффициент сложности повышающий и понижающий (применяется в случае усложнения или упрощения методики выполнения услуги, выполнения услуги высококвалифицированным специалистом и др.);
- коэффициент субспециальности (применяется в случае выполнения услуги специалистом, имеющим дополнительную специализацию, например, врач гинеколог-эндокринолог);
- коэффициент условий выполнения услуги (применяется в случае, если условия выполнения услуги требуют дополнительных затрат, например, выполнение услуги "на дому");
- коэффициент маржинальности (применяется в случае расчета УЕТ для сложной услуги, состоящей из простых услуг, выполняемых одновременно).
Значения поправочных коэффициентов представлены в таблице А.2.
Таблица А.2 - Значения поправочных коэффициентов
Наименование поправочного коэффициента | Значение поправочного коэффициента |
Коэффициент сложности: | |
- повышающий | 2,0 |
- понижающий | 0,1 |
Коэффициент субспециальности | 2,0 |
Коэффициент условий выполнения услуги: | |
- на дому | 3,0 |
- скорая и неотложная медицинская помощь в условиях сельской местности | 2,0 |
- скорая и неотложная медицинская помощь в условиях города | 1,5 |
Значения коэффициента маржинальности в зависимости от количества суммируемых услуг представлены в таблице А.3.
Таблица А.3 - Значения коэффициентов маржинальности в зависимости от количества выполняемых параллельно работ и услуг в здравоохранении
Количество услуг | Значение коэффициента маржинальности |
2 | 1,5 |
3 | 1,2 |
4 | 1,0 |
5 | 0,8 |
6 | 0,6 |
7 | 0,5 |
8 | 0,42 |
9 | 0,38 |
10 | 0,34 |
11 | 0,3 |
12 | 0,26 |
13 | 0,22 |
14 | 0,18 |
15 | 0,16 |
16 | 0,14 |
17 | 0,12 |
18 | 0,1 |
19 | 0,08 |
20 | 0,06 |
21 | 0,04 |
22 | 0,02 |
Более 22 | 0,01 |
Возможно введение дополнительных коэффициентов, связанных с квалификацией специалистов (интерн - 0,8; кандидат медицинских наук - 1,5; доктор медицинских наук - 2,0).
Приложение Б
(рекомендуемое)
Структура отчета о клинико-экономическом исследовании
1 Тема исследования, организация, выполнявшая исследование, даты исследования.
2 Руководитель исследования: фамилия, имя, отчество, место работы, должность, ученая степень и звание.
3 Координаты исследователей: фамилия, имя, отчество, место работы с указанием должности и адреса места работы, телефон, электронная почта.
4 Предпосылки для исследования, актуальность, краткий обзор литературы по проблеме с эпидемиологическим анализом.
5 Цель и задачи исследования.
6 База исследования.
7 Исследуемая медицинская технология с кратким описанием (ссылки на результаты клинических исследований, сведения об эффективности при изучаемых показаниях, аналогичных исследуемой ситуации; сведения о безопасности (побочных эффектах), сведения о разрешении к применению в Российской Федерации, если применимо).
8 Медицинская технология, с которой проводится сравнение эффективности и экономической целесообразности исследуемой технологии с обоснованием выбора (если применимо):
9 Позиция исследования (исследовалась экономическая целесообразность с точки зрения общества в целом, системы здравоохранения субъекта Российской Федерации, отдельной медицинской организации, пациента).
10 Каким образом оценивалась эффективность исследуемой медицинской технологии:
- по данным литературы (отметить тип исследования и указать выходные данные работы: метаанализ, систематический обзор, рандомизированное контролируемое исследование, проспективное сравнительное исследование, ретроспективное сравнительное исследование, проспективное несравнительное исследование, другой тип исследования);
- по результатам собственного исследования (отметить тип исследования: метаанализ, систематический обзор, рандомизированное контролируемое исследование, проспективное сравнительное исследование, ретроспективное сравнительное исследование, проспективное несравнительное исследование, другой тип исследования).
11 Краткое описание исследования (число наблюдений, характеристики пациентов, описание исследованных технологий, сроки наблюдения, результаты, статистическая достоверность полученных результатов, применение методов, снижающих вероятность систематической ошибки, - слепой метод, плацебо-контроль и др.).
12 Совпадают ли результаты собственного исследования с результатами других аналогичных исследований, если нет - дать характеристику и обоснования расхождений.
13 Какие критерии оценки эффективности были выбраны (медико-биологические критерии (например, биохимические параметры крови, уровень артериального давления и т.п.), медико-социальные критерии (например, число предотвращенных осложнений, продолжительность жизни, число лет сохраненной жизни), качество жизни - указать метод оценки, другие (указать, какие).
14 Какие типы затрат учитывались в исследовании, источники информации о ценах, используемых при расчетах затрат, анализ затрат.
15 Тип клинико-экономического анализа с обоснованием выбора, способы расчета.
16 При построении модели - какие виды моделирования применялись, предпосылки для построения модели и допущения, формулы расчетов.
17 Полученные результаты.
18 Проводилось ли дисконтирование, учет инфляции, анализ чувствительности (обязательный элемент), указать методику и полученные результаты.
19 Обсуждение результатов.
20 Выводы.
21 Используемая литература.
Приложение В
(рекомендуемое)
Рекомендуемые вопросы для оценки результатов клинико-экономического исследования
1 Ясно ли сформулированы цель и задачи исследования?
2 Указана ли позиция исследования? Соответствует ли она задаче, для решения которой предполагается использовать результаты?
3 Является ли данное исследование сравнительным?
4 Достаточно ли полно представлена информация об исследуемой медицинской технологии и технологии сравнения?
5 Есть ли обоснование выбора альтернативной медицинской технологии (кроме случаев проведения анализа стоимости болезни или влияния на бюджет)? Соответствует ли выбранная для сравнения технология задаче, для решения которой предполагается использовать результаты исследования?
6 Представлено ли подробное и понятное описание методики проведения клинико-экономического исследования?
7 Представлены ли данные об эффективности каждой из исследуемых технологий? Достаточно ли они надежны?
8 Если эффективность оценивалась по результатам собственного исследования, то совпадают ли его результаты с результатами других аналогичных исследований?
9 Соответствуют ли выбранные критерии оценки эффективности исследуемой технологии задаче, для решения которой предполагается использовать результаты?
10 Представлена ли информация об окончательных ("жестких") показателях эффективности исследуемых технологий (продолжительности и качестве жизни пациентов)?
11 Учтены ли все существенные затраты, связанные с применением исследуемых технологий (с учетом выбранной позиции исследования)?
12 Указаны ли источники информации о ценах, используемых при расчетах затрат?
13 Если период наблюдения составлял год и более, проводилось ли дисконтирование затрат?
14 Проводился ли анализ чувствительности?
15 Соответствуют ли выводы использованной методологии?
УДК 616-08:006.354 | ОКС 11.160 | Р24 | ОКП 94 4000 |
Ключевые слова: клинико-экономические исследования, клинико-экономический анализ, фармакоэкономика | |||
Электронный текст документа
и сверен по:
, 2017

