ГОСТ 34105-2017
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
Животные
ЛАБОРАТОРНАЯ ДИАГНОСТИКА БРУЦЕЛЛЕЗА
Серологические методы
Animals. Laboratory diagnostics of brucellosis. Serological methods
МКС 11.220
Дата введения 2018-07-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2015 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением "Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов" (ФГБУ "ВГНКИ")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 7 июня 2017 г. N 99-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 22 июня 2017 г. N 582-ст межгосударственный стандарт ГОСТ 34105-2017 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2018 г.
5 ВЗАМЕН ГОСТ 25385-91 в части серологических методов диагностики
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет ()
1 Область применения
Настоящий стандарт распространяется на все виды млекопитающих животных и устанавливает следующие методы серологической диагностики бруцеллеза:
- реакция агглютинации с S- и R-бруцеллезными антигенами;
- пластинчатая реакция агглютинации с антигеном, окрашенным бенгальской розовой (роз бенгал проба);
- реакция связывания комплемента;
- реакция длительного связывания комплемента на холоде;
- реакция непрямой гемагглютинации;
- реакция иммунодиффузии в геле агара с олигополисахаридным антигеном;
- реакция иммунодиффузии в геле агара с R-бруцеллезным антигеном;
- кольцевая реакция с молоком;
- иммуноферментный анализ;
- иммунохроматографический анализ.
Примечание - Методы применимы ко всем видам бактерий рода Brucella.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ 12.0.004-2015 Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.008-76 Система стандартов безопасности труда. Биологическая безопасность. Общие требования
ГОСТ 12.4.011-89 Система стандартов безопасности труда. Средства защиты работающих. Общие требования и классификация
ГОСТ 1625-2016 Формалин технический. Технические условия
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2651-78 Натрия бихромат технический. Технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
ГОСТ 4220-75 Реактивы. Калий двухромовокислый. Технические условия
ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ 5962-2013 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ ISO 7218-2015 Микробиология пищевых продуктов и кормов для животных. Общие требования и рекомендации по микробиологическим исследованиям
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия
ГОСТ 16445-2012 Сыворотка гемолитическая для реакции связывания комплемента. Технические условия
ГОСТ 16446-2012 Комплемент сухой для реакции связывания комплемента. Технические условия
ГОСТ ИСО/МЭК 17025-2009 Общие требования к компетентности испытательных и калибровочных лабораторий
ГОСТ 17206-96 Агар микробиологический. Технические условия
ГОСТ 18704-78 Кислота борная. Технические условия
ГОСТ 23519-93 Фенол синтетический технический. Технические условия
ГОСТ 25134-2013 Бруцеллин ВИЭВ. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 25794.1-83 Реактивы. Методы приготовления титрованных растворов для кислотно-основного титрования
ГОСТ 29230-91 (ИСО 835-4-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 4. Пипетки выдувные
ГОСТ 33675-2015 Животные. Лабораторная диагностика бруцеллеза. Бактериологические методы
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины, определения и сокращения
3.1 В настоящем стандарте применены термины с соответствующими определениями по ГОСТ 33675.
3.2 В настоящем стандарте применены следующие сокращения:
- РА - реакция агглютинации;
- РСК - реакция связывания комплемента;
- РБП - пластинчатая реакция агглютинации с бруцеллезным роз бенгал антигеном;
- РДСК - реакция длительного связывания комплемента;
- РИД - реакция иммунодиффузии;
- ЛПС - липополисахаридный антиген;
- О-ПС - олигополисахаридный антиген;
- РНГА - реакция непрямой гемагглютинации;
- КР с молоком - кольцевая реакция с молоком;
- ИФА - иммуноферментный анализ;
- ИХА - иммунохроматографический анализ;
- PKг-G - раствор конъюгата, конъюгированного с пероксидазой;
- ФСБ-Т - фосфатно-солевой буферный раствор с твином;
- РБР-С - разводящий буферный раствор для сывороток;
- ТМБ-субстрат - тетраметилбензидин-субстрат;
- К+ - инактивированная сыворотка крови животных, содержащая специфические антитела класса G к бактериям рода Brucella (положительный контрольный образец);
- К- - инактивированная сыворотка крови животных, не содержащая специфических антител к бактериям рода Brucella (отрицательный контрольный образец).
4 Условия выполнения исследований и требования безопасности
4.1 Условия выполнения исследований
4.1.1 Общие требования к помещениям - по ГОСТ ISO 7218.
4.1.2 Требования к персоналу - по ГОСТ ISO 7218, ГОСТ ИСО/МЭК 17025.
4.1.3 К проведению исследований допускаются квалифицированные сотрудники, имеющие опыт работы с микроорганизмами II группы патогенности*, изучившие методики микробиологических работ. В зонах неблагополучных по бруцеллезу сотрудники должны быть вакцинированы против бруцеллеза.
________________
* Группу патогенности устанавливают в соответствии с нормативными правовыми актами, действующими на территории государства, принявшего стандарт.
4.2 Требования безопасности
4.2.1 Общие требования безопасности при проведении работ с микроорганизмами - согласно ГОСТ 12.1.008.
4.2.2 Средства защиты работающих должны соответствовать требованиям ГОСТ 12.4.011.
4.2.3 Воздух рабочей зоны должен соответствовать требованиям ГОСТ 12.1.005.
4.2.4 Обучение персонала безопасности труда - в соответствии с ГОСТ 12.0.004.
4.2.5 Обеззараживание материала после исследований, а также использованных индивидуальных средств защиты, инструментов и т.д. проводят путем кипячения в течение 30 мин или автоклавирования в течение 1 ч при давлении 2 атм (0,2) МПа и температуре (132±2)°С.
5 Средства измерений, оборудование, материалы, реактивы и животные
При проведении исследований используют следующие средства измерений, оборудование, материалы, реактивы и животных:
- pH-метр с точностью калибровки ±0,1 ед.pH при температуре от 20°С до 55°С;
- спектрофотометр с диапазоном длины волны от 198 до 1000 нм, разрешением 1 нм и точностью ±2 нм;
- пипетки градуированные выдувные вместимостью от 1 до 10 см по ГОСТ 29230;
- колбы мерные по ГОСТ 1770 исполнения 2 различной вместимости 1-го класса точности;
- центрифуга лабораторная со скоростью вращения ротора 2000-3000 об/мин;
- автоклав лабораторный;
- термостат, обеспечивающий поддержание температуры от 20°С до 50°С;
- баня водяная с терморегулятором с температурой нагрева до 100°С;
- холодильник бытовой, обеспечивающий поддержание температуры от 0°С до 10°С по ГОСТ 16317;
- насос вакуумный;
- иглы препаровальные;
- штамп для формирования лунок в агаре;
- осветитель настольный с пределом поворота фонаря вокруг горизонтальной и вертикальной осей 0-360 и источником света - лампой В/Ватт-8/20;
- чашки биологические (Петри) с крышками ЧБН 2 по ГОСТ 25336;
- чашка и ступка фарфоровые по ГОСТ 9147;
- комплект инструментов и приспособлений для серологических исследований крови животных на бруцеллез, в который входят:
1) шприц-полуавтомат (капельница) для дозирования сыворотки;
2) пипетка-капельница для дозирования антигена;
3) ручной смеситель на 25 лунок диагностической пластины;
4) аппарат для автоматического покачивания диагностических пластин;
- пластины с лунками 72-гнездные полистироловые (планшеты);
- штативы 100-гнездные для пробирок Флоринского;
- групповые дозаторы Флоринского;
- пробирки серологические Флоринского;
- микропипетки вместимостью от 0,1 до 0,5 см;
- дозаторы одноканальные пипеточные переменного объема;
- наконечники для дозаторов вместимостью 0,2; 0,5; 1,0 см;
- фильтры бумажные из бумаги фильтровальной по ГОСТ 12026;
- бумага фильтровальная по ГОСТ 12026;
- салфетки марлевые;
- спирт этиловый ректификованный по ГОСТ 5962;
- вода дистиллированная по ГОСТ 6709;
- кислота соляная по ГОСТ 3118 х.ч;
- фенол по ГОСТ 23519 - 5%-ный раствор;
- формалин по ГОСТ 1625 - 1%-ный и 10%-ный растворы;
- натрий хлористый по ГОСТ 4233;
- кислота борная по ГОСТ 18704 - 3%-ный раствор;
- натрия бихромат по ГОСТ 2651;
- калий двухромовокислый по ГОСТ 4220;
- кислота серная по ГОСТ 4204;
- натрия гидроокись по ГОСТ 4328;
- сыворотка гемолитическая по ГОСТ 16445;
- комплемент сухой для РСК по ГОСТ 16446;
- кровь барана-донора;
- свинки морские массой 300-400 г;
- сыворотки крови животных;
- набор для ИФА, содержащий в своем составе:
1) планшет полистироловый 96-луночный с адсорбированной в лунках планшета смесью специфических антигенов Brucella;
2) флакон N 1 - ФСБ-Т объемом 26 см;
3) флакон N 2 - РБР-С объемом 12 см;
4) флакон N 3 - PKг-G объемом 12 см;
5) флакон N 4 - К+ объемом 1,5 см;
6) флакон N 5 - К- объемом 2,5 см;
7) флакон N 6 - ТМБ-субстрат;
8) флакон N 7 - стоп-реагент объемом 6 см;
- тест-система для определения антител к ЛПС антигену В.abortus и В.melitensis в сыворотке крови крупного рогатого скота и овец методом ИФА, содержащая в своем составе компоненты:
1) К - иммунохроматографические тест-полоски, нитроцеллюлозные мембраны на полимерной основе белого цвета, ламинированные защитными этикетками с обозначениями разного цвета: в нижней части - стрелки, указывающие направления погружения полоски в тестируемую пробу; в верхней части - название рода и вида возбудителя исключаемой болезни;
2) К - буферный раствор для разведения проб объемом 0,8 см
;
- негативная сыворотка (сыворотка крови здоровых животных);
- антиген бруцеллезный для РА и РСК (РДСК);
- роз бенгал антиген для РБП;
- антиген бруцеллезный для КР с молоком;
- 0,85%-ный раствор хлористого натрия;
- 0,85%-ный раствор хлористого натрия с 0,5% фенола;
- 5%-ный раствор хлористого натрия с 0,5% фенола;
- 10%-ный раствор хлористого натрия с 0,5% фенола;
- раствор хлорамина 5%-ный;
- взвесь формалинизированных несенсибилизированных эритроцитов;
- молоко от здоровой коровы (буйволицы);
- набор для РИД, содержащий в своем составе:
1) О-ПС бруцеллезный антиген;
2) натрий хлористый по ГОСТ 4233;
3) микробиологический агар-агар по ГОСТ 17206;
- набор для серологической диагностики бруцеллеза крупного и мелкого рогатого скота, содержащий в своем составе:
1) антиген бруцеллезный эритроцитарный для РНГА;
2) взвесь формалинизированных несенсибилизированных эритроцитов;
3) сыворотку бруцеллезную;
4) сыворотку негативную.
Допускается применение других средств измерений с метрологическими характеристиками и оборудования с техническими характеристиками не хуже, а также реактивов, дезинфицирующих средств и материалов по качеству не ниже указанных. Допускается использование посуды одноразового применения.
6 Отбор проб
6.1 Забор крови у животных для получения сыворотки проводят:
- из яремной, ушной или хвостовой вены у свиней;
- головной вены, вены предплечья или латеральной подколенной вены голени у собак;
- из бедренной вены у лисиц и песцов;
- путем отсечения подушечки среднего пальца задней лапы или кончика хвоста у норок.
Кровь берут в стерильные пробирки по 5-7 см (от пушных зверей - по 1-2 см
). Пробирки нумеруют и составляют опись проб.
6.1.1 Сыворотку крови получают методом отстоя. Для свертывания крови и отстаивания сыворотки пробирки с кровью выдерживают в термостате при 30°С-38°С в течение 1 ч или при комнатной температуре в течение 8-10 ч, сгусток крови от стенок отделяют стальной спицей, а затем пробирки выдерживают при 4°С-10°С. Через 20-24 ч после взятия крови отстоявшуюся сыворотку сливают в сухие стерильные пробирки и направляют для исследования в лабораторию в свежем или консервированном виде (сыворотку крови собак сливают через 3-4 ч и повторно через 10-12 ч).
6.1.2 Консервирование сывороток проводят:
- добавлением 0,05 см (1 капля) 5%-ного раствора фенола на 1 см
сыворотки при тщательном перемешивании;
- сухой борной кислотой (3-4% к объему сыворотки) до получения насыщенного раствора и образования на дне пробирки небольшого осадка;
- путем однократного замораживания.
Неконсервированные сыворотки пригодны для исследования в течение 6 сут со дня взятия крови при условии хранения их при температуре от 2°С до 8°С.
Сыворотки, консервированные фенолом или борной кислотой, пригодны для исследования в течение 30 сут, замороженные сыворотки - в течение 3 сут после однократного оттаивания. Мутные, проросшие, гемолизированные сыворотки к исследованию на бруцеллез не пригодны.
6.2 Для исследования молока на бруцеллез в кольцевой реакции пробу цельного свежего молока от коровы (буйволицы) берут из каждой доли вымени одного удоя в одну бактериологическую пробирку в количестве 10-15 см. При этом если молоко берут перед дойкой, то первые порции молока сдаивают. Пробы молока на рынках берут из каждой отдельной посуды (бидон, фляга и др.) после тщательного его перемешивания. Пробирки нумеруют и составляют опись проб.
6.2.1 Молоко исследуют свежее или консервированное добавлением в каждую пробу одной капли 10%-ного раствора формалина на 5 см молока. Консервированное молоко пригодно для исследования в течение 2-3 сут. Перед исследованием молоко тщательно перемешивают для равномерного распределения сливок.
6.2.2 При массовом исследовании молока работу по отбору проб и постановке кольцевой реакции можно проводить непосредственно на ферме в специально отведенном помещении.
6.2.3 Не разрешается исследовать в кольцевой реакции молоко от коров (буйволиц), больных маститом или болезнями, сопровождающимися повышением температуры тела, а также молоко животных в первые две недели после родов. Молоко, имеющее повышенную кислотность (30° по Тернеру и выше), исследованию не подлежит, т.к. антиген обесцвечивается.
6.3 На направляемый в лабораторию материал заполняют сопроводительный документ.
7 Методы серологической диагностики бруцеллеза
7.1 Сущность методов заключается в выявлении в сыворотке крови животных специфических антител к бруцеллезным антигенам.
7.2 Пластинчатая реакция агглютинации с бруцеллезным роз бенгал антигеном (РБП)
7.2.1 Сущность метода
Сущность метода заключается в выявлении специфических антител в сыворотке крови животных, основанном на способности антител сыворотки агглютинировать бруцеллезный антиген, результатом чего является формирование выраженной агглютинации окрашенных бруцелл антигена в виде крупных или мелких хлопьев розового цвета.
7.2.2 Подготовка к исследованию
7.2.2.1 Приготовление 5%-ного раствора хлорамина
Для приготовления 5%-ного раствора хлорамина 5 г хлорамина растворяют в 100 см водопроводной воды. Раствор используют свежеприготовленным.
Примечание - Могут применяться другие растворы дезинфицирующих средств, эффективные в отношении бактерий рода Brucella, которые готовят в соответствии с инструкциями к ним.
7.2.2.2 Для массовых диагностических исследований используют комплект инструментов и приспособлений для серологических исследований крови животных на бруцеллез в соответствии с разделом 5.
Перед постановкой реакции роз бенгал антиген и исследуемые сыворотки выдерживают 30-40 мин при комнатной температуре и встряхивают для получения однородной смеси.
Реакцию проводят на чистых, сухих эмалированных диагностических пластинах с лунками при температуре не ниже 18°С. На бортиках пластинки против каждой лунки записывают номер исследуемой сыворотки.
7.2.3 Проведение исследования
7.2.3.1 РБП применяют как экспресс-метод диагностики бруцеллеза у не иммунизированного противобруцеллезными вакцинами крупного рогатого скота, овец, коз, верблюдов, лошадей, северных оленей (маралов), свиней и собак.
Для исследования применяют тест-системы, используемые для диагностики бруцеллеза животных в РБП.
Исследуемые сыворотки крови в дозе 0,03 см (две капли) вносят на дно лунки при помощи шприца-полуавтомата, или микропипетки, или одноканального дозатора с наконечником.
7.2.3.2 После внесения каждой сыворотки шприц-полуавтомат (микропипетку) трижды промывают фенолизированным 0,85%-ным раствором хлористого натрия по 7.4.2 и кончик подсушивают фильтровальной бумагой. При исследовании сыворотки крови крупного рогатого скота, лошадей, верблюдов в каждую лунку рядом с сывороткой при помощи пипетки-капельницы для антигена, или микропипетки, или одноканального дозатора с наконечником вносят 0,03 см антигена (две капли), а при исследовании сывороток крови овец, коз и северных оленей (маралов), свиней и собак - 0,015 см
антигена (одну каплю). Затем антиген в каждой лунке тщательно смешивают с сывороткой активными движениями ручного смесителя до получения однородной жидкости, распределяя ее при этом по всей поверхности лунки. После смешивания сывороток во всех лунках пластинки смеситель ополаскивают 0,85%-ным фенолизированным раствором хлористого натрия по 7.4.2 и просушивают марлевой салфеткой или фильтровальной бумагой.
Пластинку с сыворотками и антигеном покачивают в течение 4 мин осторожными вращательными движениями вручную или при помощи аппарата, предназначенного для этой цели. При положительной реакции в течение 4 мин появляются мелкие или крупные хлопья агглютината розового цвета.
В начале работы ставят контроль антигена с негативной и бруцеллезной сыворотками в тех же дозах, а также антигена на спонтанную агглютинацию (к 0,03 см 0,85%-ного фенолизированного раствора хлористого натрия добавляют 0,03 см
роз бенгал антигена).
По окончании работы диагностические пластинки дезинфицируют погружением на 5 мин в 5%-ный раствор хлорамина либо другого дезинфицирующего средства в концентрации и экспозиции, определенной для возбудителя данного вида, затем обрабатывают любым моющим средством, промывают водопроводной, затем дистиллированной водой, высушивают на воздухе или в термостате при температуре 37°С-38°С и используют повторно.
7.2.4 Обработка результатов
Учет результатов реакции проводят визуально в течение 4 мин после смешивания сывороток с антигеном при слегка наклонном положении пластинки.
Реакцию считают положительной при наличии агглютината в виде мелких или крупных хлопьев розового цвета.
Реакцию считают отрицательной при отсутствии агглютинации (смесь гомогенная и равномерно окрашенная).
При не четко выраженной агглютинации проводят повторное исследование сыворотки и по его результатам дают окончательную оценку реакции (положительная или отрицательная).
При получении отрицательных результатов РБП по всему стаду его считают благополучным по бруцеллезу.
Сыворотки крови животных стада (фермы, населенного пункта), положительно реагирующие в РБП, исследуют на бруцеллез в РА и РСК (РДСК), или в РА и РИД, или в РНГА, или в ИФА, или в ИХА.
7.3 Кольцевая реакция (КР) с молоком
Сущность метода состоит в выявлении антигеном специфических антител в молоке больных бруцеллезом или иммунизированных агглютиногенными противобруцеллезными вакцинами коров. Положительная реакция проявляется в образовании синего кольца в верхнем слое сливок.
КР с молоком применяют с целью определения благополучия стад (ферм) по бруцеллезу крупного рогатого скота (буйволов) и для проверки молока при продаже его на рынках.
Исследование молока на бруцеллез в КР можно проводить в лабораториях или непосредственно в хозяйствах.
7.3.1 Подготовка к исследованию
Для постановки КР с молоком применяют тест-системы или наборы для диагностики бруцеллеза в кольцевой реакции (КР), используемые на территории государств, принявших стандарт, в состав которых входят антиген бруцеллезный для КР с молоком и сыворотка бруцеллезная. Реакцию ставят в серологических пробирках Флоринского, которые нумеруют в соответствии с описью проб молока, пробы которого отбирают по 6.1.
7.3.2 Проведение исследования
В пробирки вносят по 2 см молока пипеткой или дозатором. После каждой пробы пипетку двукратно промывают теплой водопроводной водой. Антиген вносят по 0,1 см
в каждую пробирку с пробой молока. После внесения антигена в пробирки одного ряда штатив энергично встряхивают и т.д. После внесения антигена во все пробирки штатив встряхивают дополнительно.
При исследовании каждой партии молока ставят контрольные пробы:
- молоко от заведомо здоровой коровы (буйволицы);
- смесь молока здоровой коровы (буйволицы) с бруцеллезной сывороткой (0,1 см сыворотки на 2 см
молока).
Штативы с исследуемыми контрольными пробами молока выдерживают на водяной бане при температуре 37°С-38°С в течение 1 ч или в термостате в течение 2 ч.
Результаты реакции учитывают визуально через 30-40 мин после извлечения штативов из водяной бани (термостата) и оценивают в крестах по следующей схеме:
"+++" (три креста) - четко выраженное синее кольцо в верхней части столбика молока в слое сливок, остальная часть молока остается белой;
"++" (два креста) - четко выраженное синее кольцо в верхней части столбика молока в слое сливок, остальная часть молока имеет синеватый цвет;
"+" (один крест) - синее кольцо в слое сливок выражено слабо, и весь столбик молока имеет синий цвет;
"-" (минус) - столбик молока остается равномерно окрашенным в первоначальный синий цвет, который был получен сразу после смешивания с антигеном, а слой сливок - белого или слегка желтоватого цвета.
7.3.3 Обработка результатов
Все пробы молока с оценкой в "+++" (три креста) и "++" (два креста) считают положительными, "+" (один крест) - сомнительными.
При получении отрицательных результатов КР по всему стаду его считают благополучным по бруцеллезу.
Сыворотку крови животных стада (группы, населенного пункта), в котором выявлены особи, сомнительно или положительно реагирующие в КР, исследуют на бруцеллез в РБП, или в РА и РСК (РДСК), или в РА и РИД, или в РНГА, или в ИФА. При этом проводят клинический осмотр животных и исключают их заболевание маститами.
7.4 Реакция агглютинации (РА) в пробирках
7.4.1 РА в пробирках с бруцеллезным антигеном применяют при диагностике бруцеллеза крупного рогатого скота (буйволов, яков, зебу), овец, коз, лошадей, верблюдов, оленей (маралов), собак, пушных зверей и морских свинок.
7.4.2 Приготовление фенолизированных растворов хлористого натрия с содержанием фенола 0,5%
В 1 дм дистиллированной воды растворяют соответственно 8,5, 50 и 100 г хлористого натрия и добавляют к каждому раствору по 5 г фенола. Растворы фильтруют дважды через бумажный фильтр. Растворы хранят в стеклянных бутылях, укупоренных резиновыми пробками при температуре от 2°С до 20°С, и используют в течение 1 мес.
7.4.3 Проведение исследования
7.4.3.1 При исследовании в РА сыворотки крови крупного рогатого скота, лошадей, верблюдов, собак, пушных зверей и морских свинок и антиген разводят фенолизированным 0,85%-ным раствором хлористого натрия по 7.4.2; овец и коз - фенолизированным 5%-ным раствором хлористого натрия по 7.4.2; оленей (маралов) - фенолизированным 10%-ным раствором хлористого натрия по 7.4.2.
7.4.3.2 Сыворотки крови исследуют в четырех разведениях в пробирках Флоринского в объеме 1 см:
- для крупного рогатого скота, лошадей и верблюдов - в разведениях 1:50, 1:100, 1:200 и 1:400;
- для овец, коз, оленей (маралов) и собак - в разведениях 1:25, 1:50, 1:100 и 1:200;
- для собак с R-бруцеллезным антигеном (B.canis) - в разведениях 1:50, 1:100, 1:200 и 1:400;
- для пушных зверей и морских свинок - в разведениях 1:10, 1:20, 1:40 и 1:80.
Исследование каждой сыворотки проводят в пяти пробирках.
7.4.3.3 Получение исходного разведения проб сыворотки:
- сыворотки крови крупного рогатого скота (лошадей, верблюдов) по 0,1 см вносят в пробирки первого ряда, содержащие по 2,4 см
фенолизированного 0,85%-ного раствора хлористого натрия по 7.4.2 (разведение 1:25);
- сыворотки крови овец, коз и собак по 0,2 см вносят в пробирки первого ряда, содержащие по 2,3 см
фенолизированного 5%-ного раствора хлористого натрия по 7.4.2 (разведение 1:12,5);
- сыворотку крови оленей и маралов по 0,2 см вносят в пробирки первого ряда, содержащие по 2,3 см
фенолизированного 10%-ного раствора хлористого натрия по 7.4.2 (разведение 1:12,5);
- сыворотку крови пушных зверей и морских свинок по 0,3 см вносят в пробирки первого ряда, содержащие по 1,2 см
фенолизированного 0,85%-ного раствора хлористого натрия по 7.4.2 (разведение 1:5);
- при исследовании с R-бруцеллезным антигеном (B.canis) сыворотку крови собак по 0,1 см вносят в пробирки, содержащие по 2,4 см
фенолизированного 0,85%-ного раствора хлористого натрия по 7.4.2 (разведение 1:25).
В пробирки второго ряда раствор хлористого натрия не вносят.
В пробирки третьего, четвертого и пятого рядов вносят по 0,5 см соответствующего фенолизированного раствора хлористого натрия по 7.4.2.
Затем в пробирки второго и третьего рядов вносят по 0,5 см исходного разведения сыворотки.
После пипетирования (не менее трех раз) разведение сыворотки из третьего ряда по 0,5 см переносят в пробирки четвертого ряда и после пипетирования из четвертого - в пятый. Из пробирок пятого ряда 0,5 см
жидкости удаляют. Таким образом, получают последовательные двукратные разведения образцов сыворотки.
7.4.3.4 В пробирки второго, третьего, четвертого и пятого рядов с разведенными сыворотками вносят при помощи группового дозатора Флоринского или другого дозирующего устройства по 0,5 см антигена в рабочем разведении 1:10 (1,0+9,0 см
) соответствующим фенолизированным раствором хлористого натрия по 7.4.2.
После внесения антигена разведение сыворотки в каждой пробирке удваивается.
В пробирки первого ряда антиген не вносят, они служат контролем сыворотки на самоагглютинацию. При наличии хлопьев, фибрина, эритроцитов и посторонних примесей результаты реакции агглютинации не учитывают.
После добавления к исследуемым и контрольным сывороткам антигена штативы с пробирками интенсивно встряхивают для смешивания компонентов и помещают в термостат при температуре 37°С-38°С на 16-20 ч, затем выдерживают при комнатной температуре в течение 1 ч и проводят учет реакции.
7.4.3.5 На территориях, угрожаемых или неблагополучных по бруцеллезу, проводят массовые серологические исследования. При этом допускается проведение исследований в двух разведениях. Сыворотки разливают индивидуальной микропипеткой (с резиновой грушей), или групповыми дозаторами Флоринского, или одноканальными пипеточными дозаторами в две серологические пробирки Флоринского в дозах 0,02 и 0,01 см (сыворотки крупного рогатого скота, лошадей и верблюдов) или 0,04 и 0,02 см
при исследовании сывороток овец, коз, оленей (маралов) и собак. Затем в каждую пробирку вносят по 1,0 см
антигена, разведенного соответствующим фенолизированным раствором хлористого натрия по 7.4.2 в соотношении 1:20. При этом сыворотки крови будут разведены соответственно 1:50 и 1:100 или 1:25 и 1:50.
При получении положительных или сомнительных результатов РА при массовом исследовании эти сыворотки исследуют в четырех разведениях.
Массовые исследования пушных зверей и морских свинок не проводят.
7.4.4 Обработка результатов
Результаты реакции учитывают визуально, определяя степень просветления жидкости, внешний вид агглютината (при его наличии) или антигена на дне пробирки до и затем, после легкого встряхивания, оценивают в крестах по следующей схеме:
"++++" (четыре креста) - полное просветление жидкости, микробные клетки антигена осели на дно пробирки в виде "зонтика", при легком встряхивании "зонтик" разбивается на хлопья и комочки, а жидкость остается прозрачной (100% агглютинации);
"+++" (три креста) - неполное просветление жидкости и хорошо выраженный "зонтик" агглютината (75% агглютинации);
"++" (два креста) - неполное просветление жидкости, "зонтик" агглютината умеренно выражен (50% агглютинации);
"+" (один крест) - едва заметное просветление жидкости, "зонтик" агглютината выражен слабо, при встряхивании заметно небольшое количество хлопьев или комочков (25% агглютинации);
"-" (минус) - просветления жидкости и образования "зонтика" агглютината не наступило, на дне пробирки по центру образуется небольшой осадок микробов антигена в виде точки или пятна. При встряхивании осадок легко разбивается, поднимается вверх в виде косички и равномерно распределяется в жидкости, которая при этом приобретает первоначальную мутность.
За титр антител принимают наибольшее разведение сыворотки, в котором произошла агглютинация на два креста ("++"), что соответствует количеству международных единиц (ME) антител в 1 см сыворотки (например, сыворотка с титром 1:100 содержит 100 ME, 1:200 - 200 ME и т.д.).
Для более объективной оценки результатов РА готовят образцы сравнения мутности, соответствующие 75%, 50%, 25% и 0% просветления жидкости.
В четыре пробирки последовательно вносят 0,5; 1,0; 1,5 и 2,0 см антигена, разведенного 0,85%-ным фенолизированным раствором хлористого натрия в соотношении 1:10. Затем в том же порядке в три первые пробирки добавляют 1,5; 1,0 и 0,5 см
соответствующего фенолизированного раствора хлористого натрия по 7.4.2. После перемешивания содержимого пробирок из каждой из них переносят по 1,0 см
в серологические пробирки. Полученные образцы сравнения мутности соответствуют 75%, 50% и 25% просветления жидкости. В четвертой пробирке просветление отсутствует. Образцы сравнения мутности готовят каждый раз при постановке РА и выдерживают в термостате одновременно с основной реакцией.
При массовых исследованиях в двух разведениях все сыворотки, давшие агглютинацию с оценкой не менее чем на два креста ("++") в каком-либо из указанных разведений, исследуют повторно в четырех разведениях.
В заключении лаборатории о результатах исследования должны быть отражены диагностическая оценка каждой пробы (положительная, сомнительная, отрицательная) и конечное разведение (титр) сыворотки, в котором получен соответствующий результат, выраженный в международных единицах (например: титр сыворотки крови крупного рогатого скота 1:200 с оценкой два - четыре креста - "положительная" 200 МЕ/см; титр сыворотки 1:100 с оценкой два - четыре креста - "сомнительная" 100 МЕ/см
).
Результаты исследования исследуемой и контрольных сывороток, серию антигена, срок его годности записывают в журнал серологических исследований.
7.5 Реакция связывания комплемента (РСК) и реакция длительного связывания комплемента на холоде (РДСК)
7.5.1 РСК применяют при диагностике бруцеллеза у крупного рогатого скота (буйволов, яков, зебу), овец, коз, свиней, верблюдов, лошадей, оленей (маралов), собак и пушных зверей.
Сущность реакции состоит в том, что при соответствии друг другу антигены и антитела образуют иммунный комплекс, к которому через Fc-фрагмент антител присоединяется комплемент, т.е. происходит связывание комплемента комплексом антиген - антитело.
7.5.2 РДСК применяют вместо РСК, в том числе для исследования сывороток, обладающих антикомплементарными свойствами.
Сущность реакции состоит в образовании иммунного комплекса антиген - антитело в присутствии комплемента на холоде в течение нескольких часов.
7.5.3 Подготовка к исследованию
7.5.3.1 Приготовление 0,85%-ного раствора хлористого натрия
Для приготовления 1 дм раствора 8,5 г хлористого натрия растворяют в дистиллированной воде, устанавливают pH 6,8-7,2 ед.pH 5%-ным раствором натрия гидроокиси и дважды фильтруют через бумажный фильтр. 0,85%-ный раствор хлористого натрия хранят в стеклянной бутыли, закрытой резиновой или корковой пробкой, и используют в течение 1 мес.
7.5.3.2 Приготовление 5%-ного раствора натрия гидроокиси
Для приготовления 5%-ного раствора натрия гидроокиси 5 г натрия гидроокиси растворяют в 100 см. Раствор хранят при комнатной температуре в течение месяца.
7.5.3.3 Образцы сыворотки крови и компоненты РСК и РДСК разводят 0,85%-ным раствором хлористого натрия по 7.5.3.1. Сухой комплемент регидратируют и титруют по ГОСТ 16446.
Берут такое количество флаконов (ампул), в которых содержится необходимое для проведения всего опыта количество комплемента. В каждый флакон (ампулу) вносят 0,85%-ный раствор хлористого натрия в объеме, указанном на этикетке, и, не встряхивая, помещают в холодильник на 20-30 мин. Растворившийся комплемент осторожно перемешивают путем легкого встряхивания флаконов (ампул), сливают в одну пробирку, смешивают и помещают в холодильник при температуре от 4°С до 10°С. Непосредственно перед внесением в пробирки для титрования регидратированный комплемент разводят 0,85%-ным раствором хлористого натрия в соотношении 1:20, а остальной - хранят в холодильнике. Рабочее разведение комплемента также готовят непосредственно перед внесением в пробирки при постановке реакции. Рабочий титр комплемента должен быть на два интервала больше его титра.
Количество комплемента Х, см, необходимого для проведения опыта, рассчитывают по формуле
![]() , (1)
, (1)
где А - рабочий титр комплемента, см;
В - количество пробирок в опыте, шт;
20 - исходное разведение комплемента (1:20).
Пример - |
|
Так как количество комплемента в рабочем разведении, требующемся для всей реакции (на 100 пробирок), равно 20 см (0,2·100), то к 0,6 см
регидратированного комплемента добавляют 19,4 см
0,85%-ного раствора хлористого натрия.
Гемолитическую сыворотку титруют по ГОСТ 16445 при использовании каждой новой серии и по истечении срока годности.
Рабочий титр гемолитической сыворотки для РСК и РДСК составляет удвоенную дозу от титра. Так, если титр сыворотки равен 1:1500, то рабочий титр в РСК и РДСК будет 1:750.
Эритроциты барана - 2,5%-ную взвесь эритроцитов барана в 0,85%-ном растворе хлористого натрия для РСК и РДСК готовят из свежей или консервированной крови барана по ГОСТ 16446. Дефибринированную кровь фильтруют через марлю и консервируют стрептомицином из расчета 1 г препарата, растворенного в 10-20 см стерильного 0,85%-ного раствора хлористого натрия, на 100 см
крови. Консервированная кровь при хранении в холодильнике пригодна для использования, как правило, в течение 10-14 сут.
Гемолитическую систему готовят перед каждой постановкой РСК. Для этого 2,5%-ную взвесь отмытых эритроцитов и раствор гемолитической сыворотки в рабочем разведении смешивают в равных объемах и при постановке РСК выдерживают в водяной бане при 37°С-38°С в течение 15-35 мин (в зависимости от объема и толщины стенок сосуда) при периодическом перемешивании, а при постановке РДСК - в холодильнике. При смешивании компонентов раствор гемолитической сыворотки вносят во взвесь эритроцитов.
Исследуемые и контрольные (бруцеллезная и негативная) сыворотки крови крупного рогатого скота в исходном разведении 1:5 инактивируют в день постановки реакции в водяной бане: для РСК - при 60°С-62°С в течение 30 мин (сыворотки крови ослов и мулов - 64°С-65°С, буйволов - 62°С-64°С, свиней - 58°С-60°С); для РДСК - сыворотки крови животных всех видов - при 63°С-64°С в течение 30 мин.
Рабочие разведения всех компонентов для РСК (РДСК) готовят перед постановкой реакции и проверяют их на антикомплементарные и гемотоксические свойства по следующей схеме, представленной в таблице 1.
Таблица 1 - Проверка антикомплементарных и гемотоксических свойств компонентов реакций
Наименование и объем компонентов реакции, см | Антиком- | Гемотоксичность | |||
компле- | гемоли- | антигена | 0,85%-ный раствор хлористого натрия | ||
Комплемент в разведении 1:20 | 0,2 | 0,2 | - | - | - |
Гемолитическая сыворотка в рабочем разведении | 0,2 | - | 0,2 | - | - |
Антиген в рабочем разведении | 0,4 | - | - | 0,4 | - |
Эритроциты, 2,5%-ная взвесь | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 |
0,85%-ный раствор хлористого натрия | - | 0,6 | 0,6 | 0,4 | 0,8 |
Водяная баня 10 мин при 37°С-38°С | |||||
Результат | Гемолиз | Полная задержка гемолиза эритроцитов | |||
В реакциях используют компоненты, не обладающие антикомплементарными и гемотоксическими свойствами.
7.5.4 Проведение исследования в РСК
При массовом исследовании постановку реакции проводят в одной пробирке в разведении сыворотки 1:5 с антигеном, при постановке в трех пробирках исследуемые сыворотки исследуют в разведениях 1:5 и 1:10 с антигеном и 1:5 без антигена (контроль на антикомплементарность сывороток), (таблица 2).
Необходимые разведения сывороток готовят следующим образом:
- при массовом исследовании в одной пробирке к 0,05 см исследуемой сыворотки добавляют 0,2 см
0,85%-ного раствора хлористого натрия (разведение 1:5);
- при постановке реакции в трех пробирках в первую вносят 0,1 см исследуемой сыворотки, добавляют 0,4 см
0,85%-ного раствора хлористого натрия (разведение сыворотки крови 1:5 в объеме 0,5 см
) и смешивают. Из первой пробирки переносят 0,2 см
во вторую пробирку и 0,1 см
- в третью. В третью пробирку добавляют 0,1 см
0,85%-ного раствора хлористого натрия (разведение 1:10).
Инактивирование разведенных сывороток проводят в порядке, указанном в 7.5.3.3.
Сыворотку, 0,85%-ный раствор хлористого натрия и другие компоненты реакции вносят при помощи индивидуальных пипеток, (дозаторов), групповых дозаторов Флоринского или одноканальных пипеточных дозаторов с наконечником.
Постановку реакции проводят по схеме, представленной в таблице 2.
Таблица 2
Компоненты реакции | При массовом исследовании | При исследовании в двух разведениях | ||
пробирки с исследуемыми сыворотками (разведение) | пробирки для каждой исследуемой сыворотки (разведение) | |||
1 (1:5) | 1 (1:5) | 2 (1:5) | 3 (1:10) | |
Исследуемая сыворотка, см | 0,05 | 0,1 | 0,2 | 0,1 |
0,85%-ный раствор хлористого натрия, см | 0,2 | 0,4 | - | 0,1 |
Водяная баня 30 мин при 58°С-65°С | ||||
0,85%-ный раствор хлористого натрия, см | - | 0,2 | - | - |
Антиген в рабочем разведении, см | 0,2 | - | 0,2 | 0,2 |
Комплемент в рабочем разведении, см | 0,2 | 0,2 | 0,2 | 0,2 |
Водяная баня 20 мин при 37°С-38°С | ||||
Гемолитическая система, см | 0,4 | 0,4 | 0,4 | 0,4 |
Водяная баня 20 мин при 37°С-38°С | ||||
Примечание - Допускается смешивание равных объемов рабочих разведений антигена и комплемента непосредственно перед внесением в пробирки. | ||||
При постановке реакции ставят следующие контроли:
- негативной и бруцеллезной сывороток в разведении 1:5 и 1:10 с антигеном и 1:5 без антигена (по схеме реакции);
- гемолитической системы (0,4 см гемолитической системы и 0,6 см
0,85%-ного раствора хлористого натрия) - полная задержка гемолиза;
- комплемента (0,2 см комплемента в рабочем разведении, 0,4 см
0,85%-ного раствора хлористого натрия и 0,4 см
гемолитической системы) - полный гемолиз;
- антигена (0,2 см антигена в рабочем разведении, 0,2 см
комплемента в рабочем разведении, 0,2 см
0,85%-ный раствор хлористого натрия и 0,4 см
гемолитической системы) - полный гемолиз.
При необходимости определения титра исследуемых проб сыворотки, разведения готовят следующим образом: в пробирки первого ряда (разведение 1:5) вносят по 0,8 см 0,85%-ного раствора хлористого натрия, 0,2 см
пробы сыворотки и смешивают пипетированием. В пробирки третьего, четвертого, пятого и шестого рядов вносят по 0,2 см
0,85%-ного раствора хлористого натрия. Пробы сыворотки из первого ряда пробирок вносят по 0,2 см
в пробирки второго и третьего рядов. В пробирках третьего ряда сыворотку смешивают, получая разведение 1:10; 0,2 см
разведения сыворотки вносят в пробирки четвертого ряда, смешивают, получая разведение 1:20, и так далее до шестого разведения 1:80. Из пробирок последнего ряда по 0,2 см
разведений сыворотки удаляют. В пробирки второго ряда вносят по 0,2 см
0,85%-ного раствора хлористого натрия (ряд без внесения антигена - контроль антикомплементарных свойств сыворотки). Постановку реакции проводят по схеме, представленной в таблице 2.
7.5.5 Реакция длительного связывания комплемента на холоде (РДСК)
7.5.5.1 Подготовка к исследованию
Сыворотки исследуют в разведениях 1:5 и 1:10 с антигеном и в разведении 1:5 без антигена (контроль на антикомплементарность сыворотки), при массовом исследовании реакцию проводят в одной пробирке в разведении сыворотки 1:5 с антигеном. Инактивирование разведенных сывороток крови и приготовление гемолитической системы проводят по 7.5.3.3.
Комплемент применяют в рабочем разведении 1:25 или 1:20 при титре 0,06-0,1 или в разведении 1:20-1:15 при титре 0,1-0,14.
Одновременно определяют титр гемолитической системы с использованием свежей или консервированной сыворотки по схеме, приведенной в таблице 3.
Учет результатов титрования проводят немедленно после выемки штатива из водяной бани.
Таблица 3
Компоненты реакции | Ряды пробирок в штативе | Номера пробирок | |||||||||
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | ||
Сыворотка в разведении 1:5, см | первый | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 |
второй | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | |
Водяная баня 30 мин при 63°С-64°С | |||||||||||
0,85%-ный раствор хлористого натрия, см | первый | - | - | - | - | - | - | - | - | - | - |
второй | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | |
Антиген в рабочем разведении, см | первый | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 |
второй | - | - | - | - | - | - | - | - | - | - | |
Комплемент в рабочем разведении, см | первый | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 |
второй | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | |
Холодильник 16-18 ч при 2°С-6°С | |||||||||||
Гемолитическая система, см | первый | 0,1 | 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | 0,7 | 0,8 | 0,9 | 1,0 |
второй | 0,1 | 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | 0,7 | 0,8 | 0,9 | 1,0 | |
Водяная баня 20 мин при 37°С-38°С | |||||||||||
Примерный результат | первый | ПГ | ПГ | ПГ | ПГ | ПГ | ПГ | ПГ | ЗГ | НГ | НГ |
второй | ПГ | ПГ | ПГ | ПГ | ПГ | ПГ | ПГ | ЗГ | ЗГ | НГ | |
Титром гемолитической системы считают наибольшее ее количество, в котором произошел полный гемолиз в обоих рядах пробирок с негативной сывороткой или в безантигенном ряду, если исследуемая сыворотка оказалась позитивной. Рабочая доза на один интервал ниже (например, при титре гемолитической системы 0,7 см, рабочая доза - 0,6 см
).
7.5.5.2 Проведение исследования
Внесение компонентов и последовательность постановки реакции проводят по схеме, приведенной в таблице 4.
Таблица 4
Компоненты | При массовом исследовании | При исследовании в трех пробирках | ||
пробирки с исследуемыми сыворотками (разведение) | пробирки для каждой исследуемой сыворотки (разведение) | |||
1 (1:5) | 1 (1:5) | 2 (1:5) | 3 (1:10) | |
Исследуемые сыворотки | 0,05 | 0,1 | 0,2 | 0,1 |
0,85%-ный раствор хлористого натрия | 0,2 | 0,4 | - | 0,1 |
Водяная баня 30 мин при 63°С-64°С | ||||
0,85%-ный раствор хлористого натрия | - | 0,2 | - | - |
Антиген в рабочем раведении | 0,2 | - | 0,2 | 0,2 |
Комплемент в рабочем разведении | 0,2 | 0,2 | 0,2 | 0,2 |
Холодильник 2-6°С 16-18 ч и 20 мин при комнатной температуре | ||||
Гемолитическая система в рабочей дозе | 0,6 | 0,6 | 0,6 | 0,6 |
Водяная баня 20 мин при 37°С-38°С | ||||
При постановке реакции ставят контроли:
- негативная и бруцеллезная сыворотки в разведении 1:5 и 1:10 с антигеном и в разведении 1:5 без антигена;
- гемолитическая система в рабочей дозе без сыворотки, антигена и комплемента (0,6 см гемолитической системы и 0,6 см
0,85%-ного раствора хлористого натрия) - полная задержка гемолиза;
- антиген с 0,85%-ным раствором хлористого натрия и гемолитической системой (0,2 см антигена в рабочем разведении; 0,4 см
0,85%-ного раствора хлористого натрия и 0,6 см
гемолитической системы) - полная задержка гемолиза.
7.5.6 Обработка результатов РСК и РДСК
Реакцию связывания комплемента и реакцию длительного связывания комплемента учитывают визуально. При постановке реакции в одной пробирке (при массовом исследовании) учет проводят один раз - сразу после извлечения штативов из водяной бани. При исследовании в трех пробирках - через 3-4 ч, когда в контрольных пробах с бруцеллезной сывороткой эритроциты осядут на дно пробирки, или на следующий день (в этом случае штативы с пробирками оставляют в холодильнике).
Результаты реакции оценивают в крестах по следующей схеме:
"++++" (четыре креста) - отсутствие гемолиза, надосадочная жидкость прозрачная и бесцветная, осадок 100% эритроцитов на дне пробирки;
"+++" (три креста) - гемолиз 25% эритроцитов, осадок 75% эритроцитов;
"++" (два креста) - гемолиз 50% эритроцитов, осадок 50% эритроцитов;
"+" (один крест) - гемолиз 75% эритроцитов, осадок 25% эритроцитов;
"-" (минус) - гемолиз 100% эритроцитов, осадок эритроцитов отсутствует, жидкость интенсивно окрашена гемоглобином.
Степень гемолиза эритроцитов при необходимости определяют по шкале, которую готовят перед учетом реакции. Для этого из штатива выбирают пять пробирок с полным гемолизом, сливают их содержимое в одну и разводят по схеме, представленной в таблице 5.
Таблица 5
Наименование компонентов | Номера пробирок | ||||
1 | 2 | 3 | 4 | 5 | |
Гемолизированная жидкость, см | 1,0 | 0,75 | 0,5 | 0,25 | - |
0,85%-ный раствор хлористого натрия, см | - | 0,25 | 0,5 | 0,75 | 1,0 |
Гемолиз, % | 100 | 75 | 50 | 25 | - |
Оценка в крестах | "-" | "+" | "++" | "+++" | "++++" |
Процент гемолиза эритроцитов в пробирках с исследуемыми сыворотками определяют путем сравнения со шкалой.
Реакцию считают:
- положительной - при задержке гемолиза на два-четыре креста в одном или в двух разведениях сыворотки (1:5 или 1:10) и полном гемолизе эритроцитов в контрольной пробирке (без антигена);
- сомнительной - при задержке гемолиза с оценкой в один крест в одном или двух разведениях сыворотки и полном гемолизе эритроцитов в контрольной пробирке (без антигена);
- отрицательной - при полном гемолизе эритроцитов в двух или трех пробирках.
7.6 Реакция иммунодиффузии (РИД) с О-полисахаридным антигеном (О-ПС)
7.6.1 Сущность метода состоит в выявлении бруцеллезных антител, основанном на способности антител и антигена диффундировать в агаровом геле и при взаимодействии образовывать комплекс антиген-антитело, наблюдаемый в виде линии преципитации.
7.6.2 Приготовление 0,8%-ного агар-агара и подготовка чашек Петри
Для приготовления 200 см агара 17 г хлористого натрия и 1,6 г микробиологического агар-агара переносят в стеклянную колбу вместимостью 500 см
, добавляют 200 см
дистиллированной воды.
Колбу закрывают непромокаемым материалом (пергаментной бумагой, фольгой и т.п.) и помещают на водяную баню, которую также накрывают для предотвращения испарения воды при кипении водяной бани. Для полного расплавления агара колбу выдерживают в водяной бане в течение 35-45 мин с момента закипания воды. В чашки Петри, помещенные на горизонтальную поверхность, вносят по 14-18 см расплавленного агара. Чашки оставляют в течение 1 ч с приоткрытыми крышками. После застывания агара чашки Петри закрывают крышками и помещают в холодильник при температуре от 2°С до 8°С, хранят не более 5 сут.
При помощи штампа в геле агара делают отверстия (лунки). В каждой чашке прорезают не менее шести семилуночных розеток, каждая из которых состоит из семи лунок: одна лунка в центре диаметром 3 мм, остальные шесть лунок диаметром 5 мм по окружности, расстояние между центральной и периферическими лунками - 3 мм. Образовавшиеся диски геля удаляют из лунок канюлей, соединенной с вакуумным или водоструйным насосом (или любым другим способом).
7.6.3 Проведение исследования
7.6.3.1 В РИД с О-ПС антигеном исследуют на бруцеллез сыворотку крови крупного и мелкого рогатого скота и северных оленей с целью дифференциации животных, инфицированных от вакцинированных; для дифференциации неспецифических реакций, обусловленных родственной с бруцеллами микрофлорой, в том числе иерсиниями.
Для исследования используют сыворотки крови животных неконсервированные и консервированные. Не консервированные сыворотки пригодны для исследования в течение 6 сут со дня взятия крови при условии хранения их при температуре от 4°С до 8°С. Сыворотки, консервированные фенолом или борной кислотой, пригодны для исследования в течение 30 сут; замороженные сыворотки - в течение 3 сут после однократного оттаивания. Мутные, проросшие, гемолизированные сыворотки исследованию на бруцеллез не подлежат.
7.6.3.2 Реакцию иммунодиффузии проводят в чашках Петри. В центральную лунку вносят 0,02 см О-ПС антигена, а в периферические - по 0,04 см
исследуемых сывороток крови.
На каждой чашке Петри ставят контроль с положительной бруцеллезной сывороткой (преципитирующей).
После внесения компонентов чашки Петри закрывают крышками и помещают во влажную камеру (эксикатор) и выдерживают при температуре от 18°С до 26°С.
7.6.4 Обработка результатов
7.6.4.1 Учет результатов проводят визуально в косом проходящем свете с помощью осветителя через 24 и 48 ч после постановки реакции.
Линии преципитации между лунками с антигеном и исследуемой сывороткой, сформировавшиеся через 24 ч, свидетельствует о положительной реакции.
Сыворотки крови, давшие линию преципитации через 48 ч, подлежат повторному исследованию.
Линии преципитации, сформировавшиеся через 24 или 48 ч при повторном исследовании, свидетельствуют о положительной реакции.
При получении положительного результата в реакции иммунодиффузии, животное признают больным бруцеллезом.
7.6.4.2 Применение РИД с О-ПС антигеном при диагностике бруцеллеза
а) крупного рогатого скота в случаях:
1) в благополучных по бруцеллезу хозяйствах, в которых не применяли вакцины против бруцеллеза, исследуют сыворотки крови животных, сомнительно или положительно реагирующие в РА и (или) РСК (РДСК);
2) в благополучных по бруцеллезу хозяйствах, в которых животных вакцинируют против бруцеллеза агглютиногенными вакцинами:
- для контроля эпизоотического состояния по бруцеллезу животных не ранее чем через 1,5 мес после вакцинации;
- для дифференциации положительных реакций, полученных в РА (не выше 200 ME) или (и) РСК (РДСК) не выше чем в разведении 1:10 по истечении 6 мес после введения вакцины;
3) в неблагополучных по бруцеллезу хозяйствах, в которых животных вакцинируют против бруцеллеза агглютиногенными вакцинами:
- через 1,5 мес и далее один раз в месяц в течение 6 мес после иммунизации или реиммунизации с целью раннего выявления больных бруцеллезом животных;
- через 6 мес после иммунизации (реиммунизации) для оздоровления стада от бруцеллеза в комплексе мероприятий, предусмотренных по профилактике и борьбе с бруцеллезом;
б) северных оленей в случаях:
1) в благополучных по бруцеллезу хозяйствах, в которых противобруцеллезные вакцины не применяют. Исследуют сыворотки крови животных, сомнительно или положительно реагирующие в РА и (или) РСК (РДСК);
2) в благополучных по бруцеллезу хозяйствах, где животных иммунизируют против бруцеллеза агглютиногенными вакцинами:
- для контроля эпизоотического состояния по бруцеллезу животных не ранее чем через 1,5 мес после вакцинации;
- для дифференциации положительных реакций, полученных в РА не выше 50 МЕ/см и (или) в РСК (РДСК) не выше чем в разведении 1:5 по истечении 6 мес после введения вакцины;
3) в неблагополучных по бруцеллезу хозяйствах, в которых вакцинируют против бруцеллеза агглютиногенными вакцинами:
- через 1,5 мес и далее один раз в месяц в течение 6 мес после иммунизации или реиммунизации с целью раннего выявления больных бруцеллезом животных;
- через 6 мес после иммунизации (реиммунизации) для оздоровления стада от бруцеллеза в комплексе мероприятий, предусмотренных по профилактике и борьбе с бруцеллезом;
в) овец и коз в случаях:
1) в благополучных по бруцеллезу мелкого рогатого скота хозяйствах, где противобруцеллезные вакцины не применяют:
- при исследовании сыворотки крови животных, сомнительно и положительно реагирующих в РА или (и) РСК (РДСК);
2) в благополучных по бруцеллезу мелкого рогатого скота хозяйствах, где проводится иммунизация животных противобруцеллезными агглютиногенными вакцинами:
- для дифференциальной диагностики бруцеллеза овец и коз не ранее чем через 5 мес, только после однократной их иммунизации противобруцеллезными агглютиногенными вакцинами;
- для дифференциации неспецифических реакций, обусловленных родственной с бруцеллами микрофлорой, в том числе и иерсиниями;
3) в неблагополучных по бруцеллезу мелкого рогатого скота хозяйствах:
- с целью более раннего выявления больных бруцеллезом животных не ранее чем через 5 мес, только после однократной иммунизации противобруцеллезными агглютиногенными вакцинами;
- при снятии ограничений с неблагополучных по бруцеллезу хозяйств одновременно с РБП или РА, РСК (РДСК).
7.7 Реакция иммунодиффузии (РИД) с R-бруцеллезным антигеном при диагностике бруцеллеза собак, вызываемым B.canis
7.7.1 Подготовка к исследованию
7.7.1.1 Приготовление 0,85%-ного раствора хлористого натрия
В 1 дм дистиллированной воды растворяют соответственно 8,5 г хлористого натрия. Растворы фильтруют дважды через бумажный фильтр. Растворы хранят в стеклянных бутылях, укупоренных резиновыми пробками при температуре от 2°С до 20°С и используют в течение 1 мес.
7.7.1.2 Приготовление 0,8%-ного геля агара по 7.6.2
7.7.1.3 Пробы сыворотки крови от собак исследуют в РИД в свежем или консервированном виде.
7.7.2 Проведение исследования
Для постановки реакции иммунодиффузии используют биологические чашки Петри разного диаметра. Для исследования до четырех проб - диаметром 40 мм, для исследования 6-40 проб - диаметром 90 мм.
В центральную лунку геля вносят 0,02 см антигена, в периферические - по 0,04 см
исследуемых проб сыворотки крови.
В каждой чашке ставят контроль антигена с негативной и R-бруцеллезной сывороткой для РИД.
Внутрь крышки каждой чашки вкладывают фильтровальной бумагу, вырезанную по размеру ее наружного диаметра, которую увлажняют фенолизированным 0,85%-ным раствором хлористого натрия. Чашку плотно прикрывают крышкой и оставляют при температуре от 18°С до 26°С.
7.7.3 Обработка результатов - по 7.6.4.
7.8 Реакция непрямой гемагглютинации (РНГА)
7.8.1 Сущность метода
Метод основан на выявлении бруцеллезным эритроцитарным антигеном специфических антител в сыворотке крови больных бруцеллезом животных или иммунизированных вакцинами против бруцеллеза животных.
7.8.2 Подготовка к исследованию
7.8.2.1 Приготовление 1%-ного раствора хлорамина
Для приготовления 1%-ного раствора хлорамина 1 г хлорамина растворяют в 100 см водопроводной воды. Раствор используют свежеприготовленным.
7.8.2.2 Приготовление хромовой смеси
В фарфоровую чашку вместимостью 300-500 см помещают 5 г тонкоизмельченного в фарфоровой ступке двухромовокислого калия или 6 г бихромата натрия, добавляют 100 см
концентрированной технической серной кислоты и осторожно нагревают на водяной бане до полного растворения двухромовокислого калия (бихромата натрия). Хромовую смесь хранят при комнатной температуре до момента изменения цвета с темно-оранжевого до темно-зеленого.
7.8.2.3 Подготовка планшетов
Планшеты подготавливают к работе следующим образом: новые, погружают на 20-30 мин в теплый раствор с моющим средством и каждую лунку моют в этом растворе вращательным движением ватной или ватно-марлевой пробки. Ершом не пользуются, во избежание повреждения поверхности лунки. Затем планшеты не менее 6 раз промывают проточной водопроводной водой, ополаскивают дистиллированной водой и сушат при комнатной температуре или в термостате.
Допускается обработка планшетов хромовой смесью в течение одних суток, затем их промывают проточной водопроводной водой, ополаскивают дистиллированной водой и сушат.
При работе лицо, руки, одежду защищают от попадания хромовой смеси.
Реакцию ставят на 0,85%-ном растворе хлористого натрия. Сыворотку бруцеллезную сухую регидратируют дистиллированной водой или 0,85%-ным раствором хлористого натрия.
7.8.3 Проведение исследования
Крупный рогатый скот, иммунизированный против бруцеллеза, исследуют в сроки, предусмотренные инструкциями по применению вакцин.
Мелкий рогатый скот, иммунизированный против бруцеллеза, в РНГА не исследуют.
Реакцию ставят с использованием набора для серологической диагностики бруцеллеза крупного и мелкого рогатого скота для РНГА.
Реакцию проводят в объеме 0,55 см (0,5 см
разведения сыворотки и 0,05 см
антигена) в пробирках Флоринского.
При массовых исследованиях постановку реакции можно проводить с использованием исследуемых сывороток в одном (исходном) разведении. После прогревания исследуемые и контрольные сыворотки по 0,25 см вносят в лунки планшетов и добавляют в них по 0,25 см
0,85%-ного раствора хлористого натрия.
В каждую лунку с разведением сыворотки вносят по 0,05 см антигена в рабочем разведении.
Содержимое лунок перемешивают до получения равномерной взвеси антигена в сыворотке, выдерживают при температуре от 18°С до 26°С в течение 3-4 ч и проводят учет реакции.
Сыворотки от неиммунизированного или иммунизированного неагглютиногенными противобруцеллезными вакцинами крупного рогатого скота исследуют с разведения 1:50. Исходное разведение 1:25 готовят путем внесения 0,1 см сыворотки в пробирки, содержащие 2,4 см
0,85%-ного раствора хлористого натрия.
Сыворотки от крупного рогатого скота, иммунизированного агглютиногенными противобруцеллезными вакцинами, исследуют с разведения 1:100. Исходное разведение 1:50 готовят путем внесения 0,1 см сыворотки в пробирку с 4,9 см
0,85%-ного раствора хлористого натрия или по 0,05 см
сыворотки и 2,45 см
0,85%-ного раствора хлористого натрия, если используются пробирки вместимостью до 5 см
.
Сыворотки от мелкого рогатого скота исследуют с разведения 1:25. Исходное разведение 1:12,5 готовят путем внесения 0,2 см сыворотки в пробирки, содержащие 2,3 см
0,85%-ного раствора хлористого натрия.
Одновременно с исследуемыми сыворотками аналогично готовят разведения контрольных сывороток: бруцеллезной и негативной.
Исследуемые и контрольные сыворотки в исходных разведениях в пробирках выдерживают в водяной бане, нагретой до 60°С-62°С в течение 30 мин.
При получении положительного результата исследования сыворотки крови животных в одном разведении, для определения титра гемагглютининов в РНГА постановку реакции проводят в четырех разведениях, при этом исходное разведение каждой сыворотки готовят заново.
Все сыворотки (исследуемые и контрольные) проверяют на отсутствие гемагглютинирующих свойств.
В лунки первого, второго, третьего и четвертого рядов планшета вносят по 0,5 см и пятого ряда по 0,25 см
0,85%-ного раствора хлористого натрия.
В лунки первого ряда добавляют по 0,5 см, а в лунки пятого ряда по 0,25 см
исследуемых и контрольных сывороток в исходном разведении. После смешивания путем пипетирования по 0,5 см
разведенных сывороток из лунок первого ряда переносят в лунки второго ряда, из лунок второго - в лунки третьего, из лунок третьего - в лунки четвертого, из лунок четвертого ряда по 0,5 см
разведенных сывороток удаляют.
Во все лунки первых четырех рядов с разведенными сыворотками добавляют по 0,05 см антигена в рабочем разведении, которое готовят путем смешивания равных объемов антигена и 0,85%-ного раствора хлористого натрия. В лунки пятого ряда вносят 0,05 см
взвеси несенсибилизированных эритроцитов в рабочем разведении (один объем несенсибилизированных эритроцитов + один объем 0,85%-ного раствора хлористого натрия).
Содержимое лунок перемешивают путем легкого постукивания по краю планшета до получения равномерной взвеси антигена в сыворотке, выдерживают при температуре от 18°С до 24°С в течение 3-4 ч и проводят учет реакции.
Результат контроля на самоагглютинирующие свойства исследуемых и контрольных сывороток должен быть отрицательным.
Допускается постановка реакции в два этапа: накануне готовят исходные разведения исследуемых и контрольных сывороток крови, прогревают при указанном выше режиме, хранят при температуре от 2°С до 8°С и на следующий день исследуют.
После постановки реакции планшеты выдерживают в 1%-ном растворе хлорамина или другом антисептическом растворе 1,5-2,0 ч. Впоследствии их моют, как указано выше.
7.8.4 Обработка результатов
Реакции учитывают визуально и оценивают в крестах по следующей схеме:
"++++" (четыре креста) - 100%-ная агглютинация эритроцитов, агглютинат в виде хорошо выраженного "зонтика" покрывает все дно лунки, возможно сползание и заворачивание краев агглютината в виде "зонтика";
"+++" (три креста) - 75%-ная агглютинация эритроцитов, агглютинат в виде хорошо выраженного "зонтика" меньшего диаметра, чем при оценке реакции на четыре креста. В центре лунки возможно образование с трудом различаемого кольца из осевших неагглютинированных эритроцитов;
"++" (два креста) - 50%-ная агглютинация эритроцитов, осевшие неагглютинированные эритроциты образуют на дне лунки ровное кольцо с зернистостью вокруг него;
"+" (один крест) - на дне лунки кольцо коричнево-красного цвета;
"-" (минус) - эритроциты оседают в виде компактной "пуговки" или колечка.
За титр антител принимают наибольшее разведение сыворотки, в котором произошла агглютинация эритроцитов с оценкой четыре или три креста. Реакции с оценкой два креста ("++"), один крест ("+") и минус ("-") считают отрицательными.
7.9 Иммуноферментный анализ (ИФА)
Сущность метода заключается в выявлении в образце сыворотки крови животных иммуноглобулинов класса G к бактериям рода Brucella.
7.9.1 Подготовка к исследованию
7.9.1.1 Приготовление растворов кислоты серной концентрацией 1 моль/дм и кислоты соляной концентрацией 1 моль/дм
по ГОСТ 25794.1 (пункт 2.1).
7.9.1.2 Приготовление рабочего раствора ФСБ-Т
ФСБ-Т - концентрированный раствор буфера (флакон N 1) разводят в 25 раз дистиллированной водой и тщательно перемешивают. Для этого содержимое одного флакона концентрата в объеме 26 см переносят в мерную колбу и доводят объем до 650 см
дистиллированной водой. Если в концентрате присутствуют кристаллы, то его перед разведением нагревают и тщательно взбалтывают. В случае использования одного или нескольких стрипов планшета в чистый флакон отбирают необходимое для данного исследования количество составных частей ФСБ-Т в соответствии с таблицей 6.
Таблица 6 - Разведения ФСБ-Т
Компоненты | Количество используемых стрипов | ||||||||||||
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | ||
Объем, см | Концентрат ФСБ-Т, см | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 | 22 | 26 |
Вода дистиллированная, см | 48 | 96 | 144 | 192 | 240 | 288 | 336 | 384 | 432 | 480 | 528 | 624 | |
Допускается хранить неиспользованный рабочий раствор ФСБ-Т в течение 5 сут в холодильнике при температуре от 2°С до 8°С.
Все остальные компоненты набора для ИФА по 5.3 готовы к употреблению.
Окисляющие агенты, ионы металлов, моющие средства на посуде могут разлагать ТМБ-субстрат. Во избежание ложных результатов необходимо тщательно отмывать посуду раствором кислоты серной концентрацией 1 моль/дм или кислоты соляной концентрацией 1 моль/дм
с последующей тщательной отмывкой водой дистиллированной.
7.9.2 Проведение исследования
7.9.2.1 Для исследования сывороток крови в ИФА отбирают необходимое количество стрипов, нумеруют их в соответствии с описью исследуемых проб водостойким маркером из-за возможного выпадения из рамки-держателя во время тестирования. Оставшиеся стрипы хранят в полиэтиленовом пакете с влагопоглотителем, при температуре от 2°С до 8°С.
7.9.2.2 Для внесения контрольных сывороток можно использовать любые лунки планшета. Для этого в лунку вносят по 100 мм К+ (флакон N 4), в две другие лунки планшета - по 100 мм
К- (флакон N 5). В остальные лунки планшета вносят по 80 мм
РБР-С (флакон N 2). При постановке ИФА на одном стрипе допускается использовать для К- и К+ по одной лунке.
7.9.2.3 В остальные лунки планшета с РБР-С вносят по 20 мм исследуемых сывороток. Раствор перемешивают пять раз пипетированием, не касаясь дна лунки, цвет РБР-С должен измениться: происходит незначительное просветление раствора.
7.9.2.4 После внесения проб сывороток планшет помещают в пластиковый пакет или накрывают крышкой и инкубируют 30 мин при температуре 37°С. После инкубации лунки освобождают от содержимого резким встряхиванием и пять раз промывают рабочим раствором ФСБ-Т, добавляя каждый раз по 300 мм раствора в лунку, и выждав определенное время (от 30 с до 1 мин), вытряхивают содержимое. Во время обработки большого количества планшетов можно оставлять их с промывочным раствором до 20 мин. Затем планшет подсушивают постукиванием по сложенной в несколько слоев фильтровальной бумаге. Во все используемые лунки планшета вносят по 100 мм
раствора конъюгата (флакон N 3); планшет помещают в пластиковый пакет или накрывают крышкой и выдерживают 30 мин при температуре 37°С.
После повторной инкубации проводят процедуру промывания лунок рабочим раствором ФСБ-Т по описанной выше методике. После промывки во все используемые лунки планшета вносят по 100 мм раствора ТМБ-субстрата (флакон N 6) и выдерживают 15 мин при температуре 37°С в темноте. По истечении указанного времени реакцию останавливают добавлением в каждую используемую лунку по 50 мм
стоп-реагента (флакон N 7).
7.9.3 Обработка результатов
Результаты ИФА регистрируют на спектрофотометре. Оптическую плотность измеряют при длине волны 450 нм. Нулевой уровень задают по воздуху. Результаты учитывают только в том случае, если в лунках с К- среднее значение оптической плотности (К-) не более 0,2 ед. о. п., а разница средних значений оптической плотности между (К+) и (К-) превышает 0,35 ед. оптической плотности.
Если значение оптической плотности исследуемого образца не превышает 0,3 ед.о.п., то результат анализа считают отрицательным (lg G к бактерии рода Brucella не определены).
Если значение оптической плотности исследуемого образца сыворотки попадает в интервал от 0,3 до 0,9 ед.о.п., то результат анализа сомнительный. Рекомендуется повторить исследование такой сыворотки, а в случае повторного сомнительного результата - провести исследование сыворотки, полученной из крови, взятой от данного животного повторно через 15-30 сут.
Если значение оптической плотности исследуемого образца превышает 0,9 ед.о.п., то результат анализа положительный.
Примечание - Для проведения ИФА могут применяться коммерческие тест-системы, использование которых проводится по инструкции производителя после валидации методики в лаборатории.
7.10 Иммунохроматографический анализ (ИХА)
7.10.1 Сущность метода
Сущность метода заключается в выявлении специфических антител к липополисахаридному антигену Brucella abortus и Brucella melitensis, содержащихся в сыворотке крови крупного рогатого скота и овец.
7.10.2 Подготовка к исследованию
Перед началом работы компоненты набора и анализируемые пробы сыворотки крови выдерживают в течение 30 мин при температуре от 18°С до 25°С.
7.10.3 Проведение исследования
7.10.3.1 Метод ИХА применяют для серологического исследования невакцинировованного крупного и мелкого рогатого скота; крупного рогатого скота, вакцинированного неагглюгиногенными (из штамма В.aborus* КВ17/100 или аналогичными) или слабоагглютиногенными бруцеллезными вакцинами (из штаммов В.abortus 82, 75/79-АВ или аналогичными), но не ранее чем через 8 мес после введения вакцины.
_____________
* Вероятно ошибка оригинала. Следует читать: В.aborus. - .
7.10.3.2 Для исследования используют пробы сыворотки крови животных с 4-месячного возраста без признаков гемолиза и бактериальной контаминации, объемом не менее 0,5 см.
7.10.3.3 Пробы сыворотки крови животных исследуют в разведении 1:5 с использованием компонента К2. Для этого во флаконы с компонентом К2, пронумерованные в соответствии с количеством исследуемых проб, добавляют по 0,2 см каждой исследуемой пробы сыворотки крови и перемешивают.
7.10.3.4 Компонент К1 извлекают из пакета и каждую тест-полоску в вертикальном положении (по стрелкам, направленным вниз) погружают до уровня ограничительной линии в подготовленную по 7.10.3.3 пробу сыворотки.
Через 10 мин тест-полоски извлекают из флаконов и помещают в горизонтальном положении маркированной стороной вверх на чистую сухую, не поглощающую влагу поверхность (эмалированный или металлический кювет).
Через 30 мин после начала анализа (но не позднее 40 мин) визуально учитывают результаты реакции.
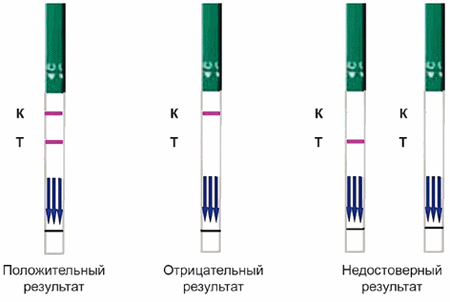
|
Рисунок 1 - Учет результатов иммунохроматографического анализа
7.10.4 Обработка результатов
Результаты реакции оценивают по наличию на тест-полосках линий розового цвета в К- и Т- зонах. Реакцию считают:
- положительной - при наличии на тест-полоске в Т- и К-зонах двух параллельных линий розового цвета. То есть в анализируемой пробе сыворотки крови содержатся специфические антитела к ЛПС антигену В.abortus и В.melitensis;
- отрицательной - при наличии окрашенной линии розового цвета только в К-зоне тест-полоски. То есть в анализируемой пробе сыворотки крови специфические антитела к ЛПС антигену В.abortus и В.melitensis отсутствуют;
- недостоверной - при наличии линии розового цвета только в Т-зоне или при отсутствии окрашенных в розовый цвет линий в Т- и К-зонах. В этом случае рекомендуется провести повторное тестирование пробы сыворотки крови с использованием новой тест-полоски.
8 Интерпретация результатов исследований
8.1 Диагноз на бруцеллез считают установленным в следующих случаях:
8.1.1 У животных всех видов, не вакцинированных против бруцеллеза живыми вакцинами:
- при положительном результате биопробы (за исключением животных, с момента иммунизации которых против бруцеллеза прошло менее 12 мес);
- положительном результате в РИД с О-ПС антигеном;
- повышении титра антител при повторном серологическом исследовании через 15-30 сут.
8.1.2 У крупного рогатого скота (буйволов, яков, зебу) не иммунизированного против бруцеллеза (B.abortus) или иммунизированного неагглютиногенными вакцинами, при положительном результате в РА с наличием 200 ME антител/см и (или) РНГА в титре 1:200, и (или) РСК (РДСК) - 1:10, и (или) - в РИД с О-ПС антигеном и (или) в ИФА.
8.1.3 У крупного рогатого скота, буйволов, яков, зебу, иммунизированного слабоагглютиногенными вакцинами, при положительном результате серологического исследования, проведенного в сроки, предусмотренные инструкцией по применению вакцины, в РА с наличием 400 ME антител/см и (или) РНГА в титре 1:400, и (или) РСК (РДСК) - 1:40, и (или) - в РИД с О-ПС антигеном и (или) ИФА.
8.1.4 У овец (коз), баранов-производителей, пробников, ярок, не иммунизированных противобруцеллезными вакцинами или иммунизированных против бруцеллеза (за исключением баранов-производителей и пробников) агглютиногенными вакцинами при положительном результате серологического исследования, проведенного в сроки, предусмотренные инструкцией по применению вакцины, при положительном результате в РА с наличием 100 ME антител/см и выше и (или) в РНГА в титре 1:100 и выше, и (или) в РСК - 1:10 и выше, и (или) в ИФА, и (или) в РИД с О-ПС антигеном, подтвержденном положительным результатом в одной из подтверждающих реакций.
8.1.5 У лошадей и верблюдов (В.abortus):
- в благополучных по бруцеллезу хозяйствах при положительном результате в РА с наличием 200 ME антител/см и выше и (или) РСК в титре 1:10 и выше.
8.1.6 У свиней (В.suis):
- при положительном результате в РБП и (или) аллергической пробе, подтвержденном положительной РСК (РДСК) в титре 1:5 и выше и (или) ИФА.
8.1.7 У оленей и маралов (B.suis):
- при положительном результате в РА с наличием 50 ME антител/см и выше и (или) в РСК в титре 1:10 и выше, и (или) в РИД с О-ПС антигеном, подтвержденном положительным результатом в одной из подтверждающих реакций.
8.1.8 У собак (В.abortus, В.suis, В.melitensis):
- при положительном результате в РА с S-антигеном с наличием 50 ME антител/см и выше и (или) в РСК в титре 1:5 и выше.
8.1.9 У собак (В.canis):
- при положительном результате в РА с R-антигенами в титре 1:100 и выше и (или) в РИД.
8.1.10 У пушных зверей:
- при положительном результате в РА с наличием 10 ME антител/см и выше, и (или) в РСК в титре 1:5 и выше.
8.1.11 У морских свинок:
- при положительном результате в РА с наличием 10 ME антител/см и выше.
8.2 При выявлении крупного рогатого скота, иммунизированного против бруцеллеза, положительно реагирующего при серологическом исследовании в РА с наличием не выше 200 ME антител/см и (или) в РСК в титре не выше 1:20; овец, коз, оленей (маралов) в РА - 25-50 МЕ/см
, и (или) в РСК в титре 1:5, эти же пробы сыворотки крови исследуют в РИД с О-ПС антигеном и ИФА.
При положительном результате исследования в РИД с О-ПС антигеном и (или) ИФА животных считают больными.
При невозможности проведения исследований в полном объеме из-за недостаточного количества сыворотки крови либо отсутствия диагностических тест-систем, проводят исследование сывороток крови от крупного рогатого скота (буйволов, яков, зебу), верблюдов и лошадей, овец, коз, оленей (маралов), взятых повторно через 15-30 сут в РА, РСК, РИД с О-ПС антигеном и ИФА.
При повышении титров РА и (или) РСК, и (или) положительном результате в РИД с О-ПС антигеном, и (или) в ИФА заболевание считают установленным.
При сохранении титров РА и (или) РСК на прежнем уровне или их снижении и отрицательном результате в РИД с О-ПС антигеном и ИФА заболевание исключают.
8.3 При выявлении среди не иммунизированного противобруцеллезными вакцинами крупного рогатого скота (буйволов, яков, зебу), верблюдов и лошадей, положительно реагирующих при серологическом исследовании в РА с наличием 50-100 ME антител/см и (или) в РСК - в титре 1:5; овец, коз, оленей (маралов) в РА - 25-50 МЕ/см
, и (или) в РСК в титре 1:5 эти же пробы сыворотки крови от крупного рогатого скота (буйволов, яков, зебу), верблюдов и лошадей, овец, коз, оленей (маралов) исследуют в РИД с О-ПС антигеном и ИФА (за исключением верблюдов, лошадей).
При положительном результате исследования в РИД с О-ПС антигеном и (или) ИФА животных считают больными.
При невозможности проведения исследований в полном объеме из-за недостаточного количества сыворотки крови либо отсутствия диагностических тест-систем проводят исследование сывороток крови от крупного рогатого скота (буйволов, яков, зебу), верблюдов и лошадей, овец, коз, оленей (маралов), взятых повторно через 15-30 сут, в РИД с О-ПС антигеном (за исключением верблюдов, лошадей) в РА, РСК и ИФА. При повышении титров в РА и (или) РСК, и (или) положительном результате РИД с О-ПС антигеном, и (или) ИФА заболевание считают установленным.
При сохранении титров РА и (или) РСК на прежнем уровне или их снижении и отрицательном результате в РИД с О-ПС антигеном и ИФА заболевание исключают.
8.4 При выявлении свиней, положительно реагирующих при серологическом исследовании в РСК в титре 1:5, эти же пробы сыворотки исследуют в РБП и дополнительно в ИФА и (или) самих животных исследуют аллергической пробой.
При положительном результате исследования в РБП и (или) ИФА и (или) аллергической пробе заболевание бруцеллезом считается установленным.
При невозможности проведения исследования в полном объеме сыворотку крови свиней отбирают повторно через 15-30 сут и исследуют в РСК, РБП и дополнительно в ИФА и (или) самих животных исследуют аллергической пробой.
При сохранении или повышении титров антител в РСК и положительном результате РБП и (или) ИФА и (или) аллергической пробы заболевание свиней считают установленным.
При сохранении титров в РСК на прежнем уровне или их снижении и отрицательном результате РБП, ИФА и аллергической пробы заболевание свиней считают не установленным.
8.5 Оценка результатов диагностических исследований в ИФА проводится согласно инструкции по применению соответствующих диагностических наборов (тест-систем). Для исследования целесообразно использовать тест-системы ИФА с О-ПС антигеном или аналогичным.
8.6 Животных всех видов неблагополучных по бруцеллезу пунктов, не иммунизированных и иммунизированных против бруцеллеза сомнительно и положительно реагирующих при серологическом исследовании в одной из подтверждающих диагноз реакций в сроки, предусмотренные действующими инструкциями по применению вакцин, считают больными бруцеллезом.
УДК 619:616.98:579.841.93:616-076:006.35 | МКС 11.220 |
Ключевые слова: животные, бруцеллез, диагностика, серологические реакции, интерпретация результатов | |
Электронный текст документа
и сверен по:
, 2017