ГОСТ ISO 16140-2011
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МИКРОБИОЛОГИЯ ПРОДУКТОВ ПИТАНИЯ И КОРМОВ ДЛЯ ЖИВОТНЫХ
Протокол валидации альтернативных методов
Microbiology of food and animal feeding stuffs. Protocol for the validation of alternative methods
МКС 07.100.30
Дата введения 2013-01-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Государственным научным учреждением "Всероссийский научно-исследовательский институт мясной промышленности имени В.М.Горбатова" Российской Академии сельскохозяйственных наук (ГНУ "ВНИИМП им.В.М.Горбатова" Россельхозакадемии) на основе собственного аутентичного перевода на русский язык международного стандарта, указанного в пункте 4
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии (Росстандарт)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 29 ноября 2011 г. N 40)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004 -97 | Код страны по МК (ИСО 3166) 004 -97 | Сокращенное наименование национального органа по стандартизации |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
Таджикистан | TJ | Таджикстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 13 декабря 2011 г. N 1474-ст межгосударственный стандарт ГОСТ ISO 16140-2011 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2013 г.
5 Настоящий стандарт идентичен международному стандарту ISO 16140:2003* Microbiology of food and animal feeding stuffs - Protocol for the validation of alternative methods (Микробиология продуктов питания и кормов для животных. Протокол валидации альтернативных методов)
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
Сведения о соответствии межгосударственных стандартов ссылочным международным стандартам и документу приведены в дополнительном приложении ДА.
Степень соответствия - идентичная (IDT).
Стандарт подготовлен на основе применения ГОСТ Р ИСО 16140-2008
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
Введение
Необходимость быстрой оценки микробиологических качеств сырья и готовых продуктов, а также микробиологического статуса методов приготовления в пищевой промышленности привела к разработке и усовершенствованию альтернативных методов микробиологического анализа, которые быстрее и/или проще в осуществлении, чем соответствующий стандартный метод, и некоторые из них можно автоматизировать.
Среди альтернативных методов есть такие, которые могут давать результаты, эквивалентные результатам стандартного метода, а результаты других могут заметно отличаться.
Поставщики и разработчики альтернативных методов, производители пищевых продуктов и напитков, службы здравоохранения и другие органы нуждаются в надежном общем протоколе валидации подобных альтернативных методов. Полученные данные могут также стать основой для сертификации метода независимой организацией.
Из-за большого числа методов, использованных лабораторией-организатором в сравнительном исследовании, представленном в настоящем стандарте, процедура не всегда подходит для "внутреннего" метода валидации альтернативного метода, применяемого отдельной лабораторией.
1 Область применения
Настоящий стандарт устанавливает основной принцип и технический протокол валидации альтернативных методов в сфере микробиологического анализа пищевых продуктов, кормов для животных, образцов окружающей среды и ветеринарных образцов (см. 5.1.1.2.1) для:
- валидации альтернативных методов, которые можно использовать, в частности, в рамках официального контроля;
- международного признания результатов, полученных альтернативным методом.
Настоящий стандарт также устанавливает основные принципы сертификации альтернативных методов, основанные на протоколе валидации, определенном в 4.1.
В тех случаях, когда альтернативный метод применяется на постоянной основе для внутрилабораторного использования и не требуется соответствие (более высоким) сторонним критериям контроля качества, может оказаться достаточной менее строгая сравнительная валидация альтернативного метода.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты*:
____________
* Таблицу соответствия национальных стандартов международным см. по ссылке. - .
ISO 3534-1 Statistics - Vocabulary and symbols - Part 1: General statistical terms and terms used in probability (Статистика. Словарь и условные обозначения. Часть 1. Общие статистические термины и термины, используемые в теории вероятности)
ISO 5725 (все части) Accuracy (trueness and precision) of measurement methods and results (Точность (правильность и прецизионность) методов и результатов измерений)
ISO/TS 11133-1 Microbiology of food and animal feeding stuffs - Guidelines on preparation and production of culture media - Part 1: General guidelines on quality assurance for the preparation of culture media in the laboratory (Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству культуральных сред. Часть 1. Общие руководящие указания по обеспечению качества приготовления культуральных сред в лаборатории)
3 Термины и определения
В настоящем стандарте применены следующие термины и соответствующие определения:
3.1 альтернативный метод (alternative): Метод анализа, обеспечивающий для продуктов данной категории обнаружение или оценку такого же аналита (3.4), какой измеряют с помощью соответствующего референтного метода (3.2).
Примечание 1 - Метод может быть патентованным или некоммерческим и не обязательно должен включать всю процедуру анализа от приготовления образцов до отчета об испытании.
Примечание 2 - Альтернативный метод должен обладать качествами, соответствующими нуждам пользователя, например:
- быстродействие проведения анализа и/или получения результата;
- простота выполнения и/или автоматизации;
- аналитические качества (прецизионность, точность, предел обнаружения и т.д.);
- миниатюризация;
- снижение затрат.
Примечание 3 - Термин "альтернативный" применяется для общего обозначения "процедуры испытания и реакционной системы". Этот термин включает в себя все компоненты - материальные и иные, необходимые для реализации метода.
3.2 референтный метод (reference): Принятый на международном уровне и широко применяемый метод.
Примечание - В настоящем стандарте под стандартным методом подразумеваются международные и европейские стандарты, а в случае их отсутствия - подходящие национальные стандарты эквивалентного статуса.
3.3 валидация альтернативного метода (validation of an alternative method): Процедура подтверждения соответствия того, что результаты, полученные альтернативным методом, сравнимы с результатами, полученными стандартным методом.
Примечание - Термин "сравнимы" определяется в настоящем стандарте техническим протоколом, адаптированным для метода каждого типа (см. разделы 5 и 6).
3.4 аналит (analyte): Компонент, измеряемый данным методом анализа. Это может быть микроорганизм.
3.5 качественный метод (qualitative method): Метод анализа, результатом которого является установление наличия или отсутствия аналита (3.4), обнаруживаемого прямо или косвенно в определенном количестве образца.
3.6 количественный метод (quantitative method): Метод анализа, результатом которого является количество аналита (3.4), измеренное прямо (подсчет по массе или объему) или косвенно (поглощение цвета, импеданс и т.д.) в определенном количестве образца.
3.7 сравнительное исследование методов (methods comparison study): Исследование, проводимое лабораторией-организатором, целью которого является сравнение альтернативного метода со стандартным методом.
3.8 межлабораторное исследование (inter-laboratory study): Исследование рабочих характеристик метода с использованием одних и тех же образцов в нескольких лабораториях под контролем лаборатории-организатора.
3.9 лаборатория-организатор (organising laboratory): Лаборатория с квалифицированными сотрудниками, имеющими опыт проведения сравнительного исследования и организации межлабораторного исследования.
Примечание - Для анализа результатов необходимо участие квалифицированного специалиста по статистическим исследованиям.
4 Общие принципы валидации и сертификации альтернативных методов
4.1 Протокол валидации
Протокол валидации включает в себя два этапа:
- сравнительное исследование (3.7) альтернативного (3.1) и референтного (3.2) методов в лаборатории-организаторе;
- межлабораторное исследование (3.8) каждого из двух методов.
Если это возможно, оба проводят параллельно.
Технические правила проведения сравнительного исследования методов и межлабораторного исследования представлены в разделах 5 и 6 соответственно в зависимости от того, является ли альтернативный метод качественным или количественным.
Если альтернативный метод прошел валидацию и соответствует требованиям другой организации, то для процедуры признания таких результатов предусмотрены специальные правила, приведенные в приложении А.
4.2 Принципы сертификации
4.2.1 При последующей сертификации альтернативного метода применяют (в дополнение к 4.1) два следующих принципа.
Подробные сведения о проведении сертификации (управление сравнительным исследованием методов и межлабораторным исследованием, перечень организаций, участвующих в процессе, включая экспертную лабораторию, называемую в настоящем стандарте "лабораторией-организатором", и приглашенных экспертов, сертифицирующий орган и т.д.) предоставляются сертифицирующим органом.
4.2.2 Изготовитель должен использовать систему качества, охватывающую весь ряд продукции, подлежащей сертификации и основанную на соответствующем стандарте, относящемся к системам качества (см. ISO 9001).
При выдаче сертификата сертифицирующая организация должна учитывать наличие сертификата системы качества, выданного сертифицирующим органом, аккредитованным в сфере систем качества.
4.2.3 После выдачи сертификата должна проводиться регулярная проверка качества сертифицированного метода. Должен регулярно проводиться аудит для установления соответствия:
- требованиям обеспечения качества (см. 4.2.1);
- требованиям контроля производства продукции (см. 4.2.1).
В дополнение к общим требованиям системы качества изготовитель регулярно предъявляет сертифицирующей организации обновленную документацию, учитывающую все изменения, внесенные в продукт или в процесс производства, которые могут отразиться на инструкциях по использованию метода и/или на рабочих характеристиках метода. После этого сертифицирующая организация решает, влияют ли внесенные изменения на результаты сертификации.
5 Качественные методы. Технический протокол валидации
5.1 Сравнительное исследование методов
5.1.1 Относительная точность, относительная специфичность и относительная чувствительность
5.1.1.1 Термины и определения
В рамках данного стандарта используются следующие термины и определения:
5.1.1.1.1 относительная точность () (relative accuracy): Степень соответствия между результатом, полученным стандартным методом, и результатом, полученным альтернативным методом, при исследовании идентичных образцов
(см. 5.1.1.3.1).
_________________
Труднодостижимо, если различаются этапы предварительного обогащения.
Примечание - Термин "относительная точность", используемый в настоящем стандарте, является дополнительным к терминам "точность" и "правильность", как они определены в ISO 5725-1 и в ISO 3534-1. В этих стандартах указывается, что точность - это "степень близости результата испытания и принятого опорного значения" и что правильность - это "степень близости среднего значения большого числа результатов испытания и принятого опорного значения". В настоящем стандарте в качестве принятого опорного значения выбрано значение, получаемое референтным методом. Таким образом, термин "относительный" указывает на то, что стандартный метод автоматически не дает принятое опорное значение.
5.1.1.1.2 положительное отклонение () (positive deviation): Альтернативный метод "ложноположителен", когда он показывает положительное отклонение, (т.е. получен положительный результат), в то время как стандартный метод дает отрицательный результат.
Положительное отклонение становится ложноположительным результатом, когда можно доказать, что истинный результат отрицателен.
Положительное отклонение считается "истинно положительным", когда можно доказать, что истинный результат положителен.
5.1.1.1.3 отрицательное отклонение () (negative deviation): Альтернативный метод показывает отрицательное отклонение (т.е. получен отрицательный результат), в то время как референтный метод дает положительный результат.
Отрицательное отклонение считается "ложноотрицательным", когда можно доказать, что истинный результат положителен.
5.1.1.2.4 относительная чувствительность () (relative sensitivity): Способность альтернативного метода обнаруживать аналит, когда его обнаруживает референтный метод (см. 5.1.1.3.1).
5.1.1.2.5 относительная специфичность () (relative specificity): Способность альтернативного метода не обнаруживать микроорганизм тогда же, когда его не обнаруживает референтный метод (см. 5.1.1.3.1).
5.1.1.2 Протокол измерений
5.1.1.2.1 Образцы пищевых продуктов
Для оценки чрезвычайно важно отобрать образцы пищевых продуктов, естественно контаминированные аналитом, подлежащим обнаружению при валидации.
Если метод нужно оценить для всех пищевых продуктов, то нужно изучить пять категорий пищевых продуктов. По просьбе изготовителя, это число категорий можно снизить до одной, двух, трех или четырех, если валидация альтернативного метода ограничена такими указанными категориями. Рекомендованные категории перечислены в приложении В.
Подходящие образцы окружающей среды также могут быть включены в качестве одной из категорий. Ветеринарные образцы можно считать еще одной категорией (см. приложение В).
Желательно, чтобы образцы пищевых продуктов происходили из как можно более широкой зоны распространения для уменьшения искажения, связанного со спецификой местной пищи, и для расширения диапазона валидации.
При анализе естественно контаминированных образцов диапазон и распределение контаминации образцов должны представлять все уровни, обычно присутствующие в этих продуктах, с упором на меньшее значение.
Если невозможно получить достаточное количество естественно контаминированных пищевых продуктов каждой категории, то допустимо использование искусственно контаминированных образцов. Метод и уровни искусственной контаминации должны обеспечивать подобие характеристик полученных образцов характеристикам естественно контаминированных образцов (см. методы инокуляции и ограничения в приложении С).
5.1.1.2.2 Число образцов
Суммарное число испытательных подобразцов для анализа равно 60 для каждой пищевой категории, выбранной из списка, приведенного в приложении В. Внутри каждой категории выбирают представительные типы пищевых продуктов и анализируют 20 испытательных подобразцов пищевого продукта каждого типа предлагаемым методом и референтным методом для получения минимум 60 результатов для каждой категории каждым методом. Для естественно контаминированных типов пищевых продуктов готовят образец, как описано в приложении D. Для искусственно контаминированных типов пищевых продуктов подстраивают уровни инокуляции таким образом, чтобы достичь частичного положительного выделения микроорганизмов в анализируемых испытательных подобразцах хотя бы одним из методов. Частичное выделение микроорганизмов достигается, когда в некотором числе, но не во всех, испытательных подобразцах обнаруживается положительный результат одним или обоими методами, альтернативным или референтным.
Желательно получить примерно 50% положительных результатов и 50% отрицательных. Это рекомендация, а не абсолютно требуемое процентное соотношение, при условии, что некоторое число испытательных подобразцов "положительно", а часть - "отрицательны" для одного и того же типа пищевого продукта.
5.1.1.2.3 Приготовление испытательных образцов
Референтный и альтернативный методы должны быть проведены, насколько это возможно, на одном и том же образце.
Так, если первая стадия обоих методов одинакова (например, тот же самый предварительно обогащенный бульон), то проводят репликацию на второй стадии (приложение D, случай 1).
В случае, когда первоначальная культуральная среда, методология или растворы различаются, готовят парные испытательные подобразцы для анализа. Имеются два основных метода для таких процедур приготовления.
В первом случае смешивают двойную навеску образца с равной по весу или объему навеской стерильной воды или другого подходящего разбавителя и тщательно гомогенизируют. Затем разделяют ее на два подобразца, обращая особое внимание на увеличение концентрации первичного обогащения примерно на 10% для компенсации эффекта разбавления разбавленного гомогенизированного образца (приложение D, случай 2).
Во втором случае непосредственно засевают образец пищевого продукта начальным посевным материалом в количестве, достаточном для получения частичного выделения микроорганизмов из анализируемых испытательных подобразцов хотя бы одним методом после того, как микроорганизмы пришли в состояние равновесия в образце пищевого продукта. Потом приготовляют испытательные подобразцы весом в 25 г и процедуру продолжают так, как описано в приложении D. Такая процедура предпочтительна для жидких продуктов, но может быть применима и для пищевого продукта любого типа при условии, что пищевой продукт тщательно гомогенизирован.
5.1.1.3 Вычисления и интерпретация результатов
5.1.1.3.1 Обработка данных
Парные данные референтного и альтернативного методов заносят в таблицу и вычисляют следующие параметры для каждой категории пищевого продукта (60 образцов), как указано в таблице 1.
Таблица 1 - Парные результаты референтного и альтернативного методов
Результаты | Референтный метод положителен ( | Референтный метод отрицателен ( |
Альтернативный метод положителен ( | +/+ положительное согласование ( | -/+ положительное отклонение ( |
Альтернативный метод отрицателен ( | +/- отрицательное отклонение ( | -/- отрицательное согласование ( |
Вычисления должны проводиться на ряде отрицательных результатов, полученных стандартным методом, число которых для результатов из таблицы 1 не может превышать удвоенное число положительных результатов. При необходимости можно выбирать отрицательные результаты, непосредственно следующие за положительным результатом, в порядке анализа образцов.
Используются три следующих критерия:
Относительная точность ():
![]() %.
%.
Относительная специфичность ():
![]() %.
%.
Относительная чувствительность ():
![]() %,
%,
где - суммарное число образцов (
![]() );
);
(Положительное отклонение (), отрицательное отклонение (
), отрицательное согласование (
), положительное согласование (
));
- суммарное число отрицательных результатов для референтного метода (
![]() );
);
- суммарное число положительных результатов для референтного метода (
![]() ).
).
5.1.1.3.2 Доверительные интервалы
Вычисление доверительных интервалов, связанных с числом испытанных образцов, приведено в приложении Е.
5.1.1.3.3 Несовпадающие результаты
Проверяют несовпадающие результаты, как описано в приложении F [критерий МакНемара (McNemar)], используя подсчет и
(см. 5.1.1.3.1).
Когда значения и
высоки и практически одинаковы, критерий МакНемара не позволяет установить статистическое различие между методами. В таком случае лаборатория-организатор должна постараться выяснить причины высоких значений
и
. Более того, из вышесказанного следует, что относительную точность метода нельзя интерпретировать, используя только критерий МакНемара.
5.1.1.3.4 Сводка вычислений
Все вычисления должны быть представлены в форме таблицы 2.
Таблица 2 - Вычисление относительной точности, относительной чувствительности и относительной специфичности
Матрицы | Сумма | Относительная точность АС (%) | Относи- | Относи- | ||||||
|
|
|
|
| ||||||
Пищевая категория 1 | ||||||||||
Пищевая категория 2 | ||||||||||
Пищевая категория 3 | ||||||||||
Пищевая категория 4 | ||||||||||
Пищевая категория 5 | ||||||||||
ВСЕГО |
5.1.1.3.5 Интерпретация результатов
Нужно сформировать таблицу, включающую необработанные результаты (то есть все положительные и отрицательные результаты из таблицы 1).
На основании числа положительных отклонений и числа отрицательных отклонений оценивают возможность альтернативного метода получать большее или меньшее число истинно положительных результатов, чем референтным методом.
В отчете об исследовании результаты, полученные с естественно контаминированными и искусственно контаминированными образцами, должны быть представлены раздельно.
Процедура искусственной контаминации испытательных образцов должна быть описана в отчете об исследовании.
Данные, опубликованные в других источниках и соответствующие условиям, указанным в приложении А, можно использовать для оценки относительной точности.
5.1.2 Относительный уровень обнаружения
5.1.2.1 Определение
В рамках данного стандарта под относительным уровнем обнаружения понимают наименьшее число культивируемых микроорганизмов (3.4), которое может быть обнаружено в образце в 50% случаев альтернативным и референтным методами.
5.1.2.2 Протокол измерений
Испытание проводят следующим образом:
- используют один пищевой продукт из каждой пищевой категории, выбранной по 5.1.1.2.1, с учетом области применения валидации (см. приложение В);
- используют пять разных целевых микроорганизмов (или меньше с учетом области применения валидации), каждый из которых предназначен для одной пищевой категории, если это возможно (определение целевых микроорганизмов приведено в приложении G.1);
- предпочтительно проводят испытания для пяти уровней (но минимум для трех уровней) по одному целевому микроорганизму на каждый пищевой продукт, включая отрицательный контрольный образец и т.д. Первым уровнем должен служить отрицательный контрольный образец. Вторым уровнем должен быть теоретический уровень обнаружения. Третий уровень - немного выше теоретического порога обнаружения, и все последующие уровни должны быть выше предыдущего. Можно использовать последовательные верхние уровни с концентрациями, разнящимися множителем, приблизительно равным 3;
- воспроизводят каждую комбинацию (пищевой продукт, уровень контаминации) шесть раз для испытания и альтернативным и референтным методами. Проводят разделение на уровне, где методы отличаются, как показано в приложении D. Таким образом, если этап 1 обоих методов одинаков (например, тот же предварительно обогащенный бульон), проводят разделение на этапе 2 (см. приложение D, случай 1). Если первый этап не одинаков, то есть культуральная среда, методология или степень разведения различаются, то смешивают удвоенную массу образца с равным по массе или объему количеством стерильной воды или другого подходящего разбавителя, а потом разделяют на два подобразца;
- используют полную процедуру альтернативного и референтного методов, включая подготовку образца. Засев каждого пищевого образца можно проводить до или после добавления культуральной среды.
Если нужно, то для обеспечения лучшей прецизионности на самом нижнем уровне посевного материала увеличивают массу пищевого образца или число реплик образцов. Например, можно использовать 75 г пищевого образца, контаминированного тремя клетками, вместо 25 г образца, контаминированного одной клеткой.
Чем больше число использованных уровней засева, тем точнее определение порога обнаружения.
5.1.2.3 Вычисления
Для каждого уровня (
от 0 до 3) и каждой комбинации пищевой продукт/штамм (
от 1 до 5) сравнивают оба метода, как указано в таблице 3.
Таблица 3 - Вычисление относительного уровня обнаружения
Метод | Результаты | ||
Отрицательные (-) | Положительные (+) | Всего | |
Референтный | |||
Альтернативный | |||
Всего |
|
| |
Для таблиц малого размера 2 на 2 использовать точные критерии Фишера.
5.1.2.4 Сравнения
Чтобы не проводить сравнение обоих методов на каждом уровне и для каждого продукта и штамма, можно использовать одно и то же испытание при сравнении двух продуктов/штаммов на одном и том же уровне.
Если есть основания считать, что продукт и штаммы сравнимы, то такое же испытание можно провести при >6 с объединением продукта/штаммов для каждого уровня
.
Уровни тоже можно объединять для проверок, но используя при этом ранжирование: ![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]() ,..., как с объединением продукта/штаммов, так и без объединения.
,..., как с объединением продукта/штаммов, так и без объединения.
В отчете указать все существенные различия между методами, продуктами/штаммами и/или уровнями.
5.1.2.5 Интерпретация результатов
Интерпретацию проводит лаборатория-организатор, на которую возложена ответственность за изучение методов сравнения.
Относительный уровень обнаружения лежит между двумя уровнями контаминирования, дающими соответственно уровень обнаружения менее и более 50%. Поэтому относительный уровень обнаружения представляют диапазоном.
5.1.3 Инклюзивность и эксклюзивность
5.1.3.1 Определение
Инклюзивность - это способность обнаружения с помощью альтернативного метода целевого аналита в широком диапазоне штаммов.
Эксклюзивность - это отсутствие интерференции от уместного для альтернативного метода диапазона нецелевых штаммов.
5.1.3.2 Протокол измерений
5.1.3.2.1 Выбор испытательных штаммов
5.1.3.2.1.1 Общие требования
Для устранения локальных отклонений используют диапазон микроорганизмов или штаммов.
Критерии для выбора испытательных штаммов приведены в приложении G.
Для каждого штамма должны быть приведены биохимические, серологические, а если уместно, то и генетические характеристики, подробные в степени, достаточной для установления их идентичности, и предпочтительно, чтобы штамм был изолирован от продукта. Кроме того, материал продукта, из которого он был выделен первоначально, должен быть известен и документирован.
5.1.3.2.1.2 Целевые микроорганизмы
Выбирают не менее 50 чистых культур микроорганизмов, подходящих для альтернативного метода и используемого пищевого продукта (см. G.3), за исключением случая Salmonella (сальмонеллы).
В случае методов для Salmonella выбирают не менее 30 чистых культур или микроорганизмов.
5.1.3.2.1.3 Нецелевые микроорганизмы
Выбирают не менее 30 чистых культур микроорганизмов из числа тех штаммов, что заведомо приводят к интерференции с целевыми микроорганизмами, и из числа штаммов, естественно содержащихся в каждом материале испытуемого продукта, включенного в валидацию (см. G.4).
5.1.3.2.2 Инокуляция
5.1.3.2.2.1 Общие требования
Каждое испытание производится однократно. Засев питательной среды производят с помощью разбавления чистой культуры каждого испытательного штамма. Образец продукта не добавляют.
5.1.3.2.2.2 Целевые микроорганизмы
Уровень засеваемой культуры должен быть в 10-100 раз больше минимального относительного уровня обнаружения для альтернативного метода. При этом нужно использовать полный протокол альтернативного метода, включая, если это необходимо, предварительное обогащение. В случае получения ложноотрицательных или сомнительных результатов штаммы нужно испытать повторно с привлечением референтного метода.
5.1.3.2.2.3 Нецелевые микроорганизмы
Уровень засеваемой культуры должен быть близок к наибольшему уровню контаминации, который ожидают обнаружить во всех категориях используемых продуктов.
Необходимо установить наличие эксклюзивности. Если конечная питательная среда культуральной среды представляет собой избирательную жидкую питательную среду (бульон), то такую среду заменяют на подходящую неизбирательную жидкую питательную среду. Если альтернативный метод дает положительные или сомнительные результаты с нецелевыми микроорганизмами, то испытание повторяют с использованием полного протокола. Измерения референтным методом проводят только один раз.
5.1.3.3 Представление результатов
Результаты представляют в виде таблицы 4.
Таблица 4 - Представление результатов по избирательности
Микроорганизмы | Результаты | |||
Референтный метод | Альтернативный метод | |||
Ожидаемый результат | Действительный результат | Ожидаемый результат | Действительный результат | |
Целевые штаммы | ||||
1 | ||||
2 | ||||
и т.д. | ||||
Нецелевые штаммы | ||||
1 | ||||
2 | ||||
и т.д. | ||||
5.1.3.4 Интерпретация результатов
Интерпретацию проводит лаборатория, на которую возложена ответственность за сравнительное изучение методов, причем в расчет должны приниматься как количественные, так и качественные аспекты (т.е. болезнетворность, распространенность, культуральные аспекты испытательных штаммов, например, подвижность, чувствительность к неблагоприятным факторам и т.д.).
Другие опубликованные данные по альтернативному методу, удовлетворяющие требованиям настоящего стандарта, также могут быть использованы лабораторией, отвечающей за сравнительное изучение методов, для получения дополнительной информации о вышеупомянутых критериях (см. приложение А, содержащее критерии признания сторонних результатов).
5.2 Межлабораторное исследование
Целью межлабораторного исследования является установление изменчивости результатов, полученных разными лабораториями при использовании идентичных образцов, и сравнение этих результатов с результатами, полученными при сравнительном исследовании методов.
5.2.1 Протокол измерений
5.2.1.1 Межлабораторное исследование должно включать в себя минимум 10 сотрудничающих лабораторий, результаты которых не содержат выбросы.
Указания и требования по организации, координации и проведению межлабораторных исследований приведены в приложении Н.
Необходимо, чтобы специалист по анализу результатов из каждой сотрудничающей лаборатории проявил достаточную компетентность в применении альтернативного и референтного методов до участия в самом исследовании.
5.2.1.2 Протокол включает следующие требования:
- для приготовления испытательных образцов используют одну подходящую пищевую матрицу (приложение В);
- протокол искусственной контаминации пищевого образца должен соответствовать выбранному пищевому субстрату. Каждый образец должен быть засеян индивидуально. Каждая "слепая" копия (реплика) должна быть приготовлена так, чтобы гарантировать гомогенность образцов при индивидуальном засеве каждой копии. Для установления гомогенности необходимо проанализировать соответствующее число образцов (см. приложение Н);
- необходимо использовать по меньшей мере три разных уровня контаминации: первым уровнем должен быть отрицательный контрольный уровень, один уровень
должен быть немного больше уровня обнаружения альтернативного метода и один уровень
должен быть примерно в 10 раз больше уровня обнаружения (например, 0; 3 и 30 клеток / 25 г);
- каждая сотрудничающая лаборатория должна проанализировать по меньшей мере 8 "слепых" копий на каждом уровне контаминации референтным и альтернативным методами;
- для анализа готовят суспензию из каждого образца;
- анализ образцов должен быть проведен в каждой лаборатории в установленный день;
- исследуемые образцы культивируют в соответствии с приложением J. Так, если первый этап культивирования одинаков и для референтного, и для альтернативного методов, эту культуру используют для засева на каждом из последующих этапов (приложение J, случай 1). Если первичные культуры для каждого метода различны, то соответствующие реплики используют для индивидуального выполнения каждого метода (приложение J, случай 2);
- в любом случае комбинация "число уровней контаминации/число реплик/число выбранных лабораторий" должна быть подобрана так, чтобы для вычислений имелось не менее 480 результатов (по 240 для каждого метода).
5.2.1.3 Лаборатория-организатор на основании всех полученных данных (см. приложение Н.3) должна определить, какие результаты являются годными, а какие результаты являются выбросами, для должного учета при вычислении данных о точности. Смотри приложение K, в котором приведены рекомендации, определяющие микробиологические условия для отбраковки данных.
ПРЕДУПРЕЖДЕНИЕ - Результаты лабораторий-участников не следует исключать, если нет четкого объяснения имеющихся грубых ошибок.
5.2.2 Вычисления
5.2.2.1 Для каждого уровня положительные результаты для каждого метода внести в таблицы 5 и 6.
Таблица 5 - Положительные результаты для стандартного метода
Лаборатории | Уровень контаминации | ||
Лаборатория 1 | /8 | /8 | /8 |
Лаборатория 2 | /8 | /8 | /8 |
Лаборатория 3 | /8 | /8 | /8 |
и т.д. | /8 | /8 | /8 |
Всего | |||
| |||
Таблица 6 - Положительные результаты для альтернативного метода
Лаборатории | Уровень контаминации | ||
Лаборатория 1 | /8 | /8 | /8 |
Лаборатория 2 | /8 | /8 | /8 |
Лаборатория 3 | /8 | /8 | /8 |
и т.д. | /8 | /8 | /8 |
Всего | |||
| |||
5.2.2.2 Для уровня и для каждого метода вычислить выраженную в процентах специфичность
по формуле
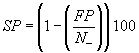 %,
%,
где - общее число всех испытаний для уровня
;
- число ложноположительных результатов.
5.2.2.3 Для каждого уровня контаминации и для каждого метода вычислить выраженную в процентах чувствительность по формуле
![]() %,
%,
где - общее число всех испытаний для уровней
и
, соответственно;
- число истинно положительных результатов.
5.2.2.4 Для каждого уровня контаминации и совокупности результатов сравнивают альтернативный метод с референтным методом для вычисления относительной точности и для изучения несовпадающих результатов.
Каждую пару результатов, полученных на образце, измеренном альтернативным и стандартным методами, представляют в таблице 7.
Таблица 7 - Парные результаты альтернативного и референтного методов, полученные в межлабораторном исследовании
Альтернативный метод | Референтный метод | Всего | |
+ | + | - | |
+ | |||
- | |||
Всего | |||
Вычисляют относительную точность , выраженную в процентах, по формуле
![]() %,
%,
где - число испытанных образцов (для уровня
или для всех уровней);
- число положительных согласований (positive agreement);
- число отрицательных согласований (negative agreement).
5.2.2.5 Вычислить доверительные интервалы для каждого соотношения (см. 5.1.1.3.2).
5.2.2.6 Изучить несовпадающие результаты в соответствии с приложением F, используя результаты подсчета и
(см. таблицу 8).
5.2.3 Интерпретация
Сравнивают (таблица 7),
и
(таблицы 5 и 6) с соответствующими им данными, полученными в сравнительном исследовании, включая естественно контаминированные образцы и относительный уровень обнаружения.
Эти критерии на самом деле не характеризуют внутрилабораторные и межлабораторные изменчивости метода (понятия повторяемости и воспроизводимости). В приложении L приведены дополнительные критерии (согласованность результатов в одной лаборатории, соответствие результатов в разных лабораториях и коэффициент расхождения между согласованностью и соответствием), которые можно использовать при изучении такой изменчивости (критерии повторяемости и воспроизводимости определены для количественных методов, и их как таковые нельзя использовать применительно к качественным методам).
6 Количественные методы. Технический протокол валидации
6.1 Общие требования
Число колоний микроорганизмов в данном образце является наиболее распространенным результатом стандартных количественных методов. Записывают всю информацию - массу образца, серию разбавления, объем посевного материала и число колоний при каждом разбавлении. В микробиологии эти дискретные данные часто сокращают, например, проводят подсчет колоний только в чашках, содержащих менее 300 колоний, потом для получения конечного результата используют коэффициент расширения, обратно пропорциональный коэффициенту разбавления. Из-за наличия других факторов, влияющих на процесс роста микроорганизмов, а также в целях получения симметричного распределения или квазинормального распределения данные подсчета часто преобразуют в логарифмический вид или в значения квадратного корня. Целесообразность такого преобразования можно проверить, используя гистограммы с набором экспериментальных точек (30 или более), полученных при одинаковых условиях.
Разделы 6.2 и 6.3, в основном, относятся к валидации количественных методов сбора непрерывных данных (или данных в интервале значений), при этом отдельно включены замечания по подсчету числа микроорганизмов.
6.2 Сравнительное исследование методов
6.2.1 Линейность и относительная точность
6.2.1.1 Определения
6.2.1.1.1 линейность (linearity): Способность метода при использовании с заданной матрицей давать результаты, пропорциональные количеству аналита в образце, т.е. увеличению аналита соответствует линейное или пропорциональное увеличение результатов.
Примечание 1 - Характеристику результата или сигнальную функцию получают путем измерения зависимости сигнала или результата метода от концентрации аналита (доз) в различных образцах референтных материалов () с известными характеристиками. В микробиологии, где стабильный референтный материал практически отсутствует, эти "известные характеристики" можно получить путем многократных повторных измерений с использованием референтного метода.
После подгонки, сглаживания или обработки другим алгоритмом данных разработчик альтернативного метода должен создать монотонную модель во всей области применения метода для преобразования результатов измерений в значения, наиболее близкие к стандартным результатам. Подгоночная модель является первой (или исходной) градуировочной характеристикой и включает все градуировочные коэффициенты в области концентраций; она часто нелинейна. Но эти аспекты не включены в процедуру валидации.
Частью процедуры валидации является проверка градуировки, которая дает конечную градуировочную характеристику, устанавливающую соотношение между преобразованными результатами измерений и соответствующими "стандартными значениями" в одинаковой системе единиц. При использовании одинаковых шкал на осях эта характеристика должна быть линейной с отсекаемым на оси отрезком, равным нулю (одинаковыми наименьшими значениями), и наклоном 1 (при одинаковых масштабных единицах по осям) и правильно оцененными характеристиками разброса.
_________________
Их получают по стандартному методу с естественно контаминированными образцами, если недоступны референтные материалы и известные значения.
Не следует проводить экстраполяцию выше и ниже испытательных концентраций, кроме случаев, когда нужно изучить поведение вблизи "нулевой" концентрации.
Примечание 2 - При обработке результатов подсчетов микроорганизмов с помощью метода регрессии линейность не всегда правильно достигается для результатов подсчета, соответствующих низким уровням или широким диапазонам. Такие результаты подсчетов имеют квазипуассоновские распределения со среднеквадратическим отклонением воспроизводимости, пропорциональным корню квадратному из среднего подсчитанного числа микроорганизмов. При этом возникают те же трудности оценки, которые упомянуты в примечании к пункту 6.2.2.1.
6.2.1.1.2 точность (accuracy): Близость результатов испытания к принятому опорному значению величины (ISO 3534-1).
Примечание - Термин "точность", когда он относится к серии результатов испытаний, включает в себя сочетание случайных составляющих и общей систематической погрешности (смещения).
6.2.1.1.3 смещение (систематическая погрешность) (bias): Разность между математически ожидаемым результатом испытания и принятым опорным значением (ISO 3534-1).
Примечание - Смещение есть полная систематическая погрешность в отличие от случайной погрешности. Могут быть одна или несколько составляющих систематической погрешности, дающих вклад в смещение. Большему систематическому отклонению от принятого опорного значения соответствует большее значение систематической погрешности.
6.2.1.1.4 относительная точность () (relative accuracy): Степень соответствия между результатом, полученным референтным методом, и результатом, полученным альтернативным методом, при исследовании идентичных образцов (см. 5.1.1.1.1).
6.2.1.2 Протокол измерений
6.2.1.2.1 План
Для проверки градуировочной характеристики требуется большое число различных образцов (при возможности, референтные материалы - см. приложение С) и исследование нескольких уровней (доз или концентраций) в зависимости от диапазона концентраций для практического использования.
Для определения градуировочной характеристики требуется использование минимум пяти различных уровней аналита для каждого типа пищевого продукта. Уровни должны равномерно распределяться по всему исследуемому диапазону, включающему минимальный (равный или не равный нулю), центральный, максимальный и два промежуточных уровня. Шкалу следует выбрать до того, как выбраны уровни концентрации, и с учетом диапазона контаминации и ожидаемого предела обнаружения (
): линейную - для небольших диапазонов (например,
![]() или от
или от ![]() до
до ![]() ), включающих ноль, и логарифмическую - для широких диапазонов (например,
), включающих ноль, и логарифмическую - для широких диапазонов (например, ![]() ). При этом может измениться соотношение между среднеквадратическими отклонениями и средними значениями результатов (см. примечание в п.6.2.1.3.1).
). При этом может измениться соотношение между среднеквадратическими отклонениями и средними значениями результатов (см. примечание в п.6.2.1.3.1).
_________________
Графические примеры неприемлемых и приемлемых распределений результатов измерений приведены в приложении Р.
Приоритет отдается естественно контаминированным образцам. Термин "уровень" используется в значении концентрации аналита, предполагаемой априори. В принципе, оптимальный план для регрессионного анализа получают путем выбора подходящего и уместного диапазона концентраций аналита, исключения исследования образцов с аналогичными подсчетами микроорганизмов или исключения повторяющихся данных с одинаковыми результатами. Для жидкостей диапазон может быть получен путем разведений, но необходимо обеспечить гомогенность как жидких, так и твердых образцов.
Образцы на одном уровне должны быть независимо продублированы путем подготовки подобразцов. На каждом уровне анализируют одинаковое число подобразцов - по меньшей мере два, а в идеальном случае - от 5 до 10. Когда и в референтном, и в альтернативном методах используют одни и те же десятикратные разведения подобразцов, испытания дублируют на уровне чашек Петри (см. случай 1 приложения М). Когда десятикратные разбавления нужно проводить только в референтном методе, проводят исследование дублирующих образцов (см. случай 2 приложения М).
Чашки Петри в двух дупликациях засевают каждым десятикратным разбавлением.
Следовательно, для проверки градуировочной характеристики альтернативным методом проводят минимум 10 измерений (в идеальном случае - от 25 до 50 измерений) с использованием естественно контаминированных образцов.
При отсутствии референтных материалов невозможно корректно оценить точность альтернативного метода, и определяют только относительную точность путем измерения тех же подобразцов референтным методом.
6.2.1.2.2 Категории пищевых продуктов
Исследуют 5 категорий пищевых продуктов. Это число можно уменьшить до 1, 2 или 3 категорий, если альтернативный метод подлежит валидации только для такой заявленной категории (например, молочные продукты). Рекомендованные категории перечислены в приложении В.
Соответствующие образцы должны быть естественно контаминированы исследуемым аналитом.
В случае возможности использования образцов окружающей среды их нужно считать отдельной категорией (см. приложение В).
Желательно, чтобы образцы пищевых продуктов происходили из как можно более широкой зоны распространения, для того чтобы уменьшить смещения, обусловленные особенностями местного пищевого ассортимента, и расширить диапазон валидации.
Диапазон контаминации должен быть распространен на весь диапазон количественного испытания.
Если невозможно получить достаточное число естественно контаминированных образцов пищевых продуктов с нужными уровнями, то допустима искусственная контаминация некоторых образцов. Такие образцы должны составлять меньшинство в общем числе испытуемых образцов. Процедура искусственной контаминации должна обеспечивать получение образцов с характеристиками аналита, подобным таковым для естественно контаминированных образцов (см. приложение С, 2-й и 3-й случаи).
Таким образом, для каждой из пяти пищевых категорий и референтным, и альтернативным методами измеряют минимум пять уровней целевого аналита, причем каждый образец реплицируется одинаковое число раз (от 2 до 10), что составляет всего от 10 до 50 измерений для каждых метода и пищевой категории. Если полученные результаты дают основания полагать, что матрица негомогенна или по составу ее компонентов или из-за вариаций в концентрации целевого аналита по матрице, то необходимо провести исследование дополнительных образцов.
После раздельной оценки по каждой пищевой категории глобальная оценка градуировочной характеристики для всех категорий пищевых продуктов является полезным инструментом для идентификации возможных расхождений между областью применения, точностью и разбросом повторяемости во всем диапазоне аналита.
6.2.1.3 Вычисления
6.2.1.3.1 Общие требования
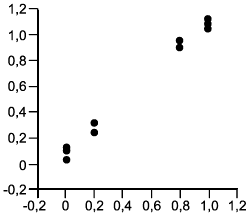
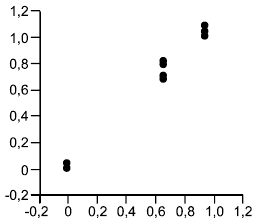
Перед тем как проводить какие-либо вычисления, строят график значений, представленных двумерными точками, для каждого образца для референтного и альтернативного методов, используя ось (вертикальную) для альтернативного метода, а ось
(горизонтальную) для референтного метода. Точки на каждом уровне должны образовывать дискретный кластер. Для обнаружения выбросов и нелинейности исследуют график визуально с целью обнаружения аномальных результатов, которыми являются те, что явно отдалены от соответствующего кластера. Если таковые имеются, то образец испытывают повторно, если это возможно. Если нет объяснения или результат по-прежнему остается вне кластера, то надо временно отбросить такой результат и повторить указанные ниже вычисления, чтобы оценить влияние отброшенного результата путем сравнения с вычислениями с учетом всех данных. Если это связано с эффектом разбавления, то внимательно исследуют эту возможность.
Если все кажется правильным, то используют программу линейной регрессии, которая дает возможность определить вероятность недостаточного согласования или нелинейности, и, что также возможно, программу регрессии с неравномерным взвешиванием (ISO 11095). Если доступна менее продвинутая программа вычислений или имеется только компьютер с меньшей производительностью, то требуемые вычисления приведены в п.6.2.1.3.2. Если простая линейная регрессия приводит к линейной аппроксимации (
![]() ), то ее коэффициента корреляции
), то ее коэффициента корреляции недостаточно для получения требуемой информации. Статистическая значимость
или наклона
не являются синонимами критерия линейности. В этом случае нужно проверить две гипотезы (
=0 и
=1).
________________
Или электронную таблицу, как в Excel.
Примечание - Если ошибка повторяемости по (или также по
) зависит от значения
(что, к сожалению, часто случается на практике), например прямо пропорционально увеличивающаяся ошибка, то лучше использовать сглаженную взвешивающую функцию (например, вес[
]=постоянная/дисперсия=постоянная/
), чтобы правильно аппроксимировать прямую линию
![]() с помощью метода линейной регрессии (аналогично методу взвешенных наименьших квадратов для взвешенных наименьших квадратов). Это приближает прямую к наблюдаемым точкам, которые имеют меньший разброс, и удаляет от точек с большим разбросом. При этом оценки наклона
с помощью метода линейной регрессии (аналогично методу взвешенных наименьших квадратов для взвешенных наименьших квадратов). Это приближает прямую к наблюдаемым точкам, которые имеют меньший разброс, и удаляет от точек с большим разбросом. При этом оценки наклона и отсекаемого отрезка
сильно зависят от такой процедуры взвешивания. Это трудный технический прием, предназначенный для статистического использования, и в настоящем стандарте не применяется. Дополнительные сведения можно найти в книгах по статистике, посвященным общему линейному моделированию GLIM/GLM, и т.д. (ISO 11095). Таким образом, если после сбора данных и изучения графиков регрессии вопрос о линейности остается сомнительным, рекомендуется использовать статистическую экспертизу для данного анализа.
6.2.1.3.2 Оценки с помощью метода регрессии
6.2.1.3.2.1 Принцип метода регрессии
В общем случае вертикальную ось (зависимую переменную) используют для альтернативного метода, а горизонтальную ось
(независимую переменную) - для референтного метода. Эта независимая переменная
должна быть точной, прецизионной и иметь вполне известные значения.
Если есть основания предполагать, что погрешность повторяемости , которая может возникнуть по
, сравнительно сопоставима или превышает таковую для
по
, то подгоночная функция
или
может привести к значительно отличающимся прямым линиям. В случае, когда среднеквадратичные отклонения повторяемости
и
сравнимы (соответственно по
и по
), вычисляют другие оценки (см. приложение R.3). Если повторяемость для
намного больше, чем для
, то меняют оси
на
и
на
для проведения регрессии
или используют регрессию
без перестановки осей (см. приложение R.4). При таких выборах (см. приложение R.2) используют критическую точку отсечения, равную 2, для отношения погрешностей повторяемости по
и
или обратного значения.
Подробности вычислений приведены в приложении R.
6.2.1.3.2.2 Дополнительные оценки
Если погрешности повторяемости или остаточная погрешность
сильно зависят от
(или от
), то есть остатки, кажется, явно увеличиваются или уменьшаются с
(или с
, то есть
не является константой), то подгоночная линия регрессии может быть неверной и может не проходить через точки с большей точностью. Более того, соотношение между
и
(или и
) может быть ненадежным в основной части диапазона измерений. В этом случае используют метод взвешенной регрессии.
Когда это представляется необходимым и для того, чтобы упростить этот шаг, можно использовать монотонные математические преобразования обеих осей и
. Например, преобразования
![]() и
и ![]() или
или ![]() и
и ![]() можно использовать для получения хорошей оценки для
можно использовать для получения хорошей оценки для (отрицательного или положительного, полуцелого или нет): выбор производят по визуальной оценке остатков или повторяемости
для каждого
. Постоянные погрешности соответствуют идеальному преобразованию.
При использовании такого преобразования отсекаемый на оси отрезок не должен очень сильно отличаться от нуля. Затем, когда проведены все оценки, как, например, оценки значений
и
, могут быть выполнены их обратные преобразования.
6.2.1.4 Интерпретация
6.2.1.4.1 Соотношение относительных точностей альтернативного и референтного методов оценивают с помощью линейной модели: ![]() .
.
При отсутствии систематической погрешности между методами (т.е. при идеальной точности) это уравнение переходит в уравнение , которое применимо в случае, когда характеристики методов эквивалентны. В этом случае отсекаемый отрезок теоретически равен нулю. Оценку величины отсекаемого отрезка
получают для обоих методов путем проверки гипотезы
![]() . Если альтернативный метод имеет систематическое смещение относительно референтного метода, то вероятность
. Если альтернативный метод имеет систематическое смещение относительно референтного метода, то вероятность ![]() менее
менее =0,005 (двухсторонний доверительный интервал).
Теоретический наклон линии, проходящей через точки, соответствующие общей истинной эквивалентности методов, равен единице. Оценочный наклон , полученный обоими методами, должен быть проверен при помощи гипотезы
![]() . Если альтернативный метод не дает достоверно совпадающих значений со значениями референтного метода, то вероятность
. Если альтернативный метод не дает достоверно совпадающих значений со значениями референтного метода, то вероятность ![]() менее
менее =0,05 (двухсторонний доверительный интервал). В этом случае альтернативный метод имеет систематическую погрешность относительно стандартного метода, зависящую от значений концентрации (
или
) и достигающую максимума на границах области.
6.2.1.4.2 Линейность или несогласование может быть представлено графически (приложение N). Лучшим является график остатков (см. приложение R.1). Строится не график зависимости значений от
(
=1 до
,
![]() ), а график зависимости оценочных остатков
), а график зависимости оценочных остатков ![]() от
от , который характеризует характер нелинейности, если она обнаружена с помощью функции
![]() , приведенной в приложении R.5.
, приведенной в приложении R.5.
6.2.1.4.3 Оценку точности методов с использованием ![]() получают, главным образом, на основании остаточного среднеквадратического отклонения
получают, главным образом, на основании остаточного среднеквадратического отклонения (см. приложение R). Такая оценка характеризует границы, в пределах которых специфицированная точность результата определяется с вероятностью 95% при
, приблизительно равном 2.
Соответствующие ![]() (см. приложение R) предпочтительнее для использования, так как они включены в справочную систему.
(см. приложение R) предпочтительнее для использования, так как они включены в справочную систему.
6.2.2 Обнаружение и предел количественного определения
6.2.2.1 Общие требования
Следующая характеристика связана с надежностью сигнала (или результата), полученного альтернативным методом, для определения ненулевой концентрации, измеренной референтным методом. Такая характеристика дает пределы прецизионности, включающие систематическую погрешность на нижнем крае области концентраций.
Фоновый шум, или "фон", (инструментального или иного происхождения) обычно определяют как минимум шестью независимыми холостыми измерениями. Результат такого измерения используют для корректировки общей систематической погрешности реальных измерений с помощью центрального (среднего) значения, и он служит важной оценкой разброса .
Часто, когда невозможно измерить или обнаружить величину ниже данного нижнего уровня, выбирают образцы с концентрацией микроорганизмов, близкой к первой оценке , взятой из предыдущей прямой линии для проверки градуировки:
![]() ,
,
где определено в приложении R. В окрестности такой концентрации оценивают среднеквадратическое отклонение, ожидаемое значение которого близко к
и которое используется вместо него. Другая процедура предусматривает использование среднего значения и среднеквадратического отклонения всех данных измерений самых низких доз, обнаруженных после реплицирования разведений по одной и той же схеме (коэффициент разведения от 1:2 до
1:10).
Примечание - Оценка среднеквадратического отклонения включает в себя много неопределенностей, в основном, связанных с диапазоном ниже нижнего уровня разведения. Таким образом, исходная оценка
(проводимая, по возможности, устойчивым методом
, приведенным в приложении Q) часто является достаточной для получения дополнительных оценок.
6.2.2.2 Определения
6.2.2.2.1 критический уровень () (critical level): Наименьшее (ненулевое) количество, которое можно обнаружить, но для которого нельзя получить точное количественное значение. Ниже этого уровня нельзя быть уверенным, что истинное значение не равно нулю.
Примечание - На этом уровне вероятность ложноотрицательных результатов равна 50% (
- статистическая ошибка второго типа, см. 6.2.2.4).
6.2.2.2.2 предел обнаружения () (detection limit): Больше, чем критический уровень (6.2.2.2.1), поскольку он включает показатель, т.е. доверительную вероятность
, который должен быть намного выше 50%, например 95%.
Например, ![]() среднее значение (холостое)+
среднее значение (холостое)+ (холостое), где
![]() есть гауссовское критическое значение при
есть гауссовское критическое значение при ![]() (односторонний доверительный интервал, см. 6.2.2.4) для достаточно большого числа
(односторонний доверительный интервал, см. 6.2.2.4) для достаточно большого числа холостых образцов.
6.2.2.2.3 предел количественного определения () (quantification limit): Наименьшее количество аналита (т.е. наименьшее реальное число организмов), которое можно измерить и количественно оценить с заданной прецизионностью и точностью в экспериментальных условиях метода, подлежащего валидации.
Примечание - Ассоциация химиков-аналитиков, состоящих на государственной службе, (AOAC), определяет предел количественного определения для количественных методов как ![]() . Это равноценно утверждению, что коэффициент изменчивости
. Это равноценно утверждению, что коэффициент изменчивости ![]() должен быть ниже 10% , см. [2].
должен быть ниже 10% , см. [2].
6.2.2.3 Протокол измерений и образцы
Для оценки базового или порогового разброса проводят по меньшей мере шесть (лучше 10) определений холостых образцов (отрицательных, с нулевой дозой или дозой, близкой к нулю).
Примечание - При подсчете числа организмов достаточно более пяти образцов на минимальном, не равном нулю, уровне, для того, чтобы удостовериться, что степень контаминации составляет <50%, когда не обнаруживается положительных образцов (доверительный уровень 95%). Если обнаруживается один положительный образец из пяти, то можно считать, что
>1%. Таким образом, если начать с трех доз аналита стандартного материала, выбранных из 3, 10, 30, 100, 300 и т.д. КОЕ/единица, и реплицируя каждый из них минимум шесть раз, можно оценить критический уровень (50%-ное обнаружение): например, в идеальном случае может быть следующее: 0/6 при 10, 2/6 при 30, 5/6 при 100, что дает оценку, близкую к 30 КОЕ/единица. Тем не менее, оценку, которую дает эта процедура, можно использовать (Данные о когерентном оценивании см. в приложении Р).
6.2.2.4 Вычисления
В общем случае критический уровень и предел обнаружения включают статистические ошибки двух типов: (соответствует определению несуществующей разницы (ложноположительный результат) и
(соответствует необнаружению истинной разницы (ложноотрицательный результат)). Показатель
является вероятностью достоверного определения значения, превышающего критический уровень (
).
Из результатов определений на холостом образце оценивают их среднеквадратическое отклонение
(по
, приложение R) и систематическую погрешность
медиане
, что свидетельствует об общей недостаточной специфичности, которая является статистически значимой, если
![]() (см. ниже).
(см. ниже).
Критический уровень ![]() (
( для альтернативного метода) для
=5% (и
=50%).
(Точнее, ![]() , где
, где является значением коэффициента Стьюдента для одностороннего уровня
и
степени свободы, для
=5% и
=6
=2,015, и при этом
![]() ; если
; если ![]() , то
, то ![]() ).
).
Предел обнаружения равен ![]() (
( для альтернативного метода) для
=5% и
=95%.
(Точнее, ![]() , где
, где является значением коэффициента Стьюдента для одностороннего уровня
и
степени свободы, например, для
=90% и
=6
=1,476, и при этом
![]() ; для
; для =80%,
=0,920).
Предел количественного определения ![]() (
( для альтернативного метода).
6.2.3 Относительная чувствительность и определение неизвестных образцов
6.2.3.1 Общие требования
Оценку чувствительности применяют для того, чтобы убедиться, что значения, получаемые альтернативным методом, заметно не отличаются от таковых для стандартного метода (разница менее 30%).
6.2.3.2 Определение
6.2.3.2.1 относительная чувствительность метода () (relative sensitivity): Способность альтернативного метода обнаруживать два разных количества аналита, измеренных референтным методом в заданной матрице с заданным средним значением или по всему диапазону измерения; т.е. это - минимальное изменение количества (увеличение концентрации
аналита), которое приводит к значимому изменению измеряемого сигнала (результат
).
Примечание - Относительная чувствительность отличается от предела обнаружения (6.2.2), так как ее вычисляют для каждого значения в диапазоне измерений. Она связана со статистическими ошибками двух типов (двухсторонний доверительный интервал) и
.
6.2.3.3 Вычисления
Протокол измерений и образцы описаны в 6.2.1.2.
Относительная чувствительность: ![]() для двухстороннего доверительного интервала с
для двухстороннего доверительного интервала с =5% и показателя
=95% при
![]() в соответствии с приложением R.6.2.
в соответствии с приложением R.6.2.
(Точнее, ![]() . Для
. Для =5% статистической мощности
=95% и
=5
=2,776 и
=1,533, при этом
![]() ).
).
Идентификация и определение неизвестных образцов: ![]() .
.
Строят график профиля прецизионности ![]() или график зависимости
или график зависимости ![]() от
от .
6.2.4 Специфичность, инклюзивность и эксклюзивность
6.2.4.1 Определения
6.2.4.1.1 специфичность (specificity): В настоящем стандарте определяется как степень, в которой на метод влияют (или не влияют) другие компоненты, присутствующие в многокомпонентном образце, т.е. способность метода точно обнаруживать данный аналит или измерять его количество в образце без интерференции со стороны нецелевых компонентов, таких как влияние матрицы или фоновый шум.
6.2.4.1.2 инклюзивность и эксклюзивность (inclusivity, exclusivity): В настоящем стандарте избирательность определяется как мера степени отсутствия интерференции при наличии нецелевых аналитов. Метод избирателен, если его можно использовать для обнаружения исследуемого аналита и если он гарантирует, что обнаруживаемый сигнал может происходить только от такого специфического аналита.
Критерий неприменим к суммарному числу жизнеспособных организмов.
6.2.4.1.2.1 Инклюзивность: Способность альтернативного метода обнаружить целевой аналит в широком спектре штаммов.
6.2.4.1.2.2 Эксклюзивность: Отсутствие интерференции от сопутствующего спектра нецелевых штаммов в альтернативном методе.
6.2.4.2 Протокол измерения
6.2.4.2.1 Образцы
В микробиологии (за исключением случая суммарного определения числа микроорганизмов, посеянных в чашки Петри) инклюзивность и эксклюзивность устанавливаются с помощью анализа:
- минимум 30 положительных чистых штаммов (исследуемого аналита);
- минимум 20 отрицательных чистых штаммов (аналитов, отличных от исследуемого) из культур, отличающихся тем, что они обычно создают постоянную и устойчивую интерференцию с целевым аналитом.
Выбирают положительные и отрицательные штаммы, которые часто контаминируют исследуемый пищевой продукт(ы). Для штаммов, не принадлежащих к данному набору, проводят полную идентификацию различных испытываемых штаммов. Необходимо знать источник происхождения штаммов, не входящих в набор.
Критерии для выбора штаммов приведены в приложении G.
Чистые штаммы из лабораторных культур составляют испытываемые образцы. Уровень инокуляции для каждого микроорганизма фиксируют на уровне, в 100 раз превышающем порог обнаружения целевых штаммов.
Каждый образец, содержащий штамм, анализируют дважды.
6.2.4.2.2 Протокол измерений
Специфичность, инклюзивность и эксклюзивность референтного метода не нужно устанавливать, если они уже известны.
6.2.4.3 Представление результатов
Характеристика избирательности дается только описательно (см. таблицу 8) относительно предела обнаружения целевого аналита, и поэтому вычисления не требуются. Отсутствие инклюзивности и эксклюзивности - это часть общей недостаточности специфичности (см. также систематическую погрешность в п.6.2.1.4).
Таблица 8 - Представление результатов для инклюзивности и эксклюзивности
Испытанный штамм | Референтный метод. Ожидаемый или полученный результат, уровень инокулята и т.д. | Альтернативный метод. Результаты (указать уровень обнаружения, и т.д.) |
(Единичное испытание) | Дупликат | |
Целевые штаммы | ||
и т.д. | ||
Нецелевые штаммы | ||
и т.д. |
Опубликованные данные, соответствующие требованиям настоящего стандарта, лаборатория-организатор, на которую возложена ответственность за сравнительное исследование методов, также могут использовать для получения информации, дополнительной к вышеуказанным критериям (см. приложение А, в котором приведены критерии для признания сторонних результатов).
6.2.4.4 Интерпретация
Для надежного использования необходимо оценить, соответствует ли альтернативный метод спецификациям изготовителя, а также конкретным требованиям.
6.2.5 Дополнительные характеристики альтернативного метода
Для альтернативного метода документируют все относящиеся к делу характеристики, влияющие на работу метода, например стабильность, достоверность, устойчивость или повышенная надежность и т.д.
6.3 Межлабораторное исследование
6.3.1 Общие требования
Проводят совместное исследование для сравнения рабочих характеристик (точности и прецизионности) альтернативного метода и референтного метода.
Рекомендации для лаборатории-организатора, относящиеся к совместному исследованию, приведены в приложении Н (также см. ISO 5725-2).
6.3.2 Термины и определения
В настоящем стандарте используются следующие термины и определения:
6.3.2.1 точность (accuracy): Степень близости результатов измерений к принятому опорному значению (ISO 3534-1).
Примечание - Это примерно оценивается как систематическая ошибка, которая является системной частью ошибки.
6.3.2.2 прецизионность (precision): Степень близости независимых результатов испытаний, полученных в конкретных регламентированных условиях повторяемости и воспроизводимости (см. 6.3.5 и 6.3.6) (ISO 3534-1).
6.3.2.3 выброс - резко отклоняющееся значение (outlier): Экстремальное значение, которое обычно случайным образом проявляется менее чем в 1% испытаний, но более часто в случае возникновения аномальных ситуаций. Для количественной оценки соответствующей вероятности нужно использовать соответствующие критерии.
Примечание - "Устойчивый" подход, используемый в настоящем стандарте, не исключает из рассмотрения выброс, за исключением того случая, когда имеются явные свидетельства разумного микробиологического обоснования. Такой подход можно использовать или в виде испытательной процедуры для обнаружения выброса, или для "устойчивых" статистических оценок.
6.3.3 Протокол измерений и образцы
6.3.3.1 Межлабораторное исследование проводят минимум в восьми сотрудничающих лабораториях, имеющих результаты без выбросов.
Оценки точности и прецизионности вычисляют по большому числу дублирующих результатов испытаний. Полученное значение должно включать в себя минимум 96 результатов для одной выбранной пищевой матрицы.
Рекомендации и требования к организации, координации и проведению межлабораторных исследований приведены в приложении Н.
На лабораторию-организатор возложена также ответственность за подготовку протокола испытаний и таблицы данных (см. ниже) для записи всех экспериментальных данных и критических экспериментальных условий, использованных каждой лабораторией (см. приложение Н.3).
Необходимо, чтобы специалист по анализу результатов из каждой сотрудничающей лаборатории проявил достаточную компетентность в применении альтернативного и референтного методов до участия в самом исследовании.
6.3.3.2 Протокол включает в себя следующие требования:
- нужно использовать одну подходящую пищевую матрицу (см. приложение В);
- концентрации аналита должны быть выбраны так, чтобы они включали, по меньшей мере, нижний, средний и верхний уровни всего диапазона для альтернативного метода. Лаборатория-организатор должна подтвердить гомогенность образцов;
- должен быть включен отрицательный контрольный образец; можно использовать пищевые образцы, искусственно контаминированные целевым аналитом;
- для сравнения альтернативного и референтного методов должны использоваться одни и те же образцы для обоих методов. Четыре подобразца на каждом уровне (или две аликвотные пробы, каждую из которых измеряют обоими методами) приготовляют для каждой лаборатории. Такие образцы кодируют слепым образом, но снабжают этикетками так, чтобы два из них измерялись референтным методом и два - альтернативным;
- жидкие образцы (по сравнению с твердыми образцами) обеспечивают большую гарантию гомогенности, если их приготавливают и рассылают без изменения микробиологического состава и правильно используют. В особых случаях может оказаться необходимым разделить образцы прямо перед измерением обоими методами;
- анализ образцов нужно проводить в каждой сотрудничающей лаборатории и в лаборатории-организаторе в указанный день с использованием сходных партий сред и комплектов оборудования для испытаний;
- округление результатов должна проводить лаборатория-организатор. После группировки результатов каждой из лабораторий окончательные табулированные данные для каждого уровня () аналита должны быть представлены, как показано в таблице 9.
Таблица 9 - Представление результатов межлабораторного исследования для каждого уровня () аналита
Лаборатории ( | Методы ( | |||
Референтный метод (кодированный) | Альтернативный метод (кодированный) | |||
Дупликат 1 | Дупликат 2 | Дупликат 1 | Дупликат 2 | |
1 | ||||
2 | ||||
и т.д. | ||||
6.3.4 Вычисления
6.3.4.1 В микробиологии данные не всегда подчиняются нормальному, т.е. гауссовскому, статистическому распределению.
Распределение данных можно проверить, если имеется достаточное число значений (намного более 30 результатов) - все для одного уровня. Часто для получения более симметричного распределения немногочисленные отсчеты лучше преобразовать в логарифмы. Также можно использовать более сложные процедуры.
Часто бывает трудно получить надежные оценки (среднее, среднеквадратическое отклонение и т.д.) с малой систематической погрешностью, особенно при наличии выбросов. ISO 5725 включает в себя критерии резко отклоняющихся значений, т.е. выбросов, для того чтобы отбросить неблагоприятно влияющие значения и получить лучшую оценку; однако при этом уменьшается число значений, используемых для статистического анализа.
Поэтому для того, чтобы избежать таких трудностей, в настоящем стандарте используют устойчивые оценочные алгоритмы, которые нечувствительны к экстремальным значениям и, более того, не слишком зависят от распределения данных. Кроме того, такие алгоритмы позволяют сохранить данные лабораторий с экстремальными значениями, если исключение данных не подтверждено вескими микробиологическими обоснованиями. Используют три согласованных значения для каждой из лабораторий-участников:
- оценку глобального центра (для оценок систематической погрешности): срединное значение (медиану) (вместо среднего значения
);
- оценку разброса между средними значениями дупликатов, включая воспроизводимость , основанную на значении рекурсивной медианы
(6) (см. приложение Q), вместо классического среднеквадратического отклонения (
);
- оценку типичного внутреннего разброса, среднеквадратического отклонения повторяемости, полученного из срединного значения (медианы) среднеквадратических отклонений дупликатов: ![]() , вместо классического обобщенного среднеквадратического отклонения, основанного на среднем значении дисперсий.
, вместо классического обобщенного среднеквадратического отклонения, основанного на среднем значении дисперсий.
6.3.4.2 Для каждого метода (например, 1 - стандартный, 2 - альтернативный) и уровня
аналита производят вычисления в соответствии с таблицей 10.
Таблица 10 - Представление результатов межлабораторного исследования по оценке согласованных значений для каждого метода
Уровень | Реплики | |||
1 | 2 | |||
Лаборатория ( |
|
| ||
2 | ... | ... | ... | ... |
... | ||||
N | ... | ... | ... | ... |
МЕДИАНА: |
|
| ||
Устойчивая | ||||
Константы =1,1926 и
=1,4826; только последняя константа зависима от того, что используются только дупликаты (значения двух лабораторий), а не большее число реплик
.
__________________
Константа вычисляется по формуле
![]() , где
, где значению
- квадрат для
=0,5 {здесь
=0,455} и
степеней свободы в повторных результатах (здесь для дубликата
=2-1).
соответствует следующей процедуре, в которой не используется оценка центра:
![]() . Она включает два этапа последовательного вычисления медианы:
. Она включает два этапа последовательного вычисления медианы:
- по каждому из значений вычисляют медиану (
) абсолютных разностей этого значения с другими значениями; и
- оценка разброса - это медиана медиан этих отклонений, подсчитанных в предыдущем шаге (например, см. приложение Р).
Примечание - Более совершенные процедуры отсутствуют. Абсолютное отклонение медианы для значений, вычисленных по процедуре ианы (или
), равно
![]() . Это устойчивая оценка разброса симметрична относительно оценки центра (
. Это устойчивая оценка разброса симметрична относительно оценки центра ().
Для распределения Гаусса: ![]() . Другая сопоставимая альтернатива основана на межквантильном диапазоне
. Другая сопоставимая альтернатива основана на межквантильном диапазоне ![]() 3-я - 1-я квартили; для распределения Гаусса
3-я - 1-я квартили; для распределения Гаусса ![]() . Последний результат легко получить с помощью процедур программы EXCEL
. Последний результат легко получить с помощью процедур программы EXCEL.
__________________
Использовать следующие статистические функции Excel:
![]() (диапазон) для 2-й квартили и
(диапазон) для 2-й квартили и ![]() (диапазон;
(диапазон; ), где
=1,2 или 3 для 1-й, 2-й и 3-й квартилей.
6.3.5 Относительная точность
6.3.5.1 Определение
В настоящем стандарте принятые опорные значения, используемые в определении правильности, задаются только результатами, полученными референтным методом на идентичных образцах.
Таким образом, отклонение результатов измерений, полученных альтернативным методом, лучше соответствует относительной точности.
6.3.5.2 Вычисления
Для каждого уровня аналита вычисляют
![]() для всех лабораторий
для всех лабораторий =1 до
,
где ![]() - среднее дупликатов лаборатории
- среднее дупликатов лаборатории , полученное альтернативным методом;
![]() - среднее дупликатов лаборатории
- среднее дупликатов лаборатории , полученное стандартным методом.
Таким образом, медиана ![]() , равная систематической погрешности
, равная систематической погрешности , и устойчивое среднеквадратическое отклонение
![]() порождают
порождают -образную статистику:
![]() с
с степенями свободы (
).
По таблице распределения Стьюдента находят вероятность того, что
=0. (Например, для
![]() критическое значение для двухстороннего доверительного интервала с
критическое значение для двухстороннего доверительного интервала с =0,05 равняется
![]() =2,201). Если
=2,201). Если ![]() , то систематическая погрешность
, то систематическая погрешность между двумя сравниваемыми методами значима, т.е. альтернативный метод имеет недостаточную точность относительно референтного метода для такого уровня
.
Соотношение между относительной точностью и уровнями можно моделировать (постоянная или пропорциональная систематическая погрешность и т.д.) с учетом линейности градуировочной характеристики.
6.3.5.3 Интерпретация
Предполагается нулевая систематическая погрешность (=0). Однако если оцененное абсолютное значение
слишком большое для цели данного метода или достигнута статистическая значимость, то альтернативный метод отличается от референтного.
6.3.6 Повторяемость
6.3.6.1 Термины и определения
6.3.6.1.1 повторяемость (сходимость) (repeatability): Характеристика близости согласования последовательных и независимых результатов анализа, полученных одним и тем же методом на идентичном испытуемом материале при одних и тех же условиях (оборудование, оператор, лаборатория и короткий промежуток времени, т.е. в условиях повторяемости).
6.3.6.1.2 предел повторяемости () (repeatability limit): Значение, которое с доверительной вероятностью 95% не превышается абсолютной величиной разности между результатами двух измерений (или испытаний), полученными в условиях повторяемости.
На практике, если разность между двумя результатами превышает (), результаты должны считаться сомнительными.
6.3.6.2 Вычисления
Для каждого метода и уровня
аналита вычисляют:
- предел повторяемости ![]() со
со среднеквадратическим отклонением повторяемости
;
- относительное среднеквадратическое отклонение повторяемости ![]() .
.
__________________
Константа
![]() с
с 1,960 и двухсторонним
=0,05 или 95% уровнем доверительной вероятности.
Повторяемость альтернативного и справочного методов проверяют, используя -распределение:
![]() с
с и
степенями свободы. По
-таблице определяют вероятность
того, что
![]() ; например, для
; например, для =12 критическое значение для двухстороннего доверительного интервала с
=0,05 равно
![]() =2,69.
=2,69.
Если или
больше
![]() , то тогда сравниваемые методы обладают разной повторяемостью для уровня
, то тогда сравниваемые методы обладают разной повторяемостью для уровня .
Соотношение между повторяемостью и уровнями можно моделировать так же, как относительное среднеквадратическое отклонение повторяемости. Дополнительные сведения содержатся в ISO 5725.
6.3.6.3 Интерпретация
Предполагается сопоставимая повторяемость для каждого уровня аналита. Однако, если получена статистическая значимость ![]() (двухсторонний доверительный интервал), альтернативный метод отличается от референтного.
(двухсторонний доверительный интервал), альтернативный метод отличается от референтного.
В настоящее время отсутствуют критерии для отбраковки альтернативного метода.
6.3.7 Воспроизводимость
6.3.7.1 Термины и определения
В настоящем стандарте используются следующие термины и определения:
6.3.7.1.1 воспроизводимость (reproducibility): Характеристика близости согласования между отдельными результатами испытаний на идентичном испытательном материале, полученными с использованием одного и того же метода операторами в разных лабораториях с использованием разного оборудования (т.е. в условиях воспроизводимости)
6.3.7.1.2 предел воспроизводимости () (reproducibility limit): Значение, которое с доверительной вероятностью 95% не превышается абсолютной величиной разности между результатами двух измерений (или испытаний), полученными в условиях воспроизводимости.
На практике, если разность между двумя результатами превышает , результаты должны считаться сомнительными.
6.3.7.2 Вычисления
Значение вычисляют по среднеквадратическому отклонению воспроизводимости
и межлабораторному среднеквадратическому отклонению
для каждого метода
и каждого уровня
аналита:
- предел воспроизводимости ![]() со среднеквадратическим отклонением воспроизводимости
со среднеквадратическим отклонением воспроизводимости
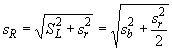 и
и ![]() лабораторной дисперсии при
лабораторной дисперсии при ![]() ;
;
- относительное среднеквадратическое отклонение воспроизводимости ![]() .
.
Воспроизводимости альтернативного и референтного методов сравнивают, используя -распределение:
![]() с (
с () и (
) степенями свободы. По
-таблице определяют вероятность
того, что
![]() , например, для
, например, для =12 (11
) критическое значение для двухстороннего доверительного интервала с
=0,05 равно
![]() =2,82. Если
=2,82. Если или
больше
![]() , то сравниваемые методы обладают разной воспроизводимостью для уровня
, то сравниваемые методы обладают разной воспроизводимостью для уровня .
Можно моделировать соотношение между воспроизводимостью и уровнями, а также относительную воспроизводимость ![]() . Дополнительные сведения содержатся в ISO 5725.
. Дополнительные сведения содержатся в ISO 5725.
После этого оценить вероятность того, что однородность "межлабораторного разброса", представляющего собой лабораторные различия, меньше, чем их собственный типичный разброс измерений:
![]() с
с ![]() и
и ![]() степеней свободы. По
степеней свободы. По -таблице определяют вероятность
, характеризующую важность межлабораторной дисперсии
.
6.3.7.3 Интерпретация
Предполагается сопоставимая воспроизводимость для каждого уровня аналита. Однако, если получена статистическая значимость ![]() (двухсторонний доверительный интервал), альтернативный метод отличается от референтного (в худшую или лучшую сторону в зависимости от
(двухсторонний доверительный интервал), альтернативный метод отличается от референтного (в худшую или лучшую сторону в зависимости от ).
В настоящее время отсутствуют критерии для отбраковки альтернативного метода.
Соотношение ![]() в целом верно. Однако это зависит от результатов метода и контекста применения. Вероятность наличия неоднородности при большом разбросе между лабораториями обычно свидетельствует о том, что стандартизацию метода нужно усовершенствовать, т.е. рабочие инструкции не вполне понятны (формулировка, объяснения и т.д.), анализы проводятся некачественно (недостаточность квалификации) или присутствуют аномальные изменения во времени для реакций, культур и т.д., а также всех внешних условий в лаборатории.
в целом верно. Однако это зависит от результатов метода и контекста применения. Вероятность наличия неоднородности при большом разбросе между лабораториями обычно свидетельствует о том, что стандартизацию метода нужно усовершенствовать, т.е. рабочие инструкции не вполне понятны (формулировка, объяснения и т.д.), анализы проводятся некачественно (недостаточность квалификации) или присутствуют аномальные изменения во времени для реакций, культур и т.д., а также всех внешних условий в лаборатории.
Приложение А
(обязательное)
Особые правила для признания сторонних результатов, полученных ранее при использовании прежней системы валидации
А.1 Общие требования
Это касается данных, полученных с помощью Международных или Европейских стандартов и других стандартных методов.
А.2 Альтернативные методы, которые претерпели изменения или ранее прошли валидацию в соответствии с Международным или Европейским Стандартом
При оценке возможности того, можно ли имеющиеся сторонние данные признать в соответствии с настоящим стандартом, устанавливают, был ли альтернативный метод каким-либо образом изменен после того, как появились эти данные.
Если изменения были и они считаются серьезными, то результаты не могут быть признаны.
Если изменений не было или они были несущественными, то тогда нужно обратиться в службу менеджмента качества лаборатории, проводящей валидацию.
Если лаборатория-организатор не была аккредитована в соответствии с ISO/IEC 17025, то необходимо провести аудит для проверки калибровки, сред, температуры, оборудования, записей об обучении со времени, когда проводилась валидация. Результаты не могут быть приняты, если результаты аудита неудовлетворительны. Результаты аудита должны быть документированы письменно.
Если, однако, лаборатория-организатор признана на основании результатов аудита или лаборатория имела аккредитацию в соответствии с ISO/IEC 17025, то критерии валидации считаются достаточно надежными.
Также должна быть оценена информация о сотрудничающих лабораториях (их возможности и их практический опыт в обеспечении качества).
А.3 Альтернативные методы, которые не проходили валидацию с использованием референтного метода в соответствии с Международным или Европейским Стандартом
Прежние исследования приемлемы в соответствии с настоящим стандартом при условии, что:
- они были проведены в соответствии с протоколами валидации, одобренными авторитетной группой технических экспертов, и результаты таких исследований были ими полностью признаны;
- технические эксперты работали под эгидой международно признанных организаций, занимающихся методами валидации (например, AFNOR, NORVAL,AOAC International, AOAC Research Institute);
- процедуры валидации включают в себя исследования, соответствующие требованиям настоящего стандарта, по меньшей мере, к полному числу образцов и к пищевой матрице.
Если альтернативный метод прошел сличение с международно признанным референтным методом (как, например, AOAC International), который отличается в несущественных аспектах от референтного метода, соответствующего Международному или Европейскому стандарту, и если протокол близок к настоящему стандарту, то результаты могут быть признаны.
Если метод значительно отличается от референтного метода, соответствующего Международному или Европейскому стандарту, то проводят оценку с целью определения того, существенно ли влияют эти отличия на работу метода. Оценка проводится с учетом дополнительных данных (если они есть), необходимых для выяснения процедурных отличий и/или отличий, связанных с референтным методом (например, разный первичный обогащенный бульон). Если решения содержат утверждения, что стандартные методы имеют существенное отличие, то они должны быть документально обоснованы лабораторией-организатором. Должны быть оговорены данные, требуемые для объяснения предполагаемых отличий.
Приложение В
(справочное)
Классификация типов образцов для исследований по валидации
В.1 Образцы пищевых продуктов и кормов для животных
Таблица В.1 - Категории пищевых продуктов и связанные с ними основные пищевые патогенные микроорганизмы
Тип продукта | Yersinia spp. | Clostri- | Listeria monocy togenes | E.coil O157 & VTEC | Staphy- | S.aureus entero- toxins | Campy- | Salmo- | Bacillus cereus | |||
Мясные продукты | ||||||||||||
Сырые | x | x | x | x | x | x | ||||||
Прошедшие теплообработку | x | x | x | |||||||||
Замороженные | x | |||||||||||
Ферментированные | x | x | ||||||||||
Вяленые | x | x | x | x | x | |||||||
Другой | Блюда/ | Паштет | ||||||||||
Домашняя птица | ||||||||||||
Сырые | x | x | x | |||||||||
Прошедшие теплообработку | ||||||||||||
Замороженные | ||||||||||||
Другие | Блюда/соусы | |||||||||||
Рыба и морепродукты | ||||||||||||
Сырые | x | x | x | x | ||||||||
Прошедшие теплообработку | ||||||||||||
Замороженные | ||||||||||||
Копченые | x | x | ||||||||||
Другие | ||||||||||||
Фрукты и овощные продукты | ||||||||||||
Сырые | x | x | x | x | x | |||||||
Прошедшие теплообработку | ||||||||||||
Замороженные | ||||||||||||
Сушеные | x | |||||||||||
Ферментированные | ||||||||||||
Вяленые/соленые | ||||||||||||
Соки/концентраты | x | x | ||||||||||
Обезвоженные продукты/ продукты питания с умеренным обезвоживанием | ||||||||||||
Другие | Переработанные грибы | |||||||||||
Молочные продукты | ||||||||||||
Сырые | x | x | x | x | x | x | x | x | ||||
Прошедшие теплообработку | x | |||||||||||
Замороженные | x | x | x | x | x | x | ||||||
Ферментированные | x | x | x | x | x | x | ||||||
Сушеные | x | x | x | x | ||||||||
Другой | ||||||||||||
Шоколад/хлебобулочные изделия | ||||||||||||
Обезвоженные продукты/продукты питания с умеренным обезвоживанием | x | |||||||||||
Сушеные | x | |||||||||||
Другие | Кондитерские изделия | Завар- | ||||||||||
Другие продукты | ||||||||||||
Пиво | ||||||||||||
Соусы | ||||||||||||
Специи | x | x | x | |||||||||
Майонез | x | x | ||||||||||
Макароны | x | |||||||||||
Яйца и производные | x | |||||||||||
Зерновые/рис | x | |||||||||||
Корма для животных | ||||||||||||
Разное | x | |||||||||||
Таблица В.2 - Пищевые категории и связанные с ними основные непатогенные микроорганизмы
Тип продукта | Дрожжи и плесневые грибки | Молочно- | Общее число жизнеспособных организмов | Кишечная палочка | Escherichia coli |
Мясные продукты | |||||
Сырые | x | x | x | x | |
Прошедшие теплообработку | x | x | x | ||
Замороженные | x | x | |||
Ферментированные | x | x | |||
Вяленые | x | ||||
Другие | x | x | |||
Продукты из домашней птицы | |||||
Сырые | x | x | x | x | |
Прошедшие теплообработку | x | x | x | ||
Замороженные | x | x | |||
Другие | |||||
Рыба и морепродукты | |||||
Сырые | x | x | x | x | |
Прошедшие теплообработку | x | x | x | ||
Замороженные | x | x | |||
Копченые | x | x | x | ||
Другие | |||||
Фруктовые и овощные продукты | |||||
Сырые | x | x | x | x | |
Прошедшие теплообработку | x | x | |||
Замороженные | x | x | |||
Сушеные | x | x | x | ||
Ферментированные | x | ||||
Вяленые/соленые | x | ||||
Соки/концентраты | x | x | |||
Обезвоженные продукты/продукты питания с умеренным обезвоживанием | x | ||||
Другие | |||||
Молочные продукты | |||||
Сырые | x | x | x | ||
Прошедшие теплообработку | x | x | |||
Замороженные | x | x | x | ||
Ферментированные | x | ||||
Сушеные | x | x | |||
Другие | |||||
Шоколад/хлебобулочные изделия | |||||
Обезвоженные продукты/продукты питания с умеренным обезвоживанием | x | x | x | ||
Сушеные | x | x | |||
Другие продукты | |||||
Пиво | x | ||||
Соусы | x | x | |||
Специи | |||||
Майонез | x | x | |||
Макароны | |||||
Яйца и производные | |||||
Зерновые/рис | |||||
Корма для животных | |||||
Разное | x | x | |||
В.2 Ветеринарные образцы
Для скрининга сельскохозяйственных животных следующие образцы проверяют на наличие Salmonella.
Таблица В.3 - Ветеринарные образцы для Salmonella
Животное, продукт или его среда | Образец для анализа |
Дегенерированные яйца | Смешанная проба фекальных образцов |
Куры-несушки | Смешанная проба фекальных образцов |
Однодневные цыплята | Подстилочная солома из коробок |
Молодки племенной птицы | Объединенная выборка фекальных образцов |
Тушки племенной птицы | Объединенная выборка мекония |
Свежее мясо домашней птицы | Кусочки кожи с шеи или кусочки тканей |
Домашняя птица | Объединенная выборка фекальных образцов |
Свежая говядина, телятина и свинина | Мазки с поверхности туш, кусочки тканей и вытекающая жидкость |
Приложение С
(обязательное)
Использование естественно контаминированных образцов и приготовление искусственно контаминированных образцов для исследований по валидации
Необходимо проводить выбор типа пищевого продукта в категории так, чтобы увеличить долю естественно контаминированных образцов. В случае, если доступно лишь ограниченное число естественно контаминированных образцов, можно воспользоваться вторым вариантом, представленным ниже, для увеличения числа образцов. Третий вариант должен использоваться только в хорошо обоснованных случаях. Можно также использовать стандартные материалы, содержащие микроорганизмы, подвергнутые стрессу, предпочтительно с вполне определенными уровнями целевого аналита (микроорганизмов) и указанным сроком хранения.
1-й вариант | Естественно контаминированные образцы |
Используют образцы, собранные из продуктов, которые поточно анализирует лаборатория-организатор или другие лаборатории. Хранение должно минимизировать микробиологические изменения и уменьшить микробный стресс. Контаминация (качественная или количественная сообразно обстоятельствам) должна быть подтверждена немедленно перед исследованием. | |
2-й вариант | Контаминирование смесью |
Засевают жидкие и полутвердые испытываемые продукты путем разбавления естественно контаминированным образцом сходного типа. Фоновая микрофлора в "разбавленном продукте" должна быть сходного типа в состоянии стресса, подобным тому, что присутствует в естественно контаминированных продуктах. | |
3-й вариант | Образцы с добавлением известного количества определяемого вещества |
Если референтный материал | |
________________ | |
Определяют протокол создания стресса целевого микроорганизма, и во время засева должен наблюдаться стресс. | |
4-й вариант | Референтные материалы |
Референтные материалы, такие как сертифицированный референтный материал, содержащие подходящие и вполне определенные уровни целевого аналита (микроорганизмов) в стабильном стрессовом состоянии, можно использовать для внесения посевного материала в испытываемые образцы для анализа как качественными, так и количественными методами. Для качественных исследований их использование должно быть ограничено, когда в качестве референтных материалов доступны только несколько штаммов или серологических типов целевого аналита пищевого происхождения. | |
Приложение D
(обязательное)
Дупликация образцов для определения относительной точности и относительного уровня обнаружения для качественных методов
D.1 Случай 1 - Все условия первой стадии культивирования одинаковы для обоих методов
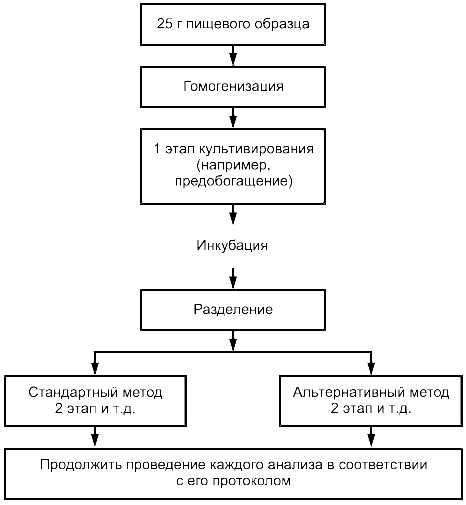
D.2 Случай 2 - Первая стадия культивирования обоих методов различается
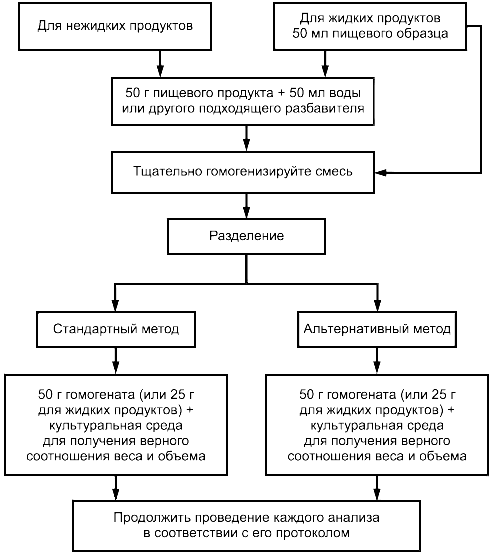
Примечание - Нужно отметить, что во втором случае из-за разбавления среды образцом и растворителем нельзя применять готовую к использованию среду, и концентрация ингредиентов в лабораторно приготовленном бульоне должна быть увеличена примерно на 10%.
Приложение Е
(обязательное)
Вычисление доверительных интервалов, связанных с числом испытуемых образцов
Для каждого значения () величин
,
и
, выраженных в процентах (см. 5.1.3.1), вычисляют доверительные интервалы (
):
________________
Объяснения этих сокращений см. в приложении U.
- если 10%<<90%, приблизительно вычисляют двусторонние доверительные интервалы при 95%
![]() с
с ![]() соответственно для
соответственно для (в %)=
,
,
;
- для 90% вычислить нижний доверительный предел при 95% (односторонний) с
![]() соответственно для
соответственно для (в %)=
,
,
.
В этом случае предпочтительно использовать биномиальную таблицу для =10, 20, 30, 40, 50, 60 (см. таблицу Е.1).
Таблица Е.1 - Нижний доверительный предел при 95% для =90% и больше
10 | 20 | 30 | 40 | 50 | 60 | |
| 0,75 | 0,83 | 0,82 | 0,84 | 0,83 | 0,84 |
0,92 | 0,85 | 0,83 | 0,85 | 0,86 | 0,87 | 0,88 |
0,94 | 0,85 | 0,88 | 0,88 | 0,89 | 0,89 | 0,89 |
0,96 | 0,85 | 0,93 | 0,92 | 0,91 | 0,93 | 0,93 |
0,98 | 0,95 | 0,93 | 0,95 | 0,96 | 0,95 | 0,96 |
0,99 | 0,95 | 0,98 | 0,98 | 0,96 | 0,97 | 0,98 |
Пример - Для =20,
=94%
(
; при 95%)=88%.
Приложение F
(обязательное)
Критерий, используемый для анализа несогласующихся результатов
Подсчитывают суммарное число несогласующихся результатов следующим образом:
![]() (например,
(например, =2,
=10, следовательно,
=12).
Проверяют, могут ли методы различаться из-за соотношения между чувствительностью и специфичностью:
- для 6 (менее шести рассогласований): испытание отсутствует;
- для 622 (т.е. между 6 и 22 рассогласованиями) определяют
как наименьшее из двух значений, т.е.
и
(например,
![]() , так как
, так как ![]() ), и используют биномиальный закон распределения в соответствии с таблицей F.1.
), и используют биномиальный закон распределения в соответствии с таблицей F.1.
Если ![]() для заданного
для заданного , то два метода различны при
0,05 (двухсторонний доверительный интервал).
Таблица F.1 - Значения М для рассогласований (6
22)
Рассогласования | От 6 до 8 | От 9 до 11 | От 12 до 14 | От 15 до 16 | От 17 до 19 | От 20 до 22 |
| 0 | 1 | 2 | 3 | 4 | 5 |
Например, для =12 рассогласований и
=2
=2 и
![]() , и таким образом, два метода различаются с
, и таким образом, два метода различаются с 0,05;
- для 22 (более 22 рассогласований) использовать критерий Мак-Немара с распределением хи-квадрат для 1 степени свободы:
![]() с
с ![]() и
и ![]() .
.
Методы различаются при 0,05 (двухсторонний доверительный интервал), если
3,841.
Этот критерий хи-квадрат соответствует минимальному для каждого
из следующей таблицы F.2 для
0,05 (т.е. для заданного
должно быть не меньше значения, приведенного в таблице F.2, чтобы сделать заключение о различии методов).
Таблица F.2 - Значения для рассогласований
(
22)
Рассогласования | От 22 до 26 | От 27 до 31 | От 32 до 37 | От 38 до 44 | От 45 до 51 | От 52 до 58 |
| 10 | 11 | 12 | 13 | 14 | 15 |
Приложение G
(обязательное)
Аспекты, подлежащие учету при выборе штаммов для испытания избирательности
G.1 Общие требования
Это приложение устанавливает минимальные требования к испытаниям для общего пользования. При выборе испытательных штаммов большинство последних должно происходить из диапазона пищевых материалов, используемых в исследовании, и охватывать рекомендованный диапазон целевого аналита с учетом следующих факторов: географическое распределение, распространенность, многообразие идентификационных характеристик, например биохимических характеристик, характеристик серотипа, типа бактериофага и т.д., и любые требования, сделанные разработчиками альтернативного метода.
G.2 Категории целевых групп
- Неопределенная группа, например суммарное число, бактерии группы кишечной палочки, дрожжевые грибки, молочнокислые бактерии;
- семейство, например Enterobacteriaceae;
- род, например Salmonella, Pseudomonas, Listeria;
- вид, например Listeria monocytogenes, Staphylococcus aureus, Escherichia coli;
- штамм, например Salmonella enteritidis тип бактериофага 4.
G.3 В соответствии с целевой группой, определенной в G.1, можно выбрать диапазон положительных микроорганизмов:
- для неопределенных групп, в которых целевая группа определена стандартным методом, используемые штаммы должны выбираться из тех, которые способны на типичный рост в референтном методе;
- для семейств: используют штаммы из диапазона родов в этом семействе и, если это возможно, включают представительный элемент всех родов семейства;
- для родов: используют диапазон видов из этого рода и, если возможно, испытывают все виды из такого рода;
- для видов: диапазон штаммов из этих видов. Определение штамма необходимо учитывать при принятии этого решения. В настоящее время патогены, такие как Salmonella и Listeria, были подразделены на серотипы, однако Listeria spp. также подразделяется на типы фагов; в будущем будут использоваться другие методы подразделения на генетические типы, такие как RAPD, PFGE и риботипирование. При определении положительных штаммов, которые будут использоваться в испытании, лаборатории-организаторы должны пользоваться доступной современной информацией для гарантии того, что эти штаммы в данное время являются подходящими к целевым пищевым категориям;
- для штамма: диапазон источников этого штамма.
G.4 Нецелевые группы, используемые в исследовании на избирательность
- Нецелевые группы (т.е. те, которые, как ожидается, должны дать отрицательный результат и которые используются в испытаниях на перекрестную реактивность) должны быть определены в соответствии с целевой группой;
- когда целевая группа - семейство: нецелевые штаммы должны включать семейства;
- когда целевая группа - род: нецелевые штаммы должны включать другие роды, которые считаются похожими на целевой род;
- когда целевая группа - вид: нецелевые штаммы должны включать другие виды внутри целевого рода;
- когда целевая группа - штамм: нецелевые штаммы должны включать другие штаммы из того же вида.
Приложение Н
(обязательное)
Рекомендации по организации и проведению совместных исследований
Н.1 Подготовка пищевых образцов
Отрицательные (контрольные) образцы
В общем случае должна использоваться только искусственная контаминация, и целевой аналит не должен присутствовать в незасеянной пище. Берут подходящее число образцов в соответствии с приложением J и анализируют их для подтверждения факта отсутствия целевого аналита. Отрицательные контрольные образцы используют в тех случаях, когда это предусмотрено во время пробного испытания.
Положительные образцы, содержащие целевой аналит
При некоторых количественных исследованиях, например испытаниях на суммарное число бактерий, дрожжей и плесневых грибков, бактерий группы кишечной палочки и т.д., для совместных исследований следует использовать естественно контаминированные образцы, содержащие целевой аналит и/или типичную микрофлору. В отсутствие подходящего числа естественно контаминированных образцов или в тех случаях, когда уровень контаминации слишком узок или непригоден, можно использовать искусственно контаминированные образцы. Образцы необходимо контаминировать, используя второй или третий вариант, описанный в приложении С. В случаях, когда используют стандартные материалы (приложение С), на лабораторию-организатора возложена ответственность за рассылку и референтных материалов, и подробных процедур инокуляции каждой сотрудничающей лаборатории.
В случае и качественных, и количественных методов пищевые материалы и целевой аналит/микроорганизмы должны допускать гомогенизацию и должны оставаться стабильными как при перевозке, так и в течение проведения анализов. Исследования на гомогенность и стабильность должны быть проведены перед отправкой испытательного материала из лаборатории-организатора.
Пищевой образец должен содержать характерную фоновую микрофлору или интерферирующие компоненты, которые также должны оставаться стабильными при перевозке и в ходе исследований, как это описано в приложении С.
Альтернативный метод должен испытываться с использованием минимум одного типа пищевого продукта, выбранного из пищевых категорий, ранее описанных в приложении В. Качество и пригодность пищевого продукта должны быть определены до исследования.
Характеристики выбранного на основе сравнительных исследований штамма микроорганизма (см. приложение G), используемого для валидации метода, должны быть типичными для искомого рода или вида, например темп роста, антигенные характеристики и чувствительность к вредным веществам и т.д.
Н.2 Транспортирование образцов
Лаборатория-организатор должна определить используемый тип пищевого продукта и проверить, подходит ли упаковка для предстоящей транспортировки.
Индивидуальные образцы должны быть дважды запечатаны для гарантии отсутствия протекания из одного образца, что нарушило бы целостность всех других образцов.
Каждая сотрудничающая лаборатория несет ответственность за передачу лаборатории-организатору подробных сведений, которые гарантируют то, что рассылка образцов для исследования будет соответствовать международным и национальным почтовым правилам.
Лаборатория-организатор должна проверить правильность рассылки образцов и методов распределения, послав набор образцов в сотрудничающую лабораторию с запросом об их немедленном возврате, для того, чтобы перед исследованием уточнить влияние условий пересылки (безопасность и стабильность микроорганизмов). Любые нежелательные влияния должны быть оценены и приняты меры для минимизации предотвращения их появления в будущем.
Для сохранения целевого аналита или естественно существующей микрофлоры неизменными во время распределения в сотрудничающие лаборатории может оказаться необходимым транспортировать образцы в охлажденном или замороженном состоянии. Лаборатория-организатор должна определить условия упаковки и наилучший способ транспортировки. В идеальном случае желательно предусмотреть средства для контроля температуры образцов при транспортировке.
Для каждой лаборатории должна быть предоставлена дополнительная посылка образцов, идентичная испытываемым образцам, для измерения температуры образцов при получении.
Н.3 Организация совместного исследования (см. ISO/TR 11133-1)
Н.3.1 Рабочие протоколы
Стандартные рабочие протоколы должны быть распределены между сотрудничающими сторонами для ознакомления и внесения комментариев до начала испытаний. Окончательный протокол должен быть опубликован до начала оценивания.
Н.3.2 Подтверждение качества образцов
Каждая сотрудничающая лаборатория должна получить указание подсчитать общее бактериальное число в обозначенном образце. Лаборатория-организатор должна направить каждой сотрудничающей лаборатории стандартный метод подсчета.
Н.3.3 Альтернативный метод и стандартный метод
Операторы, проводящие анализ в каждой сотрудничающей лаборатории, должны владеть навыками соответствующего стандарта (при необходимости их следует обучить) и быть хорошо ознакомлены с выполнением альтернативного метода и референтного метода до начала испытаний.
Н.3.4 Реагенты и рабочие условия
Дополнительные факторы, например качество и состав культуральной среды и реагентов, контроль за температурой инкубации и т.д., могут оказывать большое влияние на исход испытания. В связи с этим такую изменчивость нужно минимизировать (например, путем рассылки сред и/или реагентов всем сотрудничающим лабораториям) или это должно быть учтено при интерпретации результатов.
В протоколе должна быть указана степень допустимого отклонения в отношении всех параметров анализа, например времен, температур, масс, суммарного определения числа микроорганизмов на чашках Петри и дня анализа. Если никакие отклонения не допускаются, то должно быть сделано четкое предупреждение.
Н.3.5 Руководство
В течение всего периода валидации лаборатория-организатор должна быть доступна для предоставления консультации или рекомендации сотрудничающим лабораториям.
Н.3.6 Сбор данных
Лаборатория-организатор должна разработать опросный лист, целью которого является сбор информации, относящейся к критически важным моментам протокола. Все сотрудничающие лаборатории должны документировать такие подробности, как pH среды, время инкубации, начальная и конечная температуры инкубации, данные по контролю качества, состояние образцов по прибытии, время прибытия, температура при прибытии, условия хранения/время хранения и т.д. Содержание опросного листа должно быть согласовано лабораторией-организатором и разработчиком альтернативного метода для обеспечения соответствия критически важным этапам анализа или процедурам испытания альтернативным методом.
Н.3.7 Подтверждение качества испытуемых образцов
Лаборатория-организатор должна провести анализ типичных аликвот образцов в запланированный день начала анализа для подтверждения наличия и гомогенности целевого аналита. Образцы, которые до этого хранились в идеальных условиях, также должны быть проанализированы лабораторией-организатором в день начала анализа сотрудничающими лабораториями. Результаты таких анализов можно использовать только для подтверждения процедуры внесения посевного материала и стабильности аналита. Эти результаты нельзя использовать при статистической оценке испытываемого метода.
Приложение I
(обязательное)
Определение отсутствия целевого аналита в отрицательных контрольных образцах
Для того чтобы проверить отсутствие целевого микроорганизма в продукте, который будет использоваться в качестве отрицательных контрольных образцов или перед искусственной инокуляцией, необходимо провести анализ испытываемых материалов. Чем больше число исследованных подобразцов, тем больше уверенность в надежности определения. Отрицательные контрольные образцы также проверяют в ходе исследования.
Существует вероятность того, что очень низкие уровни аналита (единицы микроорганизмов) не обнаруживаются из-за количества испытываемого образца или в случае неоднородного распределения микроорганизмов по образцу.
С точки зрения статистики при испытании восьми образцов вероятность обнаружения наличия 1, 2, 3, 4 или 5 клеток на 600 г продукта составляет 0,33; 0,57; 0,72; 0,83 и 0,90 соответственно.
Разделяют число анализируемых образцов на 2 категории:
- минимум шесть образцов анализируют перед началом эксперимента, чтобы проверить отсутствие микроорганизмов, причем число образцов определяется протоколом испытаний;
- дополнительные отрицательные образцы исследуют в ходе эксперимента, причем число образцов определяется протоколом испытаний.
Приложение J
(обязательное)
Репликация образцов для межлабораторных исследований качественных методов
J.1 Случай 1 - Соответствует идентичности 1-го этапа культивирования референтного и альтернативного методов
Каждым методом испытывают на каждом из 3-4 уровней контаминации восемь реплик образцов.
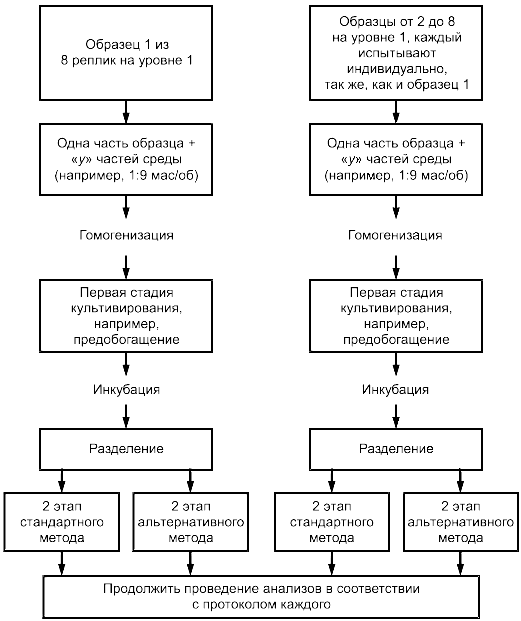
J.2 Случай 2 - Репликация путем дупликации, когда первые этапы культивирования для каждого метода различаются
Каждым методом испытывают на каждом из 3-4 уровней контаминации восемь реплик образцов.
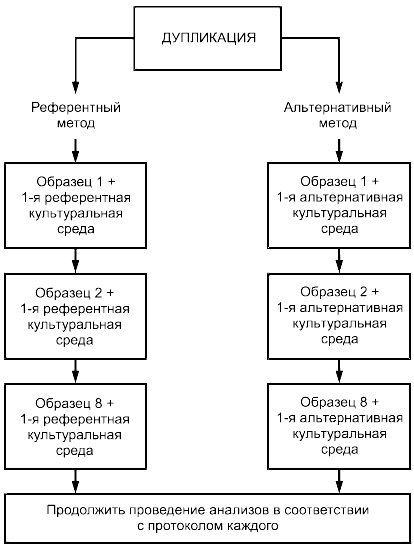
Приложение K
(обязательное)
Учет и обсуждение данных
По завершении межлабораторного исследования вся информация на таблицах данных и результаты должны быть представлены в лабораторию-организатор и изучены следующим образом:
- проверяют, что образцы/комплект испытательного оборудования и т.д. не были повреждены при перевозке;
- указывают товарный знак и номер партии используемой среды. Экспертная лаборатория проверяет, соответствует ли формула референтному методу;
- в случае повреждения образца данные должны быть отбракованы. Нужно также учитывать возможность перекрестной контаминации других образцов в этой упаковке;
- отбраковывают данные, если условия или время транспортировки выходят за рамки специфицированных допустимых отклонений;
- отбраковывают данные, если значения подсчета выходят за рамки специфицированных допустимых отклонений;
- отбраковывают данные, если из данных опросного листа видно, что лаборатория отклонилась от стандартного протокола или от критических рабочих условий.
Приложение L
(справочное)
Межлабораторное исследование качественных методов: критерии согласованности, соответствия и коэффициент расхождения между согласованностью и соответствием
L.1 Общие требования
Критерии точности, чувствительности и специфичности (см. 5.2.2) не в полной мере характеризуют изменчивость метода внутри и между лабораториями (прецизионность метода).
Это приложение содержит дополнительные критерии (согласованность, соответствие и коэффициент расхождения между согласованностью и соответствием), которые позволяют проанализировать такую изменчивость.
Критерии повторяемости и воспроизводимости характеризуют возможную разницу между двумя образцами, отправленными в одну или разные лаборатории. Поскольку разность неколичественных данных нельзя использовать, статистика качественных методов основана на вероятности (выраженной в процентах) того, что два образца дадут одинаковый результат.
Такие критерии разработаны в Европейском проекте SMT CT 96 2098, финансируемом Европейской комиссией/DG XII, для валидации шести основных стандартизованных методов, используемых в микробиологии пищевых продуктов (координатор - Др. C.Lahellec, AFSSA, Франция) [9].
Вычисления представлены в таблице L.1.
Таблица L.1 - Примеры числовых данных
Лаборатории | Номер реплики | Число положительных результатов (из 5) | ||||
1 | 2 | 3 | 4 | 5 | ||
1 | + | + | + | + | + | 5 |
2 | + | + | + | + | + | 5 |
3 | + | + | + | + | + | 5 |
4 | + | + | + | + | + | 5 |
5 | - | - | + | + | + | 3 |
6 | + | + | + | + | + | 5 |
7 | - | - | + | + | + | 3 |
8 | + | + | + | + | + | 5 |
9 | + | + | + | + | + | 5 |
10 | + | + | + | + | + | 5 |
Данные, приведенные в этой таблице, относятся только к одному уровню одного типа пищевого продукта. На практике совместное испытание является более обширным, но меньший набор данных облегчает объяснение вычислений.
L.2 Согласованность (accordance)
L.2.1 Определение
Согласованность (accordance) - это выраженная в процентах вероятность получения одинакового результата (т.е. оба положительные или оба отрицательные) от двух идентичных подобразцов, анализируемых в одной лаборатории, в условиях повторяемости (т.е. один оператор, использующий то же оборудование и те же реагенты с минимальным разумным временным интервалом).
Согласованность, таким образом, эквивалентна повторяемости в количественных методах.
L.2.2 Вычисления
Для получения согласованности по результатам межлабораторного исследования для каждой лаборатории-участника поочередно вычисляют вероятность того, что два образца дадут один и тот же результат. Затем находят среднюю вероятность по всем лабораториям.
Например, см. таблицы L.1 и L.2.
Для тех лабораторий (как, например, лаборатория 1), где все образцы оказались положительными, наилучшая оценка вероятности получения того же результата точно равна 1,00 или 100%.
Для других (например, лаборатории 5 и 7) вероятность того, что одна реплика окажется положительной, равна 3/5=0,60. Для получения вероятности положительности пары реплик возводят эту вероятность в квадрат (0,6=0,36). Проделывают ту же операцию для получения вероятности отрицательности пары реплик (0,4
=0,16). Затем суммируют эти цифры для получения полной вероятности того, что две реплики дадут одинаковый результат (0,36+0,16=0,52).
Проводят такие вычисления для всех лабораторий (см. таблицу L.2).
Таблица L.2 - Вычисление согласованности
Лабора- | Число положи- | Вероятность положи- | Вероятность пар положи- | Вероятность отрица- | Вероятность пар отрица- | Вероятность пар с одинаковыми результатами |
1 | 5 | 1,00 | 1,00 | 0,00 | 0,00 | 1,00 |
2 | 5 | 1,00 | 1,00 | 0,00 | 0,00 | 1,00 |
3 | 5 | 1,00 | 1,00 | 0,00 | 0,00 | 1,00 |
4 | 5 | 1,00 | 1,00 | 0,00 | 0,00 | 1,00 |
5 | 3 | 0,60 | 0,36 | 0,40 | 0,16 | 0,52 |
6 | 5 | 1,00 | 1,00 | 0,00 | 0,00 | 1,00 |
7 | 3 | 0,60 | 0,36 | 0,40 | 0,16 | 0,52 |
8 | 5 | 1,00 | 1,00 | 0,00 | 0,00 | 1,00 |
9 | 5 | 1,00 | 1,00 | 0,00 | 0,00 | 1,00 |
10 | 5 | 1,00 | 1,00 | 0,00 | 0,00 | 1,00 |
Среднее: 0,904=90,4% | ||||||
Согласованность - это среднее значение вероятностей, что для двух реплик будет получен одинаковый результат для каждой лаборатории. В данном случае согласованность составляет 90,4%.
Примечание - Так как повторяемость характеризует разницу, в то время как согласованность измеряет сходство, высокие значения согласованности означают, что метод надежен в отличии от количественных методов, где желательны низкие значения повторяемости.
L.3 Соответствие (concordance)
L.3.1 Определение
Соответствие (concordance) - это выраженная в процентах вероятность получения одинакового результата от двух идентичных образцов, анализируемых в разных лабораториях.
Соответствие, таким образом, является эквивалентом воспроизводимости в количественных методах.
L.3.2 Вычисления
Для вычисления соответствия по результатам межлабораторного исследования используют поочередно каждую реплику в каждой лаборатории-участнике и группируют по парам с идентичными результатами всех других лабораторий.
Соответствие - это выраженная в процентах доля всех пар, дающих одинаковые результаты, от всех возможных упомянутых пар данных.
Например, см. таблицы L.1 и L.3.
Таблица L.3 - Вычисление соответствия
Лаборатории | Число положительных образцов | Межлабораторные пары с одинаковыми результатами | Суммарное число межлабораторных пар |
1 | 5 | 205 | 225 |
2 | 5 | 205 | 225 |
3 | 5 | 205 | 225 |
4 | 5 | 205 | 225 |
5 | 3 | 133 | 225 |
6 | 5 | 205 | 225 |
7 | 3 | 133 | 225 |
8 | 5 | 205 | 225 |
9 | 5 | 205 | 225 |
10 | 5 | 205 | 225 |
Всего | 1906 | 2250 |
Поочередно используют каждую реплику из каждой лаборатории, начиная с первой реплики из лаборатории 1, которая положительна. Ее можно объединить в пару с любой из 45 реплик из других лабораторий, и все, кроме 4, из этих пар (а именно, кроме тех, что составлены из реплик из лабораторий 5 и 7) сочетаются (т.е. являются парой с двумя положительными репликами), и, таким образом, для 41 пары получают одинаковый результат.
То же самое проделывают с остальными 4 репликами лаборатории 1 так, что получается суммарное число в 225 (5·45) межлабораторных пар реплик, включающих реплики из лаборатории 1, из которых 205 (5·41) дают одинаковый результат.
То же выполняют во всех других лабораториях со всеми репликами, которые оказались положительными.
Для лаборатории 5, где 3 реплики из 5 положительны, 2 отрицательных результата совпадают лишь с 2 другими отрицательными результатами лаборатории 7, в то время как из 3 положительных каждый совпадает с 43 положительными репликами. Таким образом, суммарное число пар с одинаковым результатом 133 (2·2+3·43).
Соответствие - это процентная доля всех пар дупликатов, дающих одинаковый результат; в этом примере соответствие равно 84,7% (1906/2250·100).
Примечание - Так как воспроизводимость характеризует разницу, а соответствие характеризует подобие, высокие значения соответствия свидетельствуют о надежности метода в отличие от количественных методов, где желательны низкие значения воспроизводимости.
L.4 Коэффициент расхождения между согласованностью и соответствием
L.4.1 Общие положения и определение
Если соответствие меньше согласованности, то это свидетельствует о том, что вероятность получения одного и того же результата для двух идентичных образцов, анализируемых в одной лаборатории, больше, чем в случае анализа в разных лабораториях, что дает основание предполагать, что может существовать изменчивость рабочих характеристик между лабораториями. В случае количественного метода эта ситуация соответствует тому, что воспроизводимость больше повторяемости.
К сожалению, величины соответствия и согласованности сильно зависят от уровня точности, что затрудняет процесс оценки степени межлабораторной вариации.
Поэтому полезно вычислить коэффициент расхождения между согласованностью и соответствием (), определяемый следующим образом:
![]() .
.
L.4.2 Критерии значимости
Значение 1,00 коэффициента расхождения между согласованностью и соответствием указывает, что согласованность и соответствие одинаковы, и чем больше этот коэффициент, тем более доминирующую роль играет межлабораторная вариация.
Тем не менее значения, превышающие 1,00, могут появляться из-за случайной вариации, поэтому необходимо провести испытания на статистическую значимость для подтверждения, доказательны ли данные о повышенной межлабораторной вариации. "Точным критерием" является наилучший рекомендованный для этого критерий. Основной принцип, лежащий в основе таких критериев, заключается в том, что вероятность события вычисляется для всех наборов результатов для реплик, которые могли привести к общему числу положительных и отрицательных результатов.
_________________
Этот критерий можно вычислить, используя, например, статистические пакеты программ
![]() .
.
Например, см. таблицу L.1.
Возможные распределения общего числа 46 положительных и 4 отрицательных реплик приведены в столбцах в таблице L.4.
Таблица L.4 - Возможные распределения положительных реплик (столбцы) для получения общего числа 46 положительных
4 | 3 | 3 | 2 | 1 |
4 | 4 | 3 | 4 | 5 |
4 | 4 | 5 | 5 | 5 |
4 | 5 | 5 | 5 | 5 |
5 | 5 | 5 | 5 | 5 |
5 | 5 | 5 | 5 | 5 |
5 | 5 | 5 | 5 | 5 |
5 | 5 | 5 | 5 | 5 |
5 | 5 | 5 | 5 | 5 |
5 | 5 | 5 | 5 | 5 |
Реальное распределение показано жирным шрифтом (третий столбец)* в таблице L.4. По критерию в ходе вычислений складываются вероятности для всех тех возможных вариантов размещения результатов, которые, по меньшей мере, столь же доказательно свидетельствуют о наличии межлабораторной вариации, как и реальное распределение, - здесь это означает использование всех перестановок в трех столбцах справа. Если эта вероятность меньше, чем принятое значение в 0,05% или 5%, то маловероятно, что эта степень межлабораторных вариаций могла появиться случайно, и, таким образом, можно сделать вывод, что существует значимая межлабораторная вариация в рабочих характеристиках.
________________
* Текст документа соответствует оригиналу. Выделение жирным шрифтом в Таблице L.4 не приводится. - .
В иллюстративной таблице L.4 значение =0,039 указывает, что межлабораторная вариация значима с уровнем 5%.
В случаях, когда программное обеспечение для "Точного критерия" недоступно, в качестве альтернативы можно использовать обычный статистический анализ с помощью критерия хи-квадрат таблиц сопряженности признаков. Результаты этого критерия менее надежны, чем результаты "точного критерия" при количестве реплик, обычно используемом в совместных исследованиях, но результаты моделирования дают основания полагать, что такой критерий является разумным указателем значимости межлабораторных расхождений.
При использовании любого критерия следует учитывать, что способность обнаруживать межлабораторные расхождения зависит от числа лабораторий и числа повторных образцов, проанализированных каждой лабораторией. Незначимый результат таких критериев не должен приниматься как указание на то, что рабочие характеристики лабораторий не отличаются, а является свидетельством того, что расхождения не доказаны, особенно если значение чуть превышает 0,05. Идеальным решением было бы приводить значение коэффициента расхождения между согласованностью и соответствием с указанием среднеквадратической погрешности или доверительных пределов, но распределение коэффициента расхождения между согласованностью и соответствием сильно асимметрично, что затрудняет получение надежных пределов.
Приложение М
(обязательное)
Репликация образцов для определения относительной точности количественных методов
M.1 Случай 1 - И в референтном, и в альтернативном методах используют одинаковые десятичные разбавления каждого подобразца
Обоими методами культивируется одинаковое число подобразцов (минимум 2, а желательно - от 5 до 10).
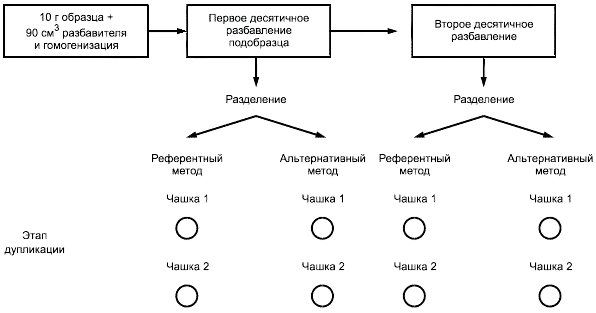
Случай 2 - Только референтный метод требует десятичных разбавлений
Обоими методами культивируется одинаковое число подобразцов (минимум 2, а желательно - от 5 до 10).
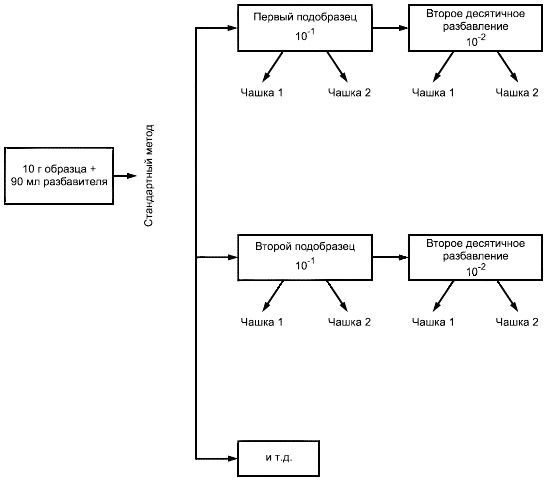
Приложение N
(обязательное)
Примеры приемлемых и неприемлемых ситуаций и диапазон измерений для оценки линии регрессии для количественных методов
Неприемлемые ситуации
|
|
Рисунок N.1 - Отсутствие центральных точек | Рисунок N.2 - Плохое разделение на кластеры |
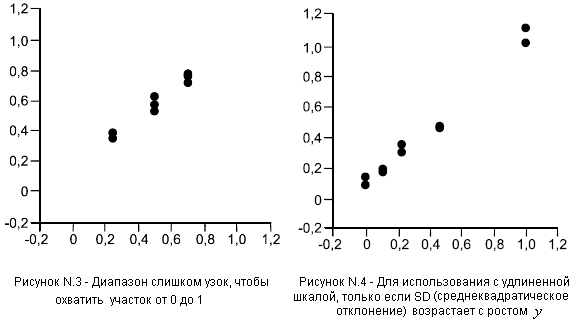
N.1 Приемлемая ситуация
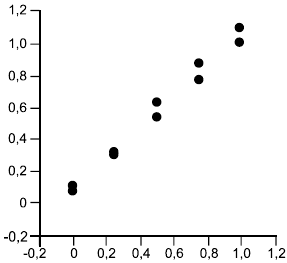
Рисунок N.5 - Приемлемая ситуация
Приложение О
(обязательное)
Оценка линейности количественных методов при помощи графического представления
О.1 Случаи нелинейности
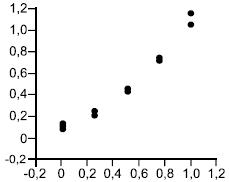
Рисунок О.1
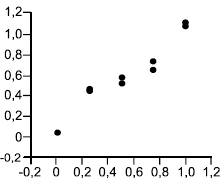
Рисунок О.2
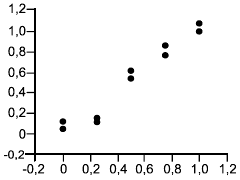
Рисунок О.3
О.2 Случаи линейности
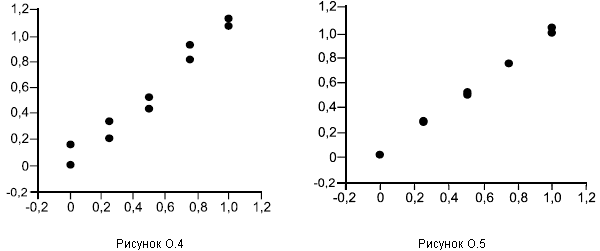
Приложение Р
(обязательное)
Предел обнаружения и предел количественного определения числа микроорганизмов
Р.1 Предел обнаружения
Обычно при наличии неопределенности метода, связанной, например, с используемым образцом, наблюдение только одной колониеобразующей единицы (КОЕ) на среде не достаточно для предположения о присутствии аналита. На таком низком уровне для качественных методов необходим дихотомический подход к событию, т.е. выявление присутствия (1 и более КОЕ) и отсутствия (нет КОЕ). Таким образом, процесс подчиняется закону Пуассона (низкие или высокие значения) или биномиальному закону (промежуточные значения) с частотой присутствия .
Учитывая, что теоретический отрицательный контрольный образец не дает результата о присутствии аналита, предел обнаружения для низкой контаминации (пуассоновский) достигается минимум по присутствиям, соответствующим порогам принятия решения
=3 (при
=95%) или 5 (при 99%). Пределы обнаружения также получают, включая статистическую ошибку 2-го типа
, например
=7 при односторонней
=5% и
![]() 90%.
90%.
Пуассоновский закон дает минимальное число положительных результатов из
(пропорционально
) для достижения значимо положительного утверждения на уровне доверительной вероятности
(см. таблицу Р.1).
Таблица Р.1 - Минимальное число положительных результатов из
|
| |
1 | 1 | 1 |
2 | 2 | 2 |
3 | 2 | 3 |
4 | 3 | 3 |
От 5 до 15 | 3 | 4 |
16 и больше | 3 | 5 |
Однако не исчезает другой тип ошибки: недостаточная статистическая мощность, если размер выборки слишком мал. Например, отсутствие положительных при
=2 образцах означает, что вероятность контаминации меньше 78% (с 95% доверительной вероятности). Один положительный из двух соответствует вероятности контаминации 2,5% или более с той же доверительной вероятностью. Можно видеть, что для достижения значимо положительного утверждения при уровнях доверительной вероятности 95% или 99% минимальная вероятность
контаминации уменьшается с увеличением
:
![]() и соответственно 5/
и соответственно 5/ (точнее 2,996/
и 4,605/
). Из этого в основном следует, что если нужно получить вероятность контаминации
=10% (при 95%), то необходимо взять более 30 образцов (
![]() ). Минимальный уровень
). Минимальный уровень , таким образом, является показательным.
Р.2 Предел определения
Применение правила Ассоциации АОАС к общему числу микроорганизмов позволяет получить значение ![]() 100. В данном стандарте априори используется Пуассоновское распределение со значениями
100. В данном стандарте априори используется Пуассоновское распределение со значениями ![]() и
и ![]() %, что дает
%, что дает 100.
Р.3 Объем образца
До сих пор объем образца не учитывался. При разделении образца на множество подобразцов и использовании всех их для определения наличия контаминации необходимо обнаружение по меньшей мере трех (или пяти) КОЕ во всем образце. Следовательно, вышеуказанные пределы можно представить в виде числа КОЕ для данного подобразца. Повторять выбор образца, пока не получатся по меньшей мере три колонии для определения окончательной оценки объема.
В общем, полученный минимальный объем нужен для микробиологического определения; его также можно получить путем разбавления. Таким образом, теоретический предел КОЕ на среде при разбавлении, в конце концов, корректируется умножением на коэффициент разбавления
, т.е. получается
. Например,
=7 КОЕ/мг во взвеси с разбавлением 1 к 10 твердого образца соответствовал бы пределу
=70 КОЕ/мг в твердом образце.
Приложение Q
(обязательное)
Устойчивая оценка дисперсии, основанная на рекурсивной медиане , [1]
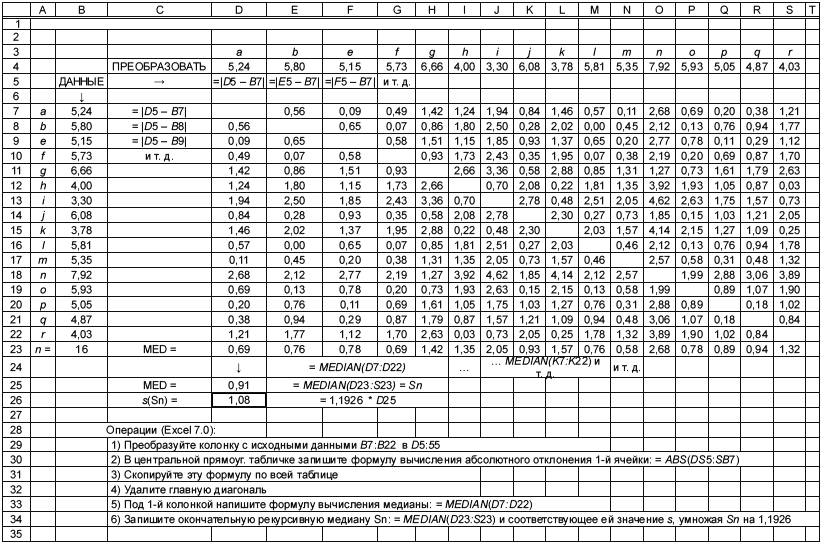
Приложение R
(обязательное)
Вычисления с помощью метода регрессии
R.1 Обозначения и предварительные оценки
- уровень (концентрации аналита), включая ноль, если не преобразован в логарифмы (
от 1 до
);
- число уровней;
- одно повторение, проведенное альтернативным методом, а также стандартным методом (
от 1 до
);
- число повторений, одно и то же число для каждого уровня
;
- число образцов (
![]() ).
).
Априори используют ось для референтного метода и ось
для альтернативного метода. При необходимости можно сделать более адекватный выбор в S.2.
R.1.1 Оценивают для уровня среднее значение для каждого образца на этом испытываемом уровне (по всем повторениям), для референтного метода () и для альтернативного метода (
).
Для каждого уровня образца от 1 до
![]() и
и ![]() .
.
R.1.2 Вычисляют среднеквадратические отклонения повторяемости на каждом уровне: () для референтного метода и (
) для альтернативного метода.
Среднеквадратические отклонения повторяемости на каждом уровне образцов от
=1 до
:
![]() , где
, где ![]() для
для =2:
![]() ;
;
![]() , где
, где ![]() [аналогично].
[аналогично].
R.1.3 Вычисляют глобальное среднеквадратическое отклонение повторяемости на всех уровнях: (
) для референтного метода и (
) для альтернативного. Глобальное среднеквадратическое отклонение повторяемости
всех уровней равно
![]() , где
, где ![]() в пределах дисперсии;
в пределах дисперсии;
![]() , где
, где ![]() в пределах дисперсии.
в пределах дисперсии.
R.1.4 Оценивают глобальные средние и
обоих методов (
от 1 до
уровней), как показано ниже:
![]() и
и ![]() .
.
R.2 Выбор
Выбирают ортогональную линейную регрессию (см. R.3, GMFR) или линейную регрессию обычных наименьших квадратов (см. R.4, OLS).
________________
OLS - обычный метод наименьших квадратов.
Коэффициент выбора ![]() .
.
- Если , продолжают использовать ось
(независимая переменная) для стандартного метода и затем используют оценки по методу OLS (S.4:
![]() ).
).
- Если ![]() , используют ось
, используют ось для альтернативного метода и ось
для референтного и затем используют оценки по методу OLS (см. S.4:
![]() ). Потом проводят замену всех оценок для
). Потом проводят замену всех оценок для на оценки для
, и наоборот, т.е.
![]() ,
, ![]() ,
, ![]() ,
, ![]() .
.
Если ![]() (случай квазиравной повторяемости по
(случай квазиравной повторяемости по и
), используют (ортогональные) оценки по методу GMFR (см. R3), сохраняя ось
за референтным методом.
R.3 Ортогональная линейная регрессия (GMFR)
R.3.1 Глобальные среднеквадратические отклонения
Вычисляют глобальные среднеквадратические отклонения: () для референтного метода и (
) для альтернативного метода, как показано:
![]() , где
, где ![]() ;
;![]() , где
, где ![]() .
.
R.3.2 Оценивают коэффициент корреляции как показано:
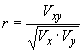 с ковариацией
с ковариацией ![]() .
.
R.3.3 Оценивают отсекаемый отрезок и наклон
линии регрессии
![]() следующим образом: наклон
следующим образом: наклон ![]() , отсекаемый отрезок
, отсекаемый отрезок ![]() .
.
R.3.4 Путем регрессии оценивают остаточное среднеквадратическое отклонение по точкам, вычисленным при помощи регрессии:
![]() ,
,
где 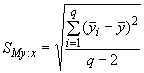
получено по точкам, вычисленным при помощи регрессии ![]() ;
; от 1 до
.
R.3.5 Оценивают среднеквадратическое отклонение отсекаемого отрезка
и проверяют гипотезу
=0
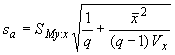 .
.
Проверка гипотезы =0:
![]() с (
с () степенями свободы.
По таблице Стьюдента получаем: ![]() ; критическое значение
; критическое значение 2 для двухсторонней
=0,05.
R.3.6 Оценивают среднеквадратическое отклонение наклона
и проверяют гипотезу
=1.
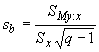 .
.
Проверка гипотезы =1:
![]() с (
с () степенями свободы.
По таблице Стьюдента получаем: ![]() ; критическое значение
; критическое значение 2 для двухсторонней
=0,05.
Затем переходят к пункту R.4.
R.4 Линейная регрессия, с использованием обычного метода наименьших квадратов (OLS)
R.4.1 Глобальные среднеквадратические отклонения
![]() ,
,
где ![]() ;
;
![]() ,
,
где ![]() .
.
R.4.2 Коэффициент корреляции
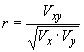
с ковариацией ![]() .
.
R.4.3 Наклон ![]() , отсекаемый отрезок
, отсекаемый отрезок ![]() для линии регрессии
для линии регрессии ![]() .
.
R.4.4 Определяют остаточное среднеквадратическое отклонение
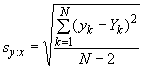
по точкам, оцененным при помощи регрессии ![]() (
(=1 до
,
![]() ).
).
R.4.5 Среднеквадратическое отклонение отсекаемого отрезка
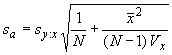 .
.
Проверка гипотезы =0:
![]() с (
с (![]() ) степенями свободы.
) степенями свободы.
Статистические функции Excel, которые здесь используются:: ![]() для коэффициента корреляции,
для коэффициента корреляции, ![]() для ковариации, но эта последняя функция смещена и умножается на
для ковариации, но эта последняя функция смещена и умножается на ![]() , где
, где ![]() , а
, а ![]() и
и ![]() , которые являются оценками для
, которые являются оценками для и
,
![]() для остаточного
для остаточного на
,
![]() для вероятности
для вероятности -распределения Стьюдента и
![]() для вероятности из
для вероятности из -распределения Snedecor-Fisher.
По таблице Стьюдента получаем: ![]() ; критическое значение
; критическое значение 2 для двухсторонней
=0,05.
R.4.6 Стандартное отклонение наклона
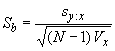 .
.
Проверка =1:
![]() с (
с (![]() ) степенями свободы.
) степенями свободы.
По таблице Стьюдента получаем: ![]() ; критическое значение
; критическое значение 2 для двухсторонней
=0,05.
R.5 Критерий линейности (недостаточная подгонка)
________________
Эти сведения отсутствуют в Excel (см. ISO 11095).
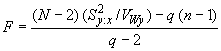
с ![]() степенями свободы для числителя
степенями свободы для числителя и
![]() для его знаменателя.
для его знаменателя.
По -таблице Снедекора можно получить
![]() и критические значения
и критические значения для
![]() 0,05, как показано в таблице R.1.
0,05, как показано в таблице R.1.
Таблица R.1 - ![]() и критические значения
и критические значения для
![]() 0,05
0,05
|
| |
| 5,41 | 3,10 |
| 4,53 | 2,78 |
Это соотношение нелинейно, если ![]() или
или ![]() .
.
R.6 Границы доверительного интервала (CL)
R.6.1 Границы доверительного интервала ![]() расчетной точки
расчетной точки в любой точке
![]() с
с 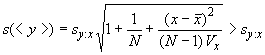 ,
,
где является значением из таблицы Стьюдента для двухстороннего уровня доверительной вероятности
и (
![]() ) степеней свободы.
) степеней свободы.
R.6.2 Обратные доверительные пределы ![]() при
при для неизвестного образца
![]() с
с ![]() при
при ![]() и где
и где является значением из таблицы Стьюдента для двухстороннего уровня доверительной вероятности
и (
![]() ) степеней свободы.
) степеней свободы.
Приложение S
(обязательное)
Примеры вычислений для количественных методов
S.1 Случай 1 - Пример регрессии OLS (сравнение альтернативного метода со стандартным методом)
N | Стандартный метод | Альтернативный метод | ||||||
Реплика 1 | Реплика 2 | Реплика 1 | Реплика 2 | |||||
1 | 4,073 | 4,214 | 4,143 | 0,100 | 4,342 | 4,652 | 4,497 | 0,219 |
2 | 5,758 | 5,778 | 5,768 | 0,014 | 5,720 | 6,289 | 6,005 | 0,402 |
3 | 6,828 | 6,816 | 6,822 | 0,008 | 6,227 | 6,252 | 6,239 | 0,018 |
4 | 6,992 | 7,000 | 6,996 | 0,006 | 6,737 | 7,719 | 7,228 | 0,694 |
5 | 7,856 | 7,737 | 7,796 | 0,084 | 6,976 | 7,932 | 7,454 | 0,676 |
MED=6,822 | 0,014 | MED=6,239 | 0,402 | |||||
|
| |||||||
Пример: стандартный метод на оси , классическая регрессия
.
Регрессия: сравнение альтернативного метода со стандартным
Из меню Excel: Tools/Data analysis/Regression (Инструменты/анализ данных/Регрессия)
Методы N | Стандартный | Альтернативный |
| ||
Репл.1 | Репл.2 | ||||
Первая реплика | 1 | 4,143 | 4,342 | 4,652 | 0,219 |
2 | 5,768 | 5,720 | 6,289 | 0,402 | |
3 | 6,822 | 6,227 | 6,252 | 0,018 | |
4 | 6,996 | 6,737 | 7,719 | 0,694 | |
5 | 7,796 | 6,976 | 7,932 | 0,676 | |
Вторая реплика | 1 | 4,143 | 4,652 | Устойчивая | |
2 | 5,768 | 6,289 | |||
=1,4826 * | |||||
3 | 6,822 | 6,252 | |||
4 | 6,996 | 7,719 | |||
5 | 7,796 | 7,932 | |||
Для использования инструментов регрессионного анализа:
a: копируют все ;
b: копируют Репл.2;
c: используют только два первых столбца для и
.
Сводка выходных данных
Регрессионная статистика | ||
Множественный | 0,9177 | |
| 0,8422 | |
Нормированный | 0,8225 | |
Стандартная ошибка | 0,491 | |
Наблюдения | 10 |
|
=2 реплики;
=5 уровней.
Дисперсионный анализ
Значимость | |||||
Регрессия | 1 | 10,287 | 10,287 | 42,701 | 1,8х10 |
Остаток ( | 8 | 1,927 | 0,241 | ||
Итого | 9 | 12,214 |
Коэффи- | Стандартная ошибка |
|
| Нижние 95% | Верхние 95% | |
Пересечение (a) | 1,207 | 0,792 | 1,523 | 0,166 | -0,620 | 3,034 |
Х Пересечение 1 (b) | 0,805 | 0,123 | 6,535 | 1,8х10 | 0,521 | 1,089 |
95% доверительный интервал включает =0 и
=1.
Недостаточная подгонка (нелинейность):
![]() (для числителя);
(для числителя);
![]() (для знаменателя);
(для знаменателя);
устойчивое ![]() ;
;
![]() .
.
Выводы: нет достаточной точности, так как 0,521,09 и -0,6
3,0, и линейности (
=0,931).
График линейной подгонки
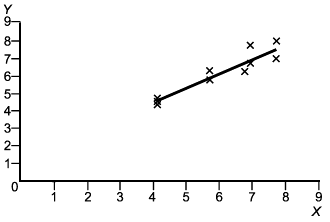
Рисунок S.1
График остатков
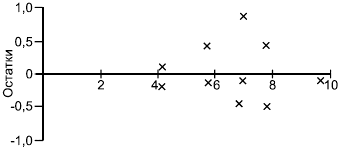
Рисунок S.2
График нормального распределения
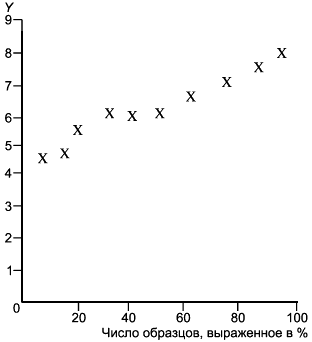
Рисунок S.3
Случай 2 - Пример GMFR / ортогональной регрессии
Регрессия: сравнение альтернативного метода со стандартным
N | Стандартный метод | Альтернативный метод | Оценка остатков | |||||||
Реплика 1 | Реплика 2 | Реплика 1 | Реплика 2 | По | ||||||
1 | 3,126 | 5,161 | 4,143 | 1,439 | 4,342 | 4,652 | 4,497 | 0,219 | 4,479 | 0,018 |
2 | 5,623 | 5,914 | 5,768 | 0,206 | 5,720 | 6,289 | 6,005 | 0,402 | 5,836 | 0,169 |
3 | 6,908 | 6,736 | 6,822 | 0,121 | 6,227 | 6,252 | 6,239 | 0,018 | 6,716 | 0,477 |
4 | 6,939 | 7,053 | 6,996 | 0,081 | 6,737 | 7,719 | 7,228 | 0,694 | 6,862 | 0,366 |
5 | 8,657 | 6,936 | 7,796 | 1,217 | 6,976 | 7,932 | 7,454 | 0,676 | 7,530 | 0,076 |
|
| |||||||
|
|
| ||||||
| 0,206 |
| 0,402 | |||||
устойчивый | =0,305 | устойчивый | ||||||
| ||||||||
|
| |||||||
| 1,95 | |||||||
Выбор: Стандартный метод по оси , ортогональная регрессия
=0,9642;
![]() =0,363;
=0,363;
![]() =0,514.
=0,514.
| ||||
| 0,129 | 1,277 | 0,291 | 1 |
| 0,830 | 1,228 | 0,307 | 0 |
Недостаточная подгонка (нелинейность):
![]() ;
;
![]() ;
;
![]() ;
;
![]() .
.
График линейной подгонки
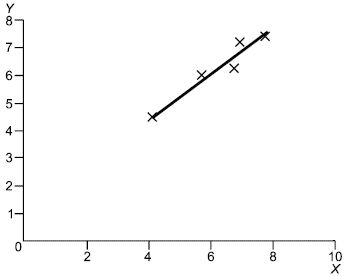
Рисунок S.4
График остатков
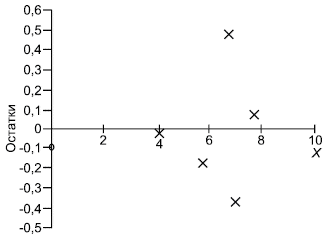
Рисунок S.5
Приложение Т
(обязательное)
Совместное исследование - результаты круговых испытаний на дупликатах
=2 реплики
Число лабораторий, =16
Лаборатории | Реплика 1 | Реплика 2 | ||
1 | 4,30 | 6,18 | 5,24 | 1,33 |
2 | 5,60 | 6,00 | 5,80 | 0,28 |
3 | 5,60 | 4,70 | 5,15 | 0,64 |
4 | 6,72 | 4,74 | 5,73 | 1,40 |
5 | 7,06 | 6,25 | 6,66 | 0,57 |
6 | 4,70 | 3,30 | 4,00 | 0,99 |
7 | 3,30 | 3,30 | 3,30 | 0,00 |
8 | 7,55 | 4,60 | 6,08 | 2,09 |
9 | 4,26 | 3,30 | 3,78 | 0,68 |
10 | 5,60 | 6,01 | 5,81 | 0,29 |
11 | 5,00 | 5,70 | 5,35 | 0,49 |
12 | 8,76 | 7,08 | 7,92 | 1,19 |
13 | 6,26 | 5,60 | 5,93 | 0,47 |
14 | 6,79 | 3,30 | 5,05 | 2,47 |
15 | 3,30 | 6,43 | 4,87 | 2,21 |
16 | 3,30 | 4,76 | 4,03 | 1,03 |
| 3,30 | 3,30 | 0,00 | |||||
| 8,76 | 7,92 | 2,47 | |||||
|
| 0,83; | ||||||
По
| устойч. |
| ||||||
| ||||||||
| устойч. | |||||||
| ||||||||
| ||||||||
Приложение U
(справочное)
Список обозначений и сокращений
- относительная точность.
- доверительный интервал.
- граница доверительного интервала.
- ложноположительный.
- критический уровень.
- предел обнаружения.
- предел количественного определения.
- отрицательное согласование.
- отрицательное отклонение.
- положительное согласование.
- положительное отклонение.
- предел повторяемости.
- предел воспроизводимости.
- относительное среднеквадратическое отклонение повторяемости.
![]() - относительное среднеквадратическое отклонение воспроизводимости.
- относительное среднеквадратическое отклонение воспроизводимости.
- среднеквадратическое отклонение повторяемости.
- среднеквадратическое отклонение воспроизводимости.
- относительная чувствительность.
- относительная специфичность.
- истинно положительный.
Приложение ДА
(справочное)
Сведения о соответствии межгосударственных стандартов ссылочным международным стандартам и документу
Таблица ДА.1
Обозначение и наименование международного стандарта (документа) | Степень соответствия | Обозначение и наименование межгосударственного стандарта |
ISO 3534-1 Статистика. Словарь и условные обозначения. Часть 1. Общие статистические термины и термины, используемые в теории вероятности | - | * |
ISO 5725 (все части) Точность (правильность и прецизионность) методов и результатов измерений | IDT | ГОСТ ИСО 5725 (все части) Точность (правильность и прецизионность) методов и результатов измерений |
ISO/TS 11133-1:2000 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству культуральных сред. Часть 1. Общие руководящие указания по обеспечению качества приготовления культуральных сред в лаборатории | IDT | ГОСТ ISO 11133-1 -2011 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству культуральных сред. Часть 1. Общие руководящие указания по обеспечению качества приготовления культуральных сред в лаборатории |
* Соответствующий межгосударственный стандарт отсутствует. До его утверждения рекомендуется использовать перевод на русский язык данного международного стандарта. Перевод данного международного стандарта находится в Федеральном информационном фонде технических регламентов и стандартов. Примечание - В настоящей таблице использовано следующее условное обозначение степени соответствия стандартов: - IDN** - идентичные стандарты | ||
________________
** Текст документа соответствует оригиналу. - .
Библиография
[1] | EN ISO 9001, Quality management systems - Requirements (ISO 9001:2000) |
[2] | EN ISO/IEC 17025, General requirements for the competenct of testing and calibration laboratories (ISO/IEC 17025:1999) |
[3] | ISO 11095, Linear calibration using reference materials |
[4] | C. Clayton, J.Hines, P.Elkins, Detections limits with specified assurance probabilities, Anal. Chem. (1987), 59, 2506-2514 |
[5] | D.Coleman, J.Auses, N.Grams, Regulation - From an industry perspective or Relationships between detection limits, quantation limits, and significant digits, Chermometric & Intel. Lab. Syst. (1997), 37, 71-80 |
[6] | L.A Currie, Limits for qualitative determination: Application to radiochemistry, Anal. Chem. (1968), 40, 586-593 |
[7] | DRAPER Norman R., YANG Younghong (Fred); Gtntralization of geometric mean functional relationship, Comput. Statist. & Data Anal. (1997), 23, 355-372 |
[8] | A.Hubaux, G.Vos, Decision and detection limits for linear calibration curves, Anal.Chem. (1970), 42, 8, 849-855 |
[9] | Rousseeuw Peter J., Croux Christope, Alternatives to the median absolute deviation, JASA 88, (1993), 424, 1273-1283 |
[10] | Gopal K. Kanji, Statistical tests, Sage publications, (1993) |
[11] | MicroVal Rules and Certification Scheme (1998), published by the VicroVal secretariat NEN, Nederlands Normalie-satie-instituut (NEN) Vlinderweg 6 P.O. Box 5059, 2600 GB Delft< Netherlands |
[12] | Langton, SD, Chevennement, R., Nagelkerke, N., and Lombard, B: Analizing cjllaborative trials for qualitative microbiological methods: accordance and concordance, International Journal of Food Microbiology (in press) |
Электронный текст документа
и сверен по:
, 2013