ГОСТ 34176-2017
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРЕПАРАТЫ ФЕРМЕНТНЫЕ
Методы определения ферментативной активности эндо--глюканазы
Enzyme preparations. Methods of endo--glucanase ferment activity detection
МКС 07.100.30
65.120
Дата введения 2018-07-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2015 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением "Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов" (ФГБУ "ВГНКИ")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 7 июня 2017 г. N 99-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 31 августа 2017 г. N 991-ст межгосударственный стандарт ГОСТ 34176-2017 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2018 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
ВНЕСЕНА поправка, опубликованная в ИУС N 12, 2019 год
Поправка внесена изготовителем базы данных
1 Область применения
Настоящий стандарт распространяется на ферментные препараты и устанавливает вискозиметрические и колориметрические методы определения ферментативной активности эндо--глюканазы.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты*
_______________
* В Российской Федерации действует ГОСТ Р 12.1.019-2009.
ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 199-78 Реактивы. Натрий уксуснокислый 3-водный. Технические условия
ГОСТ 201-76 Тринатрийфосфат. Технические условия
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ ИСО 5725-6-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике**
_______________
** В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002.
ГОСТ 5823-78 Реактивы. Цинк уксуснокислый 2-водный. Технические условия
ГОСТ 5962-2013 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 10028-81 Вискозиметры капиллярные стеклянные. Технические условия
ГОСТ 18481-81 Ареометры и цилиндры стеклянные. Общие технические условия
ГОСТ 20264.0-74 Препараты ферментные. Правила приемки и методы отбора проб*
_______________
* В Российской Федерации действует ГОСТ Р 57248-2016.
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 гидролиз: Расщепление исходного соединения на более простые в присутствии молекул воды.
3.2 ферментативный гидролиз: Гидролиз высокомолекулярных соединений под воздействием катализаторов белковой природы - гидролитических ферментов (гидролаз, класс 3 [1]).
3.3 субстрат: Соединение или вещество, на которое воздействует данный фермент.
3.4 системные названия ферментов: Названия, указывающие природу химической реакции, катализируемой данным ферментом, в соответствии с современной классификацией ферментов (КФ), принятой Международной комиссией по ферментам [1].
3.5 эндо--глюканазы: Ферменты, катализирующие гидролиз внутренних связей
-глюкана с неупорядоченным расщеплением молекулы на крупные фрагменты (олигосахариды).
Примечание - Ферменты эндо--глюканазы катализируют гидролиз внутренних связей
-глюкана:
- эндо-1,4--глюканаза (системное название: 1,4-
-D-глюкан-4-глюкано-гидролаза, КФ 3.2.1.4); лихеиназа (1,3-1,4-
-D-глюкан-4-глюканогидролаза, КФ 3.2.1.73); эндо-1,3-1,4-глюканаза (1,3-(1,3;1,4)-
-D-глюкан 3(4)-глюканогидролаза, КФ 3.2.1.6); эндо-1,3-
-глюканаза (1,3-
-D-глюканглюканогидролаза, КФ 3.2.1.39) катализируют гидролиз
-1, 3 и 1, 4 связей в цепи
-глюканов;
- эндо-1,6--глюканаза (1,6-
-D-глюканглюканогидролаза, КФ 3.2.1.75) - 1:6 связи в цепи
-глюканов;
- эндо-1,2--глюканаза (1,2-
-D-глюканглюканогидролаза, КФ 3.2.1.71) - 1:2 гликозидные связи глюкана.
3.6 -глюкан: Высокомолекулярное соединение, полимер глюкозы с
-гликозидными связями, образующее с водой коллоидный раствор, которое используется в реакции как субстрат.
3.7 азо-ячменный -глюкан и бета-глюказим таблетки (AZCL-бета-глюкан): Высокоочищенные субстраты 1,3;1,4-
-D-глюкана с низкой вязкостью, связанные с хромофором (азурином).
4 Требования безопасности и условия выполнения анализа
4.1 Применяемые в работе реактивы относятся к веществам 1-го и 2-го класса опасности по ГОСТ 12.1.007, при работе с которыми необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
4.2 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией.
4.3 Электробезопасность при работе с электроустановками - по ГОСТ 12.1.019.
4.4 К проведению анализов допускаются лица, имеющие квалификацию не ниже среднего технического образования, владеющие навыками проведения анализа и изучившие инструкции по эксплуатации используемой аппаратуры.
4.5 При выполнении анализов соблюдают следующие условия:
- температура окружающего воздуха | от 15°С до 30°С; |
- относительная влажность воздуха | от 20% до 80%. |
5 Метод определения ферментативной активности эндо- -глюканазы с использованием капиллярного вискозиметра Оствальда
-глюканазы с использованием капиллярного вискозиметра Оствальда
5.1 Сущность метода
Метод определения ферментативной активности эндо--глюканазы с использованием вискозиметра Оствальда основан на количественном определении снижения относительной вязкости (повышения текучести) субстрата - раствора
-глюкана - в результате деградации его под действием эндоглюканаз. Относительную вязкость (текучесть) определяют как отношение вязкости гидролизата субстрата к вязкости буферного раствора при той же температуре.
За единицу активности принимают такое количество фермента, которое в стандартных условиях (гидролиз в течение 10 мин при температуре 30°С) приводит к увеличению величины относительной текучести субстрата, равной 1 мин (ед. ГлА).
5.2 Средства измерений, вспомогательные устройства, материалы, посуда и реактивы
5.2.1 Для определения ферментативной активности эндо--глюканазы применяют следующие средства измерений и вспомогательные устройства:
- весы неавтоматического действия высокого класса точности по ГОСТ OIML R 76-1 с пределами допускаемой погрешности не более ±0,001 г;
- pH-метр или универсальный иономер с диапазоном измерения от 0 до 14 ед. pH с погрешностью измерения не более ±0,1 ед. pH;
- секундомеры с емкостью шкалы счетчика 1 мин, ценой деления 1 с и погрешностью не более ±1,5 с;
- сито с размером диаметра ячеек не более 1 мм;
- баню водяную лабораторную из прозрачного материала, обеспечивающую поддержание температуры нагревания 30°С с допускаемой погрешностью регулирования температуры не более ±0,1°С;
- баню водяную лабораторную, обеспечивающую температуру нагревания до 100°С с допускаемой погрешностью регулирования температуры не более ±1,0°С;
- вискозиметр Оствальда с размером диаметра капилляра 0,73 мм по ГОСТ 10028;
- измельчитель-гомогенизатор лабораторный или механическую мельницу, обеспечивающую размалывание анализируемой пробы ферментного препарата до полного ее прохода через сито;
- мешалку магнитную любой марки, которая обеспечивает скорость вращения до 800 мин;
- центрифугу лабораторную любого типа, которая обеспечивает скорость вращения не менее 4000 мин;
- холодильник бытовой с рабочим диапазоном температур от 2°С до 8°С.
(Поправка. ИУС N 12-2019).
5.2.2 Для определения ферментативной активности эндо--глюканазы применяют следующие лабораторную посуду и материалы:
- воронки ВФ-1(2)-75-ПОР 500 ТХС по ГОСТ 25336;
- колбы конические Кн-1-25(100,500,1000)-14/23 ТС по ГОСТ 25336;
- колбы мерные 1(2)-25(50,100,200,250,300,500,1000)-2 по ГОСТ 1770;
- пипетки стеклянные по ГОСТ 29227;
- пипетки автоматические вместимостью от 0,1 до 5,0 см с наконечниками;
- стаканчики для взвешивания (бюксы) СВ 19/9 и 24/10 по ГОСТ 25336;
- цилиндры 1-10(50,100,500)-1 по ГОСТ 1770;
- ступка и пестик по ГОСТ 9147.
5.2.3 При определении ферментативной активности -глюканазы применяют следующие реактивы:
- -глюкан из ячменя с содержанием основного вещества не менее 95%, (например, Sigma, кат. N G6517*);
_______________
* Данная информация не является рекламой и приведена для удобства пользователей настоящего стандарта.
- воду дистиллированную по ГОСТ 6709;
- кислоту уксусную ледяную по ГОСТ 61, х.ч.;
- натрий уксуснокислый 3-водный по ГОСТ 199, ч.д.а.;
- спирт этиловый ректификованный по ГОСТ 5962;
- образец эндо--глюканазы (образец сравнения) с активностью (3100±150) ед.ГлА/г (ед.ГлА/см
), (например, Sigma, кат. N G4423*).
_______________
* Данная информация не является рекламой и приведена для удобства пользователей настоящего стандарта.
5.2.4 Допускается применение других средств измерений и посуды, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающим необходимую точность измерения, а также вспомогательных устройств, реактивов и материалов по качеству не ниже вышеуказанных.
5.3 Приготовление растворов
5.3.1 Приготовление ацетатного буферного раствора молярной концентрации 0,1 моль/дм с кислотностью 4,7 ед. pH
5.3.1.1 Приготовление раствора уксусной кислоты
В мерную колбу вместимостью 1 дм вносят 5,7 см
ледяной уксусной кислоты, добавляют приблизительно 300 см
дистиллированной воды, перемешивают. Доводят до метки дистиллированной водой и снова перемешивают.
Срок хранения раствора в стеклянной посуде при комнатной температуре - не более 1 мес.
5.3.1.2 Приготовление раствора 3-водного уксуснокислого натрия
В мерную колбу вместимостью 1 дм вносят 13,6 г 3-водного уксуснокислого натрия и растворяют приблизительно в 300 см
дистиллированной воды. Затем доводят до метки дистиллированной водой и перемешивают.
Срок хранения при комнатной температуре - не более 1 мес.
5.3.1.3 Для приготовления ацетатного буферного раствора смешивают равные объемы растворов уксусной кислоты и 3-водного уксуснокислого натрия. Измеряют значение pH и при необходимости доводят кислотность раствора до 4,7 ед. pH одним из исходных растворов.
5.3.2 Приготовление субстрата - 0,4%-ного раствора -глюкана
В коническую колбу вместимостью 100 см вносят 400 мг
-глюкана, добавляют 3 см
этилового спирта. К суспензии добавляют приблизительно 30 см
ацетатного буферного раствора (см. 5.3.1). Смесь нагревают в водяной бане при температуре 50°С при энергичном перемешивании до полного растворения
-глюкана. При этом образуется мутный раствор. Колбу с раствором охлаждают до комнатной температуры, доливают ацетатным буферным раствором (см. 5.3.1) до 50 г (по массе) и тщательно перемешивают. При необходимости раствор осветляют центрифугированием при частоте вращения 4000 мин
в течение 10-15 мин или фильтрованием через воронку со стеклянным фильтром.
Субстрат готовят перед проведением анализа.
5.4 Отбор и подготовка проб
5.4.1 Отбор проб - по ГОСТ 20264.0.
5.4.2 Подготовка проб
5.4.2.1 Порошкообразные или микрокапсулированные анализируемые пробы используют без предварительной подготовки. Гранулированные анализируемые пробы измельчают (например, в механической мельнице или фарфоровой ступке) и просеивают через сито с размером диаметра ячеек не более 1 мм.
5.4.2.2 Для приготовления основного раствора анализируемой пробы в коническую колбу вместимостью 100 см помещают от 0,1 до 10,0 г** анализируемой пробы, взвешенной с погрешностью до 1,0 мг, и суспендируют в небольшом количестве (около 50 см
) ацетатного буферного раствора (см. 5.3.1) на магнитной мешалке в течение 15 мин. Экстракт количественно переносят в мерную колбу вместимостью от 100 до 500 см
(в зависимости от предполагаемой активности) и доводят объем ацетатным буферным раствором (см. 5.3.1) до метки. Полученную суспензию центрифугируют при частоте вращения 4000 мин
в течение 15 мин. Для анализа используют надосадочную жидкость.
_______________
** В зависимости от предполагаемой активности.
5.4.2.3 Рабочий раствор анализируемой пробы готовят из основного раствора (см. 5.4.2.2) путем разведения его ацетатным буферным раствором (см. 5.3.1). Рабочий раствор должен содержать от 0,5 до 1,0 единицы эндоглюканазной активности (ед. ГлА) в 1 см.
Используют свежеприготовленный раствор.
5.5 Проведение анализа
5.5.1 В сухой вискозиметр Оствальда, погруженный в прозрачную водяную баню с температурой 30°С, вносят 9 см ацетатного буферного раствора (см. 5.3.1), прогревают в течение 5 мин и пропускают раствор через капилляр вискозиметра от трех до пяти раз. Измеряют каждый раз время истечения раствора и рассчитывают его среднеарифметическое значение
.
5.5.2 Вискозиметр освобождают от ацетатного буферного раствора, после чего вносят 8 см раствора субстрата (см. 5.3.2) и 1 см
ацетатного буферного раствора (см. 5.3.1), выдерживают 5 мин при температуре 30°С и пропускают через капилляр от трех до пяти раз, чтобы определить контрольное время истечения исходного субстрата
, соответствующее начальному времени
.
5.5.3 Вискозиметр освобождают от раствора, после чего вносят 8 см раствора субстрата (см. 5.3.2), выдерживают при температуре 30°С в течение 5 мин. Добавляют 1 см
рабочего раствора анализируемой пробы (см. 5.4.2.3), предварительно прогретой в течение 5 мин при 30°С, перемешивают содержимое вискозиметра путем продувания воздуха в трубке. Включают секундомер и через 5 мин гидролиза вторым секундомером определяют время истечения инкубационной смеси
. Гидролиз продолжают в течение времени
, равного 15 мин, измеряя время истечения каждые 5 мин
,
,
. Каждую пробу анализируют дважды.
5.6 Обработка результатов
5.6.1 Рассчитывают относительную вязкость инкубируемой смеси для каждого времени измерения , в том числе для
, по формуле
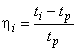 , (1)
, (1)
где - время истечения инкубационной смеси в каждый период инкубации (
, мин), с;
- время истечения ацетатного буферного раствора, с.
5.6.2 Для каждого периода инкубации , в том числе для
, рассчитывают величину, обратную относительной вязкости
![]() - относительную текучесть. Для
- относительную текучесть. Для :
![]() .
.
5.6.3 Определяют изменение относительной текучести для каждого отрезка времени в сравнении с
:
![]() .
.
5.6.4 Величину ферментативной активности эндо--глюканазы
, ед. ГлА/г (ед. ГлА/см
), определяют по формуле
![]() , (2)
, (2)
где - среднеарифметическая величин
![]() ;
;
- масса анализируемой пробы в 1 см
инкубационной смеси, г (с учетом исходного разведения и объема разведения в вискозиметре), которую рассчитывают по формуле
![]() , (3)
, (3)
где - масса анализируемой пробы препарата, г;
- объем основного раствора анализируемой пробы, см
;
- разведение основного раствора при приготовлении рабочего раствора пробы по 5.4.2.3;
- разведение рабочего раствора при добавлении раствора субстрата в вискозиметре.
Эндо-глюканазную активность рассчитывают как среднеарифметическое значение результатов двух параллельных определений, округленное до первого десятичного знака.
5.6.5 При необходимости полученные результаты можно пересчитывать на основании активности используемого образца сравнения эндо--глюканазы в единицах глюканазной активности (ед. ГлА), соответствующих количеству фермента, действующего на
-глюкан с высвобождением 1 мкмоля восстанавливающих сахаров (в пересчете на глюкозу) при стандартных условиях.
Строят градуировочный график как кривую соответствия активности по увеличению относительной текучести в ед. ГлА/г (ед. ГлА/см).
5.7 Сходимость и воспроизводимость результатов
Результаты измерений, полученные в условиях повторяемости (сходимости), признают удовлетворительными, если выполняется условие приемлемости
![]() , (4)
, (4)
где и
- результаты двух параллельных определений, полученные в условиях повторяемости при
=0,95;
- среднеарифметическое значение результатов двух параллельных определений анализируемой пробы, ед. ГлА/г (ед. ГлА/см
);
- предел повторяемости (сходимости),
=12%, (см. таблицу 1).
Результаты измерений, полученные в условиях воспроизводимости, признаются удовлетворительными, если выполняются условия приемлемости
![]() , (5)
, (5)
где и
- результаты двух определений, выполненных в двух разных лабораториях, ед. ГлА/г (ед. ГлА/см
);
- среднеарифметическое значение результатов двух определений, выполненных в двух разных лабораториях, ед. ГлА/г (ед. ГлА/см
);
- предел воспроизводимости,
=28%, (см. таблицу 1).
За результат измерений принимают среднеарифметическое значение результатов двух параллельных определений, если выполняется условие приемлемости
![]() , (6)
, (6)
где и
- результаты параллельных определений ферментативной активности эндо-
-глюканазы, ед. ГлА/г (ед. ГлА/см
);
- значение предела повторяемости,
=12%, (см. таблицу 1).
6 Метод определения ферментативной активности эндо- -глюканазы с использованием вискозиметра Гепплера (с падающим шариком)
-глюканазы с использованием вискозиметра Гепплера (с падающим шариком)
6.1 Сущность метода
Метод основан на определении времени падения шарика в растворе субстрата (-глюкана). В результате гидролиза субстрата ферментом вязкость и, соответственно, время падения шарика уменьшается. Чем выше концентрация или активность фермента, тем больше снижается динамическая вязкость анализируемого образца, т.е. время падения шарика. Концентрация фермента определяется в мкг/см
, активность - в ед. ГлА/г (ед. ГлА/см
).
Единицу эндо--глюканазной активности по Гепплеру определяют путем пересчета по активности образца сравнения в ед. ГлА, которая соответствует количеству фермента, действующего на
-глюкан с высвобождением 1 мкмоля восстанавливающих сахаров (в пересчете на глюкозу).
6.2 Средства измерений, вспомогательные устройства, материалы, посуда и реактивы
Для определения ферментативной активности эндо--глюканазы с использованием вискозиметра Гепплера применяют средства измерений, вспомогательные устройства, материалы, посуду и реактивы, указанные в 5.2, со следующими дополнениями:
- вискозиметр Гепплера с диапазоном измерения от 0,6 до 70000 мПа·с и допустимой погрешностью не более ±2% от измеряемой величины;
- шарик стеклянный N 1, диаметром 15,805 мм, с плотностью 2,22 г/см и постоянной К, равной 0,009 мПа·с/г и диапазоном измерения 0,6-3,0 мПа·с;
- ареометр АОН-1 700-760 по ГОСТ 18481;
- ультратермостат, обеспечивающий температуру нагрева 30°С с погрешностью регулирования температуры не более ±0,1°С.
6.3 Приготовление растворов
6.3.1 Приготовление ацетатного буферного раствора молярной концентрации 0,1 моль/дм с кислотностью 4,7 ед. pH
Ацетатный буферный раствор молярной концентрации 0,1 моль/дм с кислотностью 4,7 ед. pH готовят по 5.3.1.
6.3.2 Приготовление субстрата - 0,25%-ного раствора -глюкана
В коническую колбу вместимостью 100 см вносят 250,0 мг
-глюкана, добавляют 5 см
этилового спирта. К суспензии добавляют приблизительно 50 см
ацетатного буферного раствора по 5.3.1. Смесь нагревают в водяной бане при температуре от 60°С до 70°С при энергичном перемешивании до полного растворения
-глюкана. При этом образуется мутный раствор. Колбу с раствором охлаждают до комнатной температуры, доливают ацетатным буферным раствором до 100 г (по массе) и тщательно перемешивают. При необходимости раствор осветляют центрифугированием при частоте вращения 4000 мин
в течение 10-15 мин или фильтрованием через воронку со стеклянным фильтром.
Субстрат готовят перед проведением анализа.
6.3.3 Приготовление основного раствора сравнения эндо--глюканазы
В мерную колбу вместимостью 200 см вносят 400 мг образца сравнения, взятого с точностью до 1 мг, и приблизительно 70 см
ацетатного буферного раствора (см. 5.3.1), перемешивают до полного растворения. После чего раствор доводят до метки ацетатным буферным раствором, снова перемешивают. Получают раствор с известной активностью.
Используют свежеприготовленный раствор.
6.3.4 Приготовление рабочих растворов сравнения эндо--глюканазы
Рабочие растворы сравнения готовят путем последовательных разведений (от 1000 до 10000 раз) из основного раствора сравнения эндо--глюканазы и ацетатного буферного раствора (см. 5.3.1) в мерных колбах соответствующего объема, до получения растворов с активностями: 0,006; 0,012; 0,03; 0,06 ед. ГлА/см
.
Растворы готовят в день проведения анализа.
6.4 Отбор и подготовка проб
Отбор и подготовка проб по 5.4.
Для определения активности эндо--глюканазы в анализируемой пробе готовят раствор с активностью от 0,01 до 0,06 ед. ГлА/см
.
6.5 Проведение анализа
6.5.1 Подготовку вискозиметра производят в соответствии с инструкцией к прибору. Проводят юстировку прибора. Вискозиметр подсоединяют к проточной водяной бане (ультратермостату) с температурой 30°С. Расхождения во времени падения шарика зависят в основном от постоянства температуры.
6.5.2 Внутренний резервуар заполняют 30 см раствора субстрата (см. 6.3.2) и 5 см
ацетатного буферного раствора (см. 5.3.1) до уровня на 23-25 мм ниже верхнего края поворотной трубки. Жидкость в вискозиметре перемешивают 2 раза с помощью поворотной трубки.
6.5.3 Выдерживают испытуемую жидкость при 30°С в течение 5 мин, после чего опускают шарик. Измеряют первым секундомером время падения шарика между 1-й и 2-й отметками, а затем сразу с помощью второго секундомера - между 2-й и 3-й отметками. Время падения шарика позволяет рассчитать динамическую вязкость.
6.5.4 Вискозиметр освобождают от смеси субстрата с буферным раствором и вносят такой же объем субстрата и 5 см раствора анализируемой пробы (см. 6.4), предварительно по отдельности прогретых при 30°С в течение 5 мин.
Смесь перемешивают двумя поворотами трубки и засекают время начала гидролиза.
6.5.5 Через 10 мин гидролиза опускают шарик, устанавливают время его падения по секундомеру аналогично 6.5.3 и определяют изменение динамической вязкости в сравнении с исходным субстратом.
6.5.6 Для расчета ферментативной активности эндо--глюканазы анализируемой пробы в ед. ГлА/см
(ед. ГлА/г) строят градуировочный график зависимости степени уменьшения динамической вязкости раствора субстрата, определяемую по 6.5.3, от активности эндо-
-глюканазы в рабочих растворах сравнения (см. 6.3.4).
6.5.7 Действие каждого разведения рабочего стандартного раствора эндо--глюканазы на вязкость раствора субстрата определяют аналогично 6.5.2-6.5.5.
6.6 Обработка результатов
6.6.1 Динамическую вязкость раствора субстрата с ацетатным буферным раствором (см. 6.5.3) и раствора субстрата после гидролиза эндо--эндоглюканазой (мПа·с) (см. 6.5.5) рассчитывают по формуле
![]() , (7)
, (7)
где - время падения шарика, с;
- плотность шарика, г/см
;
- плотность каждого анализируемого раствора при температуре измерения, г/см
;
- постоянная для шарика, равная 0,009 мПа·с/г.
При этом ,
и
являются величиной постоянной, изменяется только
- время падения шарика. Поэтому при построении градуировочного графика можно использовать соотношение величин
- изменения времени падения шарика после обработки субстрата ферментом, в сравнении с исходным субстратом, и соответствующих им значений активности
-глюканазы.
6.6.2 За окончательный результат принимают среднеарифметическое значение результатов двух параллельных определений, округленное до первого десятичного знака.
6.7 Сходимость и воспроизводимость результатов
Сходимость и воспроизводимость результатов анализа по 5.7.
7 Определение ферментативной активности эндо- -глюканазы с использованием бета-глюказима
-глюканазы с использованием бета-глюказима
7.1 Сущность метода
Метод основан на измерении интенсивности окраски красителя, освобожденного в результате гидролиза из субстрата бета-глюказима ферментом эндо--глюканазой, при длине волны 620 нм. Количественное определение степени деградации производят в сравнении с образцом сравнения эндо-
-глюканазы, имеющим известную активность.
За единицу активности эндо--глюканазы принимают количество фермента, которое действует на
-глюкан с высвобождением 1 мкмоля восстанавливающих сахаров (в пересчете на глюкозу).
7.2 Средства измерений, вспомогательные устройства, посуда, материалы и реактивы
Для определения ферментативной активности эндо--глюканазы с использованием бета-глюказима применяют средства измерений, вспомогательные устройства, посуду, материалы и реактивы, которые указаны в 5.2, со следующими дополнениями:
- фотоэлектроколориметр или спектрофотометр любого типа, которые обеспечивают измерения при длинах волн 490-670 нм, с погрешностью измерения коэффициента пропускания не более ±1%, (не более 0,01 единицы оптической плотности);
- шейкер горизонтальный с амплитудой возвратно-поступательного движения 10 мм и диапазоном скоростей от 50 до 250 об/мин;
- шейкер вортексного типа для пробирок с амплитудой встряхивания 3 мм и диапазоном скоростей от 150 до 2500 об/мин;
- кислоту соляную по ГОСТ 3118, х.ч.;
- натрий фосфорнокислый трехзамещенный (тринатрийфосфат) по ГОСТ 201;
- таблетки азурин-структурированного ячменного бета-глюкана (бета-глюказим) в дозировке 60 мг;
- пробирки П-1-15-14/23 ХС с пробками по ГОСТ 1770;
- фильтры обеззоленные "Синяя лента".
7.3 Подготовка к анализу
7.3.1 Приготовление ацетатного буферного раствора молярной концентрации 0,1 моль/дм с кислотностью 4,7 ед. pH
Приготовление ацетатного буферного раствора молярной концентрации 0,1 моль/дм с кислотностью 4,7 ед. pH по 5.3.1.
7.3.2 Приготовление раствора соляной кислоты молярной концентрации 2 моль/дм
В мерную колбу вместимостью 100 см вносят примерно 60 см
дистиллированной воды, осторожно добавляют 15 см
соляной кислоты, доводят дистиллированной водой до метки и перемешивают.
Срок хранения при комнатной температуре - не более 1 мес.
7.3.3 Приготовление раствора для торможения реакции (стоп-реагент)
В качестве стоп-реагента используют на выбор один из двух растворов:
1) в мерную колбу вместимостью 1 дм вносят 20 г тринатрийфосфата, доводят до метки дистиллированной водой и перемешивают.
Срок хранения при комнатной температуре - не более 1 недели.
2) в коническую колбу вместимостью 500 см вносят 300 см
этилового спирта, добавляют 2 см
раствора соляной кислоты (см. 7.3.2).
Срок хранения при комнатной температуре - не более 1 недели.
7.3.4 Приготовление рабочих растворов сравнения эндо--глюканазы
7.3.4.1 Приготовление основного раствора сравнения эндо--глюканазы с известной активностью
В мерную колбу вместимостью 100 см вносят 1,000 г образца сравнения эндо-
-глюканазы и приблизительно 70 см
ацетатного буферного раствора (см. 5.3.1), полностью растворяют, после чего объем доводят до метки ацетатным буферным раствором и перемешивают.
Получают раствор с известной активностью.
7.3.4.2 Приготовление рабочих растворов сравнения эндо--глюканазы
Рабочие растворы сравнения готовят путем последовательных разведений (от 100 до 600 раз) из основного раствора сравнения эндо--глюканазы и ацетатного буферного раствора (см. 5.3.1) в мерных колбах соответствующего объема, до получения растворов с активностями: 0,01; 0,015; 0,03; 0,05; 0,06 ед. ГлА/см
.
Растворы готовят в день проведения анализа.
7.3.5 Построение градуировочного графика
7.3.5.1 В пробирки вместимостью 15 см вносят по 1 см
рабочих растворов эндо-
-глюканазы (см. 7.3.4.2), в контрольную пробирку - 1 см
ацетатного буферного раствора (см. 5.3.1) и помещают в водяную баню с температурой 50°С на 5 мин. В каждую пробирку вносят по одной бета-глюказим-таблетке и, не перемешивая, выдерживают в водяной бане при температуре 50°С в течение 20 мин с точностью по секундомеру. Реакцию останавливают, добавляя в пробирки по 10 см
стоп-реагента (см. 7.3.3).
7.3.5.2 Все пробирки перемешивают на шейкере вортексного типа в течение 30 с, затем оставляют их при комнатной температуре на 10 мин, снова перемешивают на шейкере вортексного типа и осветляют центрифугированием при 4000 мин в течение 15 мин или фильтрованием через фильтр "Синяя лента".
7.3.5.3 Измеряют фотоэлектроколориметром или спектрофотометром оптическую плотность супернатантов (фильтратов) при 620 нм в кювете толщиной поглощающего свет слоя 1 см против контрольной пробы. Для каждого градуировочного раствора выполняют два параллельных измерения.
7.3.5.4 По полученным результатам строят градуировочный график соответствия окраски супернатантов (после проведения гидролиза субстрата с разными разведениями растворов сравнения эндо--глюканазы), величинам их активности: на оси ординат откладывают величины оптической плотности; на оси абсцисс - активность разведений стандарта ед. ГлА/см
.
7.4 Отбор и подготовка проб
7.4.1 Отбор проб - по 5.1.4.
7.4.2 Подготовка проб
7.4.2.1 Приготовление основного раствора анализируемой пробы
Для приготовления основного раствора в мерную колбу вместимостью 100 см вносят от 1,0 до 5,0 г анализируемой пробы (порошок, микрокапсулы или гранулы), добавляют небольшое количество ацетатного буферного раствора (см. 5.3.1), помещают на горизонтальный шейкер для перемешивания в течение 60 мин, затем доводят до метки ацетатным буферным раствором. Полученный экстракт центрифугируют при частоте вращения 4000 мин
в течение 15 мин или фильтруют через фильтр "Синяя лента".
Для экстракции жидких анализируемых проб в мерную колбу вместимостью 50 см вносят 1,0 см
анализируемой пробы и доводят до метки ацетатным буферным раствором (см. 5.3.1).
7.4.2.2 Приготовление рабочего раствора анализируемой пробы
Рабочий раствор готовят путем последовательных разведений основного раствора анализируемой пробы (см. 7.4.2.1) и ацетатного буферного раствора (см. 5.3.1) в мерных колбах соответствующего объема, до получения раствора с активностью от 0,05 до 0,4 ед. ГлА/см.
7.5 Проведение анализа
7.5.1 В три пробирки (две опытные, одна - контрольная) вносят по 1 см раствора анализируемой пробы. В пробирку с контрольной пробой добавляют 10 см
стоп-реагента (см. 7.3.3). Пробирки помещают в водяную баню и выдерживают при температуре 50°С в течение 5 мин. В каждую пробирку вносят по одной бета-глюказим-таблетке и, не перемешивая, выдерживают в водяной бане при температуре 50°С в течение 20 мин с точностью по секундомеру.
7.5.2 В пробирках с опытными пробами реакцию останавливают добавлением 10 см стоп-реагента (см. 7.3.3). В контрольную пробирку вносят 1 см
анализируемой пробы. Содержимое всех пробирок перемешивают на шейкере вортексного типа в течение 30 с. Пробирки оставляют при комнатной температуре на 10 мин, снова перемешивают на шейкере вортексного типа и осветляют центрифугированием при 4000 мин
в течение 15 мин или фильтрованием через фильтр "Синяя лента".
7.5.3 Измеряют фотоэлектроколориметром или спектрофотометром оптическую плотность супернатантов (фильтратов) при 620 нм в кюветах толщиной поглощающего свет слоя 1 см против контрольной пробы (оптический контроль) и определяют активность по градуировочному графику в ед. ГлА/см.
7.6 Обработка результатов
Активность эндо--глюканазы
, ед. ГлА/г, вычисляют по формуле
![]() , (8)
, (8)
где - активность рабочего разведения образца по градуировочному графику, ед. ГлА/см
;
- количество ферментного препарата в 1 см
реакционной смеси, г.
![]() , (9)
, (9)
где - масса анализируемой пробы, г;
- объем разведения пробы при приготовлении основного раствора по 7.4.2.1, см
;
- разведение основного раствора ферментного препарата для приготовления рабочего раствора по 7.4.2.2.
За окончательный результат принимают среднеарифметическое значение результатов двух параллельных определений, округленное до первого десятичного знака.
7.7 Сходимость и воспроизводимость результатов
Результаты измерений, полученные в условиях повторяемости (сходимости), признают удовлетворительными, если выполняется условие приемлемости
![]() , (10)
, (10)
где и
- результаты двух параллельных определений, полученные в условиях повторяемости при
=0,95;
- среднеарифметическое значение результатов двух параллельных определений анализируемой пробы, ед. ГлА/г (ед. ГлА/см
);
- предел повторяемости (сходимости),
=10%, (см. таблицу 1).
Результаты измерений, полученные в условиях воспроизводимости, признаются удовлетворительными, если выполняются условия приемлемости
![]() , (11)
, (11)
где и
- результаты двух определений, выполненных в двух разных лабораториях, ед. ГлА/г (ед. ГлА/см
);
- среднеарифметическое значение результатов двух определений, выполненных в двух разных лабораториях, ед. ГлА/г (ед. ГлА/см
);
- предел воспроизводимости,
=17%, (см. таблицу 1).
За результат измерений принимают среднеарифметическое значение результатов двух параллельных определений, если выполняется условие приемлемости
![]() , (12)
, (12)
где и
- результаты параллельных определений ферментативной активности эндо-
-глюканазы, ед. ГлА/г;
- значение предела повторяемости,
=10%, (см. таблицу 1).
8 Определение ферментативной активности эндо- -глюканазы с использованием азо-
-глюканазы с использованием азо- -глюкана
-глюкана
8.1 Сущность метода
Метод основан на измерении интенсивности окраски красителя, освобожденного в результате гидролиза окрашенного субстрата азо-глюкана ферментом эндо--глюканазой, при длине волны 490 нм. Количественное определение степени деградации производят в сравнении с образцом эндо-
-глюканазы, имеющим известную активность
За единицу активности эндо--глюканазы принимают количество фермента, которое действует на
-глюкан с высвобождением 1 мкмоля восстанавливающих сахаров (в пересчете на глюкозу).
8.2 Средства измерений, вспомогательные устройства, посуда, материалы и реактивы
Для определения ферментативной активности эндо--глюканазы с азо-глюканом применяют средства измерений, вспомогательные устройства, посуду, материалы и реактивы, которые указаны в 7.2, со следующим дополнением:
- азо-глюкан (субстрат из ячменя с азо-хромофором), (например, Sigma, кат. N G50263*);
_______________
* Данная информация не является рекламой и приведена для удобства пользователей настоящего стандарта.
- натрий уксуснокислый безводный, х.ч.;
- цинк уксуснокислый 2-водный по ГОСТ 5823, х.ч.
8.3 Подготовка к анализу
8.3.1 Приготовление ацетатного буферного раствора молярной концентрации 0,1 моль/дм с кислотностью pH 4,7 ед. pH
Приготовление ацетатного буферного раствора молярной концентрации 0,1 моль/дм с кислотностью 4,7 ед. pH по 5.3.1.
8.3.2 Приготовление раствора соляной кислоты молярной концентрации 4 моль/дм
В мерную колбу вместимостью 100 см вносят примерно 60 см
дистиллированной воды, осторожно прибавляют 33 см
соляной кислоты, доводят до метки дистиллированной водой и перемешивают.
Срок хранения при комнатной температуре - не более 1 мес.
8.3.3 Приготовление раствора для торможения реакции (стоп-реагент)
В коническую колбу вместимостью 1 дм вносят 150 см
дистиллированной воды и 24,1 г натрия уксуснокислого безводного, перемешивают. Добавляют 4,8 г цинка уксуснокислого 2-водного и перемешивают до полного растворения. Измеряют значение pH и, при необходимости, доводят кислотность раствора до 5,0 ед. pH раствором соляной кислоты (см. 8.3.2). Добавляют 50 см
дистиллированной воды, 800 см
этилового спирта и перемешивают.
Используют свежеприготовленный раствор.
8.3.4 Приготовление раствора окрашенного субстрата
В коническую колбу вместимостью 25 см вносят 20 см
ацетатного буферного раствора (см. 5.3.1) и при постоянном перемешивании медленно прибавляют к нему 250,0 мг сухого азо-глюкана. Смесь выдерживают в водяной бане при температуре 70°С в течение 15-30 мин до полного растворения субстрата, после чего охлаждают до комнатной температуры. Раствор переносят в мерную колбу вместимостью 25 см
, доводят объем до метки ацетатным буферным раствором (см. 5.3.1), перемешивают.
Срок хранения раствора при температуре от 2°С до 8°С не более 96 ч.
Перед применением раствор азо-глюкана выдерживают при комнатной температуре в течение 30 мин и перемешивают.
8.3.5 Приготовление растворов сравнения эндо--глюканазы
8.3.5.1 Приготовление основного раствора сравнения эндо--глюканазы с известной активностью
В мерную колбу вместимостью 100 см вносят 1,000 г образца сравнения эндо-
-глюканазы с известной активностью, приблизительно 70 см
ацетатного буферного раствора (см. 5.3.1), перемешивают до полного растворения. После чего раствор доводят до метки ацетатным буферным раствором, снова перемешивают.
Получают раствор с известной активностью.
8.3.5.2 Приготовление рабочих растворов сравнения эндо--глюканазы
Из основного раствора, в мерных колбах вместимостью 100 см, готовят рабочие растворы сравнения эндо-
-глюканазы различной активности аналогично 7.3.4.2.
Растворы готовят в день проведения анализа.
8.4 Построение градуировочного графика
8.4.1 В пробирки вносят по 0,5 см рабочих растворов сравнения эндо-
-глюканазы (см. 8.3.5.2), в контрольную пробирку - 0,5 см
ацетатного буферного раствора (см. 5.3.1), добавляют по 0,5 см
раствора окрашенного субстрата (см. 8.3.4), перемешивают на шейкере вортексного типа в течение 30 с и помещают в водяную баню с температурой 50°С на 10 мин. Реакцию останавливают, добавляя в пробирки по 2,5 см
стоп-реагента (см. 8.3.3).
8.4.2 Все пробирки выдерживают при комнатной температуре в течение 10 мин и осветляют центрифугированием при частоте вращения 4000 мин в течение 15 мин или фильтруют через фильтр "Синяя лента".
8.4.3 Измеряют оптическую плотность супернатантов (фильтратов) при 490 нм в кювете толщиной поглощающего свет слоя 1 см против контрольной пробы. Для каждого градуировочного раствора выполняют два параллельных измерения.
8.4.4 По полученным результатам строят градуировочный график соответствия окраски супернатантов (фильтратов), после проведения гидролиза субстрата с разными разведениями образца сравнения, величинам их активности: на оси ординат откладывают величины оптической плотности; на оси абсцисс - активность разведений стандарта ед. ГлА/см.
8.5 Отбор и подготовка проб
8.5.1 Отбор проб - по 5.1.4.
8.5.2 Подготовка проб - по 7.4.2.
8.6 Проведение анализа
8.6.1 В три пробирки (две - опытные, одна - контрольная) вносят по 0,5 см раствора окрашенного субстрата (см. 8.3.4) и помещают в водяную баню при температуре 50°С на 5 мин.
8.6.2 В опытные пробирки добавляют по 0,5 см предварительно прогретого в водяной бане при температуре 50°С раствора анализируемой пробы и перемешивают на шейкере вортексного типа в течение 30 с.
8.6.3 В контрольную пробирку добавляют 2,5 см стоп-реагента (см. 8.3.3), перемешивают на шейкере вортексного типа в течение 30 с и вносят 0,5 см
раствора анализируемой пробы.
8.6.4 Пробирки закрывают пробками и выдерживают в водяной бане при температуре 50°С в течение 10 мин.
8.6.5 В пробирках с опытными пробами реакцию останавливают добавлением 2,5 см стоп-реагента (см. 8.3.3). Содержимое всех пробирок перемешивают на вортексе в течение 30 с. Пробирки оставляют при комнатной температуре на 10 мин и осветляют центрифугированием при частоте вращения 4000 мин
в течение 10 мин или фильтрованием через фильтр "Синяя лента".
8.6.6 Измеряют оптическую плотность супернатантов (фильтратов) при 490 нм толщиной поглощающего свет слоя 1 см против контрольной пробы (оптический контроль).
8.7 Обработка результатов
Обработку результатов анализа проводят по 7.6.
8.8 Сходимость и воспроизводимость результатов
Сходимость и воспроизводимость результатов по 7.7.
9 Метрологические характеристики
Установленные в настоящем стандарте методы обеспечивают выполнение измерений ферментативной активности эндо--глюканазы с относительной расширенной неопределенностью результатов измерений при коэффициенте охвата
=2 и доверительной вероятности
=0,95, указанной в таблице 1.
Таблица 1 - Показатели точности и прецизионности методов при определении ферментативной активности эндо--глюканазы
Диапазон измерений ферментативной активности эндо- | Значение относительной расширенной неопределен- | Относительное стандартное отклонение повторяемости | Относитель- | Предел повторя- | Предел воспроизво- |
Вискозиметрические методы | 22 | 4,3 | 10 | 12 | 28 |
Колориметрические методы | 14 | 3,6 | 6 | 10 | 17 |
10 Оформление результатов измерений
Результат измерения ферментативной активности эндо--глюканазы ед. ГлА/г (ед. ГлА/см
), представляют в виде:
![]() , при
, при =0,95, (13)
где - среднеарифметическое значение двух параллельных измерений активности эндо-
-глюканазы ед. ГлА/г (ед. ГлА/см
);
- значение относительной расширенной неопределенности, % (в соответствии с таблицей 1).
Числовое значение результата измерений должно оканчиваться цифрой того же разряда, что и значение расширенной неопределенности в абсолютных единицах.
11 Контроль стабильности результатов измерений
Если условия по (6) или (12) не выполняются, выясняют причины превышения критического диапазона, устраняют их и повторяют выполнение измерений по ГОСТ ИСО 5725-6-2003 (пункт 5.2.2).
Библиография
[1] | Enzyme Nomenclature, recommendations of the nomenclature Committee of the IUB, N.Y., Academic Press, 1984 |
УДК 577.15:543.06:006.354 | МКС | 07.100.30 |
65.120 | ||
Ключевые слова: препараты ферментные, ферментативная активность эндо- | ||
Редакция документа с учетом
изменений и дополнений подготовлена

